细胞分选系统及使用方法
文献发布时间:2023-06-19 11:27:38
本申请要求于2018年8月16日提交的美国临时申请第62/765,129号和于2019年1月29日提交的美国临时申请第62/798,206的优先权,其各自的内容整体并入本文以作参考,并要求其各自的优先权。
概述
本公开的主题提供用于分离表达特定构建体的细胞的方法和组合物。其涉及包含膜结合多肽和可溶性多肽的系统及其使用方法。
背景技术
将大量遗传信息稳定整合到原代T细胞中代表了当前细胞工程的局限性。当病毒载体插入物的大小超过病毒的包装极限时(逆转录病毒约为6-8kb,慢病毒约为10-12kb),逆转录病毒和慢病毒都显示出病毒滴度的显著降低。病毒滴度低导致转导效率低以及单位细胞的拷贝数整合低,导致基因构建体表达不佳。因此,仍然需要包含多个载体的基因表达系统,并且需要分离包含此类系统的细胞。
发明内容
本公开的主题提供膜结合多肽。该膜结合多肽可用于分选细胞。
在某些实施方式中,膜结合多肽包含:a)跨膜结构域,和b)细胞外结构域,其包含第一二聚化结构域和能够在细胞表面与第一二聚化结构域二聚化的第二二聚化结构域。在某些实施方式中,第一和第二二聚化结构域的每一个包含亮氨酸拉链结构域。在某些实施方式中,第一二聚化结构域包含如SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列,第二二聚化结构域包含如SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列。在某些实施方式中,细胞外结构域还包含在第一二聚化结构域和第二二聚化结构域之间的接头。在某些实施方式中,接头包含如SEQ ID NO:3所示的氨基酸序列。
在某些实施方式中,细胞外结构域还包含在第一二聚化结构域和跨膜结构域之间的间隔区/铰链结构域。在某些实施方式中,间隔区/铰链结构域包含被抗体识别的表位,其中抗体与表位的结合介导表达膜结合多肽的细胞的耗竭。在某些实施方式中,间隔区/铰链结构域包含Thy1.1分子或截短的EGFR分子(EGFRt)。在某些实施方式中,Thy1.1分子包含或具有如SEQ ID NO:68所示的氨基酸序列。在某些实施方式中,EGFRt包含或具有如SEQ IDNO:70所示的氨基酸序列。
在某些实施方式中,细胞外结构域还包含共刺激配体。在某些实施方式中,共刺激配体选自肿瘤坏死因子(TNF)家族成员、免疫球蛋白(Ig)超家族成员及其组合。在某些实施方式中,TNF家族成员选自4-1BBL、OX40L、CD70、GITRL、CD40L、CD30L及其组合。在某些实施方式中,共刺激配体是4-1BBL。
在某些实施方式中,Ig超家族成员选自CD80、CD86、ICOSLG及其组合。在某些实施方式中,共刺激配体是CD80。
在某些实施方式中,细胞外结构域还包含分子的显性负型。在某些实施方式中,该分子选自免疫检查点分子的抑制剂、肿瘤坏死因子受体超家族(TNFRSF)成员和转化生长因子β(TGFβ)受体。在某些实施方式中,免疫检查点分子选自PD-1、CTLA-4、B7-H3(也称为“CD276”)、B7-H4、BTLA、TIM-3、LAG-3、TIGIT、LAIR1、CD200、CD200R、HVEM、2B4、CD160、半乳凝素9及其组合。在某些实施方式中,免疫检查点分子是PD-1。在某些实施方式中,TNFRSF成员选自Fas、肿瘤坏死因子受体、OX40、CD40、CD27、CD30、4-1BB(也称为“CD137”)及其组合。在某些实施方式中,显性负受体包含TGFβRII的细胞外结构域或其片段。
在某些实施方式中,膜结合多肽还包含细胞内结构域。在某些实施方式中,细胞内结构域包含CD3-ζ结构域、共刺激结构域、自杀基因或其组合。
在某些实施方式中,膜结合多肽自载体表达。
本公开的主题还提供用于分离包含至少两个表达载体的细胞的系统。
在某些实施方式中,该至少两个表达载体包括:a)由第一表达载体编码的本文公开的膜结合多肽,和b)由第二表达载体编码的可溶性多肽,其包含标签和能够与第一二聚化结构域二聚化的第三二聚化结构域。在某些实施方式中,第三二聚化结构域在第一二聚化结构域和第二二聚化结构域之间的二聚化之前与第一二聚化结构域二聚化。在某些实施方式中,第三二聚化结构域与内质网中的第一二聚化结构域二聚化。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够形成二聚体。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够在内质网中形成二聚体。在某些实施方式中,可溶性多肽和膜结合多肽在从不同细胞表达时,由于第一多聚化结构域和第二二聚化结构域之间的二聚化,两者不能形成二聚体。在某些实施方式中,第三二聚化结构域包含如SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列。
在某些实施方式中,标签包括被第一抗体识别的表位标签。在某些实施方式中,表位标签选自Myc标签、HA标签、Flag标签、V5标签、T7标签、CD34标签及其组合。在某些实施方式中,标签包括与底物结合的亲和标签。在某些实施方式中,亲和标签选自His标签、Strep标签、E标签、链霉亲和素结合蛋白标签(SBP标签)及其组合。
在某些实施方式中,标签还包括被第二抗体识别的模拟表位。在某些实施方式中,第二抗体与模拟表位的结合介导包含膜结合多肽的细胞的耗竭。在某些实施方式中,模拟表位是CD20模拟表位,第二抗体是抗CD20抗体。在某些实施方式中,抗CD20抗体是利妥昔单抗。
在某些实施方式中,可溶性多肽还包含抗原结合结构域。在某些实施方式中,抗原结合结构域包含单链可变片段(scFv)、可溶性配体、细胞因子、基于非scFv的抗原识别基序或其组合。
在某些实施方式中,可溶性多肽还包含细胞因子或趋化因子。在某些实施方式中,细胞因子选自IL-1、IL-2、IL-3、IL-7、IL-10、IL-12、IL-15、IL-17、IL-18、IL-21、IL-22、IL-36及其组合。在某些实施方式中,趋化因子选自CCL1、CCL8、CCL16、CCL17、CCL18、CCL22及其组合。在某些实施方式中,膜结合多肽由第一载体表达。在某些实施方式中,可溶性多肽由第二载体表达。第一载体可以与第二载体相同。在某些实施方式中,第一载体与第二载体相同,例如,第一载体和第二载体的载体主链可以相同,而由第一载体和第二载体编码/表达的多肽或蛋白质可以不同。
在某些实施方式中,该至少两个表达载体包含:a)由第一表达载体编码的膜结合多肽,其包含跨膜结构域和细胞外结构域,其中所述细胞外结构域包含第一二聚化结构域和阻断间隔区;和b)由第二表达载体编码的可溶性多肽,其包含标签和第二二聚化结构域,其中第一和第二二聚化结构域各自包含亮氨酸拉链结构域,并且其中当膜结合多肽和可溶性多肽不是自同一细胞中表达时,阻断间隔区阻止膜结合多肽和可溶性多肽的二聚化。
在某些实施方式中,第一二聚化结构域包含如SEQ ID NO:1、SEQ ID NO:2或SEQID NO:106所示的氨基酸序列,并且第二二聚化结构域包含如SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列。
在某些实施方式中,阻断间隔区不超过约25个氨基酸残基。在某些实施方式中,阻断间隔区在约5个氨基酸残基至约25个氨基酸残基之间。在某些实施方式中,阻断间隔区是截短的CD28间隔区或IgG1铰链。
此外,本公开的主题提供分离包含至少两个表达载体的细胞的方法,以及分选包含至少两个表达载体的多个细胞的方法。
在某些实施方式中,分离包含至少两个表达载体的细胞的方法包括:a)在细胞中表达i)由第一表达载体编码的本文公开的膜结合多肽,和ii)由第二表达载体编码的本文公开的可溶性多肽,其包含标签和能够与第一二聚化结构域二聚化的第三二聚化结构域,b)使细胞与结合至标签的底物接触,并分离与底物结合的细胞。
在某些实施方式中,分选包含至少两个表达载体的多个细胞的方法包括:a)用以下i)和ii)转染多个细胞:i)编码本文公开的膜结合多肽的第一表达载体,和ii)编码本文公开的可溶性多肽的第二载体,例如,可溶性多肽包含标签和能够与第一二聚化结构域二聚化的第三二聚化结构域,b)使细胞与结合至标签的底物接触,以及c)分离与底物结合的一个或多个细胞。
在某些实施方式中,第三二聚化结构域能够在第一二聚化结构域和第二二聚化结构域之间的二聚化之前与第一二聚化结构域二聚化。在某些实施方式中,第三二聚化结构域能够与内质网中的第一二聚化结构域二聚化。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够形成二聚体。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够在内质网中形成二聚体。在某些实施方式中,可溶性多肽和膜结合多肽在从不同细胞表达时,由于第一二聚化结构域和第二二聚化结构域之间的二聚化,两者不能形成二聚体。在某些实施方式中,步骤c)之前是洗涤底物以去除不与底物结合的细胞的步骤。
在某些实施方式中,分离包含至少两个表达载体的细胞的方法包括:a)在细胞中表达i)由第一表达载体编码的本文公开的膜结合多肽,例如膜结合多肽包含跨膜结构域和细胞外结构域,其中细胞外结构域包含第一二聚化结构域和阻断间隔区,和ii)由第二表达载体编码的本文公开的可溶性多肽,例如,包含标签和第二二聚化结构域的可溶性多肽,其中第一和第二二聚化结构域均包含亮氨酸拉链结构域,并且其中当膜结合多肽和可溶性多肽不是从同一细胞表达时,阻断间隔区阻止膜结合多肽与可溶性多肽的二聚化,b)使细胞与结合至标签的底物接触,和c)分离与底物结合的细胞。
在某些实施方式中,分选包含至少两个表达载体的多个细胞的方法包括:a)用以下i)和ii)转染多个细胞:i)编码本文公开的膜结合多肽的第一表达载体,例如膜结合的多肽包含跨膜结构域和包含第一二聚化结构域的细胞外结构域,和ii)编码本文公开的可溶性多肽的第二表达载体,例如,可溶性多肽包含标签和能够与第一二聚化结构域二聚化的第二二聚化结构域,其中第一和第二二聚化结构域各自包含亮氨酸拉链结构域,并且其中当膜结合多肽和可溶性多肽不是自同一细胞表达时,膜结合多肽不与可溶性多肽二聚化,b)使细胞与结合至标签的底物接触,和c)分离结合至底物的一个或多个细胞。
在某些实施方式中,细胞选自T细胞、自然杀伤(NK)细胞、可从中可分化出淋巴样细胞的干细胞。在某些实施方式中,细胞是T细胞。在某些实施方式中,T细胞选自细胞毒性T淋巴细胞(CTL)、调节性T细胞、自然杀伤T(NKT)细胞。在某些实施方式中,细胞是自体的。
在某些实施方式中,亮氨酸拉链是正交拉链。
本公开的主题还提供编码本文公开的膜结合多肽的核酸分子,包括包含此类核酸分子的载体。本公开的主题还提供包含本文公开的核酸分子和载体的宿主细胞。在某些实施方式中,宿主细胞是T细胞。在某些实施方式中,载体是病毒载体。在某些实施方式中,病毒载体是逆转录病毒载体,例如慢病毒载体。在某些实施方式中,载体是基于转座子的载体。
附图说明
以下通过实例的方式给出的详细描述可以结合附图加以理解,但其并非旨在将本发明限制于所描述的具体实施方式。
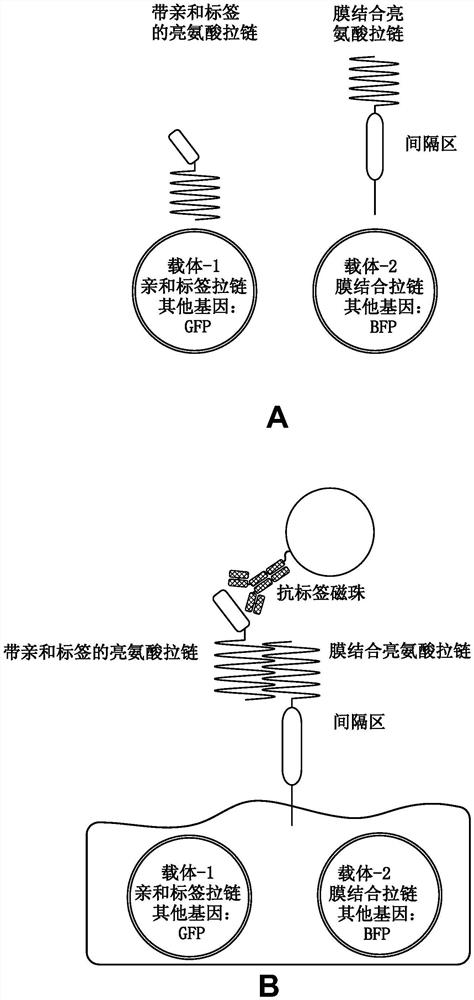
图1A描绘了根据本公开主题的某些实施方式的细胞分选系统。图1B描绘了用图1A中所示的两个载体的共转导允许磁珠仅分选具有两个病毒载体整合的细胞。
图2描绘了在某些情况下,分泌的带亲和标签的亮氨酸拉链可以在细胞外与膜结合亮氨酸拉链配对。
图3描绘了“阻断的”膜结合亮氨酸拉链的产生导致细胞内配对优于细胞外配对。
图4描绘了有意用非双重转导细胞污染的双重转导细胞的纯化。
图5描绘了用iCaspase 9和CD20-CAR双重转导的细胞的纯化和测试。在存在或不存在二聚化化学诱导剂(CID)的情况下,将包含RR12EE345L-FLAG iCaspase 9(载体1)和RR12EE345L-接头-EE12RR345L-Thy1.1 CD20-CAR(载体2)的T细胞与EL4-CD19和EL4-CD20靶标孵育。
图6描绘了使用本公开的分选系统用于纯化多功能CAR T细胞(A)亮氨酸拉链分选系统用于将细胞纯化至高于95%,其中所述细胞包含表达CD19-CAR、CD20-CAR和iCaspase9以及任选地IL-18(左上图)的两个载体。这些细胞能够杀伤CD19或CD20+靶标(右图),与iCaspase9二聚体一起孵育可导致约90%的细胞死亡(左下图)。(B)对CD19和CD20具有特异性并且被工程化以分泌IL-18的多功能CAR T细胞。小鼠T细胞用编码(1)FLAG-RR12EE345L亮氨酸拉链、iCaspase9和CD19-CAR和(2)接头阻断的RR12EE345L/EE12RR345L Thy1.1亮氨酸拉链(分选耗竭构建体)、具有完整前肽(pro-IL-18)或小鼠IL-2信号肽(sIL-18)的CD20-CAR +/-IL-18的载体进行共转导。用抗FLAG珠对T细胞进行单步MACS分选至纯度>90%,并针对C1498 CD19、C1498 CD20和CD1498进行靶标裂解测试。通过ELISA评估IL-18分泌。干扰素γ分泌通过细胞计数珠阵列进行评估。
图7A-7C描绘了固有阻断的截短的CD28膜近端铰链-间隔区跨膜亮氨酸拉链促进双转导细胞群的MACS分选。图7A显示用载体1(FLAG-RR12EE345L 2A CBR-2A-GFP)和载体2(EE12RR345L Myc CD28EC-9C CD2TM 2A Thy1.1)双重转导的C1498细胞系。图7B显示,由于截短的九氨基酸铰链-间隔区,FLAG染色仅限于GFP+BFP+双重转导的群体。图7C显示通过单步抗FLAG磁珠MACS分选产生的纯化的GFP+BFP+双重转导的群体。
图8A-8C描绘了接头阻断的截短的EGFR-间隔区跨膜亮氨酸拉链促进双转导细胞群的MACS分选。图8A显示用载体1(FLAG-RR12EE345L 2A CBR-2A-GFP)和载体2(RR12EE345L接头EE12RR345L EGFRt 2A BFP)双重转导的C1498细胞系。图8B显示由于连接的阻断RR12EE345L亮氨酸拉链,FLAG染色仅限于GFP+BFP+双转导群体。图8C显示通过单步抗FLAG磁珠MACS分选产生的纯化的GFP+BFP+双重转导的群体。
图9描述了与iCaspase9和阻断的Thy1.1亮氨酸拉链分选自杀构建体结合的双串联CAR构造。编码亮氨酸拉链分选系统构建体和串联CAR的两个逆转录病毒载体被用于转导T细胞。载体1编码带标签的分泌型亮氨酸拉链、iCaspase9和以下串联CAR,其包含与IL-3细胞因子(链间接头)连接的CD38 scFv、CD8铰链、CD8TM和CD28ζ信号传导基序。载体2编码阻断的Thy1.1亮氨酸拉链和以下串联CAR,其包含与CD19 scFv(链间接头)连接的CD20 scFv、CD8铰链、CD8TM和CD28ζ信号传导基序。
图10A和10B描绘了亮氨酸拉链分选系统能够对表达双串联CAR的T细胞进行单步MACS分选。图10A显示双转导T细胞的高纯度MACS分选(左图)。串联CD20-CD19 CAR的Myc标签染色比CD19单CAR的弱(右图,对比图5)。但是,Thy1.1在CD20-CD19 CAR载体上共表达,并显示与CD38-IL-3串联CAR的高度共纯化(中间图)。图10B显示单个T细胞系裂解的靶标各自表达4种单独抗原中的1种。通过在培养开始后24小时检测萤火虫荧光素酶转导的C1498靶细胞中残留的荧光素酶活性来确定靶标裂解。
图11A和11B描绘了亮氨酸拉链分选系统使得能够使用两个自杀基因删除分选的T细胞。用编码带标签的分泌型亮氨酸拉链分选构建体+串联CD38-IL-3CAR+iCaspase9(载体1)和串联CD20-CD19 CAR+阻断的Thy1.1亮氨酸拉链分选自杀构建体(载体2)的两个逆转录病毒载体转导T细胞。在对经两种载体转导的细胞进行单步同时MACS分选纯度>90%后,测试T细胞的自杀基因活性。图11A显示将分选的或模拟转导的T细胞与抗Thy1.1和10%的兔补体一起孵育40分钟。对照细胞仅与培养基一起孵育。图11B显示分选的或模拟转导的T细胞在100nM均二聚体AP20187或培养基中孵育24小时。在图A和图B中,将相对存活率计算为处理细胞与对照细胞中的存活细胞的百分比。通过流式细胞仪使用CountBright珠和DAPI对存活的T细胞进行定量。
图12A-12C描绘了与接头-阻断的亮氨酸拉链融合的截短EGFR间隔区(EGFRt)促进细胞分选和抗体依赖性细胞介导的细胞毒性(ADCC)。图12A显示用FLAG-RR12EE345L 2AiCaspase9和RR12EE345L/EE12RR345L-EGFRt BFP载体共转导的BM185细胞系和用抗FLAG微珠的MACS分选。图12B显示分选的BM185 FLAG-RR iC9|RR/EE-EGFRt或对照BM185(共表达萤火虫荧光素酶)在培养基中或在10nM AP20187二聚体中孵育过夜以激活iCaspase9。图12C:分选的BM185 FLAG-RR iC9|RR/EE-EGFRt或对照BM185细胞与各种比例的效应子NK细胞系NK92-MI+/-10μg/mL西妥昔单抗孵育过夜。在图12B和12C中,通过评估与未处理的细胞相比的残余荧光素酶活性来确定24小时后的相对存活率。
图13描绘了带细胞因子标签的拉链-“拉链因子”,其被工程化以促进细胞因子的分泌和反式呈递,同时保留亲和标签分泌型亮氨酸拉链的分选功能。可以将细胞因子(例如IL-7、IL-15和IL-21)融合到亲和标签和异二聚体亮氨酸拉链上。可以分泌拉链因子与T细胞上的细胞因子受体相互作用,或与内在阻断的跨膜亮氨酸拉链共表达,以促进双载体共转导细胞的分选和细胞因子的反式呈递。
图14A-14C描绘了拉链因子保留亮氨酸拉链分选系统的功能分选特征并促进T细胞增殖。图14A显示用编码(细胞因子-RR12EE345L-FLAG 2A BFP)和固有阻断的跨膜亮氨酸拉链(EE12RR345L-Myc-CD28EC-9C CD28TM CD3zδ2A Thy1.1)的逆转录病毒载体共转导的C1498细胞系。检测到IL-7、IL-15和IL-21拉链因子在细胞表面呈反式呈递(FLAG染色),并用抗FLAG微珠对细胞进行分选以获得高度纯化的共转导细胞。图14B显示用IL-15-RR12EE345L-FLAG 2A BFP和EE12RR345L-Myc-CD28EC-9C CD28TM CD3zδ2A Thy1.1转导并用抗FLAG珠分选的原代T细胞。FLAG染色(上)和BFP(下)证实载体1表达,而Thy1.1证明载体2表达。图14C显示原代T细胞与辐照的脾细胞、0.5ug/mL抗CD3和辐照的分选的反式呈递IL-7、IL-15和IL-21拉链因子的C1498细胞孵育或与仅转导跨膜亮氨酸拉链的对照C1498细胞一起孵育。72小时后通过流式细胞仪对T细胞计数。
图15示出了根据本公开主题的某些实施方式的分选系统。
图16描绘了通过使用IgGl铰链CD28TM CD3zΔ和CD28-9C CD28TM CD3zΔ捕获亮氨酸拉链进行的有效的CD34和CD20染色。
图17描绘了在通过抗CD34磁珠分选的细胞中圆形CD20模拟表位的均匀表面展示。
图18描绘了使用抗CD20抗体选择性耗竭双重转导的细胞。
图19描绘了通过分开的CD20和CD34结合结构域实现的选择性磁性分选和抗体介导的耗竭。
图20描绘了突变体阻断亮氨酸拉链对分泌的亮氨酸拉链的捕获和呈递的影响。
图21A和21B描绘了功能化以呈递阻断的捕获亮氨酸拉链的CD80(B7-1)分子,允许用FLAG-RR12EE345L亮氨酸拉链进行磁性分选。图21A描绘分选的细胞对CD19和CD20 CAR(分别为Myc,Streptag)和CD80功能化的亮氨酸拉链显示出高纯度。图21B显示表达RR12EE345L接头EE12RR345L CD80的T细胞在培养物中形成缀合物并结合至可溶性CD28-Fc。
具体实施方式
本公开的主题提供膜结合多肽,其包含跨膜结构域和细胞外结构域,该细胞外结构域包含第一二聚化结构域和能够在细胞表面与第一二聚化结构域二聚化的第二二聚化结构域,其中第一和第二二聚化结构域各自包含亮氨酸拉链。本文公开的膜结合多肽可用于分选包含此类膜结合多肽的细胞。此外,本公开的主题提供用于分离表达特定构建体例如本文公开的膜结合多肽的细胞的系统。在某些实施方式中,该系统包含膜结合多肽和可溶性多肽,其中该可溶性多肽能够与该膜结合多肽二聚化。在某些实施方式中,当可溶性多肽和膜结合多肽从不同细胞表达时,两者不能形成二聚体,这使得能够对表达特定构建体组合的细胞进行分选。
1.定义
除非另有定义,否则本文中使用的所有技术和科学术语具有本发明所属领域的技术人员通常理解的含义。以下参考文献为技术人员提供对于本发明中使用的许多术语的一般定义:Singleton等人,《微生物学和分子生物学词典》(Dictionary of Microbiologyand Molecular Biology)(1994年第2版);剑桥科学技术词典(The Cambridge Dictionaryof Science and Technology)(Walker编辑,1988);遗传学词汇(The Glossary ofGenetics),第5版,R.Rieger等(编辑),Springer Verlag(1991);和Hale&Marham,《哈珀·柯林斯生物学词典》(The Harper Collins Dictionary of Biology)(1991年)。除非另有说明,否则如本文所用的以下术语具有以下赋予它们的含义。
如本文所用,术语“约”或“近似”是指在特定值的可接受误差范围内,如本领域普通技术人员所确定的,其将部分取决于如何测量或确定该值,即,测量系统的局限性。例如,根据本领域的实践,“约”可以表示在3个或超过3个的标准偏差之内。或者,“约”可以表示给定值的至多约20%,优选至多约10%,更优选至多约5%,更优选至多约1%的范围。或者,尤其是关于生物系统或方法,该术语可以意指在数值的一个数量级内,例如在一个值的约5倍之内,更优选在约2倍之内。
如本文所用,术语“抗体”不仅是指完整的抗体分子,而且还指保留免疫原结合能力的抗体分子片段。这样的片段在本领域中也是众所周知的,并且在体外和体内均经常使用。因此,如本文所用,术语“抗体”不仅是指完整的免疫球蛋白分子,而且还指众所周知的活性片段F(ab')
如本文所用,术语“单链可变片段”或“scFv”是共价连接以形成V
如本文所用,“接头”是指共价连接两个或更多个多肽或核酸以使它们彼此连接的官能团(例如,化学的或多肽)。在某些实施方式中,接头包含用于将两个蛋白质偶联在一起(例如,偶联V
如本文所用,术语“载体”是指当与适当的控制元件关联时能够复制并且可以将基因序列转移到细胞中的任何遗传元件,例如质粒、噬菌体、转座子、粘粒、染色体、病毒、病毒粒子等。因此,该术语包括克隆和表达载体,以及病毒载体和质粒载体。
如本文所用,术语“表达载体”是指重组核酸序列,例如重组DNA分子,其包含与对于编码序列在特定的宿主机体内表达所必需的适当核酸序列可操作地连接的所需编码序列。在原核生物中表达所必需的核酸序列通常包括启动子,操纵子(可选)和核糖体结合位点,通常与其他序列一起。在真核细胞中表达所必需的核酸序列可以包括但不限于启动子、增强子以及终止和聚腺苷酸化信号。
在某些实施方式中,可用于本公开的主题的核酸分子包括编码抗体或其抗原结合片段的核酸分子。这样的核酸分子不需要与内源核酸序列100%相同,但是通常将显示出基本同一性。与内源序列具有“基本同源性”或“基本同一性”的多核苷酸通常能够与双链核酸分子的至少一条链杂交。
如本文所用,术语“疾病”是指损害或干扰细胞、组织或器官的正常功能的任何状况或病症。疾病的实例包括瘤形成或细胞、组织或器官的病原体感染。
“有效量”(或“治疗有效量”)是足以在治疗后产生有益或期望的临床结果的量。可以以一剂或多剂剂量将有效量施用于受试者。就治疗而言,有效量是足以减轻、改善、稳定、逆转或减缓疾病(例如瘤形成)的进展、或减轻疾病(例如瘤形成)的病理后果的量。包含有效量的剂量通常由医生根据具体情况确定,并且这种确定在本领域普通技术人员的能力范围内。当确定合适的剂量以达到有效量时,通常要考虑几个因素。这些因素包括受试者的年龄、性别和体重,所治疗的病症,病症的严重程度以及所施用的细胞(例如工程免疫细胞)的形式和有效浓度。
如本文所用,术语“肿瘤(neoplasm)”是指以细胞或组织的病理性增生及其随后向其它组织或器官的迁移或侵袭为特征的疾病。瘤形成的生长通常是不受控制的和进行性的,并且在不会引起正常细胞增殖或者导致正常细胞增殖停止的条件下发生。瘤形成可影响多种细胞类型、组织或器官,包括但不限于选自以下的器官:皮肤、膀胱、结肠、骨骼、大脑、乳房、软骨、神经胶质、食道、输卵管、胆囊、心脏、肠、肾脏、肝脏、肺、淋巴结、神经组织、卵巢、胸膜、胰腺、前列腺、骨骼肌、脊髓、脾脏、胃、睾丸、胸腺、甲状腺、气管、泌尿生殖道、输尿管、尿道、子宫和阴道、或其组织或细胞类型。瘤形成包括癌症,例如黑素瘤、肉瘤、癌(carcinomas)或浆细胞瘤(浆细胞的恶性肿瘤)。
如本文所用,术语“免疫应答细胞”是指在免疫应答中起作用的细胞,并且包括该细胞的祖细胞和该细胞的后代。
如本文所用,术语“分离的细胞”是指与天然伴随细胞的分子和/或细胞组分相分离的细胞。
如本文所用,术语“分离的”、“纯化的”或“生物学上纯的”是指物质在不同程度上不含在其天然状态下通常与其伴随的组分。“分离”表示与原始来源或环境隔离的程度。“纯化”表示高于分离的隔离度。“纯化的”或“生物纯的”蛋白质充分不含其它物质,以使任何杂质均不会实质性地影响蛋白质的生物学特性或引起其它不利后果。也就是说,如果本公开主题的核酸或肽通过重组DNA技术生产而基本不含细胞材料、病毒材料或培养基,或者通过化学合成而基本不含化学前体或其它化学品,则其是纯化的。纯度和均质性通常使用分析化学技术确定,例如聚丙烯酰胺凝胶电泳或高效液相色谱法。术语“纯化的”可以表示核酸或蛋白质在电泳凝胶中产生基本上一个条带。对于可以进行修饰(例如磷酸化或糖基化)的蛋白质,不同的修饰可以产生不同的分离的蛋白质,可以将其分别纯化。
如本文所用,术语“分泌的”是指多肽通过内质网、高尔基体、以及作为在细胞质膜上瞬时融合从而将蛋白质释放到细胞外的囊泡通过分泌通路而从细胞释放。
如本文所用,术语“治疗(treating)”或“治疗(treatment)”是指试图改变所治疗的个体或细胞的疾病进程的临床干预,并且可以用于预防或在临床病理过程中进行。治疗的治疗作用包括但不限于预防疾病的发生或复发、减轻症状、减少疾病的任何直接或间接病理后果、预防转移、降低疾病进展的速度、改善或减轻疾病状态、以及缓解或改善预后。通过预防疾病或病症的进展,治疗不仅可以预防在受影响或被诊断的受试者或怀疑患有该病症的受试者中由于病症引起的恶化,而且治疗可以在有病症风险或怀疑患有该病症的受试者中预防该病症的发作或该病症的症状。
如本文所用,术语“受试者”指任何动物(例如哺乳动物),包括但不限于人类、非人灵长类动物、啮齿动物等(例如,将成为特定治疗的接受者)。
如本文所用,术语“嵌合抗原受体”或“CAR”是指包含与能够激活或刺激免疫应答细胞的细胞内信号传导结构域融合的细胞外抗原结合结构域和跨膜结构域的分子。在某些实施方式中,CAR的细胞外抗原结合结构域包含scFv。scFv可以源自将抗体的可变重区和轻区融合。替代地或另外,scFv可以源自Fab’s(而不是抗体,例如获自Fab文库)。在某些实施方式中,将scFv融合至跨膜结构域,然后融合至细胞内信号传导结构域。在某些实施方式中,CAR对抗原具有高结合亲和力或亲合力。
在某些非限制性实施方式中,CAR或ZipR-CAR的细胞内信号传导结构域包含CD3ζ多肽,其可以激活或刺激细胞(例如,淋巴谱系的细胞,例如T细胞)。CD3ζ包含三个免疫受体酪氨酸激活基序(ITAM),并在抗原结合后将激活信号传递至细胞(例如,淋巴谱系的细胞,例如T细胞)。CD3ζ链的细胞内信号传导结构域是来自内源性TCR的信号的主要传递者。
在某些非限制性实施方式中,CAR或ZipR-CAR还可以包含将细胞外抗原结合结构域与跨膜结构域连接的间隔区/铰链区。间隔区可以有足够柔性,以允许抗原结合结构域在不同方向上定向以促进抗原识别。间隔区可以是来自IgG1的铰链区,或者是免疫球蛋白的CH
如本文所用,“共刺激分子”是指淋巴细胞对抗原的应答所需的除抗原受体或其配体以外的细胞表面分子。至少一个共刺激信号传导区可包括CD28多肽(例如CD28的细胞内结构域或其片段)、4-1BB多肽(例如4-1BB的细胞内结构域或其片段)、OX40多肽(例如OX40的细胞内结构域或其片段)、ICOS多肽(例如ICOS的细胞内结构域或其片段)、DAP-10多肽(例如DAP-10的细胞内结构域或其片段)、或其组合。共刺激分子可以结合共刺激配体。如本文所用,术语“共刺激配体”是指在细胞表面表达的蛋白质,其与其受体结合后会产生共刺激反应,即影响激活信号传导结构域(例如CD3ζ信号传导结构域)提供的刺激的细胞内反应。共刺激配体的非限制性实例包括肿瘤坏死因子(TNF)家族成员、免疫球蛋白(Ig)超家族成员或其组合。共刺激配体选自肿瘤坏死因子(TNF)家族成员、免疫球蛋白(Ig)超家族成员及其组合。TNF家族成员的非限制性实例包括4-1BBL、OX40L、CD70、GITRL、CD40L和CD30L。Ig超家族成员的非限制性实例包括CD80、CD86和ICOSLG。例如,4-1BBL可以结合4-1BB以提供细胞内信号,该细胞内信号与CAR信号一起诱导CAR
如本文所用,术语“多聚化”是指多聚体(包括二聚体)的形成。多聚化包括二聚化。
如本文所用,术语“保守序列修饰”是指不显著影响或改变本公开的包含氨基酸序列的多肽(例如,多肽的细胞外抗原结合结构域)的结合特征的氨基酸修饰。保守修饰可包括氨基酸取代、添加和缺失。可以通过本领域已知的标准技术(例如定点诱变和PCR介导的诱变)将修饰引入本公开的多肽的人scFv中。氨基酸可根据其物理化学性质(例如电荷和极性)分为几组。保守氨基酸取代是其中氨基酸残基被相同组内的氨基酸取代的氨基酸取代。例如,氨基酸可以按电荷分类:带正电荷的氨基酸包括赖氨酸、精氨酸、组氨酸,带负电荷的氨基酸包括天冬氨酸、谷氨酸,中性电荷氨基酸包括丙氨酸、天冬酰胺、半胱氨酸、谷氨酰胺、甘氨酸、异亮氨酸、亮氨酸、蛋氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸和缬氨酸。另外,氨基酸可以按极性分类:极性氨基酸包括精氨酸(碱性极性)、天冬酰胺、天冬氨酸(酸性极性)、谷氨酸(酸性极性)、谷氨酰胺、组氨酸(碱性极性)、赖氨酸(碱性极性)、丝氨酸、苏氨酸和酪氨酸;非极性氨基酸包括丙氨酸、半胱氨酸、甘氨酸、异亮氨酸、亮氨酸、蛋氨酸、苯丙氨酸、脯氨酸、色氨酸和缬氨酸。因此,CDR区内的一个或多个氨基酸残基可以被来自相同组的其它氨基酸残基取代,并且可以使用本文所述的功能测定法测试改变的抗体的保留功能(即,上述(c)至(l)中列出的功能)。在某些实施方式中,在指定序列或CDR区内不超过一个、不超过两个、不超过三个、不超过四个、不超过五个残基被改变。
如本文所用,两个氨基酸序列之间的同源性百分比等同于两个序列之间的同一性百分比。两个序列之间的同一性百分比是该序列共享的相同位置数的函数(即,%同源性=相同位置数#/位置总数#×100),其中考虑了空位数和每个空位的长度,需要引入这些空位以实现两个序列的最佳比对。序列的比较和两个序列之间同一性百分比的确定可以使用数学算法来完成。
可以使用E.Meyers和W.Miller(Comput.Appl.Biosci.,4:11-17(1988))的算法确定两个氨基酸序列之间的同源性百分比,该算法已合并到ALIGN程序(2.0版)中,使用PAM120权重残基表,空位长度罚分为12,空位罚分为4。此外,两个氨基酸序列之间的同源性百分比可以使用Needleman和Wunsch(J.Mol.Biol.48:444-453(1970))算法来确定,该算法已被整合到GCG软件包(可从www.gcg.com获得)中的GAP程序中,使用Blossum 62矩阵或PAM250矩阵,并且空位权重为16、14、12、10、8、6或4,长度权重为1、2、3、4、5或6。
另外或可替代地,本公开的主题的氨基酸序列可以进一步用作“查询序列”以对公共数据库进行搜索以例如识别相关序列。可以使用Altschul等((1990)J.Mol.Biol.215:403-10)的XBLAST程序(2.0版)执行此类搜索。可以使用XBLAST程序进行BLAST蛋白质搜索,得分=50,字长=3,以获得与本文公开的指定序列(例如,scFv m903、m904、m905、m906和m900的重链和轻链可变区序列)同源的氨基酸序列。为了获得用于比较目的的空位比对,可以如Altschul等,(1997)Nucleic Acids Res.25(17):3389-3402中所述使用GappedBLAST。当使用BLAST和Gapped BLAST程序时,可以使用各个程序(例如XBLAST和NBLAST)的默认参数。
2.膜结合多肽和可溶性多肽
本公开的主题提供包含膜结合多肽和可溶性多肽的系统,其中所述可溶性多肽能够与所述膜结合多肽二聚化。
在某些实施方式中,膜结合多肽包含跨膜结构域和细胞外结构域。在某些实施方式中,膜结合多肽还包含细胞内结构域。
2.1.1细胞外结构域
在某些实施方式中,膜结合多肽的细胞外结构域包含含有亮氨酸拉链结构域的二聚化结构域。在某些实施方式中,二聚化结构域能够与包含在膜结合多肽中的一个或多个二聚化结构域二聚。在某些实施方式中,二聚化结构域能够与本文公开的可溶性多肽内的一个或多个二聚化结构域二聚。
在某些实施方式中,膜结合多肽的细胞外结构域包含第一二聚化结构域和能够与第一二聚化结构域在细胞表面二聚的第二二聚化结构域。在某些实施方式中,第一二聚化结构域和第二二聚化结构域各自包含亮氨酸拉链结构域。在某些实施方式中,第一二聚化结构域包含第一亮氨酸拉链结构域。在某些实施方式中,第二二聚化结构域包含第二亮氨酸拉链结构域。
在某些实施方式中,亮氨酸拉链结构域包含真核转录因子的碱性区亮氨酸拉链(bZIP)类的二聚化结构域。在某些实施方式中,亮氨酸拉链结构域包含可以与另一α螺旋单体二聚化的特定α螺旋单体。在某些实施方式中,亮氨酸拉链结构域包含EE结构域,该EE结构域包含一个或多个酸性氨基酸,例如谷氨酸(E)。在某些实施方式中,亮氨酸拉链结构域包含RR结构域,其包含一个或多个碱性氨基酸,例如精氨酸(R)。在某些实施方式中,第一亮氨酸拉链结构域包含RR结构域,而第二亮氨酸拉链结构域包含EE结构域。
在某些实施方式中,RR结构域包含与如SEQ ID NO:1所示的氨基酸序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列。在某些实施方式中,RR结构域包含SEQ ID NO:1或其片段的修饰。在某些实施方式中,修饰包含最多一个、最多两个或最多三个氨基酸取代。SEQ ID NO:1在下面提供。
LEIRAAFLRQRNTALRTEVAELEQEVQRLENEVSQYETRYGPL GGGK [SEQ ID NO:1]
编码SEQ ID NO:1的氨基酸序列的示例性核苷酸序列如SEQ ID NO:97所示,其在下面提供。
在某些实施方式中,RR结构域包含SEQ ID NO:1的修饰,其中该修饰由一个氨基酸取代组成或具有一个氨基酸取代。在某些实施方式中,RR结构域包含如SEQ ID NO:98或SEQID NO:99所示的氨基酸序列。SEQ ID NO:98和SEQ ID NO:99在下面提供。
编码SEQ ID NO:98的氨基酸序列的示例性核苷酸序列如SEQ ID NO:100所示,其在下面提供。
编码SEQ ID NO:99的氨基酸序列的示例性核苷酸序列如SEQ ID NO:101所示,其在下面提供。
在某些实施方式中,RR结构域包含SEQ ID NO:1的修饰,其中该修饰由两个氨基酸取代组成或具有两个氨基酸取代。在某些实施方式中,RR结构域包含如SEQ ID NO:102或SEQ ID NO:103所示的氨基酸序列。SEQ ID NO:102和SEQ ID NO:103在下面提供。
编码SEQ ID NO:102的氨基酸序列的示例性核苷酸序列如SEQ ID NO:104所示,其在下面提供。
编码SEQ ID NO:103的氨基酸序列的示例性核苷酸序列如SEQ ID NO:105所示,其在下面提供。
在某些实施方式中,RR结构域包含SEQ ID NO:1的修饰,其中该修饰由三个氨基酸取代组成或具有三个氨基酸取代。在某些实施方式中,RR结构域包含如SEQ ID NO:106或SEQ ID NO:107所示的氨基酸序列。SEQ ID NO:106和SEQ ID NO:107在下面提供。
编码SEQ ID NO:106的氨基酸序列的示例性核苷酸序列如SEQ ID NO:108所示,其在下面提供。
编码SEQ ID NO:107的氨基酸序列的示例性核苷酸序列如SEQ ID NO:109所示,其在下面提供。
在某些实施方式中,修饰位于亮氨酸拉链的RR结构域的“g”残基。在某些实施方式中,修饰降低了膜结合多肽和连接的可溶性多肽之间的异二聚化亲和力。
在某些实施方式中,EE结构域包含与SEQ ID NO:2所示的氨基酸序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列。在某些实施方式中,EE结构域包含SEQ ID NO:2或其片段的修饰。在某些实施方式中,修饰包含最多一个、最多两个或最多三个氨基酸取代。SEQ ID NO:2在下面提供。LEIEAAFLERENTALETRVAELRQRVQRLRNRVSQYRTRYGPL GGGK[SEQ ID NO:2]
编码SEQ ID NO:2的氨基酸序列的示例性核苷酸序列如SEQ ID NO:110所示,其在下面提供。
在某些实施方式中,细胞外结构域还包含在第一二聚化结构域和第二二聚化结构域之间的接头。在某些实施方式中,接头包含如SEQ ID NO:3或SEQ ID NO:20所示的氨基酸序列。SEQ ID NO:3和SEQ ID NO:20在下面提供。
在某些实施方式中,二聚化结构域包含正交拉链。正交拉链是卷曲的螺旋结构域,仅与它们的特定配偶体形成异二聚体,而不与其他拉链结构域形成异二聚体。在某些实施方式中,正交性是指与其他分子组非交叉反应(即“正交”)的分子组(例如,亮氨酸拉链)。例如,A+B=AB,C+D=CD,但A和B均不与C或D结合,反之亦然。
在某些实施方式中,膜结合多肽的第一和第二亮氨酸拉链结构域是一对正交拉链,即,第一和第二亮氨酸拉链结构域是彼此形成异二聚体的特定配偶体。正交拉链包括但不限于RR/EE拉链、Fos/Jun拉链和Fos/synZip拉链。Fos/Jun拉链先前已公开于Ransone等人,Genes Dev.1989Jun;3(6):770-81;Kohler等人,Biochemistry.(2001Jan);9;40(1):130-42,其通过引用并入本文。Fos/synZip拉链先前已公开于Grigoryan等人,Nature.(2009);458,859-864;Reinke等人,JAm Chem Soc.(2010);132,6025-6031,其通过引用并入本文。
在某些实施方式中,正交拉链包含与RR/EE拉链、Fos/Jun拉链或Fos/synZip拉链或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可包含最多一个、最多两个或最多三个氨基酸取代。
synZip-9、Fos和Jun拉链的实例分别如SEQ ID NO:4、5和6所示。
在某些实施方式中,膜结合多肽的细胞外结构域还包含二聚化结构域和跨膜结构域之间的间隔区/铰链结构域。
在某些实施方式中,间隔区/铰链结构域可以具有足够柔韧性以允许二聚化结构域在不同方向上定向以促进在与本文公开的可溶性多肽二聚化之后的抗原识别。间隔区可以是来自IgG1的铰链区,或者是免疫球蛋白的CH
在某些实施方式中,间隔区/铰链结构域包含抗体识别的表位。在某些实施方式中,抗体与表位的结合介导包含膜结合多肽的细胞的耗竭。在某些实施方式中,间隔区/铰链结构域包含Thy1.1分子、截短的EGFR分子(EGFRt)、CD22免疫球蛋白样结构域表位、IgG/Fc结构域(可以是来自任何IgG的Fc)、CD2、CD20环状模拟表位、CD30、CD52或HER2。
在某些实施方式中,膜结合多肽还包含阻断间隔区,其中当膜结合多肽和可溶性多肽不是从同一细胞表达时,阻断间隔区能够阻止膜结合多肽与可溶性多肽的二聚化。在某些实施方式中,阻断间隔区包含不超过约20至约30个氨基酸残基的最小间隔区。在某些实施方式中,阻断间隔区包含不超过约25个氨基酸残基。在某些实施方式中,阻断间隔区包含约1、约2、约3、约4、约5、约6、约7、约8、约9、约10、约11、约12、约13、约14、约15、约16、约17、约18、约19或约20个氨基酸残基。在某些实施方式中,阻断间隔区包含约5个氨基酸残基至约25个氨基酸残基,约5个氨基酸残基至约20个氨基酸残基,约10个氨基酸残基至约25个氨基酸残基,或约10个氨基酸残基至约20个氨基酸残基。
在某些实施方式中,阻断间隔区包含与SEQ ID NO:7或SEQ ID NO:21所示的截短的CD28间隔区或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列。在某些实施方式中,阻断间隔区包含与SEQ ID NO:8或22所示的IgG1铰链或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性的氨基酸序列。在某些实施方式中,阻断间隔区包含SEQ IDNO:7、SEQ ID NO:8、SEQ ID NO:21、SEQ ID NO:22的修饰,其中所述修饰为最多一个、最多两个或最多三个氨基酸取代。
在某些实施方式中,阻断间隔区的长度不超过约25个氨基酸。在某些实施方式中,阻断间隔区的长度为约5个氨基酸至约25个氨基酸。在某些实施方式中,阻断间隔区是截短的CD28间隔区或IgG1铰链。
在某些非限制性实施方式中,膜结合多肽的细胞外结构域包含至少一种共刺激配体或其片段。
在某些实施方式中,共刺激配体选自肿瘤坏死因子(TNF)家族成员、免疫球蛋白(Ig)超家族成员及其组合。在某些实施方式中,共刺激性配体选自肿瘤坏死因子(TNF)家族成员、免疫球蛋白(Ig)超家族成员及其组合。在某些实施方式中,TNF家族成员选自4-1BBL、OX40L、CD70、GITRL、CD40L和CD30L。
在某些实施方式中,Ig超家族成员选自CD80、CD86和ICOSLG。
在某些实施方式中,共刺激配体是CD80。在某些实施方式中,CD80是小鼠CD80。在某些实施方式中,CD80包含如SEQ ID NO:111所示的氨基酸序列。在某些实施方式中,CD80是人CD80。在某些实施方式中,CD80包含如SEQ ID NO:112所示的氨基酸序列。SEQ ID NO:111和SEQ ID NO:112在下面提供。
在某些实施方式中,共刺激配体是4-1BBL。在某些实施方式中,4-1BBL是小鼠4-1BBL。在某些实施方式中,4-1BBL包含如SEQ ID NO:113所示的氨基酸序列。在某些实施方式中,4-1BBL是人4-1BBL。在某些实施方式中,4-1BBL包含如SEQ ID NO:114所示的氨基酸序列。SEQ ID NO:113和114在下面提供。
在某些非限制性实施方式中,膜结合多肽的细胞外结构域还包含显性负分子或其片段。在某些实施方式中,显性负分子选自免疫检查点分子的抑制剂、肿瘤坏死因子受体超家族(TNFRSF)成员和TGFβ受体。在某些实施方式中,免疫检查点分子选自PD-1、CTLA-4、B7-H3、B7-H4、BTLA、TIM-3、LAG-3、TIGIT、LAIR1、CD200、CD200R、HVEM、2B4、CD160、半乳凝素9及其组合。在某些实施方式中,免疫检查点分子是PD-1。在某些实施方式中,TNFRSF成员选自Fas、肿瘤坏死因子受体、OX40、CD40、CD27、CD30、4-1BB及其组合。在某些实施方式中,显性负受体包含TGFβRII的细胞外结构域或其片段。
在某些非限制性实施方式中,显性负分子是免疫检查点分子的抑制剂。免疫检查点分子的抑制剂的显性负(DN)型的细节在WO2017/040945和WO2017/100428中公开,其各自的内容整体并入本文以作参考。在某些实施方式中,膜结合多肽的细胞外结构域还包含WO2017/040945中公开的免疫检查点抑制剂的显性负型。在某些实施方式中,膜结合多肽的细胞外结构域还包含WO2017/100428中公开的免疫检查点抑制剂的显性负型。
在某些实施方式中,显性负分子是PD-1显性负(即,PD-1DN)分子。在某些实施方式中,PD-1DN包含(a)包含配体结合区的PD-1的细胞外结构域的至少一个片段和(b)跨膜结构域。
在某些实施方式中,PD-1DN是小鼠PD-1DN。在某些实施方式中,PD-1DN包含或具有如SEQ ID NO:115所示的氨基酸序列,其在下面提供。在某些实施方式中,PD-1DN是人PD-1DN。
在某些实施方式中,膜结合多肽的细胞外结构域还包含标签。在某些实施方式中,标签包含被第一抗体识别的表位标签。表位标签的非限制性实例包括Myc标签、HA标签、Flag标签、V5标签、T7标签和CD34标签。在某些实施方式中,表位标签是CD34标签。
在某些实施方式中,标签包含与底物结合的亲和标签。亲和标签的非限制性实例包括His标签、Strep标签、E标签和链霉亲和素结合蛋白标签(SBP标签)。
此外,膜结合多肽的细胞外结构域可还包含被第二抗体识别的模拟表位。第二抗体与模拟表位的结合可介导包含膜结合多肽的细胞的耗竭。在某些实施方式中,模拟表位是被抗CD20抗体识别的CD20模拟表位。在某些实施方式中,抗CD20抗体是利妥昔单抗。
在某些实施方式中,膜结合多肽的细胞外结构域包含被第一抗体识别的表位标签和被第二抗体识别的模拟表位。在某些实施方式中,表位标签是CD34表位标签,第一抗体是抗CD34抗体,模拟表位是CD20模拟表位,第二抗体是抗CD20抗体。在某些实施方式中,抗CD34抗体是QBEND10。在某些实施方式中,抗CD20抗体是利妥昔单抗。在某些实施方式中,CD20模拟表位是环状CD20模拟表位。
在某些实施方式中,CD20模拟表位包含或具有如SEQ ID NO:116所示的氨基酸序列,其在下面提供。
CPYSNPSLC[SEQ ID NO:116]
在某些实施方式中,CD34表位标签包含或具有如SEQ ID NO:117所示的氨基酸序列,其在下面提供。
ELPTQGTFSNVSTNVS[SEQ ID NO:117]
在某些实施方式中,膜结合多肽的细胞外结构域包含两个CD34表位标签,例如,每个CD34表位标签包含或具有如SEQ ID NO:117所示的氨基酸序列。在某些实施方式中,两个CD34表位标签通过接头连接。在某些实施方式中,接头包含或具有如SEQ ID NO:118所示的氨基酸序列,其在下面提供。
GGGGSGGGS[SEQ ID NO:118]
在某些实施方式中,膜结合多肽的细胞外结构域包含如SEQ ID NO:119所示的氨基酸序列,其在下面提供。SEQ ID NO:119具有两个CD34表位标签,其通过具有如SEQ IDNO:118所示氨基酸序列的接头连接,SEQ ID NO:119称为“Q2”或“Q2序列”。
ELPTQGTFSNVSTNVSGGGGSGGGSELPTQGTFSNVSTNVS[SEQ ID NO]:119]
在某些实施方式中,膜结合多肽的细胞外结构域包含两个CD20模拟表位,例如每个CD20模拟表位包含或具有如SEQ ID NO:116所示的氨基酸序列。在某些实施方式中,两个CD20模拟表位通过接头连接。在某些实施方式中,接头包含或具有如SEQ ID NO:120所示的氨基酸序列,其在下面提供。
SGGGGSSGGGGSD[SEQ ID NO:120]
在某些实施方式中,膜结合多肽的细胞外结构域包含如SEQ ID NO:121所示的氨基酸序列,其在下面提供。SEQ ID NO:121具有两个CD20模拟表位,其通过具有如SEQ IDNO:120所示氨基酸序列的接头连接,SEQ ID NO:121称为“R2”或“R2序列”。
CPYSNPSLCSGGGGSSGGGGSDCPYSNPSLC[SEQ ID NO:121]
在某些实施方式中,膜结合多肽的细胞外结构域包含两个CD20模拟表位和一个CD34表位标签,例如,每个CD20模拟表位包含或具有如SEQ ID NO:116所示的氨基酸序列,且CD34表位标签包含或具有如SEQ ID NO:117所示的氨基酸序列。在某些实施方式中,CD34表位标签通过接头连接至每个CD20模拟表位。在某些实施方式中,接头是人CD8多肽,例如,包含或具有如SEQ ID NO:122所示氨基酸序列的人CD8多肽,其在下面提供。
PAKPTTT[SEQ ID NO:122]
在某些实施方式中,接头包含或具有如SEQ ID NO:123所示的氨基酸序列,其在下面提供。
SGGGGS[SEQ ID NO:123]
在某些实施方式中,膜结合多肽的细胞外结构域包含如SEQ ID NO:124所示的氨基酸序列,其在下面提供。SEQ ID NO:124具有两个CD20模拟表位和一个CD34表位标签,其中,CD34表位标签通过具有如SEQ ID NO:122所示氨基酸序列的接头与一个CD20模拟表位连接,并通过具有如SEQ ID NO:123所示氨基酸序列的接头与另一个CD20模拟表位连接,SEQ ID NO:124称为“RQR”或“RQR序列”。
CPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLC[SEQ ID NO:124]
2.1.2跨膜结构域
不同的跨膜结构域可导致不同的受体稳定性。根据本公开的主题,跨膜结构域可包含:CD8多肽(例如CD8的跨膜结构域或其片段)、CD28多肽(例如CD28的跨膜结构域或其片段)、CD3ζ多肽(例如CD3ζ的跨膜结构域或其片段)、CD4多肽(例如CD4的跨膜结构域或其片段)、4-1BB多肽(例如4-1BB的跨膜结构域或其片段)、OX40多肽(例如OX40的跨膜结构域或其片段)、ICOS多肽(例如ICOS的跨膜结构域或其片段)、CD2多肽(例如CD2的跨膜结构域或其片段)、合成肽(不基于与免疫反应相关的蛋白质)、或其组合。
在某些实施方式中,膜结合多肽的跨膜结构域包含CD8多肽(例如CD8的跨膜结构域或其片段)。在某些实施方式中,CD8多肽包含或具有与NCBI参考编号为NP_001139345.1(SEQ ID NO:9)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD8多肽包含或具有作为SEQ ID NO:9的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多235个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD8多肽包含或具有如下氨基酸序列,其为SEQ ID NO:9的氨基酸1至235、1至50、50至100、100至150、150至200、183至203、或200至235。在某些实施方式中,膜结合多肽的跨膜结构域包含CD8多肽,该CD8多肽包含或具有SEQ ID NO:9的氨基酸183至203的氨基酸序列。
SEQ ID NO:9在下面提供。
在某些实施方式中,CD8多肽包含或具有与NCBI参考编号为AAA92533.1(SEQ IDNO:10)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD8多肽包含或具有作为SEQ ID NO:10的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50、或至少60、或至少70、或至少100、或至少200且至多247个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD8多肽包含或具有SEQ ID NO:10的氨基酸1至247、1至50、50至100、100至150、150至200、或200至247的氨基酸序列。SEQ IDNO:10在下面提供。
在某些实施方式中,CD8多肽包含或具有如SEQ ID NO:11所示的氨基酸序列,其在下面提供:
IYIWAPLAGICVALLLSLIITLICY[SEQ ID NO:11]
在某些实施方式中,CD8多肽包含或具有如SEQ ID NO:12所示的氨基酸序列,其在下面提供:
IYIWAPLAGTCGVLLLSLVIT[SEQ ID NO:12]
在某些实施方式中,膜结合多肽的跨膜结构域包含CD28多肽(例如CD28的跨膜结构域或其片段)。CD28多肽可具有与NCBI参考编号为P10747或NP_006130(SEQ ID NO:14)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD28多肽包含或具有作为SEQ ID NO:14的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多220个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD28多肽包含或具有SEQ ID NO:14的氨基酸1至220、1至50、50至100、100至150、114至220、150至200、153至179、或200至220的氨基酸序列。在某些实施方式中,本文公开的膜结合多肽的跨膜结构域包含CD28多肽,该CD28多肽包含或具有SEQ ID NO:14的氨基酸153至179的氨基酸序列。SEQ ID NO:14在下面提供:
在某些实施方式中,膜结合多肽的跨膜结构域包含CD28多肽,该CD28多肽包含或具有如以下提供的SEQ ID NO:22所示的氨基酸序列。
FWVLVVVGGVLACYSLLVTVAFIIFWV[SEQ ID NO:22]
在某些实施方式中,膜结合多肽的跨膜结构域包含CD28多肽,该CD28多肽包含或具有如以下提供的SEQ ID NO:23所示的氨基酸序列。
FWALVVVAGVLFCYGLLVTVALCVIWT[SEQ ID NO:23]
在某些实施方式中,膜结合多肽的跨膜结构域包含CD4多肽(例如CD4的跨膜结构域或其片段)。CD4多肽可具有与NCBI参考编号为NP_038516.1(SEQ ID NO:125)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD4多肽包含或具有作为SEQ ID NO:125的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多457个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD4多肽包含或具有SEQ ID NO:125的氨基酸1至457、1至50、50至100、100至150、150至200、200至250、250至300、300至350、350至400、395至417、或400至457的氨基酸序列。在某些实施方式中,膜结合多肽的跨膜结构域包含CD4多肽,该CD4多肽包含或具有SEQ ID NO:125的氨基酸395至417。SEQ ID NO:125在下面提供:
在某些实施方式中,膜结合多肽的跨膜结构域包含CD4多肽(例如CD4的跨膜结构域或其片段)。CD4多肽可具有与NCBI参考编号为NP_000607.1(SEQ ID NO:126)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD4多肽包含或具有作为SEQ ID NO:126的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多458个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD4多肽包含或具有SEQ ID NO:126的氨基酸1至457、1至50、50至100、100至150、150至200、200至250、250至300、300至350、350至400、397至418或400至457的氨基酸序列。在某些实施方式中,膜结合多肽的跨膜结构域包含CD4多肽,该CD4多肽包含或具有SEQ ID NO:126的氨基酸397至418的氨基酸序列。SEQ ID NO:126在下面提供:
2.1.3细胞内结构域
在某些非限制性实施方式中,膜结合多肽还包含细胞内结构域。在某些非限制性实施方式中,细胞内结构域向细胞(例如淋巴谱系的细胞,例如T细胞)提供激活信号。在某些实施方式中,膜结合多肽的细胞内结构域包含免疫活化分子。在某些实施方式中,免疫活化分子是CD3ζ多肽。
在某些非限制性实施方式中,膜结合多肽的细胞内结构域包含CD3ζ多肽或其片段。CD3ζ多肽可以激活或刺激细胞。CD3ζ包含3个ITAM,并在抗原结合后将激活信号传递至细胞(例如,淋巴谱系的细胞,例如T细胞)。CD3ζ-链的细胞内信号传导结构域是来自内源性TCR的信号的主要传递者。在某些实施方式中,CD3ζ多肽包含或具有与NCBI参考编号为NP_932170(SEQ ID NO:15)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,CD3ζ多肽包含或具有作为SEQ ID NO:15的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多164个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD3ζ多肽包含或具有SEQ ID NO:15的氨基酸1至164、1至50、50至100、52至164、100至150、或150至164的氨基酸序列。在某些实施方式中,CD3ζ多肽包含或具有SEQ ID NO:15的氨基酸52至164的氨基酸序列。SEQ ID NO:15在下面提供:
在某些实施方式中,CD3ζ多肽包含或具有与NCBI参考编号为NP_001106864.2(SEQID NO:13)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,CD3ζ多肽包含或具有作为SEQ ID NO:13的连续片段的氨基酸序列,其长度为至少约20、或至少约30、或至少约40、或至少约50、或至少约90、或至少约100且至多188个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD3ζ多肽包含或具有SEQ ID NO:13的氨基酸1至164、1至50、50至100、52至142、100至150、或150至188的氨基酸序列。SEQ IDNO:13在下面提供:
在某些实施方式中,CD3ζ多肽包含或具有如SEQ ID NO:17所示的氨基酸序列,其在下面提供:
在某些实施方式中,膜结合多肽的细胞内结构域包含鼠CD3ζ多肽。
在某些实施方式中,膜结合多肽的细胞内结构域包含人CD3ζ多肽。
在某些非限制性实施方式中,膜结合多肽的细胞内结构域向细胞提供激活信号和刺激信号。在某些实施方式中,膜结合多肽的细胞内结构域包含至少一个共刺激分子或其片段。
在某些实施方式中,该至少一个共刺激信号传导区包含CD28多肽(例如CD28的细胞内结构域或其片段)、4-1BB多肽(例如4-1BB的细胞内结构域或其片段)、OX40多肽(例如OX40的细胞内结构域或其片段)、ICOS多肽(例如ICOS的细胞内结构域或其片段)、DAP-10多肽(例如DAP-10的细胞内结构域或其片段)、或其片段或组合。在某些实施方式中,该至少一个共刺激信号传导区包含CD28多肽。在某些实施方式中,该至少一个共刺激信号传导区包含CD28的细胞内结构域或其片段。
在某些实施方式中,共刺激分子是CD28多肽。CD28多肽可包含或具有与NCBI参考编号为P10747或NP_006130(SEQ ID NO:14)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD28多肽包含或具有作为SEQ ID NO:14的连续片段的氨基酸序列,其长度为至少20、或至少30、或至少40、或至少50且至多220个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD28多肽包含或具有SEQ ID NO:14的氨基酸1至220、1至50、50至100、100至150、150至200、或200至220的氨基酸序列。在某些实施方式中,CD28多肽包含或具有SEQ ID NO:14的氨基酸181至220的氨基酸序列。
在某些实施方式中,CD28多肽可包含或具有与NCBI参考编号为NP_031668.3(SEQID NO:16)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,CD28多肽包含或具有作为SEQ ID NO:16的连续片段的氨基酸序列,其长度为至少约20、或至少约30、或至少约40、或至少约50且至多218个氨基酸。可替代地或另外地,在非限制性的各种实施方式中,CD28多肽包含或具有SEQ ID NO:16的氨基酸1至218、1至50、50至100、100至150、150至200或200至218的氨基酸序列。SEQ ID NO:16在下面提供:
在某些实施方式中,共刺激分子是小鼠CD28多肽。在某些实施方式中,共刺激分子是人CD28多肽。
在某些实施方式中,膜结合多肽的细胞内结构域包含两个共刺激分子,例如,CD28和4-1BB或CD28和OX40。
在某些实施方式中,该至少一个共刺激信号传导区包含4-1BB多肽。在某些实施方式中,该至少一个共刺激信号传导区包含4-1BB的细胞内结构域或其片段。
在某些实施方式中,共刺激分子是4-1BB多肽(例如,4-1BB的细胞内结构域或其片段)。4-1BB可以充当肿瘤坏死因子(TNF)配体并具有刺激活性。4-1BB多肽可包含或具有与NCBI参考编号为P41273或NP_001552(SEQ ID NO:3)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。SEQ ID NO:3在下面提供:
根据本公开的主题,“4-1BB核酸分子”是指编码4-1BB多肽的多核苷酸。
在某些实施方式中,该至少一个共刺激信号传导区包含OX40多肽。在某些实施方式中,该至少一个共刺激信号传导区包含OX40的细胞内结构域或其片段。
在某些实施方式中,共刺激分子是OX40多肽(例如,OX40的细胞内结构域或其片段)。OX40多肽可包含或具有与NCBI参考编号为P43489或NP_003318(SEQ ID NO:18)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。SEQ ID NO:18在下面提供:
根据本公开的主题,“OX40核酸分子”是指编码OX40多肽的多核苷酸。
在某些实施方式中,该至少一个共刺激信号传导区包含ICOS多肽。在某些实施方式中,该至少一个共刺激信号传导区包含ICOS的细胞内结构域或其片段。
在某些实施方式中,共刺激分子是ICOS多肽。ICOS多肽可包含或具有与NCBI参考编号为NP_036224(SEQ ID NO:19)的序列或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。SEQ ID NO:19在下面提供:
根据本公开的主题,“ICOS核酸分子”是指编码ICOS多肽的多核苷酸。
在某些实施方式中,该至少一个共刺激信号传导区包含两个共刺激分子或其片段。在某些实施方式中,该至少一个共刺激信号传导区包含CD28多肽(例如,CD28的细胞内结构域或其片段)和4-1BB多肽(例如,4-1BB的细胞内结构域或其片段)。
在某些非限制性实施方式中,单独的膜结合多肽的细胞内结构域不向细胞提供激活信号。在某些实施方式中,膜结合多肽的细胞内结构域不包含共刺激分子。在某些实施方式中,膜结合多肽的细胞内结构域不包含CD3ζ多肽。
在某些实施方式中,膜结合多肽的细胞内结构域还包含自杀基因。合适的自杀基因包括但不限于单纯疱疹病毒胸苷激酶(hsv-tk)和诱导型半胱天冬酶9自杀基因(iCasp-9)。在某些实施方式中,膜结合多肽的细胞内结构域还包含截短的人表皮生长因子受体(EGFRt)多肽。截短的EGFRt多肽可通过施用抗EGFR单克隆抗体(例如西妥昔单抗)来消除T细胞。
在某些实施方式中,膜结合多肽包含synNotch模块。SynNotch模块公开在美国专利申请第9,670,281号和Morsut等人,Cell,164,780-791,2016中,其各自均整体并入本文以作参考。
本公开的用于分离包含至少两个表达载体的细胞的系统和方法包含由第一表达载体编码的膜结合多肽和由第二表达载体编码的可溶性多肽。在某些实施方式中,膜结合多肽是本文中例如在第2.1节中公开的膜结合多肽。
在某些实施方式中,可溶性多肽包含能够与包含在本文公开的膜结合多肽中的二聚化结构域二聚化的二聚化结构域。在某些实施方式中,二聚化结构域包含亮氨酸拉链结构域。二聚化结构域可以是2.1.1节中公开的任何二聚化结构域。
在某些实施方式中,可溶性多肽包含二聚化结构域和能够结合抗原的抗原结合结构域。
在某些实施方式中,可溶性多肽包含二聚化结构域和细胞因子或趋化因子。在某些实施方式中,可溶性多肽还包含标签。
在某些实施方式中,膜结合多肽的亮氨酸拉链结构域和可溶性多肽的亮氨酸拉链结构域是一对正交拉链,即它们是彼此形成异二聚体的特定配偶体。
2.2.1细胞因子/趋化因子
在某些实施方式中,可溶性多肽还包含细胞因子或趋化因子。在某些实施方式中,细胞因子/趋化因子能够增强免疫应答细胞的免疫应答和/或引起恶性或感染细胞的细胞死亡。在某些实施方式中,细胞因子/趋化因子是抗肿瘤细胞因子/趋化因子。在某些实施方式中,细胞因子或趋化因子包含或具有与天然细胞因子/趋化因子或其片段具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源性或同一性的氨基酸序列,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。细胞因子的非限制性实例包括IL-1、IL-2、IL-3、IL-7、IL-10、IL-12、IL-15、IL-17、IL-18、IL-21、IL-22、IL-36、粒细胞巨噬细胞集落刺激因子(GM-CSF)、IFN-γ、CXCL1、IL-23和CXCL10。趋化因子的非限制性实例包括CCL1、CCL8、CCL16、CCL17、CCL18、CCL22或其组合。
在某些实施方式中,趋化因子是CCL1。在某些实施方式中,CCL1是小鼠CCL1。在某些实施方式中,CCL1包含SEQ ID NO:127所示的氨基酸序列。在某些实施方式中,CCL1是人CCL1。在某些实施方式中,CCL1包含SEQ ID NO:128所示的氨基酸序列。SEQ ID NO:127和SEQ ID NO:128在下面提供。
在某些实施方式中,趋化因子是CCL17。在某些实施方式中,CCL17是小鼠CCL17。在某些实施方式中,CCL17包含SEQ ID NO:129所示的氨基酸序列。在某些实施方式中,CCL17是人CCL17。在某些实施方式中,CCL17包含SEQ ID NO:130所示的氨基酸序列。SEQ ID NO:129和SEQ ID NO:130在下面提供。
在某些实施方式中,趋化因子是CCL18。在某些实施方式中,CCL18是人CCL18。在某些实施方式中,CCL18包含SEQ ID NO:131所示的氨基酸序列。SEQ ID NO:131在下面提供。
在某些实施方式中,趋化因子是CCL22。在某些实施方式中,CCL22是小鼠CCL22。在某些实施方式中,CCL22趋化因子包含SEQ ID NO:132所示的氨基酸序列。在某些实施方式中,CCL22是人CCL22。在某些实施方式中,CCL22包含SEQ ID NO:133所示的氨基酸序列。SEQID NO:132和SEQ ID NO:133在下面提供。
2.2.2抗原结合结构域
在某些实施方式中,可溶性多肽的抗原结合结构域包含单链可变片段(scFv)、可溶性配体、细胞因子或基于非scFv的抗原识别基序,或其组合。
在某些非限制性实施方式中,可溶性多肽的抗原结合结构域(具体化为,例如scFv或其类似物)与抗原结合的解离常数(K
抗原结合结构域(例如,scFv或其类似物中)的结合可以通过例如酶联免疫吸附测定法(ELISA)、放射免疫测定法(RIA)、FACS分析、生物测定法(例如生长抑制)或Western印迹测定法来证实。这些测定法中的每一种通常通过采用对目标复合物具有特异性的标记试剂(例如抗体或scFv)来检测特定目标蛋白质-抗体复合物的存在。例如,scFv可以被放射性标记并用于放射免疫测定法(RIA)(参见,例如,Weintraub,B.,放射免疫测定原理,放射配体测定技术的第七培训课程,内分泌学会,1986年3月(Weintraub,B.,Principles ofRadioimmunoassays,Seventh Training Course on Radioligand Assay Techniques,TheEndocrine Society,March,1986),通过引用并入本文)。放射性同位素可通过诸如使用γ计数器或闪烁计数器的方法或通过放射自显影来检测。在某些实施方式中,细胞外抗原结合结构域用荧光标记物标记。荧光标记物的非限制性实例包括绿色荧光蛋白(GFP)、蓝色荧光蛋白(例如EBFP、EBFP2、Azurite和mKalama1)、青色荧光蛋白(例如ECFP、Cerulean和CyPet)和黄色荧光蛋白(例如,YFP、Citrine、Venus和YPet)。
在某些实施方式中,可溶性多肽的抗原结合结构域特异性结合抗原。在某些实施方式中,抗原结合结构域是scFv。在某些实施方式中,scFv是人scFv。在某些实施方式中,scFv是人源化的scFv。在某些实施方式中,scFv是鼠scFv。在某些实施方式中,抗原结合结构域是Fab,其任选地被交联。在某些实施方式中,抗原结合结构域是F(ab)
2.2.3抗原
在某些实施方式中,可溶性多肽的抗原结合结构域与肿瘤抗原结合。任何肿瘤抗原可以用于本文所述的肿瘤相关的实施方式中。抗原可以表达为肽或完整蛋白或其片段。完整蛋白或其片段可以是天然的或诱变的。肿瘤抗原的非限制性实例包括CD2、CD3、CD4、CD5、CD7、CD8、CD19、CD20、CD22、VpPreB、CD30、CD33、CD38、CD40、CD44v6、CD70、CD79a、CD70b、CLL-1/CLEC12A、CD123、IL-3R复合物、TIM-3、BCMA、CD244、E-钙粘蛋白、B7-H3、B7-H4、碳酸酐酶IX(CAlX)、癌胚抗原(CEA)、CD10、CD34、CD38、CD41、CD44、CD49f、CD56、CD74、CD133、CD138、CD44V6、巨细胞病毒(CMV)感染细胞的抗原(例如细胞表面抗原)、上皮糖蛋白2(EGP-2)、上皮糖蛋白40(EGP-40)、上皮细胞粘附分子(EpCAM)、受体酪氨酸蛋白激酶erb-B2,3,4(erb-B2,3,4)、叶酸结合蛋白(FBP)、胎儿乙酰胆碱受体(AChR)、叶酸受体α、神经节苷脂G2(GD2)、神经节苷脂G3(GD3)、人表皮生长因子受体2(HER-2)、人端粒酶逆转录酶(hTERT)、白介素13受体亚基α-2(IL-13Rα2)、κ轻链、激酶插入结构域受体(KDR)、Lewis Y(LeY)、Ll细胞粘附分子(L1CAM)、黑色素瘤抗原家族A,1(MAGE-A1)、粘蛋白16(MUC16)、粘蛋白1(MUC1)、间皮素(MSLN)、ERBB2、MAGEA3、p53、MART1、GP100、蛋白酶3(PR1)、酪氨酸酶、存活蛋白、hTERT、EphA2、NKG2D配体、癌-睾丸抗原NY-ESO-1、癌胚抗原(h5T4)、前列腺干细胞抗原(PSCA)、前列腺特异性膜抗原(PSMA)、ROR1、肿瘤相关糖蛋白72(TAG-72)、血管内皮生长因子R2(VEGF-R2)、Wilms肿瘤蛋白(WT-1)、NKCS1、EGF1R、EGFR-VIII、CD99、ADGRE2、CCR1、LILRB2、PRAME和ERBB。
在某些实施方式中,可溶性多肽的抗原结合结构域结合人CD19多肽。在某些实施方式中,可溶性多肽的抗原结合结构域与人CD19蛋白的细胞外结构域结合。
在某些实施方式中,可溶性多肽的抗原结合结构域与免疫检查点分子结合。免疫检查点分子的非限制性实例包括PD-L1、CD200、B7-H3、B7-H4、HVEM、半乳凝素9、PD-1、CTLA-4、CD200R、TIM-3、Lag-3和TIGIT。
在某些实施方式中,可溶性多肽的抗原结合结构域与活化受体结合,其中抗原结合结构域与活化受体的结合能够活化抗原呈递细胞(APC)。免疫检查点分子的非限制性实例包括CD40、Toll样受体(TLR)、FLT3、RANK和GM-CSF受体。
在某些实施方式中,可溶性多肽的抗原结合结构域与造血谱系细胞的生物标志物结合。免疫检查点分子的非限制性实例包括CD3、CD16、CD33、c-Kit、CD161、CD19、CD20、vPreB(preB细胞受体)、促黄体生成素受体(LHCGR)、CD123、IL-3R复合物、CLEC12A/CLL-1。
在某些实施方式中,可溶性多肽的抗原结合结构域与病原体抗原结合,例如用于治疗和/或预防病原体感染或其他感染性疾病,例如在免疫受损的受试者中。病原体的非限制性实例包括能够引起疾病的病毒、细菌、真菌、寄生虫和原生动物。
病毒的非限制性实例包括,逆转录病毒科(Retroviridae)(例如,人免疫缺陷病毒,例如HIV-1(也称为HDTV-III、LAVE或HTLV-III/LAV或HIV-III;以及其他分离株,例如HIV-LP);小RNA病毒科(Picornaviridae)(例如脊髓灰质炎病毒、甲型肝炎病毒;肠病毒、人柯萨奇病毒、鼻病毒、艾柯病毒);杯状病毒科(Calciviridae)(例如引起肠胃炎的菌株);披膜病毒科(Togaviridae)(例如马脑炎病毒、风疹病毒);黄病毒科(Flaviridae)(例如登革热病毒、脑炎病毒、黄热病毒);冠状病毒科(Coronoviridae)(例如冠状病毒);弹状病毒科(Rhabdoviridae)(例如水疱性口炎病毒、狂犬病病毒);丝状病毒科(Filoviridae)(例如埃博拉病毒);副粘病毒科(Paramyxoviridae)(例如副流感病毒、腮腺炎病毒、麻疹病毒、呼吸道合胞病毒);正粘病毒科(Orthomyxoviridae)(例如流感病毒);布尼亚病毒科(Bungaviridae)(例如汉坦病毒、bunga病毒、白蛉病毒和奈拉病毒);沙粒病毒科(Arenaviridae)(出血热病毒);呼肠孤病毒科(Reoviridae)(例如呼肠孤病毒、环状病毒(orbiviurses)和轮状病毒);双RNA病毒科(Birnaviridae);嗜肝DNA病毒科(Hepadnaviridae)(乙型肝炎病毒);细小病毒科(Parvovirida)(细小病毒);乳多空病毒科(Papovaviridae)(乳头瘤病毒、多瘤病毒);腺病毒科(Adenoviridae)(大多数腺病毒);疱疹病毒科(Herpesviridae)(单纯疱疹病毒(HSV)1和2、水痘带状疱疹病毒、巨细胞病毒(CMV)、疱疹病毒);痘病毒科(Poxviridae)(天花病毒、牛痘病毒、痘病毒);和虹彩病毒科(Iridoviridae)(例如非洲猪瘟病毒);以及未分类的病毒(例如,丁型肝炎的病原体(被认为是乙肝病毒的缺陷卫星(defective satellite)),非甲、非乙型肝炎的病原体(类1=内部传播;类2=经肠胃外传播(即,丙型肝炎);诺沃克(Norwalk)和相关病毒,以及星状病毒)。
细菌和/或真菌的非限制性实例包括巴斯德菌(Pasteurella)、葡萄球菌(Staphylococci)、链球菌(Streptococcus)、大肠杆菌(Escherichia coli)、假单胞菌属(Pseudomonas species)和沙门氏菌属(Salmonella species)。感染细菌的具体实例包括但不限于,幽门螺杆菌(Helicobacter pyloris)、伯氏疏螺旋体(Borelia burgdorferi)、嗜肺军团菌(Legionella pneumophilia)、分枝杆菌属(Mycobacteria sps)(例如结核分枝杆菌(M.tuberculosis)、鸟分枝杆菌(M.avium)、胞内分枝杆菌(M.intracellulare)、堪萨斯分枝杆菌(M.kansaii)、戈登分枝杆菌(M.gordonae))、金黄色葡萄球菌(Staphylococcusaureus)、淋病奈瑟氏菌(Neisseria gonorrhoeae)、脑膜炎奈瑟氏球菌(Neisseriameningitidis)、单核细胞增生性李斯特菌(Listeria monocytogenes)、酿脓链球菌(Streptococcus pyogenes)(A组链球菌)、无乳链球菌(Streptococcus agalactiae)(B组链球菌)、链球菌(viridans组)、粪链球菌(Streptococcus faecalis)、牛链球菌(Streptococcus bovis)、链球菌(厌氧属)、肺炎链球菌(Streptococcus pneumoniae)、致病性弯曲杆菌属(pathogenic Campylobacter sp.)、肠球菌属(Enterococcus sp.)、流感嗜血杆菌(Haemophilus influenzae)、炭疽杆菌(Bacillus anthracis)、白喉棒状杆菌(corynebacterium diphtheriae)、棒状杆菌属(corynebacterium sp.)、红斑丹毒丝菌(Erysipelothrix rhusiopathiae)、产气荚膜梭菌(Clostridium perfringens)、破伤风梭菌(Clostridium tetani)、产气肠杆菌(Enterobacter aerogenes)、肺炎克雷伯菌(Klebsiella pneumoniae)、多杀性巴斯德氏菌(Pasturella multocida)、拟杆菌属(Bacteroides sp.)、具核梭杆菌(Fusobacterium nucleatum)、念珠状链杆菌(Streptobacillus moniliformis)、梅毒螺旋体(Treponema pallidium)、极细密螺旋体(Treponema pertenue)、钩端螺旋体(Leptospira)、立克次氏体(Rickettsia)、曲霉属物种(Aspergillus species)和衣氏放线菌(Actinomyces israelli)。
2.2.4标签
在某些实施方式中,可溶性多肽包含标签。在某些实施方式中,标签包括表位标签,其包含被第一抗体识别的表位。在某些实施方式中,表位标签选自Myc标签、HA标签、Flag标签、V5标签、T7标签、CD34标签及其组合。在某些实施方式中,标签包含与底物结合的亲和标签。在某些实施方式中,亲和标签选自His标签、Strep标签、E标签、链霉亲和素结合蛋白标签(SBP标签)及其组合。
2.2.5.模拟表位
在某些实施方式中,可溶性多肽还包含被第二抗体识别的模拟表位。第二抗体与模拟表位的结合可介导包含可溶性多肽的细胞的耗竭。
在某些实施方式中,可溶性多肽包含被第一抗体识别的表位标签和被第二抗体识别的模拟表位。在某些实施方式中,表位标签是CD34表位标签,第一抗体是抗CD34抗体,模拟表位是CD20模拟表位,第二抗体是抗CD20抗体。在某些实施方式中,抗CD34抗体是QBEND10。在某些实施方式中,抗CD20抗体是利妥昔单抗。在某些实施方式中,CD20模拟表位是环状CD20模拟表位。
在某些实施方式中,CD20模拟表位包含或具有SEQ ID NO:116所示的氨基酸序列,其在下面提供。
CPYSNPSLC[SEQ ID NO:116]
在某些实施方式中,CD34表位标签包含或具有SEQ ID NO:117所示的氨基酸序列,其在下面提供。
ELPTQGTFSNVSTNVS[SEQ ID NO:117]
在某些实施方式中,可溶性多肽包含两个CD34表位标签,例如,每个CD34表位标签包含或具有SEQ ID NO:117所示的氨基酸序列。在某些实施方式中,两个CD34表位标签通过接头连接。在某些实施方式中,接头包含或具有SEQ ID NO:118所示的氨基酸序列,其在下面提供。
GGGGSGGGS[SEQ ID NO:118]
在某些实施方式中,可溶性多肽包含SEQ ID NO:119所示的氨基酸序列,其在下面提供。SEQ ID NO:119具有两个CD34表位标签,其通过氨基酸序列如SEQ ID NO:118所示的接头连接,SEQ ID NO:119称为“Q2”。
ELPTQGTFSNVSTNVSGGGGSGGGSELPTQGTFSNVSTNVS[SEQ ID NO:119]
在某些实施方式中,可溶性多肽包含两个CD20模拟表位,例如,每个CD20模拟表位包含或具有SEQ ID NO:116所示的氨基酸序列。在某些实施方式中,两个CD20模拟表位通过接头连接。在某些实施方式中,接头包含或具有SEQ ID NO:120所示的氨基酸序列,其在下面提供。
sGGGGSsGGGGSD[SEQ ID NO:120]
在某些实施方式中,可溶性多肽包含SEQ ID NO:121所示的氨基酸序列,其在下面提供。SEQ ID NO:121具有两个CD20模拟表位,其通过氨基酸序列如SEQ ID NO:120所示的接头连接,SEQ ID NO:121称为“R2”。
CPYSNPSLCSGGGGSSGGGGSDCPYSNPSLC[SEQ ID NO:121]
在某些实施方式中,可溶性多肽包含两个CD20模拟表位和一个CD34表位标签,例如,每个CD20模拟表位包含或具有SEQ ID NO:116所示的氨基酸序列,并且CD34表位标签包含或具有SEQ ID NO:117所示的氨基酸序列。在某些实施方式中,CD34表位标签通过接头连接至每个CD20模拟表位。在某些实施方式中,接头是人CD8多肽,例如,包含或具有SEQ IDNO:122所示氨基酸序列的人CD8多肽,其在下面提供。
PAKPTTT[SEQ ID NO:122]
在某些实施方式中,接头包含或具有SEQ ID NO:123所示的氨基酸序列,其在下面提供。
SGGGGS[SEQ ID NO:123]
在某些实施方式中,可溶性多肽包含SEQ ID NO:124所示的氨基酸序列,其在下面提供。SEQ ID NO:124具有两个CD20模拟表位和一个CD34表位标签,其中,所述CD34表位标签通过氨基酸序列如SEQ ID NO:124中所示的接头与一个CD20模拟表位连接,并通过氨基酸序列如SEQ ID NO:124中所示的接头与另一个CD20模拟表位连接,且SEQ ID NO:124称为“RQR”。
CPYSNPsLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLC[SEQ ID NO:124]
本公开的主题还提供包含编码本公开的多肽(例如,膜结合多肽或可溶性多肽)的核苷酸序列的核酸。在某些实施方式中,核酸还包含用于在人细胞中表达核酸序列的启动子。用于表达多肽的启动子可以是组成型启动子(例如泛素C(UbiC)启动子、MSCV、SFFV、EF1α、RSV、PGK和MMLV LTR)或诱导型启动子(例如NFAT转录应答元件(TRE)启动子、CD69启动子、CD25启动子、IL-2启动子、IL-6应答元件、sis诱导元件(SIE)、干扰素γ应答元件、GAS/IRES元件、NFkB应答元件、Gal应答元件和四环素应答元件)。
本文还提供表达载体,其包含编码如本文公开的膜结合多肽或如本文公开的可溶性多肽的核酸分子。表达载体可以是病毒载体或基于转座子的载体。在某些实施方式中,病毒载体是逆转录病毒载体。在某些实施方式中,逆转录病毒载体是慢病毒载体。本公开的主题还提供包含本公开的核酸分子的宿主细胞。在某些实施方式中,宿主细胞是T细胞。
3.系统
本公开的主题提供用于分离细胞(例如用于分离包含至少两个表达载体的细胞)和/或免疫疗法的系统。在某些实施方式中,该系统包含由第一表达载体编码的本公开的膜结合多肽和由第二表达载体编码的本公开的可溶性多肽。
3.1.包含带自阻断特征的膜结合多肽的细胞分选系统
本公开的主题提供一种用于分离包含至少两个表达载体的细胞的系统。在某些实施方式中,该系统包括:a)由第一表达载体编码的本公开的膜结合多肽,和b)由第二表达载体编码的本公开的可溶性多肽。在某些实施方式中,可溶性多肽包含标签和能够与第一二聚化结构域二聚化的第三二聚化结构域。在某些实施方式中,第三二聚化结构域在第一二聚化结构域和第二二聚化结构域之间的二聚化之前与第一二聚化结构域形成二聚体。在某些实施方式中,第三二聚化结构域与内质网中的第一二聚化结构域形成二聚体。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够形成二聚体。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够在内质网中形成二聚体。在某些实施方式中,可溶性多肽和膜结合多肽在从不同细胞表达时,由于第一二聚化结构域和第二二聚化结构域之间的二聚化,两者不能形成二聚体。在某些实施方式中,第三二聚化结构域包含SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列。
3.2.包含带阻断间隔区的膜结合多肽的细胞分选系统
本公开的主题提供一种用于分离包含至少两个表达载体的细胞的系统。在某些实施方式中,该系统包括:a)由第一表达载体编码的膜结合多肽,其中该膜结合多肽包含跨膜结构域和细胞外结构域,其中细胞外结构域包含第一二聚化结构域和阻断间隔区,和b)由第二表达载体编码的可溶性多肽,其中该可溶性多肽包含标签和第二二聚化结构域。在某些实施方式中,第一和第二二聚化结构域各自包含亮氨酸拉链结构域,并且其中当膜结合多肽和可溶性多肽不是从同一细胞表达时,阻断间隔区阻止膜结合多肽与可溶性多肽的二聚化。在某些实施方式中,第一二聚化结构域包含SEQ ID NO:1、SEQ ID NO:2或SEQ ID NO:106所示的氨基酸序列。在某些实施方式中,第二二聚化结构域包含SEQ ID NO:1、SEQ IDNO:2或SEQ ID NO:106所示的氨基酸序列。在某些实施方式中,阻断间隔区不超过约25个氨基酸残基。在某些实施方式中,阻断间隔区在约5个氨基酸残基至约25个氨基酸残基之间。在某些实施方式中,阻断间隔区是截短的CD28间隔区或IgG1铰链。
3.3.本文公开的系统的共同特征
本文公开的膜结合多肽或可溶性多肽的任何特征(例如,如第2节中公开的)可以应用于本文公开的系统。
在某些实施方式中,标签包括被第一抗体识别的表位标签。在某些实施方式中,表位标签选自Myc标签、HA标签、Flag标签、V5标签、T7标签、CD34标签及其组合。在某些实施方式中,标签包括与底物结合的亲和标签。在某些实施方式中,亲和标签选自His标签、Strep标签、E标签、链霉亲和素结合蛋白标签(SBP标签)及其组合。
在某些实施方式中,可溶性多肽还包含抗原结合结构域。在某些实施方式中,抗原结合结构域包含单链可变片段(scFv)、可溶性配体、细胞因子、趋化因子、基于非scFv的抗原识别基序或其组合。在某些实施方式中,可溶性多肽还包含细胞因子或趋化因子。
在某些实施方式中,膜结合多肽由第一载体表达。在某些实施方式中,可溶性多肽由第二载体表达。第一载体可以与第二载体相同,或不同于第二载体。在某些实施方式中,第一载体与第二载体相同,例如,第一和第二载体的载体主链可以相同,而由第一和第二载体编码/表达的多肽或蛋白质可以不同。
3.4.示例性的膜结合多肽、可溶性多肽和系统
在某些实施方式中,膜结合多肽包含V5标签,EE12RR345L亮氨酸拉链,CD28EC-9C铰链,CD2跨膜(TM)结构域和截短的细胞质结构域,E2A肽和Thy1.1肽。(V5标签染色鉴定出膜结合多肽表面表达)。在某些实施方式中,膜结合多肽包含SEQ ID NO:24所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含V5标签,EE12RR345L亮氨酸拉链,CD28EC-9C铰链,CD28 TM结构域,CD3zδ结构域,E2A肽和Thy1.1肽。(V5标签染色鉴定出膜结合多肽表面表达)。在某些实施方式中,膜结合多肽包含SEQ ID NO:25所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含EE12RR345L亮氨酸拉链,myc标签,CD28EC-9C铰链,CD2 TM结构域和截短的细胞质结构域,E2A肽和Thy1.1肽。(无myc染色)。在某些实施方式中,膜结合多肽包含SEQ ID NO:26所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含EE12RR345L亮氨酸拉链,myc标签,CD28EC-9C铰链,CD28 TM结构域,CD3zδ结构域,E2A肽和Thy1.1肽。(无myc染色)。在某些实施方式中,膜结合多肽包含SEQ ID NO:27所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含V5标签,EE12RR345L亮氨酸拉链,IgG1铰链,CD2 TM结构域和截短的细胞质结构域,E2A肽和Thy1.1肽。(V5标签染色鉴定出膜结合多肽表面表达)。在某些实施方式中,膜结合多肽包含SEQ ID NO:28所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含V5标签,EE12RR345L亮氨酸拉链,IgG1铰链,CD28 TM结构域,CD3ζδ结构域,E2A肽和Thy1.1肽。(V5标签染色鉴定出膜结合多肽表面表达)。在某些实施方式中,膜结合多肽包含SEQ ID NO:29所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如,RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如,EE12RR345L亮氨酸拉链),EGFRt多肽,P2A肽和蓝色荧光蛋白(BFP)。在某些实施方式中,该系统包含SEQ ID NO:30所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如,RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如,EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽和蓝色荧光蛋白(BFP)。在某些实施方式中,该系统包含SEQ ID NO:31所示的氨基酸序列。
在某些实施方式中,膜结合多肽包含EE12RR345L亮氨酸拉链,myc标签,MHC-I铰链/TM结构域,P2A肽和蓝色荧光蛋白(BFP)。(无myc染色)。在某些实施方式中,膜结合多肽包含SEQ ID NO:32所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含带FLAG标签的RR12EE345L亮氨酸拉链,P2A肽,iCaspase9多肽和F2A肽。在某些实施方式中,可溶性多肽构建体包含SEQ ID NO:33所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含带FLAG标签的RR12EE345L亮氨酸拉链,P2A肽,iCaspase9多肽,F2A肽,CD19 scFv,myc标签,CD8EC铰链/TM结构域,CD28共刺激结构域和CD3z多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:34和SEQ ID NO:35所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含带FLAG标签的RR12EE345L亮氨酸拉链,P2A肽,iCaspase9多肽,F2A肽,IL-3多肽,CD8EC铰链/TM结构域,CD28共刺激结构域和CD3ζ多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:36所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含带FLAG标签的RR12EE345L亮氨酸拉链,P2A肽,iCaspase9多肽,F2A肽,CD38 scFv,链间接头,IL-3多肽,CD8EC铰链/TM结构域,CD28共刺激域和CD3z多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:37和SEQ ID NO:38所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,CD20 scFv,twin streptag-II,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽和E2A多肽。在某些实施方式中,该系统包含SEQ ID NO:39和SEQ ID NO:40所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,CD20 scFv,twin streptag-II,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽,E2A多肽和前IL-18多肽(包含IL-18前肽序列)。在某些实施方式中,该系统包含SEQ ID NO:41和SEQ ID NO:42所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,CD20 scFv,twin streptag-II,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽,E2A多肽和sIL-18多肽(包含小鼠IL-2信号肽序列)。在某些实施方式中,该系统包含SEQ ID NO:43和SEQ ID NO:44所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,CD20 scFv,链间接头,CD19scFv,myc标签,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽和E2A多肽。在某些实施方式中,该系统包含SEQ ID NO:45、SEQ ID NO:46和SEQ ID NO:47所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,CD20 scFv,链间接头,IL-3多肽,twin streptag-II,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽和E2A多肽。在某些实施方式中,该系统包含SEQ ID NO:48和SEQ ID NO:49所示的氨基酸序列。
在某些实施方式中,系统包含可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(例如EE12RR345L亮氨酸拉链),Thy1.1多肽,P2A肽,IL-3多肽,链间接头,CD20scFv,twin streptag-II,CD8EC铰链/TM结构域,CD28共刺激结构域,CD3ζ多肽和E2A多肽。在某些实施方式中,该系统包含SEQ ID NO:50和SEQ ID NO:51所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含与带FLAG标签的RR12EE345L亮氨酸拉链融合的小鼠IL-7多肽,P2A肽,iCaspase9多肽,F2A肽,CD19 scFv,myc标签,CD8EC铰链/TM结构域,CD28共刺激结构域和CD3ζ多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:52和SEQ ID NO:53所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含与带FLAG标签的RR12EE345L亮氨酸拉链融合的小鼠IL-15多肽,P2A肽,iCaspase9多肽,F2A肽,CD19 scFv,myc标签,CD8EC铰链/TM结构域,CD28共刺激结构域和CD3ζ多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:54和SEQ ID NO:55所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含与带FLAG标签的RR12EE345L亮氨酸拉链融合的小鼠IL-21多肽,P2A肽,iCaspase9多肽,F2A肽,CD19 scFv,myc标签,CD8EC铰链/TM结构域,CD28共刺激结构域和CD3ζ多肽。在某些实施方式中,可溶性多肽包含SEQ ID NO:56和SEQ ID NO:57所示的氨基酸序列。
在某些实施方式中,可溶性多肽包含RQR序列(具有两个CD20模拟表位和一个CD34表位),接头和RR12EE345L亮氨酸拉链。在某些实施方式中,可溶性多肽包含SEQ ID NO:134所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:134的氨基酸序列的示例性核苷酸序列在SEQ ID NO:135中示出,其在下面提供。
在某些实施方式中,可溶性多肽包含Q2序列(具有两个CD34表位),接头和RR12EE345L亮氨酸拉链。在某些实施方式中,可溶性多肽包含SEQ ID NO:136所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:136的氨基酸序列的示例性核苷酸序列在SEQ ID NO:137中示出,其在下面提供。
在某些实施方式中,膜结合多肽包含R2序列(具有两个CD20模拟表位),接头,EE12RR345L亮氨酸拉链,CD28-9C铰链,CD28跨膜结构域和截短的CD3ζ(δ)。在某些实施方式中,膜结合多肽包含SEQ ID NO:138所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:138的氨基酸序列的示例性核苷酸序列在SEQ ID NO:139中示出,其在下面提供。
在某些实施方式中,该系统包含可溶性多肽(包含R2序列和RR12EE345L亮氨酸拉链),接头,膜结合多肽(包含EE12RR345L亮氨酸拉链,PD1显性负型分子,CD4 TM结构域和截短的CD3z(δ))。在某些实施方式中,该系统包含SEQ ID NO:140所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:140的氨基酸序列的示例性核苷酸序列在SEQ ID NO:141中示出,其在下面提供。
在某些实施方式中,系统包含κ信号肽,可溶性多肽(例如RR12EE345L亮氨酸拉链),接头,膜结合多肽(具有EE12RR345L亮氨酸拉链和CD80多肽)。在某些实施方式中,该系统包含SEQ ID NO:142所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:142的氨基酸序列的示例性核苷酸序列在SEQ ID NO:143中示出,其在下面提供。
在某些实施方式中,膜结合多肽包含EE12RR345L亮氨酸拉链,接头和4-1BBL多肽。在某些实施方式中,膜结合多肽包含SEQ ID NO:144所示的氨基酸序列,其在下面提供。
编码SEQ ID NO:144的氨基酸序列的示例性核苷酸序列在SEQ ID NO:145中示出,其在下面提供。
亮氨酸拉链构建体中包含的元件的示例性序列如下。
链间接头:GTGGSTGGGGSGGGGSGGGGS[SEQ ID NO:58]
可替代的链间接头1:GGGGSGGGGSGGGGSGGGGSGGGS[SEQ ID NO:59]
可替代的链间接头2:GGGGSSGGGGSD[SEQ ID NO:146]
可替代的链间接头3:GGGGSGGGS[SEQ ID NO:118]
可替代的链间接头4:GSTSGSGKPGSGEGSTKG[SEQ ID NO:147]
可替代的链间接头5:EFTGSTSGSGKPGSGEGSTKG[SEQ ID NO:148]
可替代的链间接头6:GGGGSGGGSALG[SEQ ID NO:149]
在基于细胞因子的受体结合区中使用的小鼠IL-3序列:
将在相似的基于IL-3的CAR中使用的人IL-3序列:
用于CAR的小鼠CD8间隔区,也是用于ZipR-CAR的非阻断间隔区:
STTTKPVLRTPSPVHPTGTSQPQRPEDCRPRGSVKGTGLDFACD[SEQ ID NO:62]
人CD8间隔区等同序列:
TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACD[SEQ ID NO:63]
用于CAR的小鼠CD28长间隔区:
IEFMYPPPYLDNERSNGTIIHIKEKHLCHTQSSPKL[SEQ ID NO:64]
人CD28长间隔区等同序列:
IEVMYPPPYLDNEKSNGTIIHVKGKHLCPSPLFPGPSKP[SEQ ID NO:65]
小鼠Thy1.1(CD90)间隔区(非阻断):
小鼠Thyl.1(CD90)前肽(用作Thy1.1/CD90间隔区的一部分,以将构建体引导至细胞膜,紧跟Thyl.1间隔区序列):
GGISLLVQNTSWMLLLLLSLSLLQALDFISL[SEQ ID NO:67]
人CD90间隔区-基于与小鼠的同源性而推定是非阻断的(Thy1.1/Thy1.2等位基因变体限于小鼠):
人CD90前肽(用作CD90间隔区的一部分以将构建体引导至细胞膜,紧跟CD90间隔区序列):
EGISLLAQNTSWLLLLLLSLSLLQATDFMSL[SEQ ID NO:69]
人EGFRt间隔区(非阻断):
人EGFRt跨膜结构域:IATGMVGALLLLLVVALGIGLFM[SEQ ID NO:71]
小鼠CD2跨膜结构域和短的细胞内区域:
与CD28跨膜+CD3ζ相比,该元件可促进较弱的构建体表达,并可用于控制细胞表面亮氨酸拉链密度的表达。KRKK可充当内质网滞留信号。
人CD2跨膜结构域和短的细胞内区域:
小鼠MHC I类跨膜结构域(H2-Kd)和短的细胞质接头:
包含信号肽的小鼠IL-7序列:
小鼠IL-15序列+小鼠IL-2信号肽:
小鼠IL-21序列+小鼠IL-2信号肽:
亮氨酸拉链接头+FLAG标签+RR12EE345L(序列在上面列出的细胞因子序列之后):
2A肽序列:
标签序列:
信号肽序列:
其他元件:
4.使用方法
本公开的主题提供分离包含至少两个表达载体的细胞的方法。在某些实施方式中,该方法包括:
a)在细胞中表达i)由第一表达载体编码的本公开的膜结合多肽,和ii)由第二表达载体编码的本公开的可溶性多肽,
b)使细胞与结合至标签的底物接触,和
c)分离与底物结合的细胞。
在某些实施方式中,分离包含至少两个表达载体的细胞的方法包括:
a)在细胞中表达i)由第一表达载体编码的膜结合多肽,其包含跨膜结构域和细胞外结构域,其中细胞外结构域包含第一二聚化结构域和阻断间隔区,和ii)由第二表达载体编码的可溶性多肽,其包含标签和第二二聚化结构域,其中第一和第二二聚化结构域均包含亮氨酸拉链结构域,并且其中当膜结合多肽与可溶性多肽不是从同一细胞表达时,阻断间隔区阻止膜结合多肽与可溶性多肽的二聚化,
b)使细胞与结合至标签的底物接触,和
c)分离与底物结合的细胞。
此外,本公开的主题提供分选包含至少两个载体的多个细胞的方法。在某些实施方式中,该方法包括:
a)用以下i)和ii)转染多个细胞:i)编码本文公开的膜结合多肽的第一表达载体,和ii)编码本文公开的可溶性多肽的第二表达载体,
b)使细胞与结合至标签的底物接触,和
c)分离与底物结合的一个或多个细胞。
在某些实施方式中,步骤c),例如,分离与底物结合的一个或多个细胞的步骤,之前是步骤d),例如,洗涤底物以去除不与底物结合的细胞。
在某些实施方式中,分选包含至少两个表达载体的多个细胞的方法包括:
a)用以下i)和ii)转染多个细胞:i)编码膜结合多肽的第一表达载体,该膜结合多肽包含跨膜结构域和包含第一二聚化结构域的细胞外结构域,和ii)编码可溶性多肽的第二表达载体,该可溶性多肽包含标签和能够与第一二聚化结构域二聚化的第二二聚化结构域,其中第一和第二二聚化结构域各自包含亮氨酸拉链结构域,并且其中当膜结合多肽与可溶性多肽不是从同一细胞表达时,膜结合多肽不与可溶性多肽二聚化,
b)使细胞与结合至标签的底物接触,和
c)分离与底物结合的一个或多个细胞。
在某些实施方式中,可溶性多肽包含标签和能够与包含在膜结合多肽中的第一二聚化结构域二聚化的第三二聚化结构域。在某些实施方式中,第三二聚化结构域能够在第一二聚化结构域和第二二聚化结构域之间的二聚化之前与第一二聚化结构域二聚化。在某些实施方式中,第三二聚化结构域能够与内质网中的第一二聚化结构域二聚化。
在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够形成二聚体。在某些实施方式中,当可溶性多肽和膜结合多肽从同一细胞表达时,两者能够在内质网中形成二聚体。在某些实施方式中,可溶性多肽和膜结合多肽在从不同细胞表达时,由于第一二聚化结构域和第二二聚化结构域之间的二聚化,两者不能形成二聚体。在某些实施方式中,步骤c),例如,分离与底物结合的一个或多个细胞的步骤,之前是步骤d),洗涤底物以去除不与底物结合的细胞。
在某些实施方式中,细胞选自T细胞、自然杀伤(NK)细胞、细胞毒性T淋巴细胞(CTL)、调节性T细胞、自然杀伤T(NKT)细胞、人胚胎干细胞和从中可分化出淋巴样细胞的多能干细胞。在某些实施方式中,细胞是T细胞。在某些实施方式中,细胞是自体的。在某些实施方式中,亮氨酸拉链是正交拉链。在某些实施方式中,正交拉链是RR/EE拉链、Fos/Jun拉链或Fos/synZip拉链。synZip-9、Fos和Jun拉链的实例分别示于SEQ ID NO:4、SEQ ID NO:5和SEQ ID NO:6中。
5.细胞
本公开的主题提供包含本文公开的膜结合多肽、可溶性多肽和/或系统的细胞。在某些实施方式中,多肽和/或系统能够激活或抑制免疫应答细胞。在某些实施方式中,多肽和/或系统能够促进免疫应答细胞的抗肿瘤作用。可以用多肽和/或系统转导细胞,使得细胞共表达多肽和/或系统。在某些实施方式中,细胞是免疫应答细胞。该细胞可以是淋巴谱系的细胞或骨髓谱系的细胞。
淋巴谱系的细胞可以产生抗体、调节细胞免疫系统、检测血液中的外源物质以及检测宿主中的外源细胞等等。淋巴谱系的细胞的非限制性实例包括B细胞、T细胞、自然杀伤(NK)细胞、树突状细胞,从中可分化出淋巴样细胞的干细胞。在某些实施方式中,干细胞是多能干细胞。在某些实施方式中,多能干细胞是胚胎干细胞或诱导的多能干细胞。
在某些实施方式中,细胞是T细胞。T细胞可以是在胸腺中成熟的淋巴细胞,主要负责细胞介导的免疫。T细胞参与适应性免疫系统。本公开的主题的T细胞可以是任何类型的T细胞,包括但不限于:辅助T细胞、细胞毒性T细胞、记忆T细胞(包括中央记忆T细胞、干细胞样记忆T细胞(或干样记忆T细胞)和两种效应记忆T细胞:例如T
在某些实施方式中,细胞是自然杀伤(NK)细胞。自然杀伤(NK)细胞可以是淋巴细胞,它是细胞介导的免疫的一部分,并在先天免疫应答中起作用。NK细胞不需要事先激活即可对靶细胞执行细胞毒性作用。
在某些实施方式中,细胞是人淋巴细胞。在某些实施方式中,人淋巴细胞包括但不限于外周供体淋巴细胞,例如在以下中公开的那些:Sadelain,M.等,2003Nat Rev Cancer3:35-45(公开了经遗传修饰以表达CAR的外周供体淋巴细胞),Morgan,R.A.等,2006Science 314:126-129(公开了经遗传修饰以表达包含α和β异二聚体的全长肿瘤抗原识别性T细胞受体复合物的外周供体淋巴细胞),Panelli,M.C.,等.2000J Immunol 164:495-504;Panelli,M.C.,等.2000J Immunol 164:4382-4392(公开了在肿瘤活组织检查中衍生自肿瘤浸润淋巴细胞(TIL)的淋巴细胞培养物)和Dupont,J.,等.2005Cancer Res 65:5417-5427;Papanicolaou,G.A.,等.2003Blood 102:2498-2505(公开了使用人工抗原递呈细胞(AAPC)或脉冲树突状细胞在体外选择性地扩增的抗原特异性外周血白细胞)。
细胞(例如,T细胞)可以是自体的、非自体的(例如,同种异体的)、或者是从工程化的祖细胞或干细胞体外衍生的。
在某些实施方式中,本公开主题的细胞是骨髓谱系的细胞。在某些实施方式中,骨髓谱系的细胞包括但不限于:单核细胞、巨噬细胞、嗜碱性粒细胞、嗜中性粒细胞、嗜酸性粒细胞、肥大细胞、红细胞和血小板细胞。
本公开的细胞能够调节肿瘤微环境。肿瘤具有如下微环境,其可通过一系列机制中的任一种抑制宿主免疫反应,从而保护自身免受免疫监视、识别和消除。免疫抑制因子包括但不限于,浸润调节性CD4
在某些实施方式中,本公开的细胞具有增强的细胞持久性。在某些实施方式中,本公开的细胞具有降低的凋亡和/或无反应性。
CTL的未纯化来源可以是本领域已知的任何来源,例如骨髓、胎儿、新生儿或成年或其他造血细胞来源,例如胎儿肝、外周血或脐带血。可以采用各种技术来分离细胞。例如,阴性选择方法可以初步除去非CTL。单克隆抗体(mAb)对于鉴定与特定细胞谱系和/或阳性和阴性选择的分化阶段相关的标志物特别有用。
最初可以通过相对粗略的分离除去大部分终末分化的细胞。例如,最初可以使用磁珠分离来去除大量不相关的细胞。在某些实施方式中,在分离细胞之前将去除总造血细胞的至少约80%,通常至少约70%。
分离的程序包括但不限于,密度梯度离心;重置;偶联至改变细胞密度的颗粒;用抗体包被的磁珠进行磁分离;亲和色谱;与mAb连接或共同使用的细胞毒性剂,包括但不限于补体和细胞毒素;以及利用附着在固体基质(例如板、芯片、淘析)上的抗体进行淘选或任何其它方便的技术。
分离和分析的技术包括但不限于流式细胞术,其可以具有不同的复杂程度,例如多个颜色通道、低角度和钝角光散射检测通道、阻抗通道。
通过使用与死细胞相关的染料,例如碘化丙啶(PI),可以将细胞与死细胞区分开。在某些实施方式中,将细胞收集在包含2%胎牛血清(FCS)或0.2%牛血清白蛋白(BSA)的培养基或任何其它合适的培养基中,例如无菌等渗培养基中。
6.载体
免疫应答细胞(例如,T细胞)的遗传修饰可以通过转导具有重组DNA构建体的基本上均质的细胞组分来实现。在某些实施方式中,逆转录病毒载体用于将DNA构建体引入细胞。例如,可以将编码本文公开的任何多肽或系统的多核苷酸克隆到逆转录病毒载体中,并且可以从其内源启动子、从逆转录病毒长末端重复序列或对目标靶细胞类型特异性的启动子驱动表达。在某些实施方式中,逆转录病毒载体是γ逆转录病毒载体。在某些实施方式中,逆转录病毒载体是慢病毒载体。也可以使用非病毒载体。
对于免疫应答细胞的初始遗传修饰以包括本文公开的多肽和/或系统,通常采用逆转录病毒载体用于转导,然而可以使用任何其他合适的病毒载体或非病毒递送系统。可以在单个多顺反子表达盒中、在单个载体的多个表达盒中或在多个载体中构建多肽和/或系统。产生多顺反子表达盒的元件的实例包括但不限于,各种病毒和非病毒内部核糖体进入位点(IRES,例如,FGF-1IRES、FGF-2IRES、VEGF IRES、IGF-II IRES、NF-κB IRES、RUNX1IRES、p53 IRES、甲型肝炎IRES、丙型肝炎IRES、瘟病毒IRES、口蹄疫病毒IRES、小核糖核酸病毒IRES、脊髓灰质炎病毒IRES和脑心肌炎病毒IRES)和可裂解的接头(例如2A肽,例如P2A、T2A、E2A和F2A肽)。逆转录病毒载体和合适的包装系的组合也是合适的,其中衣壳蛋白将具有感染人细胞的功能。已知各种产生两性病毒的细胞系,包括但不限于PA12(Miller等,(1985)Mol.Cell.Biol.5:431-437);PA317(Miller等,(1986)Mol.Cell.Biol.6:2895-2902);和CRIP(Danos等,(1988)Proc.Natl.Acad.Sci.USA85:6460-6464)。非两性粒子也是合适的,例如,用VSVG、RD114或GALV包膜的假型化粒子和本领域已知的任何其它粒子。
可能的转导方法还包括细胞与生产细胞的直接共培养,例如通过Bregni等.(1992)Blood 80:1418-1422的方法,或单独用病毒上清液或含有或不含有适当生长因子和聚阳离子的浓缩载体原种培养,例如通过Xu,等.(1994)Exp.Hemat.22:223-230;和Hughes,等.(1992)J.Clin.Invest.89:1817的方法。
其它转导病毒载体可用于修饰免疫应答细胞。在某些实施方式中,所选择的载体表现出高的感染效率,稳定的整合入宿主细胞基因组和重组基因产物的持久表达(参见,例如,Cayouette等,Human Gene Therapy 8:423-430,1997;Kido等,Current Eye Research15:833-844,1996;Bloomer等,Journal of Virology 71:6641-6649,1997;Naldini等,Science 272:263-267,1996;和Miyoshi等,Proc.Natl.Acad.Sci.U.S.A.94:10319,1997)。可以使用的其它病毒载体包括,例如,腺病毒、慢病毒和腺相关病毒载体、牛痘病毒、牛乳头瘤病毒或疱疹病毒,例如爱泼斯坦-巴尔病毒(Epstein-Barr Virus)(也参见例如以下中的载体:Miller,Human Gene Therapy 15-14,1990;Friedman,Science 244:1275-1281,1989;Eglitis等,BioTechniques 6:608-614,1988;Tolstoshev等,Current Opinion inBiotechnology 1:55-61,1990;Sharp,The Lancet337:1277-1278,1991;Cornetta等,Nucleic Acid Research and Molecular Biology 36:311-322,1987;Anderson,Science226:401-409,1984;Moen,Blood Cells 17:407-416,1991;Miller等,Biotechnology 7:980-990,1989;LeGal La Salle等,Science 259:988-990,1993;和Johnson,Chest107:77S-83S,1995)。逆转录病毒载体发展地特别好,并已用于临床(Rosenberg等,N.Engl.J.Med 323:370,1990;Anderson等,U.S.Pat.No.5,399,346)。
非病毒方法也可以用于免疫应答细胞的遗传修饰。例如,可以通过在脂质转染(Feigner等,Proc.Natl.Acad.Sci.U.S.A.84:7413,1987;Ono等,Neuroscience Letters17:259,1990;Brigham等,Am.J.Med.Sci.298:278,1989;Staubinger等,Methods inEnzymology 101:512,1983),脱唾液酸血清类粘蛋白-聚赖氨酸缀合(Wu等,Journal ofBiological Chemistry 263:14621,1988;Wu等,Journal of Biological Chemistry264:16985,1989)的存在下,或通过手术条件下的微注射(Wolff等,Science 247:1465,1990)施用核酸来将核酸分子引入免疫应答细胞中。其它非病毒的基因转移方法包括使用磷酸钙、DEAE葡聚糖、电穿孔和原生质体融合的体外转染。脂质体也可能对将DNA递送到细胞中有益。也可以通过将正常核酸转移到可离体培养的细胞类型(例如,自体或异源原代细胞或其后代)中来完成将正常基因移植到受试者的受影响组织中,之后,将细胞(或其后代)注射到目标组织中或全身注射。重组受体也可以使用转座酶或靶向核酸酶(例如锌指核酸酶、大范围核酸酶或TALEN核酸酶、CRISPR)衍生或获得。瞬时表达可通过RNA电穿孔获得。在某些实施方式中,重组受体可以通过基于转座子的载体而引入。在某些实施方式中,基于转座子的载体包含转座子(又称可转座元件)。在某些实施方式中,转座子可以由转座酶识别。在某些实施方式中,转座酶是睡美人转座酶。
所得细胞可以在与未修饰的细胞相似的条件下生长,由此修饰的细胞可以被扩增并用于多种目的。
7.多肽和类似物
本公开的主题中还包括:CD28、CD8、CD80、4-1BBL、PD-1和CD3ζ多肽,本文公开的膜结合多肽,以及本文公开的可溶性多肽,或它们的以增强它们在免疫应答细胞中表达时的治疗功效的方式进行修饰的片段。本公开的主题提供通过产生序列改变来优化氨基酸序列或核酸序列的方法。这样的改变可以包括某些突变、缺失、插入或翻译后修饰。本文公开的主题还包括本文公开的任何天然存在的多肽(包括但不限于CD8、CD28、CD80、4-1BBL、PD-1和CD3ζ)的类似物。类似物可以通过氨基酸序列差异、通过翻译后修饰或通过两者与本文公开的天然存在的多肽不同。类似物可表现出与本公开主题的天然存在的氨基酸序列的全部或部分是至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%或至少约100%同源的。序列比较的长度是至少5、10、15或20个氨基酸残基,例如至少25、50或75个氨基酸残基,或超过100个氨基酸残基。同样,在确定同一性程度的示例性方法中,可以使用BLAST程序,概率得分在e
除了全长多肽,本公开主题还提供本文公开的任一多肽或肽结构域的片段。如本文所用,术语“片段”是指至少5、10、13或15个氨基酸。在某些实施方式中,片段包含至少20个连续氨基酸、至少30个连续氨基酸或至少50个连续氨基酸。在某些实施方式中,片段包含至少60至80、100、200、300或更多个连续氨基酸。片段可以通过本领域技术人员已知的方法产生,或者可以由正常的蛋白质加工产生(例如,从新生多肽中去除生物活性不需要的氨基酸,或者通过另外可选的mRNA剪接或另外可选的蛋白质加工事件去除氨基酸)。
非蛋白质类似物具有设计为模仿本文公开的蛋白质/肽的功能活性的化学结构。这样的类似物可能超过原始多肽的生理活性。类似物设计的方法在本领域中是众所周知的,并且可以根据这样的方法通过修饰化学结构来进行类似物的合成,以使所得的类似物在免疫应答细胞中表达时增加原始多肽的抗肿瘤活性。这些化学修饰包括但不限于取代另外可选的R基团和改变参考多肽在特定碳原子处的饱和度。在某些实施方式中,蛋白质类似物对体内降解具有相对抗性,从而在给药后导致更长久的治疗效果。用于测量功能活性的测定包括,但不限于,以下实施例中描述的那些。
实施例
除非另有说明,否则本公开的实践采用分子生物学(包括重组技术)、微生物学、细胞生物学、生物化学和免疫学的常规技术,其在技术人员的能力范围内。这些技术在以下文献中充分地解释:例如,“分子克隆:实验室手册(Molecular Cloning:A LaboratoryManual)”,第二版(Sambrook,1989);“寡核苷酸合成(Oligonucleotide Synthesis)”(Gait,1984);“动物细胞培养(Animal Cell Culture)”(Freshney,1987);“酶学方法(Methods in Enzymology)”“实验免疫学手册(Handbook of Experimental Immunology)”(Weir,1996);“哺乳动物细胞的基因转移载体(Gene Transfer Vectors for MammalianCells)”(Miller和Calos,1987年);“分子生物学的最新方法(Current Protocols inMolecular Biology)”(Ausubel,1987年);“PCR:聚合酶链反应(PCR:The PolymeraseChain Reaction)”,(Mullis,1994年);“免疫学的最新方法(Current Protocols inImmunology)”(Coligan,1991年)中充分地解释了这些技术。这些技术适用于本发明的多核苷酸和多肽的产生,并且因此可以在制备和实施本发明中考虑。在以下部分中将讨论用于具体实施方式的特别有用的技术。
提出以下实施例以向本领域普通技术人员提供关于如何制备和使用本发明的组合物和测定、筛选和治疗方法的完整公开和描述,而不旨在限制发明人认作其发明的范围。
实施例1-亮氨酸拉链细胞分选亲和标签
开发了如下的方法,其允许对用两个病毒载体同时共转导的细胞进行选择性分选,以允许在不超过病毒包装极限的情况下转移更大量的遗传信息。为实现这一目标,设计一种基于亮氨酸拉链的二元亲和标签方法,以允许磁性选择共转导有两个病毒载体的细胞,其中每个载体表达基于亮氨酸拉链的亲和标签系统的一半。在该系统中,一种病毒载体编码带有连接亲和标签(例如FLAG、streptag、myc等)的亮氨酸拉链(例如RR12EE345L)(图1)。第二病毒载体编码膜结合亮氨酸拉链(例如,EE12RR345L),其对与RR12EE345L-亲和标签拉链形成异二聚体具有高偏好性。当被共转导到同一靶细胞中时,发生膜结合EE12RR345L亮氨酸拉链对RR12EE345L-亲和标签的表面捕获,从而允许通过流式细胞术以及使用了与亲和标签特异性抗体缀合的磁珠的免疫磁化选择对亲和标签进行表面检测。
在某些情况下,分泌的RR12EE345L-亲和标签亮氨酸拉链能够与仅表达膜结合EE12RR345L亮氨酸拉链的细胞在细胞外配对(图2)。为了防止这种配对,对膜结合EE12RR345L亮氨酸拉链进行修饰,使其具有“自阻断”功能,因此,RR12EE345L-亲和标签亮氨酸拉链与膜结合EE12RR345L亮氨酸拉链的配对仅在转导有两种逆转录病毒载体的细胞内发生,而细胞外配对途径受到抑制(图3和图4)。如图4所示,用抗FLAG磁珠分选带FLAG标签的亮氨酸拉链分选构建体,产生了双重转导的原代小鼠T细胞的纯化群体。“自阻断”特征是通过生成具有连接的RR12EE345L链而缺少亲和标签的膜结合EE12RR345L亮氨酸拉链来实现的。与亮氨酸拉链分选系统共表达的可能基因包括但不限于:嵌合抗原受体(CAR)、共刺激嵌合受体(CCR)、细胞因子和趋化因子、自杀基因、synNotch受体和相应的反式激活基因构建体、以及共刺激配体。
使iCaspase 9自杀基因在一个载体上且CD20-CAR在另一载体上而进行的初步研究表明,CD20-CAR T细胞对靶细胞具有很高的溶细胞活性,并且通过二聚化的化学诱导剂引起的iCaspase 9的活化诱导90%以上的T细胞凋亡(图5)。
此外,图6显示亮氨酸拉链分选系统用于将细胞纯化至95%以上,其中细胞包含表达CD19-CAR、CD20-CAR和iCaspase9以及任选地IL-18的两个载体。这些细胞能够杀伤CD19或CD20+靶标,并具有增强的细胞因子表达,与iCaspase9二聚体一起孵育可导致约90%的细胞死亡。
另外,单克隆抗体可以靶向包含在膜结合亮氨酸拉链内的间隔区分子,以允许体内耗竭表达构建体的细胞(图3)。对于小鼠和人T细胞,除了将两种载体整合在一起的特定细胞分选方法外,Thy1.1和截短的EGFR(EGFRt)分子还可分别用作间隔区,以实现抗体介导的耗竭。例如,图12A-12C证明,截短的EGFR间隔区(EGFRt)融合至接头阻断的亮氨酸拉链促进细胞分选和抗体依赖性的细胞介导的细胞毒性(ADCC)。
图8A-8C进一步证明,通过阻断由不同细胞表达的膜结合亮氨酸拉链和可溶性亮氨酸拉链之间的配对,接头阻断的截短型EGFR-间隔区跨膜拉链促进了双转导细胞群的MACS分选。
作为二元系统的另一个实例,图9描绘了与iCaspase9和阻断的Thy1.1亮氨酸拉链分选自杀构建体结合的双串联CAR构造。编码亮氨酸拉链分选系统构建体和串联CAR的两个逆转录病毒载体被用于转导T细胞。在同一细胞上表达的两个独立的CAR中使用相同的间隔区/铰链(如CD8)可促进异源二聚化。可以使用不同的间隔区组合(例如CD8间隔区/CD28间隔区)来避免异源二聚化。图10A-10B证明亮氨酸拉链分选系统能够对表达双串联CAR的T细胞进行单步MACS分选。图11A-11B进一步证明亮氨酸拉链分选系统能够利用两个自杀基因清除分选的T细胞。
实施例2-亮氨酸拉链细胞分选系统,其在膜结合多肽中包含短的间隔区/铰链区
开发了膜结合亮氨酸拉链的新设计,其可以抑制其他细胞分泌的可溶性带标签亮氨酸拉链的结合,但是仍然允许内部产生的带标签亮氨酸拉链的结合,而没有实施例1中描述的自阻断特征。这种膜结合多肽包含非常小的细胞外结构域,其不包含抗体表位,如Thy1.1或EGFRt。例如,包含CD8间隔区的膜结合亮氨酸拉链多肽证实了以下可溶性scFv亮氨酸拉链的结合,所述可溶性scFv亮氨酸拉链从表达膜结合多肽的相同细胞和其他细胞表达。然而,包含截短的CD28九氨基酸间隔区或IgG1铰链的膜结合亮氨酸拉链多肽仅结合与膜结合多肽在同一细胞中表达的可溶性scFv亮氨酸拉链。
如图7A-7C所示,截短的CD28膜近端铰链-间隔区跨膜亮氨酸拉链通过阻断膜结合亮氨酸拉链和从不同细胞表达的可溶性亮氨酸拉链之间的配对,促进双转导细胞群的MACS分选。
实施例3-亮氨酸拉链细胞分选系统,其在可溶性多肽中包含转座的细胞因子
如图13所示,改造出带细胞因子标签的拉链——“拉链因子”,以促进细胞因子的分泌和反式呈递(trans-presentation),同时保留了带亲和标签的分泌型亮氨酸拉链的分选功能。细胞因子(例如IL-7、IL-15和IL-21)可以与亲和标签和异二聚化亮氨酸拉链融合。分泌出的拉链因子与T细胞上的细胞因子受体相互作用,或与固有阻断的跨膜亮氨酸拉链共表达,以促进双载体共转导细胞的分选和细胞因子的反式呈递。图14A-14C表明,拉链因子保留亮氨酸拉链分选系统的功能分选特征并促进T细胞的增殖。
实施例4-包含表位标签和模拟表位的亮氨酸拉链细胞分选系统
如图15所示,生成包括串联的两个CD20模拟表位和CD34表位标签的分选系统(RQR-RR12EE345L)。通过使用包含抗CD34抗体的珠来评估分选系统的能力。如图16所示,最佳的CD20模拟表位CD34亮氨酸拉链标签捕获和呈递需要高度表达截短的捕获亮氨酸拉链。当使用IgG1-铰链CD28TM CD3zΔ和CD28-9C CD28TM CD3zΔ捕获亮氨酸拉链时,观察到有效的CD34和CD20染色。用如图17所示的捕获亮氨酸拉链和编码CD20模拟表位CD34亮氨酸拉链标签(RQR-RR12EE345L)的第二载体双重转导C1498细胞。随后使用抗CD34磁珠对细胞进行磁性分选。如图17所示,通过抗CD34磁珠对细胞进行分选。
接下来,用如图18所示的捕获亮氨酸拉链和编码串联CD20模拟表位/CD34亮氨酸拉链标签(RQR-RR12EE345L)的第二载体双重转导C1498细胞。随后,在补体存在下,将细胞与抗CD20抗体利妥昔单抗或无关抗体西妥昔单抗一起孵育。如图18所示,仅用RQR标记的亮氨酸拉链和捕获亮氨酸拉链载体转导的细胞被抗CD20抗体耗竭。因此,通过使用抗CD20抗体利妥昔单抗实现双转导细胞的选择性清除。
此外,用编码(1)串联的带CD34结合基序标签的分泌型亮氨酸拉链(Q2-RR12EE345L)和(2)串联的带环状CD20模拟表位标签的捕获亮氨酸拉链(R2-EE12RR345LCD28-9cδ)的载体对C1498细胞进行双重转导。接下来,用CD34磁珠对细胞进行磁性分选。随后,在补体存在下将细胞与抗体一起孵育。如图19所示,分开的CD20和CD34结合结构域使得能够进行选择性磁性分选和抗体介导的耗竭。
实施例5-包含突变体膜结合多肽的亮氨酸拉链细胞分选系统
突变体阻断亮氨酸拉链增加了分泌型亮氨酸拉链的捕获和呈递,但是可以显示增加的细胞外配对模式(“表面涂染”(“Surface Painting”))。在阻断亮氨酸拉链的“g”残基中进行了一系列突变,以减少捕获亮氨酸拉链与连接的阻断亮氨酸拉链之间的异二聚化亲和力。产生以下六个突变体:1N突变体:E1R2EE345L(氨基酸序列如SEQ ID NO:98所示),1M突变体:RR123E45L(氨基酸序列如SEQ ID NO:99所示),2N突变体:EE12345L(氨基酸序列如SEQ ID NO:102所示),2M突变体:RR1234E5L(氨基酸序列如SEQ ID NO:103所示),3N突变体:EE12R3E45L(氨基酸序列如SEQ ID NO:106所示)和3C突变体:RR12345L(氨基酸序列如SEQ ID NO:107所示)。
用FLAG-RR12EE345L GFP载体和六个突变体之一作为RR12EE345L接头EE12RR345LBFP载体构建体的一部分共同转导C1498细胞。如图20所示,3N突变体使分泌型亮氨酸拉链的呈递增强。3N突变体不仅在双重转导的细胞中显示出增加的FLAG结合(细胞内配对),还在单转导的仅捕获亮氨酸拉链的细胞中显示出增加的FLAG结合(细胞外配对)。EE12RR345L用于捕获和阻断亮氨酸拉链的对称使用导致单转导细胞和双转导细胞均强烈捕获FLAG拉链。因此,在“g”位残基处突变RR12EE345L亮氨酸拉链以包括排斥性氨基酸相互作用,可以降低通过基于连接的RR12EE345L的突变体亮氨酸拉链的阻断程度。
实施例6-亮氨酸拉链细胞分选系统,其包含功能化的膜结合多肽
CD80(B7-1)分子被功能化以呈现阻断的捕获亮氨酸拉链,从而允许用FLAG-RR12EE345L亮氨酸拉链进行磁性分选。用编码(a)FLAG-RR12EE345L iCaspase9 CD19-myc-CAR和(b)RR12EE345L接头EE12RR345L CD80 CD20-streptag-CAR的载体转导T细胞。接下来,用抗FLAG磁珠对细胞进行磁性分选。如图21A所示,分选的细胞对CD19和CD20 CAR(分别为Myc,Streptag)和CD80功能化的亮氨酸拉链显示出高纯度。如图21B所示,表达RR12EE345L接头EE12RR345L CD80的T细胞在培养物中形成缀合物并结合至可溶性CD28-Fc。
本公开的主题的实施方式
从前面的描述中将显而易见的是,可以对本公开的主题进行变型和修改以将其应用于各种用途和条件。这样的实施方式也在所附权利要求的范围内。
本文述及的任何变量定义中的元素列表包括将变量定义为列出的元素的任何单个元素或组合(或子组合)。本文述及的实施方式包括将该实施方式作为任何单一实施方式或与任何其它实施方式或其部分相结合。
本说明书中提到的所有专利和出版物都以相同的程度并入本文以供参考,就如同每个独立的专利和出版物都被具体单独地指出以并入以供参考一样。
- 流式细胞术细胞分选系统及其使用方法
- 细胞分选系统及使用方法
