一种双层微流控芯片、检测新型冠状病毒的试剂盒及方法
文献发布时间:2023-06-19 11:37:30
技术领域
本发明属于病毒检测技术领域,涉及一种用于病毒核酸检测的双层微流控芯片及试剂盒和方法。
背景技术
冠状病毒是一个大型病毒家族,已知可引起感冒以及中东呼吸综合征(MERS) 和严重急性呼吸综合征(SARS)等较严重疾病。新型冠状病毒是以前从未在人体中发现的冠状病毒新毒株。新型冠状病毒的确诊需通过核酸检测,呈阳性才能确诊。目前使用实时荧光定量PCR方法检测核酸呈现较高的假阴性率,会使很多已经感染的患者误以为还没有感染,进而造成更大范围的人传人感染。因此,为了更好的控制新型冠状病毒疫情,急需使用新的检测方法降低核酸检测的假阴性率。标记技术,从而达到2019新型冠状病毒核酸的快速、灵敏、准确检测。
RdRP基因、E基因是2019新型冠状病毒(2019-nCoV)特异性最高的两种基因,也是目前2019新型冠状病毒(2019-nCoV)常规检测试剂盒中最常被检测的两种基因。自2020年初通过对2019新型冠状病毒(2019-nCoV)的全基因组序列测序得出。2019新型冠状病毒(2019-nCoV)的RdRp基因含有98个RNA碱基,位于全序列的中端;E基因含有112个RNA碱基,位于全序列的末端。
现有的新型冠状病毒检测试剂盒在检测中存在准确率低,假阳性和假阴性率高等问题,并且检测过程耗时,不能满足快速检测的需要。
发明内容
本发明的目的是提供一种能够快速、简便、准确的检测血浆中新型冠状病毒(2019-nCoV)RdRP基因和E基因的微流控芯片、试剂盒,以及检测新型冠状病毒(2019-nCoV)含量的方法。
本发明解决其技术问题首先提供了一种双层微流控芯片,该芯片包括加样层和检测层,所述加样层上设有至少两个加样口;所述检测层上设有检测腔、出样口;所述检测腔与所述加样口通过进样微流道连接;所述出样口与所述检测腔通过出样微流道连接。
作为本发明的一种优选方式,每个加样口与检测腔之间连接一条进样微流道。
进一步优选地,所述双层微流控芯片设置10-50个检测单元。
为了解决本发明的技术问题,本发明还提供一种检测新型冠状病毒的试剂盒,包括所述的双层微流控芯片、含有RdRP基因荧光探针及E基因荧光探针的检测溶液、冠状病毒标准溶液、纳米材料溶液和阳离子溶液。
进一步优选地,所述含有RdRP基因荧光探针及E基因荧光探针的检测溶液由缓冲液、0.5~21μM的3’端荧光分子标记的RdRP基因荧光探针及E基因荧光探针混合而成。
进一步优选地,所述的纳米材料选自纳米金颗粒、纳米石墨烯或纳米氧化石墨烯材料、纳米硫化钨、纳米硒化钨中的任一种,其溶液浓度为2~50ug/mL。
进一步优选地,所述阳离子溶液中,各组分的浓度为:2.5mM氯化镁,0.5mM 氯化钙,0.5mM氯化钠,0.05mM硝酸钠,0.05mM磷酸氢钠,0.01mM氯化铁,0.01mM硫酸铜,0.01mM硫酸锌,0.01mM氯化钴,0.01mM氯化锰。
进一步优选地,所述冲洗液为浓度0.05%的柠檬酸钠溶液。
本发明进一步提供了一种检测新型冠状病毒的方法,包括:
(1)从其中一个加样口注入含有RdRP基因荧光探针及E基因荧光探针的检测溶液、纳米材料溶液、阳离子溶液到检测腔中,此时DNA探针被纳米材料吸附,荧光淬灭;
(2)将冠状病毒待测溶液从另一个加样口注入,使其进入到检测腔中;
(3)将芯片置于室温~60℃孵育5~40分钟后,对检测腔中的荧光信号进行检测,并记录荧光值;
(4)根据病毒标准溶液梯度浓度及荧光强度,计算标准线性回归方程;
(5)将测定的待测溶液的荧光强度,代入所述的标准线性回归方程,计算出待测溶液中新型冠状病毒基因的浓度。
本发明提供的另一种检测新型冠状病毒的方法,包括:
(1)从不同的加样口分别注入含有RdRP基因荧光探针及E基因荧光探针的检测溶液和冠状病毒待检测溶液,两种溶液进入到检测腔中,在室温~60℃孵育 5~40分钟;
(2)将纳米材料溶液从加样口注入,使其进入到检测腔中;
(3)对检测腔中的荧光信号进行检测,并记录荧光值;
(4)根据病毒标准溶液梯度浓度及荧光强度,计算标准线性回归方程;
(5)将测定的待测溶液的荧光强度,代入所述的标准线性回归方程,计算出待测溶液中新型冠状病毒基因的浓度。
本发明的有益效果是:本发明采用了封闭的双层微流控芯片检测体系,不同的物品或试剂从不同的加样口加入,减少交叉污染,能减少外界核酸带来的污染干扰。本发明的试剂盒采用纳米技术与微流控技术相结合,对新型冠状病毒 (2019-nCoV)进行检测,能够在1小时内获得检测结果,特异性强,灵敏度高。本发明将含有RdRP基因及E基因荧光探针的检测溶液、待测样本、阳离子溶液、冲洗液在一个检测单元中进行检测,过程一步完成,反应过程完全封闭,既能减少实验操作步骤,节省时间,同时还避免了开盖操作可能带来的样本污染。
本发明所使用的探针为3’端CY3标记的荧光探针,即单链时荧光基团发出的荧光被纳米材料吸收;但待测物出现与探针发生杂交反应后报告基团就可释放出荧光,被荧光计检测到。因此本发明不仅可用于简单的定性检测,亦可用做样本具体含量的定量检测。
附图说明
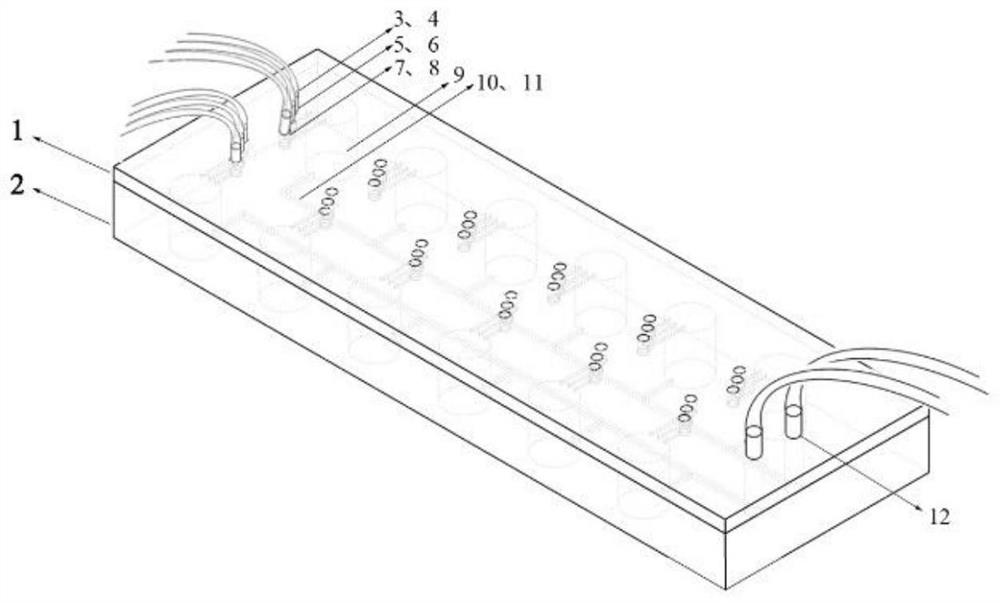
图1为本发明实施例的核酸检测双层微流控芯片的结构示意图;
图2为图一的分解图;
图3为本发明实施例的核酸检测双层微流控芯片的结构正视图;
图4为加样层结构示意图;
图5为检测层结构示意图;
图6为RdRp基因样本浓度与荧光强度的线性回归方程;
图7为E基因样本浓度与荧光强度的线性回归方程;
图8为不同浓度冠状病毒标准溶液实际检测水平与理论预测水平对比。
具体实施方式
为了便于理解本发明,下面结合附图和具体实施例,对本发明进行更详细的说明。附图中给出了本发明的较佳的实施例。但是,本发明可以以许多不同的形式来实现,并不限于本说明书所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
本发明的提供的第一个实施例是:一种双层微流控芯片,如图1-3所示,该芯片由加样层1和检测层2组成。加样层1主要作用是用来加入DNA探针、待测样品和其他试剂;检测层2主要是用来提供反应容器、及反应后检测反应物的荧光信号。
如图1所示,在一个双层微流控芯片上设有12个检测单元,其中,如图4 所示,每一个检测单元包括:加样层1上设有3个加样口,分别为第一加样口3、第二加样口5和第三加样口7。每个加样口分别连接一条进样微流道,分别是第一微流道4、第二微流道6和第三微流道8。这3条微流道之间相互独立,通过各自的加样口加入样本,可以避免交叉污染。
如图5所示,在检测层2上设有检测腔9、出样口12和出样微流道11。加样层1上的3条微流道均与检测腔9连接。通过3个加样口及相应的微流道,可将检测试剂、样本注入到检测腔9中。
如图1-3所示,每一个检测单元的出样微流道11与出样主流道10连接,主出样主流道10再与出样口12连接。
本实施例的双层微流控芯片,制做材料为聚二甲基硅氧烷(PDMS)和与之配对的固化剂,按照10:1比例混合,制备而成。
本实施例的双层微流控芯片的工作原理为:首先从第二进样口5,第三进样口7和第二流道6、第三微流道8分别注入CY3修饰的DNA探针(激发波长在532 nm,发绿光)、纳米材料溶液到检测腔9中,此时DNA探针已经被纳米材料吸附,荧光淬灭。
5分钟后,从第一进样口3和第一微流道4注入5μL待检测样本,使其进入到检测腔9。
将芯片置于60℃孵育30分钟后,用光谱仪532nm激发波长对微流控芯片的荧光信号进行检测。
检测完成后可通过出样主流道、出样微流道11和出样口12对检测腔9进行冲洗,达到检测腔9反复使用的目的。
需要说明的是,本实施例中,加样层1上的加样口至少要有2个,一个用来加入待测样本,另一个用来加入检测试剂,例如:DNA探针溶液、纳米材料或其他试剂等。可以增加一个加样口作为备用加样口。
本发明提供的第二个实施例是:一种检测新型冠状病毒的试剂盒,该试剂盒中含有:上述实施例中提供的双层微流控芯片、检测溶液、阳离子溶液、冠状病毒标准溶液、冲洗溶液等。
检测溶液由缓冲液、0.5~21μM的3’端荧光分子标记的RdRP基因荧光探针及E基因荧光探针混合而成。其中,RdRP基因荧光探针及E基因荧光探针等比例混合。
纳米材料溶液为选自纳米金溶液、纳米石墨烯溶液,纳米氧化石墨烯溶液,纳米硫化钨、纳米硒化钨溶液中的任一种,其浓度为2~50ug/mL。
RdRP基因及E基因DNA探针:
根据中国科学院武汉病毒研究所公布的2019新型冠状病毒(2019-nCoV)全基因组序列和各特异性基因的序列为模板设计、合成,其序列、位置见表1。
表1:DNA探针序列、位置
新冠病毒标准品:合成与DNA荧光探针完全互补的RNA序列作为冠状病毒特异性基因的标准品,如表2所示。使用时,配置成系列梯度浓度标准溶液。
表2:互补RNA序列、位置
阳离子溶液中,各组分的浓度为:2.5mM氯化镁,0.5mM氯化钙,0.5mM氯化钠,0.05mM硝酸钠,0.05mM磷酸氢钠,0.01mM氯化铁,0.01mM硫酸铜, 0.01mM硫酸锌,0.01mM氯化钴,0.01mM氯化锰。溶剂为去离子水。
冲洗液由0.05%柠檬酸钠组成。
本实施例试剂盒中,双层微流控芯片的制作过程如下:
首先设计微流控芯片结构,并制成芯片模板,然后按以下步骤制备微流控芯片:
(1)PDMS的配置:将PDMS本体与固化剂以质量比10:1的比例混合,搅拌均匀后产生大量气泡,置于真空干燥桶中抽真空去除气泡。
(2)PDMS倒模和固化:将硅片固定在倒模夹具上,将抽真空后的PDMS 倒入模具内,将模具整体置于80℃烘箱中1h固化。
(3)剥离打孔:PDMS固化后将其从模具上剥离,使用打孔器在PDMS芯片流道的进出口位置垂直打孔。
(4)清洗:将打好孔的PDMS芯片浸泡于异丙醇中,超声清洗2min后吹干,备用。
(5)双层芯片的键合:使用光学对准平台将双层芯片的结构对齐,使用夹具固定后置于80℃烘箱中1h键合。
本发明提供的第三个实施例是:采用上述试剂盒,检测新冠病毒的方法,具体包括:
1、标本制备
将冠状病毒标准溶液配制成不同浓度的溶液作为待测溶液,检测荧光值,用于计算标准线性方程。
2、检测
(1)从其中一个进样口注入5μL浓度为1μM含有RdRP基因荧光探针及E 基因荧光探针的检测溶液、10μL阳离子溶液、10μL浓度为25ug/mL的纳米材料溶液到检测腔中;
(2)将5μL冠状病毒待测溶液从另一个加样口注入,使其进入到检测腔中;
(3)将芯片置于室温孵育30分钟后,使用光谱仪对微流控芯片的荧光信号进行检测,并记录荧光值;
(4)根据冠状病毒标准溶液梯度浓度及荧光强度,计算标准线性回归方程: RdRP基因Y=0.5003(lgX)+3.265(R
3、结果判断
将测量的冠状病毒待测溶液的荧光强度带入相应的线性回归方程,推算出对应的基因浓度,从而实现对冠状病毒的定量检测。
本实施例的方法,单链探针荧光基团发出的荧光被纳米材料吸收;当待测溶液中存在目标物质时,目标物质与探针发生杂交反应后报告基团就可释放出荧光,被荧光计检测到。检测到的荧光强度与目标物质的浓度呈线性关系。
本发明提供的第四个实施例是:检测新冠病毒的方法,大体步骤与实施例三相同,其中的检测步骤2还可以采用另一种方法,具体为:
(1)从其中一个进样口注入5μL浓度为1μM含有RdRP基因荧光探针及E 基因荧光探针的检测溶液、15μL阳离子溶液;将5μL冠状病毒待测溶液从另一个加样口注入,使其进入到检测腔中;将芯片置于60℃孵育30分钟;
(2)从加样口将12μL浓度为20ug/mL的纳米材料溶液注入到检测腔中;
(3)使用光谱仪对微流控芯片的荧光信号进行检测,并记录荧光值;
(4)根据病毒标准溶液梯度浓度及荧光强度,计算标准线性回归方程:RdRP 基因Y=0.5003(lgX)+3.265(R
本实施例的方法,先将荧光探针与待测溶液孵育,待测溶液中存在目标物质时,目标物质与探针发生杂交反应后报告基团就可释放出荧光,其中未被结合的单链探针也会发出荧光。此时加入纳米材料溶液,未被结合的单链探针的荧光被纳米材料吸收,荧光淬灭;剩下的全部是双链发出的荧光,从而被荧光计检测到。检测到的荧光强度与目标物质的浓度呈线性关系。
图8为不同浓度冠状病毒标准溶液实际检测水平与理论预测水平对比,通过该图可知,采用本发明提供的试剂盒和方法检测新型冠状病毒,准确率较高,并且检测耗时短,快速。
- 一种双层微流控芯片、检测新型冠状病毒的试剂盒及方法
- 一种微流控检测芯片及基于其的试剂盒、全血多指标检测方法和应用
