一种两亲性木聚糖载体及其制备方法
文献发布时间:2023-06-19 11:47:31
技术领域
本发明属于药物制剂技术领域,具体涉及一种具有一定结肠靶向性能的两亲性木聚糖载体及其制备方法。
背景技术
木聚糖是半纤维素的主要成分,是生物质废物中存在的最丰富的生物聚合物之一。木聚糖的特征结构普遍含有D-木糖主干,由β-(1→4)糖苷键连接。根据各种资料表明,该主干可以被各种糖单位和侧基取代,如阿拉伯糖、葡萄糖醛酸和乙酰基等。木聚糖结构式如下:
由于木聚糖具有抗氧化、生物相容性、无毒和生物可降解性等优点,木聚糖在医药领域的应用引起了人们的极大关注。据报道,木聚糖在胃和小肠中不能被降解,因为在其降解过程中需要人类结肠微生物菌群产生的特定酶。该特性使木聚糖具有应用于结肠特异性药物输送系统的潜在特性。然而,市售的木聚糖由于其提取来源和方法的不同通常表现出不同的水溶性,不能很好地将药物嵌入或与之形成复合物。
为了解决上述问题,可以对木聚糖进行改性。目前对木聚糖改性的方法主要集中在将具有活性的基团接枝到木聚糖上[CN108079001A],或者制备成水凝胶[CN111961230A]来实现药物或生物大分子的递送。或者将木聚糖改性后增强木聚糖自身的药用活性[CN110698594A,CN111961144A]。
两亲性化合物由亲水端和疏水端共同组成,其在水中可以自组装成为胶束,疏水端的空腔可以与各种疏水性药物相互作用并稳定在水溶液中,而亲水端则可以保护药物免受外环境的影响。对木聚糖进行改性合成两亲性化合物的研究较少。Qin等人将木聚糖与胆固醇酯化后负载阿霉素以注射给药的方式抑制肿瘤生长(Y.Qin,et al.ACS BiomaterialsScience&Engineering,2020,6(3),1582-1589)。Sauraj等人提出将木聚糖和姜黄素通过双硫键结合在一起,负载5-氟尿嘧啶,通过姜黄素与5-氟尿嘧啶的共同作用提高对人结肠直肠癌细胞的毒性(Sauraj,et al.Materials Science and Engineering:C,2020,107,110356)。该两亲性化合物药物包封率低,制备技术难度高。上述两亲性化合物都对亲脂端的要求苛刻,制备成本高,并且合成流程复杂。所以开发一种亲脂端易获得,制备流程简单,制备成本低,药物包封率高的木聚糖载体具有迫切的必要性。目前还未有木聚糖与饱和脂肪酸酯化后,作为两亲性载体负载药物的报道。
发明内容
针对现有木聚糖不宜作为药物载体等的问题,本发明的目的在于提供一种以木聚糖为骨架的两亲性木聚糖载体的制备方法,所制备的两亲性木聚糖载体具有较高的药物负载能力,能提高难溶性药物的溶出度,保护药物不受胃肠道生理环境的影响,具有将药物被靶向运送到结肠的潜力,并且能提高药物的生物利用度,可用于运载治疗结肠炎、结肠癌等药物。
本发明所述的一种两亲性木聚糖载体的制备方法,其特征包括以下步骤:
(1)木聚糖与氢氧化钠溶液在反应温度为20~40℃下进行碱化反应25~40分钟,得到碱化木聚糖反应液;
(2)将步骤(1)中的碱化木聚糖反应液的温度升至65~85℃,加入氯乙酸钠进行反应70~90分钟,得到反应体系;
(3)用稀醋酸将步骤(2)中的反应体系pH值调节至中性,加入无水乙醇使反应体系中的产物沉淀,所得沉淀物先用95%乙醇洗涤,再将沉淀物溶解于蒸馏水中,用透析袋于去离子水环境中透析2~4天,所得溶液冷冻干燥,获得羧甲基木聚糖(简称为CX);
(4)取部分步骤(3)的羧甲基木聚糖溶于去离子水中,并用NaOH溶液调节pH值至7.5~8.5;同时将H
B——每克羧甲基木聚糖消耗的H
Mr
M——配置的H
V——滴定所消耗的H
m——称取的羧甲基木聚糖的质量,单位g;
0.132(g/mmol)为一个木糖单位的摩尔质量;
0.08(g/mmol)为每取代一个羧甲基,一个木糖单位质量的净增加量;
(5)以二甲基亚砜为反应介质,使用N,N'-二异丙基碳二亚胺和4-二甲氨基吡啶活化脂肪酸,活化反应温度为60~80℃,反应时间为4~8小时,得到反应体系;
(6)将步骤(3)中的羧甲基木聚糖和对甲基苯磺酸加入DMSO中预溶解得混合溶液,将混合溶液加入到步骤(5)所得的反应体系中,于反应温度为20~40℃下反应24~48小时,得反应体系;
(7)将步骤(6)所得的反应体系中加入无水乙醇得到沉淀,沉淀复溶于DMSO中,用200Da的透析袋,去离子水环境中透析2~4天,所得溶液冷冻干燥,获得产物两亲性木聚糖载体。
进一步地,本发明还限定了步骤(1)中的NaOH溶液的质量分数为20-30%,优选为25%,木聚糖与NaOH溶液中NaOH的摩尔比为1:0.5~4。
进一步地,本发明还限定了步骤(1)中木聚糖和步骤(2)中加入的氯乙酸钠的摩尔比为1:2~4。
进一步地,本发明还限定了步骤(3)中的稀醋酸的质量分数为4-6%,优选为5%。
进一步地,本发明还限定了步骤(4)中的羧甲基木聚糖溶液用NaOH溶液调节pH至7.8;用H
进一步地,本发明还限定了步骤(4)中的NaOH溶液质量分数为1-5%,优选为2%;H
进一步地,本发明还限定了步骤(4)中测得羧甲基木聚糖单元分子量范围为0.140~0.196g/mmol。
进一步地,本发明还限定了步骤(5)中的脂肪酸为C5-C18脂肪酸,优选为壬酸、肉豆蔻酸。
进一步地,本发明还限定了步骤(5)中脂肪酸和N,N'-二异丙基碳二亚胺的摩尔比为1:0.5~2,脂肪酸和4-二甲氨基吡啶的摩尔比例为1:0.002~0.1,脂肪酸与反应介质摩尔比例为1:14~25。
更进一步地,本发明还限定了步骤(6)中羧甲基木聚糖和步骤(5)中脂肪酸摩尔为1:0.5~6;羧甲基木聚糖和对甲基苯磺酸的摩尔比例为1:0.5~3。
通过采用上述技术,与现有技术相比,本发明的有益效果如下:
1)本发明涉及一种两亲性两亲性木聚糖载体制备方法,具有反应温度低,条件温和;步骤简短、操作简便;反应介质毒性小,污染少;透析法除杂质,纯化简单;冷冻干燥法除水,产物稳定;反应物和催化剂常见易得,反应成本低等优点,适于工业化推广应用;
2)亲水性的羧甲基木聚糖形成的外壳保护药物不受胃肠道生理环境的影响,如10-羟基喜树碱(HCPT)作为一种强效抗肿瘤药物,由于其内在结构不稳定、溶解度差、在胃肠道环境中易开环产生全身毒性。本发明可以降低此类药物毒性,拓展其应用途径;
3)本发明可以使药物释放能力增强,同时提高了药物在体内的生物利用度;
4)本发明工艺上具有条件温和、操作简便、污染少、纯化简单、产物稳定、成本低等优势,所制备的两亲性载体既能解决部分药物难以口服给药的问题,提高了药物的释放能力和生物利用度,又具有优良的药物负载能力和靶向给药的能力,载体无需与原药反应。因此,本发明具有显著的技术进步。
附图说明
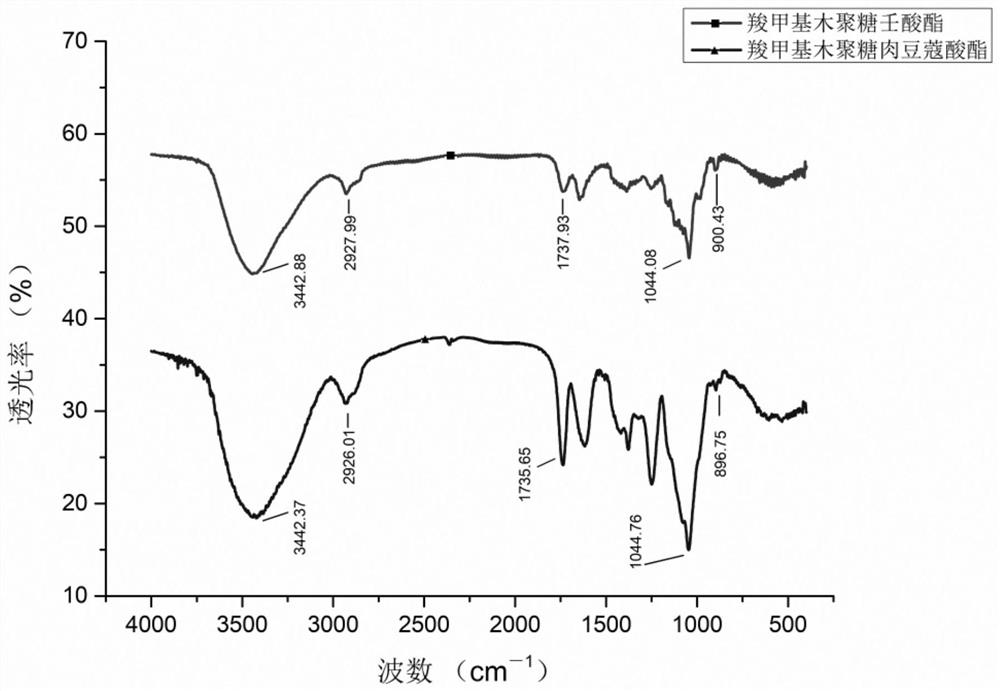
图1为实施例1-2所得的两种产物的红外谱图(下图为实施例1,上图为实施例2);
图2为不同的pH环境下,HCPT负载在羧甲基木聚糖壬酸脂上后的释放量;
图3为不同浓度羧甲基木聚糖壬酸的HepG-2细胞毒性图(a);羧甲基木聚糖壬酸负载HCPT固体分散体(HCPT-SD)与HCPT原料药的HepG-2细胞毒性图(b);
图4为HCPT原料药和羧甲基木聚糖壬酸负载HCPT固体分散体(HCPT-SD)的血药浓度曲线。
具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
实施案例1:
(1)0.66g木聚糖与3.0ml20%浓度的氢氧化钠溶液进行碱化反应,木聚糖与溶液中NaOH摩尔比为1:3,反应温度为25℃,反应时间为30分钟;将反应温度提高到至70℃后,加入17.5g氯乙酸钠进行反应。体系中木聚糖与氯乙酸钠的摩尔比为1:3,反应时间为75分钟,得到反应体系;
(2)用4%的稀醋酸将步骤(1)得到的反应体系pH值调节至中性,用15ml无水乙醇沉淀产品,沉淀用95%乙醇洗涤四次后,将沉淀溶解在10ml蒸馏水中,去离子水环境中透析4天,所得溶液在冷冻干燥,获得羧甲基木聚糖(简称CX);
(3)将0.2g CX溶于50ml去离子水中,使用2%NaOH溶液调节溶液的pH值至8.3;H
B——每克羧甲基木聚糖消耗的H
Mr
M——配置的H
V——滴定所消耗的H
m——称取的羧甲基木聚糖的质量,单位g;
0.132(g/mmol)为一个木糖单位的摩尔质量;
0.08(g/mmol)为每取代一个羧甲基,一个木糖单位质量的净增加量;
经计算得到羧甲基木聚糖单元的分子量Mr
(4)使用0.76gN,N'-二异丙基碳二亚胺(DIC)和0.037g4-二甲氨基吡啶(DMAP)活化2.3g肉豆蔻酸,肉豆蔻酸和DIC的摩尔比例为1:1.2,和DMAP的摩尔比例为1:0.006,DMSO体积为20ml,反应温度为65℃,反应时间为5小时;
(5)0.93g CX和1.72g对甲基苯磺酸在10ml DMSO中预溶解,CX和对甲基苯磺酸的摩尔比例为1:2,将混合溶液加入到上述反应体系中进行反应,反应温度为30℃下,反应时间为24小时;
(6)上述反应结束后,向反应体系中加入40ml无水乙醇得到沉淀,沉淀复溶于10mlDMSO中,用200Da的透析袋,去离子水环境中透析4天。所得溶液冷冻干燥,获得最终两亲性产物:羧甲基木聚糖肉豆蔻酸酯,其红外谱图如图1所示,3442.37cm
实施案例2:
(1)0.66g木聚糖与2.7ml 30%浓度的氢氧化钠溶液进行碱化反应,木聚糖与溶液中NaOH摩尔比为1:4,反应温度为40℃,反应时间为40分钟;将反应温度提高到至85℃后,加入2.33g氯乙酸钠进行反应,体系中木聚糖与氯乙酸钠的摩尔比为1:4,反应时间为90分钟;
(2)用6%的稀醋酸将上述中的反应体系pH值调节至中性,用15ml无水乙醇沉淀产品,沉淀用95%乙醇洗涤四次后,将沉淀溶解在10ml蒸馏水中,去离子水环境中透析4天。所得溶液在冷冻干燥,获得羧甲基木聚糖(CX);
(3)将0.2g CX溶于50ml去离子水中,使用2%NaOH溶液调节溶液的pH值至7.8,H
B——每克羧甲基木聚糖消耗的H
Mr
M——配置的H
V——滴定所消耗的H
m——称取的羧甲基木聚糖的质量,单位g;
0.132(g/mmol)为一个木糖单位的摩尔质量;
0.08(g/mmol)为每取代一个羧甲基,一个木糖单位质量的净增加量;
经计算羧甲基木聚糖单元的分子量Mr
(4)使用1.3gN,N'-二异丙基碳二亚胺(DIC)和0.037g4-二甲氨基吡啶(DMAP)活化0.79g壬酸,壬酸和DIC的摩尔比例为1:2,脂肪酸和DMAP的摩尔比例为1:0.06,DMSO体积为25ml,反应温度为65℃,反应时间为8小时。
(5)0.97gCX和2.58g对甲基苯磺酸在10ml DMSO中预溶解,CX和对甲基苯磺酸的摩尔比例为1:3,将混合溶液加入到上述反应体系中进行反应,反应温度为40℃下,反应时间为40小时;
(6)上述反应结束后,向反应体系中加入40ml无水乙醇得到沉淀。沉淀复溶于10mlDMSO中,用200Da的透析袋,去离子水环境中透析4天。所得溶液冷冻干燥,获得最终两亲性产物:羧甲基木聚糖壬酸酯,其红外谱图图1所示,3442.88cm
(7)将10-羟基喜树碱(HCPT)作为模型药物负载到羧甲基木聚糖壬酸脂上,不同的pH环境下,HCPT负载在羧甲基木聚糖壬酸脂上后的释放量如图2所示,从图2的结果可以看出,在模拟胃和小肠(pH=1.2,pH=6.8)环境中,HCPT释放量很低(<12%);而在结肠模拟环境(pH=7.4)中,HCPT释放量达到40%以上,证明羧甲基木聚糖壬酸脂能使药物在胃和小肠之中保持稳定,并在结肠处开始释放。图3(b)说明HCPT通过羧甲基木聚糖壬酸脂载体的负载(HCPT-SD)相比纯HCPT显著提高其细胞毒性,并且图3(a)显示羧甲基木聚糖壬酸脂载体的浓度达到1000μg/ml,也没有表现出明显的细胞毒性,细胞存活率仍在90%以上,具有良好的生物相容性。图4中羧甲基木聚糖壬酸脂负载HCPT后的血药浓度-时间曲线下面积一直大于纯HCPT组,其峰浓度(C
最后说明的是,上述举例仅仅描述了本发明的技术方案,本发明并不被其限制。本领域内的普通技术人员可以对上述说明加以修改或增进,这些修改或增进都应属于本发明权利要求的保护范围内。
- 一种两亲性木聚糖载体及其制备方法
- 一种两亲性聚合物、其制备方法、复合纳米药物载体及其制备方法
