家禽类动物羽毛中喹诺酮类药物残留的检测方法
文献发布时间:2023-06-19 12:08:44
技术领域
本发明设计一种家禽类动物羽毛中喹诺酮类药物残留的检测方法药物残留检测方法。
背景技术
喹诺酮类药物是以4-喹诺酮(或称吡酮酸)为基本结构的合成类抗菌药。在4-喹诺酮母核的 N1、C5、C6、C7、C8,引入不同的基团形成各具特点的喹诺酮类药物。喹诺酮类药物其作用机理是作用于细菌的DNA螺旋酶,使细菌DNA不能形成超螺旋,染色体受损从而产生杀菌作用。其作用机理是作用于细菌的DNA螺旋酶,使细菌DNA不能形成超螺旋,染色体受损从而产生杀菌作用。喹诺酮类药物属于广谱抗菌药,被广泛应用于畜牧养殖中用于疾病防治。如果人长期过量使用含有喹诺酮类药物残留的动物源性食品,可能会产生药物积蓄作用,一方面可能会使人体产生耐药性,另一方面可能会有毒害作用,如引起患者肠胃不适;出现头晕、头疼和四肢麻木;出现过敏、皮疹、荨麻疹等;造成肝脏损伤等。因此,建立检测家禽类动物中喹诺酮类药物的检测方法是非常必要的。
在GB31650《食品安全国家标准食品中兽药最大残留限量》中规定,喹诺酮类药物在家禽类动物组织中最高残留限量为10-300μg/kg。目前,对喹诺酮类药物的检测多以动物内部组织测定为主,如肌肉、内脏、血液、尿液等,仪器多为气相色谱法、液相色谱法、气相色谱质谱联用仪法、液相色谱质谱联用仪法等。以上这些方法均有前处理复杂,假阳性率高,回收率低等问题。更为关键的是,其检测对象均是禽类动物身体内部,创伤性大,多为禽类处死后才进行检测,难以实现对兽药残留实时动态监测。家禽类动物摄入药物后,部分药物残留会保留在其羽毛中。毛发检测具有易采集、检测时限长、可反映用药信息等独特的优势。对本发明检测目标对象是禽类动物的羽毛,羽毛不仅方便获取,而且可以实现被检测动物长期活体动态监测。由于药物残留是在动物体内长期积蓄的过程,因此研究其含量在活体的变化过程具有重要意义。
静电场轨道阱-高分辨率质谱是近年来兴起的分析测试技术,其原理是被测物质离子化后进入轨道阱内,在电场作用下围绕中心做纵向和横向的往复运动,仪器记录其物质运动轨迹,通过傅里叶变换,测得精确质量数。其分辨率高达140000FWHM,可达到小于3ppm的质量精度,既保证了分析的可靠性,同时也兼顾了灵敏度和宽线性范围。
目前对禽类羽毛喹诺酮药物检测国内外尚未见报道
被测物质的物理化学性质:
恩诺沙星:Enrofloxacin,CAS:93106-60-6,分子式:C
环丙沙星:Oxociprofloxacin,CAS号:103237-52-1,分子式:C
沙拉沙星:Sarafloxacin,CAS:98105-99-8,分子式:C
发明内容
本发明旨在提供一种全新的检测家禽羽毛中喹诺酮药物残留的技术,它应用静电场轨道阱-高分辨率质谱技术,对目标物提取精确质量数对被测物进行定量测定,从而实现对喹诺酮类药物在家禽羽毛中的精确测定。本发明的方法具有如下优势:前处理简单、快速,回收率高、灵敏度高、稳定性和重现性好。
本发明提供一种检测家禽羽毛中喹诺酮药物残留的方法,含有如下步骤:
1)家禽羽毛的前处理,
2)液液萃取,
3)液相-高分辨率质谱联用检测。
其中,步骤1)中家禽羽毛的前处理包括清理和研磨。
其中,所述清理是用剪刀分别从被检测动物的颈部、翅部、尾部剪下羽毛,擦去表面污染物,冲洗羽毛,干燥,所述研磨是将干燥的羽毛弃去主梗,取纯羽毛部分剪成小段,研磨成细粉末状。
其中,所述清理是用剪刀分别从被检测动物的颈部、翅部、尾部剪下代表性羽毛2-3根,用无尘纸轻轻擦去表面污染物,依次用二级水、正己烷各冲洗羽毛2-3次,室温下晾干。
其中,所述研磨是将晒干的羽毛弃去主梗,取纯羽毛部分剪成长度小于5mm的小段,称取约500mg左右放入液氮研磨器中,加入研磨球,仪器预冷3分钟后,以15次/秒的频率研磨2分钟,静置70秒后取出,将羽毛研磨成细粉末状,如果有未粉碎的残渣,也可重复上述步骤1到2次,直至研磨彻底充分。
其中,步骤2)中所述液液萃取的萃取溶剂为乙腈、乙酸乙酯、甲醇。
其中,步骤2)中所述液液萃取的萃取溶剂为乙腈或甲醇。
其中,步骤2)中所述液液萃取的萃取溶剂为乙腈。
其中,步骤2)中所述液液萃取含有如下步骤:称取研磨后的羽毛,于离心管中,加入萃取溶剂,涡旋提取,超声,使用离心机离心,取上清液过微孔滤膜后氮气吹干,用乙腈水混合溶液复溶,得到供步骤3)上机测定的样品。
其中,步骤2)中所述液液萃取含有如下步骤:称取研磨后的羽毛100mg左右,于10mL 离心管中,加入5mL萃取溶剂,涡旋提取1分钟,超声5min后,使用离心机在4℃在10000g/min 的离心力下离心3分钟,取全部上清液过0.22μm微孔滤膜后氮气吹干,用200μL乙腈水混合溶液(v/v=1:3)复溶,得到供步骤3)上机测定的样品。
其中,步骤3)中所述液相-高分辨率质谱联用检测所用的检测器为静电场轨道阱-高分辨率质谱检测。
其中,步骤3)中所述液相的色谱条件为:waters ACQUITY BEH C18 1.7μm,2.1*100mm;色谱柱温度:35℃;流动相A:0.1%甲酸水溶液(V/V);流动相B:0.1%甲酸乙腈溶液(V/V);梯度洗脱,洗脱条件:0-2分钟,10%B;2-7分钟,线性升高至95%B;7-9分钟,线性降低至10%B,9-10分钟,10%B。流速为0.3mL/分钟,进样量为2μL。
其中,步骤3)中所述质谱的质谱条件为:电喷雾离子源(high electrosprayionization, HESI);电喷雾电压Spray Voltage:3500V;毛细管温度CapillaryTemperature 350℃;鞘气 Sheath Gas:35arb;碰撞能CE:30;
辅助气Aux Gas:15arb;辅助加热温度Pro Heater Temp:300;S-lens RF level:50。
扫描模式:
正模式全扫描/实时二级质谱扫描Full MS/dd MS2模式,一级全扫描(m/z50-750)分辨率70000,二级扫描(dd-MS2)分辨率17500。
本发明的有益效果如下:
1、在添加水平为2μg/kg、10μg/kg、100μg/kg三水平下,恩诺沙星、环丙沙星、沙拉沙星三种被测物质的方法回收率可达到90%以上,精密度标准方差在10%之内,符合生物样品检测方法的方法学要求。
2、本方法的方法检出限恩诺沙星、环丙沙星、沙拉沙星均为2μg/kg。
附图说明
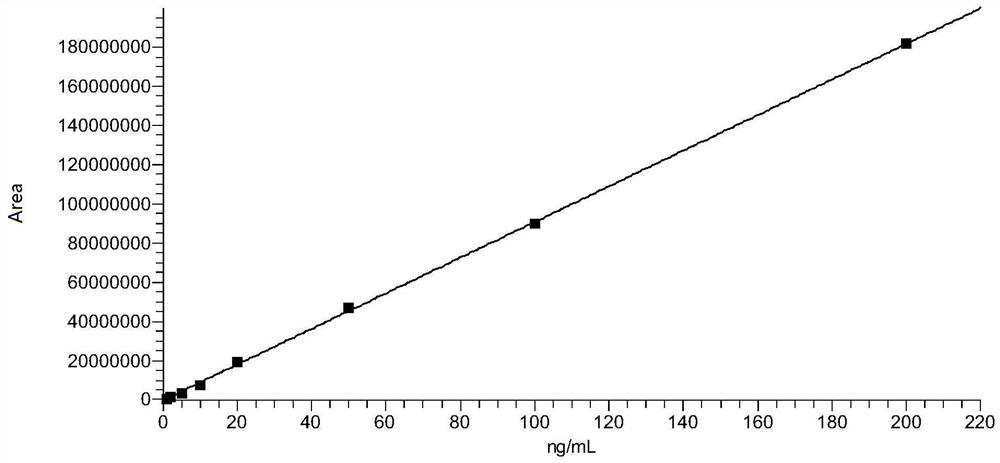
图1、恩诺沙星标准工作曲线
图2、环丙沙星标准工作曲线
图3、沙拉沙星标准工作曲线
图4、空白样品中恩诺沙星、环丙沙星、沙拉沙星质谱提取流图
图5、加标样品中恩诺沙星、环丙沙星、沙拉沙星质谱提取流图
图6、恩诺沙星二级质谱图
图7、环丙沙星二级质谱图
图8、沙拉沙星二级质谱图
具体实施方式
第一部分家禽类动物羽毛中喹诺酮类药物的检测方法
1.实验部分
1.1.实验材料
1.1.1.标准品和试剂
恩诺沙星、环丙沙星、沙拉沙星标液购自天津阿尔塔公司,浓度均为100μg/mL。
甲醇、乙腈购自Merck公司,色谱纯
一级水、二级水均为Mliipore纯水制备系统制备
甲醇、乙腈、乙酸乙酯购自天津国药试剂公司,分析纯
0.22μm滤膜购自天津博纳艾吉尔公司
1.1.2.生物样品来源
羽毛采自石家庄市某养鸡场
1.1.3.标准溶液的配置
储备液的配置:分别移取1mL恩诺沙星、环丙沙星、沙拉沙星标液于10mL容量瓶中,加入甲醇定容至刻度。配置成三者浓度均为10μg/mL的三种物质混合储备液,再从混合储备液(下述内容中简称为混合储备液1)中取1mL定容至10mL,配置成三者浓度均为1μg/mL 的三种物质混合储备液(下述内容中简称为混合储备液2),4℃储存于冰箱中备用。
1.1.4.基质加标标准工作液的配置
在6个离心管中分别放入100mg左右研磨成细粉末状的空白羽毛(空白羽毛取自未服用过任何药物的鸡的羽毛),依次加入混合储备液2,使加入标准物质量(这里指恩诺沙星、环丙沙星、沙拉沙星各自的质量)达到0.2ng、0.4ng、1ng、2ng、4ng、10ng、20ng、40ng,然后加入5mL乙腈,涡旋提取1分钟,超声5min后,使用离心机在4℃在10000g/min的离心力下离心3分钟,取全部上清液过0.22μm微孔滤膜后氮气吹干,用200μL乙腈水混合溶液复溶,得到浓度分别为1ng/mL、2ng/mL、5ng/mL、10ng/mL、20ng/mL、50ng/mL、100ng/mL、 200ng/mL的基质加标标准工作液,现用现配。
1.2.仪器以及参考条件
静电场轨道阱-四极杆串联高分辨率质谱仪Q Exactive plus(美国赛默飞公司)
超高效液相色谱仪Ultimate3000(美国赛默飞公司)
电子天平BSA2245最小感量0.1mg(瑞士赛利多斯公司)
液氮冷冻研磨机YM-48LD(上海豫明仪器有限公司)
Millipore超纯水净化系统(美国密理博公司)
Wiggens涡旋震荡器Vortex3000(维根技术公司)
超声波清洗器KQ500E(昆山超声仪器有限公司)
高速离心机CT15RE,CR22N(日本日立公司)
移液枪(10μL,100μL,1000μL)(德国eppendorf公司)
1.3.样品制备方法
用剪刀分别从被检测动物的颈部、翅部、尾部剪下代表性羽毛2-3根,用无尘纸轻轻擦去表面污染物,依次用二级水冲洗羽毛2次、正己烷冲洗羽毛2次,室温下晾干。将晒干的羽毛剪成长度小于0.5cm的小段,称取约500mg左右放入液氮研磨器的4mL研磨罐中,加入研磨球,仪器预冷3分钟后,以35HZ的频率研磨5分钟,静置70秒后取出。将羽毛研磨成细粉末状,如果有未粉碎的残渣,重复上述步骤2次,直至研磨彻底充分。
液液萃取步骤:称取研磨后的羽毛100mg左右,加入5mL乙腈,涡旋提取1分钟,超声5min后,使用离心机在4℃在10000g/min的离心力下离心3分钟,取全部上清液过0.22μm 微孔滤膜后氮气吹干,用200μL乙腈水混合溶液(体积比1:9)复溶,进行液相-质谱联用检测。
1.4.仪器参考条件
1.4.1.液相色谱-四极杆-静电场轨道阱串联高分辨率质谱仪条件
色谱条件:
色谱柱:waters ACQUITY BEH C18 1.7μm,2.1*100mm;
色谱柱温度:35℃;
流动相A:0.1%甲酸水溶液(V/V);流动相B:0.1%甲酸乙腈溶液(V/V)洗脱程序:梯度洗脱
洗脱条件:0-3分钟,5%B;3-7分钟,线性升高至95%B;7-9分钟,线性降低至5%B,9-10 分钟,5%B。流速为0.3mL/分钟,
进样量2μL。
质谱条件:
电喷雾离子源(high electrospray ionization,HESI);
电喷雾电压Spray Voltage:3500V;
毛细管温度Capillary Temperature 350℃;
鞘气Sheath Gas:35arb;
辅助气Aux Gas:15arb;
辅助加热温度Pro Heater Temp:300;
S-lens RF level:50;
扫描模式:
正模式全扫描/实时二级质谱扫描Full MS/dd MS2;
一级全扫描(m/z50-750)分辨率70000;
二级扫描(dd-MS2)分辨率17500。
碰撞能(CE):30
表1恩诺沙星、环丙沙星、沙拉沙星理论精确分子量、加合精确分子量、二级子离子精确分子量
2.方法验证
按照1.3、1.4所述对样品进行前处理,仪器检测,对方法进行验证,验证包括方法线性范围、抗干扰性、灵敏度、回收率、精密度等指标。
2.1.线性范围
按照1.1.4配置成恩诺沙星、环丙沙星、沙拉沙星均为1ng/mL、2ng/mL、5ng/mL、10ng/mL、20ng/mL、50ng/mL、100ng/mL、200ng/mL系列基质加标标准工作溶液,各取2μL进样,以外标峰面积纵坐标(Y),以外标浓度为横坐标(X)进行线性回归,求得的恩诺沙星、环丙沙星、沙拉沙星三种物质的回归方程分别为恩诺沙星Y=-362124+909708*X,R
2.2.方法抗干扰性
取空白羽毛,加入一定量的恩诺沙星、环丙沙星、沙拉沙星,按照按照1.3、1.4所述对样品进行前处理,仪器检测,同时做空白对照试验,图谱见附图4和5,结果表明,在目标物出峰时间内,空白样品未出现明显色谱峰,表明方法不存在干扰。
2.3.方法回收率
取空白羽毛,加入一定量的恩诺沙星、环丙沙星、沙拉沙星,使其浓度达到2μg/kg、10μg/kg、100μg/kg三个水平,每个水平重复测定6次,按照按照1.3、1.4所述对样品进行前处理以及分析检测,测得添加样品中回收率结果见表2。
表2空白样品中添加恩诺沙星、环丙沙星、沙拉沙星的平均回收率(%)n=6
2.4.方法精密度
取空白样品,加入一定量的恩诺沙星、环丙沙星、沙拉沙星,使其浓度达到2μg/kg、10μg/kg、100μg/kg三个水平,按照1.3、1.4所述对样品进行前处理以及分析检测,每个水平每天重复测定6次,得到日内精密度,每个水平测定1次,连续测定6天,得到日间精密度,日内精密度和日间精密度见表3。结果表明:日内精密度在3.3%-10.2%之间,日间精密度在1.2%-9.6%之间,该方法重现性较好。
表3日内和日间精密度
2.5.方法灵敏度
取空白羽毛,加入一定量的恩诺沙星、环丙沙星、沙拉沙星,按照1.3、1.4所述对样品进行前处理以及分析检测,使其信噪比达到S/N=3,测得此时对应的样品添加浓度即为方法检出限为2μg/kg。
3.结果与讨论
3.1.提取方法的选择
萃取溶剂的选择,本发明比较了乙腈、乙酸乙酯、甲醇3种常用的萃取溶剂,取空白样品,加入一定量的恩诺沙星、环丙沙星、沙拉沙星,改变提取溶剂,其他条件不变,按照1.3、1.4 所述对样品进行前处理以及分析检测。通过考察回收率来比较不同提取溶剂的提取效果,结果见表4,乙腈、甲醇作为溶剂时的回收率较高,乙酸乙酯作为提取溶剂的回收率较低。考虑到甲醇毒性较大,最终选择乙腈作为提取溶剂。
表4空白样品中添加恩诺沙星、环丙沙星、沙拉沙星的回收率(%)n=3
3.2.标准溶液配置的选择
由于质谱检测中普遍存在基质效应,导致测定回收率时偏差较大,在制定本发明过程中,我们比较基质添加标线和有机溶剂直接配置标线对定量的区别。使用基质配标、乙腈配置恩诺沙星、环丙沙星、沙拉沙星分别为1ng/mL、2ng/mL、5ng/mL、10ng/mL、20ng/mL、50ng/mL、 100ng/mL、200ng/mL的系列标准溶液每个浓度点测定3次,比较相同浓度下峰面积的差异(纯溶剂配标和基质配标的同浓度峰面积之比平均值),见表5,经过比较发现基质效应较为明显,因此选择基质加标配置标线。
表5基质效应(基质配标和纯溶剂配标的同浓度峰面积之比,%)
3.3.质谱条件的选择
本发明将提取精确质量数的偏差设定在5ppm之内,应用精确分子量达到了定量的目的,在此基础上利用二级特征碎片离子进行辅助定性(二级特征碎片图谱见图6-8),最大程度的降低了质量偏差,有效降低了仪器噪音干扰以及杂质干扰以及假阳性的产生。
4.稳定性考察
恩诺沙星、环丙沙星、沙拉沙星可能随着储存时间对其稳定性的产生影响,因此需要考察其稳定性。
4.1.实验部分
4.1.1.纯溶液中稳定性考察
分别配置含1ng/mL、5ng/mL、50ng/mL的恩诺沙星、环丙沙星、沙拉沙星的乙腈溶液,每份3平行,置于冰箱中4℃储存,放置0,7,14,21,28,35天后按照按照1.4所述对样品进行分析检测。比较出峰面积大小差异,经比较,浓度无统计学意义(P>0.05),说明恩诺沙星、环丙沙星、沙拉沙星在冰箱中4℃储存条件下具有1个月以上稳定性。
4.1.2.基质加标溶液稳定性考察
用空白基质配置1ng/mL、5ng/mL、50ng/mL三个水平基质加标溶液,-20℃保存,分别放置24小时、48小时、72小时后,按照1.3、1.4所述对样品进行前处理以及分析检测,考察每次分析结果之间差异,结果表明浓度无统计学意义(P>0.05),说明三种物质在基质加标溶液中72小时具有稳定性。
5.结论
本发明建立了家禽类动物羽毛中喹诺酮类药物的检测方法,该方法回收率高、重现性好、特异性好。方法前处理简便、快速、廉价高效。该方法可用于家禽类动物药物残留量的活体动态监测。
恩诺沙星、环丙沙星、沙拉沙星在甲醇溶液、基质配置溶液中具有较好的稳定性。
实施例1:
应用本发明的方法对鸡羽毛中三种兽药残留进行检测
随机选择正常饲养的,未服用任何药物的健康白羽肉鸡5只(日龄35天,重量2kg左右),每日服用恩诺沙星、沙拉沙星各10mg(环丙沙星是恩诺沙星的代谢产物,因此不需要服用环丙沙星),持续服用5天,后终止服药,5天后宰杀,宰杀前取鸡身上羽毛按照上述方法进行检测,宰杀后取肌肉并应用SN/T1751.2-2007对鸡肉三种兽药残留进行对比检测,检测结果见下表。
表6三种喹诺酮类兽药残留检测结果对比
由表中数据可以得出,经过对比恩诺沙星和环丙沙星之和、沙拉沙星,发现羽毛检测与肌肉检测相比呈现正相关性,如果肌肉中沙星类药物残留量较高,则羽毛中药物残留量也较高。由此可见,该方法可用于对家禽类动物兽药残留的检测。
- 家禽类动物羽毛中喹诺酮类药物残留的检测方法
- 一种兽药中喹诺酮类药物残留的检测方法
