包封多核苷酸及使用方法
文献发布时间:2023-06-19 12:25:57
相关申请的交叉引用
本申请要求2018年11月13日提交的美国临时申请No.62/760,422的优先权,所述临时申请的内容以引用的方式整体并入本文中。
关于序列表的声明
与本申请相关的序列表以文本格式而非纸质副本形式提供,并据此以引用的方式并入本说明书中。含有序列表的文本文件的名称为ONCR_014_01WO_ST25.txt。文本文件为23KB,创建于2019年11月13日,并且通过EFS-Web以电子方式提交。
技术领域
本公开总体上涉及免疫学、炎症和癌症治疗领域。更具体地说,本公开涉及编码具有复制能力的病毒基因组的颗粒包封的多核苷酸。本公开还涉及例如癌症的增生性疾病的治疗和预防。
背景技术
溶瘤病毒是具有复制能力的病毒,其具有能够感染并溶解肿瘤细胞的溶菌生命周期(lytic life-cycle)。直接肿瘤细胞溶解不仅导致细胞死亡,而且还导致针对由局部抗原呈递细胞吸收并呈递的肿瘤抗原的适应性免疫应答的产生。因此,溶瘤病毒通过直接细胞溶解和促进能够在病毒清除后维持抗肿瘤应答的抗原特异性适应性应答来对抗肿瘤细胞的生长。
但是,具有复制能力的病毒的临床使用带来了一些挑战。通常,病毒暴露会激活先天免疫途径,从而导致广泛的非特异性炎症反应。如果患者以前未曾暴露于该病毒,则这种初始的先天免疫应答可导致适应性抗病毒应答的发展和中和抗体的产生。如果患者以前曾暴露于该病毒,则现有的中和抗病毒抗体可以阻止所需的溶解作用。在两种情况下,中和抗体的存在不仅阻止靶细胞的病毒溶解,而且使病毒治疗剂的重新施用无效。这些因素限制了病毒治疗剂在转移性癌症治疗中的应用,因为天然存在的抗病毒应答阻碍了治疗此类癌症所需的反复全身施用的功效。即使没有这类障碍,随后在未患病的细胞中进行病毒复制也会导致对周围细胞和组织的实质性疾病外附带损害。
在本领域中对与具有复制能力的病毒的治疗用途有关的组合物和方法仍然存在长期未满足的需求。本公开提供了这样的组合物和方法等等。
发明内容
本公开提供了编码自主复制型多核苷酸的DNA多核苷酸以及相关组合物和方法。在一些实施方案中,所述多核苷酸包含编码具有复制能力的病毒基因组的核酸序列,其中所述多核苷酸在通过非病毒性递送媒介物引入细胞中时能够产生具有复制能力的病毒。
在一些实施方案中,本公开提供了一种脂质纳米颗粒(LNP),所述脂质纳米颗粒包含重组DNA分子,所述重组DNA分子包含编码具有复制能力的病毒基因组的多核苷酸序列,其中所述多核苷酸序列可操作地连接于能够结合哺乳动物RNA聚合酶II(Pol II)的启动子序列并且侧接3'接合裂解序列和5'接合裂解序列,其中所述3'接合裂解序列和所述5'接合裂解序列属于不同类型,并且其中编码所述具有复制能力的病毒基因组的所述多核苷酸序列是非病毒来源的。
在一些实施方案中,3'接合裂解序列是核酶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是核酶序列并且5'接合裂解序列是人工miR(AmiR)靶序列。在一些实施方案中,3'接合裂解序列是微小RNA(miR)靶序列并且5'接合裂解序列选自核酶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是人工miR(AmiR)靶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、核酶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是向导RNA(gRNA)靶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、核酶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是pri-miR序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、核酶序列和适体酶序列。在一些实施方案中,3'接合裂解序列是适体酶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和核酶序列。
在一些实施方案中,具有复制能力的病毒基因组是单链RNA(ssRNA)病毒。在一些实施方案中,单链RNA(ssRNA)病毒是正义((+)-义)或负义((-)-义)ssRNA病毒。在一些实施方案中,具有复制能力的病毒基因组是(+)-义ssRNA病毒并且所述(+)-义ssRNA病毒是小核糖核酸病毒。在一些实施方案中,所述小核糖核酸病毒是塞内加谷病毒(Seneca ValleyVirus,SVV)或柯萨奇病毒(Coxsackievirus)。
在一些实施方案中,LNP与细胞接触引起细胞产生病毒颗粒,并且其中所述病毒颗粒是感染性的和溶解性的。
在一些实施方案中,重组DNA分子还包含编码外源有效载荷蛋白的多核苷酸序列。在一些实施方案中,LNP还包含编码外源有效载荷蛋白的第二多核苷酸序列。
在一些实施方案中,外源有效载荷蛋白是荧光蛋白、酶蛋白、细胞因子、趋化因子、细胞表面受体的配体或能够结合于细胞表面受体的抗原结合分子。在一些实施方案中,细胞因子选自IL-18、IL-36γ、LIGHT和IL-2。在一些实施方案中,细胞表面受体的配体是Flt3配体。在一些实施方案中,趋化因子选自CCL21、CCL5、CXCL10和CCL4。
在一些实施方案中,抗原结合分子能够结合和抑制免疫检查点受体。在一些实施方案中,免疫检查点受体是PD1。在一些实施方案中,抗原结合分子能够结合于选自DLL3、EpCam和CEA的肿瘤相关抗原。在一些实施方案中,抗原结合分子是包含对肿瘤抗原具有特异性的第一结构域和对T细胞表面分子具有特异性的第二结构域的双特异性T细胞衔接分子。在一些实施方案中,T细胞表面分子是CD3。
在一些实施方案中,微小RNA(miRNA)靶序列(miR-TS)盒被插入编码具有复制能力的病毒基因组的核酸序列中,其中所述miR-TS盒包含一种或多种miRNA靶序列,并且其中细胞中一种或多种相应miRNA的表达抑制具有复制能力的病毒基因组在细胞中的复制。在一些实施方案中,一种或多种miRNA选自miR-124、miR-1、miR-143、miR-128、miR-219、miR-219a、miR-122、miR-204、miR-217、miR-137和miR-126。在一些实施方案中,miR-TS盒包含miR-124靶序列的一个或多个拷贝、miR-1靶序列的一个或多个拷贝和miR-143靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-219a靶序列的一个或多个拷贝和miR-122靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-204靶序列的一个或多个拷贝和miR-219靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-217靶序列的一个或多个拷贝、miR-137靶序列的一个或多个拷贝和miR-126靶序列的一个或多个拷贝。
在一些实施方案中,重组DNA分子是包含编码具有复制能力的病毒基因组的多核苷酸序列的质粒。
在一些实施方案中,LNP包含阳离子型脂质、胆固醇和中性脂质。在一些实施方案中,所述阳离子型脂质是1,2-二油酰基-3-三甲基铵-丙烷(DOTAP),并且其中所述中性脂质是1,2-二月桂酰基-sn-甘油基-3-磷酸乙醇胺(DLPE)或1,2-二油酰基-sn-甘油基-3-磷酸乙醇胺(DOPE)。
在一些实施方案中,LNP还包含磷脂-聚合物缀合物,其中所述磷脂-聚合物缀合物是1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-聚(乙二醇)(DSPE-PEG)或1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-N-[氨基(聚乙二醇)](DSPE-PEG-胺)。
在一些实施方案中,所述阳离子型脂质是D-Lin-MC3-DMA(MC3)并且其中所述中性脂质是1,2-二硬脂酰基-sn-甘油基-3-磷酸胆碱(DSPC)。
在一些实施方案中,LNP还包含1,2-二肉豆蔻酰基-rac-甘油基-3-甲氧基聚乙二醇(DMG-PEG)的磷脂-聚合物缀合物。
在一些实施方案中,透明质酸缀合于LNP的表面。在一些实施方案中,RGD肽缀合于LNP的表面。
在一些实施方案中,本公开提供了一种治疗性组合物,所述治疗性组合物包含多个根据权利要求1-37中的任一项的脂质纳米颗粒,其中所述多个LNP具有约50nm至约500nm的平均尺寸。在一些实施方案中,多个LNP具有约50nm至约200nm、约100nm至约200nm、约150nm至约200nm、约50nm至约150nm、约100nm至约150nm、约200nm至约500nm、约300nm至约500nm、约350nm至约500nm、约400nm至约500nm、约425nm至约500nm、约450nm至约500nm或约475nm至约500nm的平均尺寸。
在一些实施方案中,多个LNP具有小于约-20mV、小于约-30mV、小于约35mV或小于约-40mV的平均ζ-电位。在一些实施方案中,多个LNP具有介于约-50mV至约-20mV、约-40mV至约-20mV或约-30mV至约-20mV之间的平均ζ-电位。在一些实施方案中,多个LNP具有约-30mV、约-31mV、约-32mV、约-33mV、约-34mV、约-35mV、约-36mV、约-37mV、约-38mV、约-39mV或约-40mV的平均ζ-电位。
在一些实施方案中,施用所述治疗性组合物至受试者将所述重组DNA多核苷酸递送至受试者的靶细胞,并且其中重组DNA多核苷酸产生能够溶解所述受试者的靶细胞的感染性病毒。在一些实施方案中,组合物经静脉内或经肿瘤内递送。在一些实施方案中,靶细胞是癌细胞。
在一些实施方案中,本公开提供了一种抑制有需要的受试者中癌性肿瘤的生长的方法,所述方法包括施用本文所述的治疗性组合物至所述有需要的受试者,其中所述组合物的施用抑制所述肿瘤的生长。在一些实施方案中,施用是在肿瘤内或静脉内。在一些实施方案中,癌症是肺癌或肝癌。
在一些实施方案中,本公开提供了一种重组DNA分子,所述重组DNA分子包含编码具有复制能力的病毒基因组的多核苷酸序列,其中所述多核苷酸序列可操作地连接于能够结合哺乳动物RNA聚合酶II(Pol II)的启动子序列并且侧接3'接合裂解序列和5'接合裂解序列,其中所述3'接合裂解序列和所述5'接合裂解序列属于不同类型,并且其中编码所述具有复制能力的病毒基因组的所述多核苷酸序列是非病毒来源的。
在一些实施方案中,3'接合裂解序列是核酶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是核酶序列并且5'接合裂解序列是人工miR(AmiR)靶序列。在一些实施方案中,3'接合裂解序列是微小RNA(miR)靶序列并且5'接合裂解序列选自核酶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是人工miR(AmiR)靶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、核酶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是向导RNA(gRNA)靶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、核酶序列、pri-miR序列和适体酶序列。在一些实施方案中,3'接合裂解序列是pri-miR序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、核酶序列和适体酶序列。在一些实施方案中,3'接合裂解序列是适体酶序列并且5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和核酶序列。
在一些实施方案中,编码病毒是单链RNA(ssRNA)病毒。在一些实施方案中,ssRNA病毒是正义((+)-义)或负义((-)-义)ssRNA病毒。在一些实施方案中,(+)-义ssRNA病毒是小核糖核酸病毒。在一些实施方案中,小核糖核酸病毒是塞内加谷病毒(SVV)或柯萨奇病毒。
在一些实施方案中,重组DNA分子在通过非病毒性递送媒介物引入细胞中时能够产生感染性的溶解性病毒。
在一些实施方案中,重组DNA分子还包含编码外源有效载荷蛋白的多核苷酸序列。在一些实施方案中,外源有效载荷蛋白是荧光蛋白、酶蛋白、细胞因子、趋化因子、细胞表面受体的配体或能够结合于细胞表面受体的抗原结合分子。
在一些实施方案中,细胞因子是IL-18、IL-36γ、LIGHT和IL-2。在一些实施方案中,细胞表面受体的配体是Flt3配体。在一些实施方案中,趋化因子选自CCL21、CCL5、CXCL10和CCL4。在一些实施方案中,抗原结合分子能够结合和抑制免疫检查点受体。在一些实施方案中,免疫检查点受体是PD1。在一些实施方案中,抗原结合分子能够结合于选自DLL3、EpCam和CEA的肿瘤相关抗原。在一些实施方案中,抗原结合分子是包含对肿瘤抗原具有特异性的第一结构域和对T细胞表面分子具有特异性的第二结构域的双特异性T细胞衔接分子。在一些实施方案中,T细胞表面分子是CD3。
在一些实施方案中,微小RNA(miRNA)靶序列(miR-TS)盒被插入编码具有复制能力的病毒基因组的核酸序列中,其中所述miR-TS盒包含一种或多种miRNA靶序列,并且其中细胞中一种或多种相应miRNA的表达抑制所述细胞中所述编码病毒的复制。在一些实施方案中,一种或多种miRNA选自miR-124、miR-1、miR-143、miR-128、miR-219、miR-219a、miR-122、miR-204、miR-217、miR-137和miR-126。在一些实施方案中,miR-TS盒包含miR-124靶序列的一个或多个拷贝、miR-1靶序列的一个或多个拷贝和miR-143靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-219a靶序列的一个或多个拷贝和miR-122靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-204靶序列的一个或多个拷贝和miR-219靶序列的一个或多个拷贝。在一些实施方案中,miR-TS盒包含miR-217靶序列的一个或多个拷贝、miR-137靶序列的一个或多个拷贝和miR-126靶序列的一个或多个拷贝。在一些实施方案中,重组DNA分子是包含编码具有复制能力的病毒基因组的多核苷酸序列的质粒或NanoV。
附图说明
图1展示了可以衍生出多核苷酸基因组的各种DNA或RNA病毒的实例。
图2展示了其中包封自主复制型多核苷酸的用糖胺聚糖(CAG)透明质酸(HA)包被的基于脂质的纳米颗粒的实例。
图3展示了用包封在靶向肿瘤的纳米颗粒中的自主复制型多核苷酸治疗癌症的实例。
图4A-图4B展示了用于繁殖其中Rep 52和Rep 78反式表达的包含5'和3'ITR的自主复制型病毒基因组(图4A)和带内部Rep盒的包含5'和3'ITR的自主复制型病毒基因组(图4B)的复制型HSV载体的实例。gB:NT=gB基因中增强病毒进入的双重突变;BAC=侧接loxP的抗氯霉素和lacZ序列;Δ联合=删除包括ICP4基因的一个拷贝的完整内部重复区域;ITR=源自AAV的反向末端重复序列;Pol IIp=组成型Pol II启动子;Rep盒=用于复制侧接ITR的病毒基因组DNA的编码AAV Rep 52和Rep 78的盒;任选的miRNA减毒用对角线散列框表示。
图5A-图5B展示了用于繁殖其中Rep 52和Rep 78反式表达的包含5'和3'ITR的自主复制型多核苷酸(图5A)和带内部Rep盒的包含5'和3'ITR的自主复制型病毒基因组(图5B)的非复制型HSV载体的实例。gB:NT=gB基因中增强病毒进入的双重突变;BAC=侧接loxP的抗氯霉素和lacZ序列;Δ联合=删除包括ICP4基因的一个拷贝的完整内部重复区域;ITR=源自AAV的反向末端重复序列;Pol IIp=组成型Pol II启动子;Rep盒=用于复制侧接ITR的病毒基因组DNA的编码AAV Rep 52和Rep 78的盒;任选的miRNA减毒用对角线散列框表示。
图6A-图6B展示了编码正链RNA I型脊髓灰质炎病毒基因组的多核苷酸插图。该多核苷酸可以任选地在5'和3'末端侧接AAV来源的ITR(图6A和图6B)。该多核苷酸可以任选地包含一个或多个用于miRNA减毒的miRNA靶序列盒(miR-TS盒)(图6B)。
图7A-图7B展示了用于产生编码I型脊髓灰质炎病毒基因组的自主复制型多核苷酸的复制型HSV载体的实例。脊髓灰质炎病毒基因组可以任选包含用于miRNA减毒的miRNA靶位点(用对角线散列框表示)。图7B示出了用于产生编码I型脊髓灰质炎病毒基因组的在5'和3'末端侧接AAV来源的ITR的自主复制型多核苷酸的复制型HSV载体。gB:NT=gB基因中增强病毒进入的双重突变;BAC=侧接loxP的抗氯霉素和lacZ序列;ΔUL19=删除编码主要衣壳蛋白VP5的UL19基因;Δ联合=删除包括ICP4基因的一个拷贝的完整内部重复区域;Pol IIp=组成型RNA Pol II启动子;Rep盒=用于复制侧接ITR的病毒基因组DNA的编码AAV Rep 52和Rep 78的盒;脊髓灰质炎病毒基因组盒=插入HSV基因组(通过转录产生的正链基因组)的基因间基因座中;任选的miRNA减毒用对角线散列框表示。
图8A-图8C展示了用于治疗特定癌症(例如非小细胞肺癌(图8A)、肝细胞癌(图8B)和前列腺癌(8C))的I型脊髓灰质炎病毒多核苷酸基因组的实例。
图9A-图9B展示了编码水泡性口炎病毒(VSV)基因组的自主复制型多核苷酸的实例。该多核苷酸可以任选地在5'和3'末端侧接AAV来源的ITR(图9B)。该多核苷酸可以任选地包含一个或多个用对角线散列框表示的用于miRNA减毒的miRNA靶序列(图9B)。
图10A-图10B展示了用于产生VSV基因组多核苷酸基因组的复制型HSV载体的实例。VSV基因组可以任选地包含用于miRNA减毒的miRNA靶位点(图10A和图10B)。图10B示出了用于产生在5'和3'末端侧接AAV来源的ITR的VSV基因组的复制型HSV载体。gB:NT=gB基因中增强病毒进入的双重突变;BAC=侧接loxP的抗氯霉素和lacZ序列;Δ联合=删除包括ICP4基因的一个拷贝的完整内部重复区域;ΔUL19=删除编码主要衣壳蛋白VP5的UL19基因;VSV基因组盒=反基因组(负链)VSV基因组和编码必需VSV基因N、P和L的哺乳动物表达盒,其利用双向Pol II启动子(BD Pol IIp)转录被插入HSV基因组的基因间基因座中负链VSV基因组和必需VSV基因;任选的miRNA减毒用对角线散列框表示;Rep盒=用于复制侧接ITR的病毒基因组DNA的编码AAV Rep 52和Rep 78的盒;Pol IIp=组成型Pol II启动子。
图11A-图11C展示了用于治疗特定癌症(例如肝细胞癌(图11A)、前列腺癌(图11B)和非小细胞肺癌(图11C))的VSV多核苷酸基因组的实例。
图12A-图12B展示了腺病毒多核苷酸基因组的实例。AAV基因组可以任选地包含用对角线散列框表示的用于miRNA减毒的miRNA靶位点(图12B)。
图13A-图13C展示了用于治疗特定癌症(例如肝细胞癌(图13A)、前列腺癌(图13B)和非小细胞肺癌(图13C))的AAV多核苷酸基因组的实例。
图14展示了CVB3病毒基因组的示意图。CVB3是基因组尺寸为约7.4kb的正义ssRNA小核糖核酸病毒。
图15展示了柯萨奇病毒A21构建体的示意图。
图16展示了塞内加谷病毒(SVV)构建体的示意图。
图17展示了一种重组的HSV-1细菌人工染色体(BAC)载体,其包含侧接ITR的溶瘤病毒(OV)DNA盒和Rep盒。
图18展示了通过Rep盒和A/C异二聚体AP21967对Rep表达的控制。
图19A-图19D展示了由图17所示的系统产生的NanoV构建体的单体和二聚体。图19A展示了NanoV单体和二聚体的结构和尺寸。图19B展示了在限制酶消化后预测的单体和二聚体的凝胶分析。图19C展示了具有内部PCR引物的位置的NanoV构建体的示意图。图19D展示了使用内部引物的NanoV的PCR扩增。
图20A-图20C展示了在预测取向上NanoV串联体(concatamer)的产生。图20A展示了NanoV单体中AflII裂解位点的位置。图20B展示了AflII裂解产物的可能的串联体取向和预测的大小。图20C展示了AflII消化的NanoV DNA的凝胶分析。
图21展示了mCherry从NanoV DNA构建体的表达。
图22展示了包含3'和5'核酶序列的小核糖核酸病毒构建体的示意图。
图23A-图23B描绘了编码具有复制能力的塞内加谷病毒(SVV)的多核苷酸的设计和培养方案的示意图。图23A展示了包含哺乳动物5'和3'UTR序列、锤头状核酶和肝炎δ核酶的加帽的聚腺苷酸化的转录物。图23B示出了用于产生感染性SVV的培养方案的示意图。
图24展示了结晶紫染色,其展现了从转染了编码SVV-核酶(WT)和SVV-mCherry-核酶的dsDNA的293T细胞产生的病毒的单层溶解。
图25A-图25C示出了三种不同的外来有效载荷从图23中所示的SVV转录物的表达。图20A展示了mCherry的明场和荧光显微镜。图20B展示了纳米荧光素酶测定的结果。图25C展示了CXCL10表达。
图26A-图26B示出了编码SVV的质粒构建体的miRNA减毒。图26A展示了miR-122和miR-1减毒的SVV构建体的示意图。图26B显示结晶紫染色,其展现了已经用miR-122和/或miR-1模拟物转染并感染了图26A中所示的SVV-WT或SVV-miRT构建体的H1299细胞的溶解。
图27A-图27B展示了通过肿瘤内递送的编码SVV的DNA质粒在体内产生感染性病毒和抑制肿瘤生长的情况。图27A展示了在肿瘤内施用编码SVV的质粒后肿瘤生长的抑制。图27B展示了从图27A所示的实验收获的粉碎的肿瘤中分离活病毒。
图28A-图28B展示了通过肿瘤内递送的编码SVV的DNA质粒在体内表达外源有效载荷的情况。图28A展示了在肿瘤内注射质粒DNA后在肿瘤溶解物中检测到的平均辐射度。图28B展示了在肿瘤内注射质粒DNA后在肿瘤溶解物中检测到的CXCL10水平。
图29展示了静脉内递送后编码SVV的质粒至肿瘤部位的递送。
图30展示了静脉内递送编码LNP包封的SVV的质粒DNA后肿瘤生长的抑制。
图31A展示了编码SVV的质粒的图。图31B展示了编码CVA21的质粒的图。
图32A-图32B示出了用于产生具有离散3'和5'天然末端的正义ssRNA病毒基因组的系统。
图33示出了用于产生具有离散3'和5'天然末端的正义ssRNA病毒基因组的不对称末端系统。
图34A-图34B展示了结晶紫染色,其展现了具有5'和3'核酶(SVV WT-R)的SVV和具有3'核酶和5'siRNA靶序列的SVV(5siRNA)对H1299单层的溶解。
图35示出了用于产生具有离散3'和5'天然末端的正义ssRNA病毒基因组的不对称末端系统。靶向5'siRNA靶序列的Ami-RNA在3'核酶之后和bGH多聚A终止子之前编码。
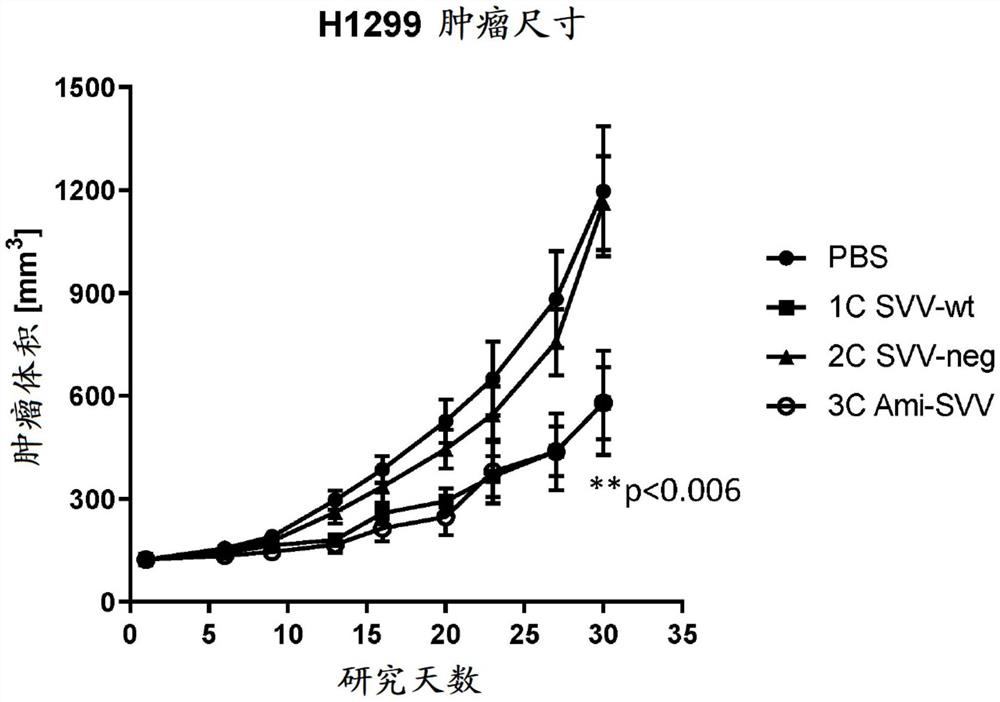
图36A-图36B示出了具有5'和3'核酶(SVV-wt)或不对称末端裂解系统(3'核酶和5'amiRNA靶序列(ami-SVV))的编码LNP包封的SVV的质粒DNA的功效。图36A展示了在肿瘤内施用LNP包封的SVV-wt或ami-SVV后H446肿瘤生长的抑制。图36B展示了在肿瘤内施用LNP包封的SVV-wt或ami-SVV后H1299肿瘤生长的抑制。
图37展示了在静脉内递送编码LNP包封的SVV的质粒DNA(SVV-Neg、SVV-wt或Ami-SVV)后肿瘤生长的抑制。
具体实施方式
本领域需要如下自主复制型病毒疗法,其在中和抗体的存在下是有效的,能够重复全身性使用并且其复制仅限于患病细胞,从而最大化治疗功效,同时最大程度地减少对正常的非癌细胞的附带损害。本公开克服了这些障碍,并提供了编码具有复制能力的病毒基因组的多核苷酸,所述多核苷酸可以包封在例如脂质纳米颗粒、聚合物纳米颗粒或外泌体的非免疫原性颗粒中。在一些实施方案中,本公开提供了编码具有复制能力的病毒的重组DNA分子,以及用于治疗和预防增生性疾病和病症(例如癌症)的方法。在一些实施方案中,重组DNA分子还包含编码治疗分子的多核苷酸。本公开使得能够全身递送适于治疗广泛的增生性疾病(例如癌症)的安全有效的重组多核苷酸载体。
本文所使用的章节标题仅出于组织性目的并且不应被解释为限制所描述的主题。本文引用的所有文献或文献的一部分,包括但不限于专利、专利申请、文章、书籍和论文,出于任何目的明确地以引入的方式整体并入本文中。如果一个或多个所并入的文献或文献的一些部分定义的术语与本申请中该术语的定义相矛盾,则以本申请中出现的定义为准。然而,本文所引用的任何参考文献、文章、公布、专利、专利公布和专利申请的提及,并不也不应被视为承认或任何形式的建议,它们构成有效的现有技术或形成世界上任何国家的公知常识的一部分。
I.定义
在本描述中,除非另有指示,否则任何浓度范围、百分比范围、比率范围或整数范围均应理解为包括所述范围内的任何整数的值,以及在适当情况下,其分数(例如整数的十分之一和百分之一)。应当理解,除非另外指示,否则本文所用的术语“一(a/an)”是指所列举的组分中的“一种或多种”。替代方案(例如“或”)的使用应理解为意指替代方案中的一个、两个或其任何组合。如本文所用,术语“包括”和“包含”同义使用。如本文所用,“多个”可以指一种或多种组分(例如一种或多种miRNA靶序列)。在本申请中,除非另外说明,否则使用“或”意指“和/或”。
如本申请中所用,术语“约”和“大约”作为等同物使用。本申请中使用的带或不带约/大约的任何数字旨在涵盖相关领域的普通技术人员所理解的任何正常波动。在某些实施方案中,除非另有说明或从上下文中另外明显看出(除非该数字超过可能值的100%),否则术语“大约”或“约”是指在任一方向上(大于或小于)落入所说明的参考值的25%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%或更少内的值的范围。
“降低”或“减少”是指与参考值相比,特定值降低或减少至少5%,例如5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%或100%。特定值的降低或减少也可以表示为与参考值相比值的倍数变化,例如与参考值相比降低至少1倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍、200倍、500倍、1000倍或更多倍。
“增加”是指与参考值相比,特定值增加至少5%,例如5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%、100%、200%、300%、400%、500%或更多。特定值的增加也可以表示为与参考值相比值的倍数变化,例如与参考值的水平相比增加至少1倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍、200倍、500倍、1000倍或更多倍。
术语“序列同一性”是指两个多核苷酸或多肽序列之间相同且处于相对位置处的碱基或氨基酸的百分比。因此,一个多核苷酸或多肽序列与另一多核苷酸或多肽序列相比具有一定百分比的序列同一性。为了进行序列比较,通常将一个序列用作参考序列,测试序列将与之进行比较。术语“参考序列”是指测试序列进行比较的分子。
“互补”是指在两个包含天然或非天然存在的(例如,如上所述修饰的)碱基(核苷)或其类似物的序列之间通过碱基堆积和特定氢键合而配对的能力。例如,如果核酸的一个位置处的碱基能够与靶标的相应位置处的碱基氢键合,则认为所述碱基在该位置处彼此互补。核酸可包含通用碱,或惰性无碱基间隔子,它们对氢键合不提供正的或负的贡献。碱基配对可以包括规范的沃森-克里克碱基配对(Watson-Crick base pairing)和非沃森-克里克碱基配对(例如,摆动碱基配对(Wobble base pairing)和胡斯坦碱基配对(Hoogsteenbase pairing))。应当理解,对于互补碱基配对,腺苷型碱基(A)与胸苷型碱基(T)或尿嘧啶型碱基(U)互补,胞嘧啶型碱基(C)与鸟苷型碱基(G)互补,并且例如3-硝基吡咯或5-硝基吲哚之类的通用碱基可以与任何A、C、U或T杂交并认为是互补的。Nichols等人,Nature,1994;369:492-493和Loakes等人,Nucleic Acids Res.,1994;22:4039-4043。肌苷(I)在本领域中也被认为是通用碱基,并且被认为与任何A、C、U或T互补。参见Watkins和SantaLucia,Nucl.Acids Research,2005;33(19):6258-6267。
“表达盒”或“表达构建体”是指可操作地连接于启动子的DNA多核苷酸序列。“可操作地连接”是指一种并置关系,其中所描述的组件处于允许它们以其预期方式起作用的关系中。例如,如果启动子影响多核苷酸序列的转录或表达,则将其可操作地连接于多核苷酸序列。
术语“受试者”包括动物,例如哺乳动物。在一些实施方案中,哺乳动物是灵长类动物。在一些实施方案中,哺乳动物是人。在一些实施方案中,受试者是牲畜,例如牛、绵羊、山羊、母牛、猪等;或驯养的动物,例如狗和猫。在一些实施方案中(例如,特别是在研究背景下),受试者是啮齿动物(例如,小鼠、大鼠、仓鼠)、兔子、灵长类动物或猪,例如近交系猪等。术语“受试者”和“患者”在本文中可互换使用。
“施用”在本文中是指将剂或组合物引入受试者中。
如本文所用,“治疗”是指将剂或组合物递送至受试者以影响生理结果。在一些实施方案中,治疗包括将细胞群体递送至受试者。在一些实施方案中,治疗是指治疗哺乳动物,例如人的疾病,包括(a)抑制疾病,即阻止疾病的发展或预防疾病的进展;(b)减轻疾病,即引起疾病状态的消退;以及(c)治愈疾病。
术语“有效量”是指剂或组合物引起特定生理作用所需的最小量(例如,增加、激活和/或增强特定的生理效果所需的量)。特定剂的有效量可以根据剂的性质以多种方式表示,例如质量/体积、细胞数目/体积、颗粒/体积、(剂的质量)/(受试者的质量)、细胞数目/(受试者的质量)或颗粒/(受试者的质量)。特定剂的有效量也可以表示为半最大有效浓度(EC
细胞“群体”是指大于1的任意细胞数目,但优选至少1×10
“效应子功能”是指与针对靶细胞或靶抗原的免疫应答的产生、维持和/或增强相关的免疫细胞功能。
术语“微小RNA”、“miRNA”和“miR”在本文中可互换使用,是指长度约21-25个核苷酸的小型非编码内源RNA,其可以通过指导其靶信使RNA(mRNA)进行降解或翻译抑制来调节基因表达。
如本文所用,术语“组合物”是指本文所述的自主复制型多核苷酸或颗粒包封的自主复制型多核苷酸的制剂,其能够被施用或递送至受试者或细胞。
短语“药学上可接受的”在本文中用以指在合理的医学判断范围内,适合与人和动物的组织接触而没有过度的毒性、刺激性、过敏反应或其它问题或并发症,与合理的效益/风险比相称的那些化合物、材料、组合物和/或剂型。
如本文所用,“药学上可接受的载体、稀释剂或赋形剂”包括但不限于已被美国食品药物管理局(the United States Food and Drug Administration)批准为可用于人和/或家畜的任何佐剂、载体、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增香剂、表面活性剂、润湿剂、分散剂、悬浮剂、稳定剂、等渗剂、溶剂、表面活性剂和/或乳化剂。
术语“自主复制型多核苷酸”是指在不存在其它外源多核苷酸或外源载体的情况下能够在宿主细胞内复制的外源多核苷酸。
术语“具有复制能力的病毒基因组”是指由本文所述的自主复制型多核苷酸编码的病毒基因组,其编码病毒复制和感染性病毒颗粒产生所必需的所有病毒基因。
术语“溶瘤病毒”是指已被修饰成或天然地优先感染癌细胞的病毒。
术语“载体”在本文中用以指能够转移或转运另一种核酸分子的核酸分子。
分子和细胞生物化学中的通用方法可以在标准教科书中找到,例如MolecularCloning:A Laboratory Manual,第3版(Sambrook等人,HaRBor Laboratory Press 2001);Short Protocols in Molecular Biology,第4版(Ausubel等人编辑,John Wiley&Sons1999);Protein Methods(Bollag等人,John Wiley&Sons 1996);Nonviral Vectors forGene Therapy(Wagner等人编辑,Academic Press 1999);Viral Vectors(Kaplift和Loewy编辑,Academic Press 1995);Immunology Methods Manual(I.Lefkovits编辑,AcademicPress 1997);以及Cell and Tissue Culture:Laboratory Procedures inBiotechnology(Doyle和Griffiths,John Wiley&Sons 1998),其公开内容以引用的方式并入本文中。
II.自主复制型多核苷酸
在一些实施方案中,本公开提供了一种重组核酸分子,所述重组核酸分子包含编码具有复制能力的病毒基因组的多核苷酸,所述多核苷酸在通过非病毒性递送媒介物引入细胞中时能够产生感染性的溶解病毒。本文所述的自主复制型多核苷酸不需要额外的外源基因或蛋白质存在于细胞中即可复制并产生感染性病毒。而是,宿主细胞中的内源转录机制介导自主复制型多核苷酸的初始第一轮转录或翻译,以产生具有复制能力的病毒基因组。由自主复制型多核苷酸编码的病毒基因组能够表达对于病毒基因组的持续复制和装配成包含具有复制能力的病毒基因组的感染性病毒颗粒(可能包含衣壳蛋白、包膜蛋白和/或膜蛋白)来说必需的病毒蛋白。这样,由本文所述的自主复制型多核苷酸编码的具有复制能力的病毒基因组能够产生能够感染宿主细胞的病毒。
在一些实施方案中,重组核酸分子是包含编码具有复制能力的病毒基因组的DNA多核苷酸的重组DNA分子。在一些实施方案中,重组DNA分子是复制子、质粒、粘粒、噬菌粒、转座子、细菌人工染色体或酵母人工染色体。在一些实施方案中,重组DNA分子是包含自主复制型多核苷酸的质粒。
在一些实施方案中,在一些实施方案中,本文所述的重组核酸分子包含可操作地连接于转录控制元件的自主复制型多核苷酸(例如,编码具有复制能力的病毒基因组的多核苷酸),所述转录控制元件例如是驱动或调节自主复制型多核苷酸转录的启动子。在一些实施方案中,转录控制元件是哺乳动物启动子序列。在一些实施方案中,哺乳动物启动子序列能够结合哺乳动物RNA聚合酶。例如,在一些实施方案中,哺乳动物启动子序列是RNA聚合酶II(Pol II)启动子。在一些实施方案中,哺乳动物启动子是组成型启动子,例如CAG、UbC、EF1a或PGK启动子。在一些实施方案中,转录控制元件是噬菌体来源的启动子序列,例如T7启动子。在这样的实施方案中,在细胞的细胞质中在T7启动子控制下转录多核苷酸。
在一些实施方案中、启动子是诱导型启动子、例如四环素(tetracycline)诱导型启动子(例如TRE-Tight)、强力霉素(doxycline)诱导型启动子、温度诱导型启动子(例如Hsp70或Hsp90来源的启动子)、乳糖诱导型启动子(例如pLac启动子)。在一些实施方案中,启动子序列包含一种或多种调节转录的转录增强子元件。例如,在一些实施方案中,启动子包含一种或多种低氧反应元件或一种或多种辐射反应元件。在一些实施方案中,启动子主要驱动癌细胞中自主复制型多核苷酸的转录。例如,在一些实施方案中,转录控制元件是源自在癌细胞中表达增加的基因的启动子,例如hTERT、HE4、CEA、OC、ARF、CgA、GRP78、CXCR4、HMGB2、INSM1、间皮素、OPN、RAD51、TETP、H19、uPAR、ERBB2、MUC1、Frz1、IGF2-P4、Myc或E2F。
在一些实施方案中,本文所述的重组核酸分子包含编码具有复制能力的病毒基因组的多核苷酸,其中所述多核苷酸在5'和3'末端侧接反向末端重复(ITR)序列。在本文中,术语“反向末端重复”或“ITR”是指位于异源多核苷酸序列(例如,编码具有复制能力的病毒基因组的核酸序列)的3'端和/或5'端并包含被一个或多个非回文序列片段隔开的回文序列的多核苷酸序列。“回文”序列是指当均以5'至3'方向读取时与互补链相同的核酸序列。通过回文序列之间的互补碱基配对,ITR的多核苷酸序列将形成茎环结构(例如,发夹环)。ITR多核苷酸序列可以是任何长度,只要该序列能够形成茎环结构即可。在一些实施方案中,多核苷酸包含以下结构:
(a)5'–ITR–有义病毒基因组–ITR–3';或者
(b)3'–ITR–反义病毒基因组–ITR–5'。
在一些实施方案中,本文所述的ITR序列最少包含能够形成茎环结构的回文序列、Rep结合位点和末端解链位点。在一些实施方案中,本文所述的ITR源自腺相关病毒(AAV)。在这样的实施方案中,ITR可以源自任何已知的AAV血清型(例如,AAV1、2、3、4、5、6、7、8、9、10或11)(参见例如美国专利No.9,598,703)。在一些实施方案中,本文所述的ITR可以源自细小病毒(参见例如美国专利No.5,585,254)。适用于本公开的其它反向末端重复序列描述于国际PCT公布No.WO 2017/152149和WO 2016/172008以及美国专利申请公布No.US 2017-0362608中。
在一些实施方案中,本文所述的重组核酸分子包含两个侧接ITR的多核苷酸分子,其中第一分子的5'ITR与第二分子的3'ITR共价连接并且第一分子的3'ITR与第二分子的5'ITR共价连接。在这样的实施方案中,共价连接的侧接ITR的多核苷酸形成末端封闭的线性双链溶瘤病毒核酸分子。在一些实施方案中,本文所述的重组核酸分子包含(i)第一单链DNA(ssDNA)分子,其包含编码病毒基因组的有义序列的多核苷酸;(ii)第二ssDNA分子,其包含编码病毒基因组的反义序列的多核苷酸,其中第一ssDNA分子和第二ssDNA分子中的每一个均包含3'ITR和5'ITR,其中第一ssDNA分子的3'末端与第二ssDNA分子的5'末端共价连接,而第一ssDNA分子的5'末端与第二ssDNA分子的3'末端共价连接以形成末端封闭的线性双链体溶瘤病毒(Ov)DNA分子,在本文中称为“NanoV分子”。
在一些实施方案中,自主复制型多核苷酸编码具有复制能力的DNA或RNA病毒基因组。在一些实施方案中,具有复制能力的病毒基因组是单链基因组(例如ssRNA基因组或ssDNA基因组)。在这样的实施方案中,单链基因组可以是正义或负义基因组。在一些实施方案中,具有复制能力的病毒基因组是双链基因组(例如dsRNA基因组或dsDNA基因组)。在一些实施方案中,自主复制型多核苷酸编码具有复制能力的溶瘤病毒。如本文所用,术语“溶瘤病毒”係指被修饰成或天然优先感染癌细胞的病毒。溶瘤病毒的实例是本领域已知的,包括但不限于单纯疱疹病毒、腺病毒、脊髓灰质炎病毒、牛痘病毒、麻疹病毒、水疱性口腔炎病毒、正粘病毒、细小病毒、马拉巴病毒(maraba virus)或柯萨奇病毒。
在一些实施方案中,由多核苷酸产生的具有复制能力的病毒是腺病毒科(Adenoviridae)中的任何病毒,例如腺病毒;小核糖核酸病毒科(Picornaviridae)中的任何病毒,例如柯萨奇病毒、脊髓灰质炎病毒或塞内加谷病毒;疱疹病毒科(Herpesviridae)中的任何病毒,例如马疱疹病毒或1型单纯疱疹病毒(HSV-1);沙粒病毒科(Arenaviridae)中的任何病毒,例如拉沙病毒(lassa virus);反转录病毒科(Retroviridae)中的任何病毒,例如鼠白血病病毒;正粘病毒科(Orthomyxoviridae)中的任何病毒,例如甲型流感病毒;副粘病毒科(Paramyxoviridae),例如新城鸡瘟病毒(Newcastle disease virus)或麻疹病毒;细小病毒科(Parvoviridae)中的任何病毒;呼肠孤病毒科(Reoviridae)中的任何病毒,例如哺乳动物的正呼肠孤病毒属(orthoreovirus);披膜病毒科(Togaviridae)中的任何病毒,例如辛德毕斯病毒(sindbis virus);痘病毒科(Poxviridae)中的任何病毒,例如牛痘病毒或粘液瘤病毒;或弹状病毒科(Rhabdoviridae)中的任何病毒,例如水疱性口腔炎病毒(VSV)或马拉巴病毒,它们的实例显示在图1中。在一些实施方案中,由多核苷酸产生的具有复制能力的病毒是嵌合病毒,例如修饰的脊髓灰质炎病毒(例如PVS-RIPO)。
在一些实施方案中,当将重组核酸分子引入细胞中时,本文公开的重组核酸分子被细胞的内源聚合酶转录,以产生能够装配成感染性病毒的病毒基因组。产生的感染性病毒的量可以通过本领域已知的方法来测量,所述方法包括但不限于,对培养中生长的细胞的上清液中或受试者的组织中存在于靶细胞或靶细胞群中的病毒RNA或病毒DNA的量进行定量。在这样的实施方案中,可以从靶细胞中分离总DNA或RNA,并且可以使用对病毒基因组中存在的RNA或DNA序列具有特异性的引物进行qPCR。在一些实施方案中,由重组核酸中的细胞群产生的病毒颗粒的数目被引入靶细胞群(例如,体外样品或从体内肿瘤分离的样品),可以通过本领域已知的方法定量。在一些实施方案中,本公开的制剂包含至少约10
在一些实施方案中,本文公开的重组核酸分子包含与SEQ ID NO:1-2具有约75%、约76%、约77%、约78%、约79%、约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同一的多核苷酸序列。
A.单链RNA病毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码单链RNA(ssRNA)病毒基因组。在一些实施方案中,ssRNA病毒为正义ssRNA(+义ssRNA)病毒或负义ssRNA(-义ssRNA)病毒。
1.正义单链RNA病毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码正义单链RNA(+义ssRNA)病毒基因组。示例性+义ssRNA病毒包括小核糖核酸病毒科(例如柯萨奇病毒、脊髓灰质炎病毒和塞内加谷病毒(SVV),包括SVV-A)、冠状病毒科(Coronaviridae)(例如α冠状病毒属(Alphacoronavirus),例如HCoV-229E和HCoV-NL63;β冠状病毒属(Betacoronoavirus),例如HCoVV-HKU1、HCoV-OC3和MERS-CoV)、反转录病毒科(例如鼠白血病病毒)和披膜病毒科(例如辛德毕斯病毒)的成员。在一些实施方案中,本文所述的自主复制型多核苷酸编码柯萨奇病毒。在一些实施方案中,柯萨奇病毒选自CVB3、CVA21和CA9。正义ssRNA病毒的其它示例性属和种示于下表4中。
表4:正义ssRNA病毒
+义ssRNA病毒的基因组包含呈5'-3'取向的ssRNA分子,并且可以被宿主细胞直接翻译成病毒蛋白。因此,编码+义ssRNA病毒的自主复制型多核苷酸不需要存在任何另外的病毒复制蛋白即可产生感染性病毒。
在一些实施例中,由本文所述的多核苷酸编码的具有+义ssRNA复制能力的病毒基因组需要病毒天然的离散的5'和3'末端。哺乳动物RNA Pol II产生的mRNA转录物含有哺乳动物5'和3'UTR,因此不含产生感染性ssRNA病毒所需的离散的天然末端。因此,在一些实施方案中,感染性+义ssRNA病毒(例如,表5中所示的病毒)的产生需要另外的5'和3'序列,这些序列能够在病毒ssRNA和哺乳动物mRNA序列的接合处裂解Pol II编码的病毒基因组转录物,从而为了保持病毒的内源性5'和3'离散末端,从转录物中除去非病毒RNA。这样的序列在本文中称为接合裂解序列(JCS)。举例来说,在一些实施方案中,自多核苷酸包含以下结构:
(a)5'–Pol II–JCS–有义病毒基因组–JCS–3';
(b)5'–Pol II–JCS–反义病毒基因组–JCS–3'。
在一些实施方案中,自主复制型多核苷酸包含用于产生病毒转录物的天然离散末端的5'和3'接合裂解序列,并且侧接5'和3'ITR。举例来说,在一些实施方案中,自多核苷酸包含以下结构:
(a)5'–ITR–Pol II–JCS–有义病毒基因组–JCS–ITR–3';或
(b)5'–ITR–Pol II–JCS–反义病毒基因组–JCS–ITR–3'。
可以通过多种方法实现接合裂解序列和从病毒基因组转录物中去除非病毒RNA。例如,在一些实施方案中,接合裂解序列是RNA干扰(RNAi)分子的靶标。如本文所用,“RNA干扰分子”是指通过内源基因沉默途径(例如切丁酶和RNA诱导沉默复合物(RISC))介导靶mRNA序列的降解的RNA多核苷酸。示例性RNA干扰剂包括微小RNA(miRNA)、人工miRNA(AmiR)、短发夹RNA(shRNA)和小干扰RNA(siRNA)。在图32A、图32B和图33中描绘了示例性构建体设计。此外,当前在本领域已知或将来定义的用于在特定位点裂解RNA转录物的任何系统均可用于产生由本文所述的自主复制型多核苷酸编码的病毒所固有的离散末端。
在一些实施方案中,RNAi分子是miRNA。miRNA是指天然存在的长度为约18-25个核苷酸的小的非编码RNA分子,其与靶mRNA序列至少部分互补。在动物中,miRNA的基因被转录成初级miRNA(pri-miRNA),后者是双链的,并形成茎环结构。然后,在核中通过包含2类RNase III Drosha和微处理亚基DCGR8的微处理复合物将Pri-miRNA裂解,形成70-100个核苷酸的前体miRNA(pre-miRNA)。pre-miRNA形成发夹结构,并被转运至细胞质,在这里被RNase III酶Dicer加工成约18-25个核苷酸的miRNA双链体。尽管双链体的任一链都可能充当功能性miRNA,但通常会降解miRNA的一条链,仅将一条链加载到Argonaute(AGO)核酸酶上,以产生效应子RNA诱导沉默复合物(RISC),其中miRNA和其mRNA靶标相互作用(Wahid等人,1803:11,2010,1231-1243)。在一些实施方案中,5'和/或3'接合裂解序列是miRNA靶序列。
在一些实施方案中,RNAi分子是源自miRNA嵌入的shRNA(shmiRNA)构建体的人工miRNA(AmiR)。(参见例如Liu等人,Nucleic Acids Res(2008)36:9;2811-2834;Zeng等人,Molecular Cell(2002),9;1327-1333;Fellman等人,Cell Reports(2013)5;1704-1713)。在一些实施方案中,5'和/或3'接合裂解序列是AmiR靶序列。
在一些实施方案中,RNAi分子是siRNA分子。siRNA是指长度通常约为21-23个核苷酸的双链RNA分子。双链体siRNA分子在细胞质中进行加工,与称为RNA诱导沉默复合物(RISC)的多蛋白复合物缔合,在此过程中,从双链体中酶切“乘客”有义链。然后,通过序列互补性,激活的RISC中所含的反义“向导”链将RISC导向相应的mRNA,而AGO核酸酶切割靶mRNA,从而导致特定的基因沉默。在一些实施方案中,siRNA分子源自shRNA分子。shRNA是长度为约50-70个核苷酸的单链人工RNA分子,其形成茎环结构。通过用质粒或病毒载体引入编码shRNA的DNA多核苷酸来实现shRNA在细胞中的表达。然后将shRNA转录成模仿pri-miRNA茎环结构的产物,并通过Drosha在细胞核中进行类似加工,形成具有发夹环结构的单链RNA。将发夹RNA输出到细胞质后,发夹经Dicer加工形成双链体siRNA分子,然后被RISC进一步加工以介导靶基因沉默。在一些实施方案中,5'和/或3'接合裂解序列是siRNA靶序列。
在一些实施方案中,接合裂解序列是向导RNA(gRNA)靶序列。在这样的实施方案中,可以设计gRNA并将其与具有RNase活性的Cas核酸内切酶(例如,Cas13)一起引入,以在精确的接合位点介导病毒基因组转录物的裂解。在一些实施方案中,5'和/或3'接合裂解序列是gRNA靶序列。
在一些实施方案中,接合裂解序列是pri-miRNA编码序列。在编码次级病毒基因组的多核苷酸转录后,这些序列形成pri-miRNA茎环结构,然后在细胞核中被Drosha裂解,以在精确的接合位点裂解转录物。在一些实施方案中,5'和/或3'接合裂解序列是pri-mRNA靶序列。
在一些实施方案中,接合裂解序列是核酶编码序列,并介导病毒转录物的自裂解以产生次级溶瘤病毒的天然离散末端。示例性核酶包括锤头状核酶、Varkud卫星(VS)核酶、发夹状核酶、GIR1分支核酶、glmS核酶、绕线核酶(twister ribozyme)、绕线姐妹核酶(twister sister ribozyme)、手枪状核酶、斧状核酶和肝炎病毒核酶。在一些实施方案中,5'和/或3'接合裂解序列是核酶编码序列。
在一些实施方案中,接合裂解序列是编码配体诱导的自裂解核酶的序列,称为“适体酶”。适体酶是含有对配体具有特异性的整合适体结构域的核酶序列。配体与适体结构域的结合触发了核酶的酶活性的激活,从而导致RNA转录物的裂解。示例性适体酶包括茶碱依赖性的适体酶(例如,与茶碱依赖性的适体连接的锤头状核酶,描述于Auslander等人,MolBioSyst.(2010)6,807-814)、四环素依赖性的适体酶(例如与Tet依赖性的适体连接的锤头状核酶,描述于Zhong等人,eLife 2016;5:e18858 DOI:10.7554/eLife.18858;Win和Smolke,PNAS(2007)104;14283-14288;Whittmann和Suess,Mol Biosyt(2011)7;2419-2427;Xiao等人,Chem&Biol(2008)15;125-1137;以及Beilstein等人,ACS Syn Biol(2015)4;526-534)、鸟嘌呤依赖性的适体酶(例如,与鸟嘌呤依赖性的适体连接的锤头状核酶,描述于Nomura等人,Chem Commun.,(2012)48(57);7215-7217)。在一些实施方案中,5'和/或3'接合裂解序列是适体酶编码序列。
在一些实施方案中,接合裂解序列是siRNA分子、miRNA分子、AmiR分子或gRNA分子的靶序列。在这样的实施方案中,靶RNA分子与RNAi或gRNA分子的向导序列至少部分互补。用于比较和确定序列同一性百分比和互补性百分比的序列比对方法是本领域众所周知的。可以通过例如以下来进行序列的最佳比对以进行比较:Needleman和Wunsch的同源性比对算法,(1970)J.Mol.Biol.48:443;通过Pearson和Lipman的相似性搜索方法,(1988)Proc.Nat’l.Acad.Sci.USA 85:2444;通过这些算法的计算机化实施(Wisconsin Genetics软件包中的GAP、BESTFIT、FASTA和TFASTA,Genetics Computer Group,575Science Dr.,Madison,WI);手动比对和目视检查(参见例如Brent等人,(2003)Current Protocols inMolecular Biology);使用本领域已知的算法,包括BLAST和BLAST 2.0算法,其分别描述于Altschul等人,(1977)Nuc.Acids Res.25:3389-3402和Altschul等人,(1990)J.Mol.Biol.215:403-410。可通过国家生物技术信息中心(the National Center forBiotechnology Information)公开获得进行BLAST分析的软件。
在一些实施方案中,5'接合裂解序列和3'接合裂解序列来自同一组(例如,均为RNAi靶序列,均为核酶编码序列等)。例如,在一些实施方案中,接合裂解序列是RNAi靶序列(例如,siRNA、AmiR或miRNA靶序列),并掺入编码次级溶瘤病毒的多核苷酸的5'和3'末端。在这样的实施方案中,5'和3'RNAi靶序列可以相同(即,相同siRNA、AmiR或miRNA的靶标)或不同(即,5'序列是一种siRNA、shmiRNA或miRNA的靶标,而3'序列是另一种siRNA、AmiR或miRNA的靶标)。在一些实施方案中,接合裂解序列是向导RNA靶序列,并掺入编码次级溶瘤病毒的多核苷酸的5'和3'末端。在这样的实施方案中,5'和3'gRNA靶序列可以相同(即,相同gRNA的靶标)或不同(即,5'序列是一种gRNA的靶标,而3'序列是另一种gRNA的靶标)。在一些实施方案中,接合裂解序列是pri-mRNA编码序列,并掺入编码次级溶瘤病毒的多核苷酸的5'和3'末端。在一些实施方案中,接合裂解序列是核酶编码序列,并掺入编码次级溶瘤病毒的多核苷酸中靠近编码病毒基因组的多核苷酸序列的5'和3'末端。
在一些实施方案中,5'接头裂解序列和3'接头裂解序列来自相同组,但是是不同的变体或类型。例如,在一些实施方案中,5'和3'接合裂解序列可以是RNAi分子的靶序列,其中5'接合裂解序列是siRNA靶序列,而3'接合裂解序列是miRNA靶序列(或反之亦然)。在一些实施方案中,5'和3'接合裂解序列可以是核酶编码序列,其中5'接合裂解序列是锤头状核酶编码序列,而3'接合裂解序列是肝炎δ病毒核酶编码序列。
在一些实施方案中,5'接合裂解序列和3'接合裂解序列是不同类型。举例来说,在一些实施方案中,5'接合裂解序列是RNAi靶序列(例如siRNA、AmiR或miRNA靶序列),而3'接合裂解序列是核酶序列,适体酶序列,pri-miRNA序列或gRNA靶序列。在一些实施方案中,5'接合裂解序列是核酶序列,而3'接合裂解序列是RNAi靶序列(例如siRNA、AmiR或miRNA靶序列)、适体酶序列、pri-miRNA编码序列或gRNA靶序列。在一些实施方案中,5'接合裂解序列是适体酶序列,而3'接合裂解序列是RNAi靶序列(例如siRNA、AmiR或miRNA靶序列)、核酶序列、pri-miRNA序列或gRNA靶序列。在一些实施方案中,5'接合裂解序列是pri-miRNA序列,而3'接合裂解序列是RNAi靶序列(例如siRNA、AmiR或miRNA靶序列)、核酶序列、适体酶序列或gRNA靶序列。在一些实施方案中,5'接合裂解序列是gRNA靶序列,而3'接合裂解序列是RNAi靶序列(例如siRNA、AmiR或miRNA靶序列)、核酶序列、pri-miRNA序列或适体酶序列。
在一些实施方案中,5'接合裂解序列是AmiR靶序列,而3'接合裂解序列是核酶序列。
接合裂解序列相对于自主复制型多核苷酸的示例性排列在下表A和B中示出。
表A:对称接合裂解序列(JSC)排列
表B:不对称JCS排列
2.负义ssRNA病毒
在一些实施方案中,多核苷酸编码负义单链RNA(-义ssRNA)病毒基因组。-义ssRNA病毒的基因组包含呈3'-5'取向的ssRNA分子,并且无法直接翻译成蛋白。而是,负义ssRNA病毒的基因组必须首先通过RNA聚合酶转录为+义mRNA分子。示例性-义ssRNA病毒包括副粘病毒科(例如,麻疹病毒和新城鸡瘟病毒)、弹状病毒科(例如,水疱性口腔炎病毒(VSV)和马拉巴病毒)、沙粒病毒科(Arenaviridae)(例如,拉沙病毒)和正黏病毒科(例如,甲型、乙型、丙型和丁型流感等流感病毒)。
在一些实施方案中,编码-义ssRNA病毒基因组的自主复制型多核苷酸包含第一多核苷酸序列,所述第一多核苷酸序列编码可以直接翻译成复制-义ssRNA基因组所需的病毒蛋白的mRNA转录物;和第二多核苷酸序列,所述第二多核苷酸序列包含病毒基因组的反基因组序列。在一些实施方案中,第一多核苷酸序列和第二多核苷酸序列可操作地连接于能够在真核细胞中表达的启动子,例如哺乳动物启动子。在一些实施方案中,第一多核苷酸序列和第二多核苷酸序列可操作地连接于双向启动子,例如双向Pol II启动子(参见例如图9、10和11)。
在一些实施方案中,从相同的表达盒表达-义ssRNA基因组复制所需的病毒基因。在一些实施方案中,从不同的表达盒,例如两个或三个表达盒,例如每个基因一个表达盒,或三个基因中的两个为一个表达盒,第三个基因为另一个表达盒,表达-义ssRNA基因组复制所需的病毒基因。-义ssRNA基因组复制所需的病毒基因可以从相同的开放阅读框或两个或三个不同的开放阅读框翻译而来。在一个实施方案中,从单个开放阅读框共翻译表达-义ssRNA基因组复制所需的病毒基因,并在翻译后加工成成熟多肽。在一个实施方案中,-义ssRNA基因组复制所需的病毒基因通过2A肽序列连接,导致从开放阅读框翻译而来的成多肽自裂解成单个多肽。-义ssRNA基因组基因复制所需的病毒基因可以呈任何顺序排列。在一些实施方案中,表达盒包含-义ssRNA基因组复制所需的病毒基因中的一种或多种的功能变体。本领域技术人员将认识到如何根据特定的-义ssRNA病毒所需的遗传元件来工程化上述系统的适当变体。该工程化可以采取添加复制必需的附加基因的形式。
在一些实施方案中,将编码可直接翻译成复制所需的病毒蛋白的mRNA转录物的第一多核苷酸序列可操作地连接于能够在真核细胞中表达的启动子,例如哺乳动物Pol II启动子,并进一步编码T7聚合酶。在这样的实施方案中,第二多核苷酸序列可操作地连接于T7启动子。举例来说,在一些实施方案中,自主复制型多核苷酸包含以下结构:
(a)5'–[复制所需的病毒基因]–双向启动子–[反基因组病毒基因组]–3';
(b)5'–Pol II–[复制所需的病毒基因+T7 pol]–T7启动子–[反基因组病毒基因组]–3'。
(c)在某些实施方案中,编码-义ssRNA病毒基因组的自主复制型多核苷酸在5'和3'末端侧接AAV来源的ITR,例如:
(d)5'–ITR–[复制所需的病毒基因]–双向启动子–[反基因组病毒基因组]–ITR–3';
(e)5'–ITR–Pol II–[复制所需的病毒基因+T7 pol]–T7启动子–[反基因组病毒基因组]–ITR–3'。
B.双链RNA病毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码双链RNA(dsRNA)病毒基因组。示例性dsRNA病毒包括阿马尔加病毒科(Amalgaviridae)、伯纳德病毒科(Birnaviridae)、金病毒科(Chrysoviridae)、梭状病毒科(Cystoviridae)、内生病毒科(Endornaviridae)、次病毒科(Hypoviridae)、巨生物病毒科(Megabirnaviridae)、分体病毒科(Partitiviridae)、小双核糖核酸病毒科(Picobirnaviridae)、四组分病毒科(Quadriviridae)、呼肠孤病毒科、整体病毒科(Totiviridae)的成员。
在一些实施方案中,本文所述的自主复制型多核苷酸编码dsRNA病毒基因组。在一些实施方案中,dsRNA病毒基因组被编码为在负义(互补链)5'的正义链。因此,在一些实施方案中,dsRNA病毒基因组被转录为两个RNA分子,它们与DNA多核苷酸的相同链中的另一个互补。在一些实施方案中,dsRNA病毒基因组的两个RNA分子被转录为单个RNA,其例如通过核酶、核酸内切酶、基于CRISPR的系统等裂解成正义和负义分子。
在一个实施方案中,dsRNA病毒基因组是从共享的dsDNA模板转录的,该模板可操作地连接于侧接共享的dsDNA模板的启动子。一个启动子引起DNA多核苷酸的沃森链转录,从而产生dsRNA基因组的正链。另一启动子引起DNA多核苷酸的克里克链转录,从而产生dsRNA基因组的负链。一些dsRNA病毒(例如呼肠孤病毒)是分段病毒,这意味着它们的基因组由多个RNA分子构成,在某些情况下是dsRNA和ssRNA的混合物。本公开提供了DNA多核苷酸包含每个区段的转录单元的实施方案。在一些实施方案中,所述区段是从DNA多核苷酸的沃森和/或克里克链上的几个启动子转录而来的。在一些实施方案中,RNA区段是通过例如用核酶、核酸内切酶、基于CRISPR的系统等对一个或多个RNA区段的转录后裂解而产生。在一些实施方案中,系统的一个或多个启动子是T7启动子,并且该系统包含编码T7 RNA聚合酶的多核苷酸。在一些实施方案中,使用T7系统产生用于dsRNA病毒基因组的一个或多个区段的天然5'末端。在一些实施方案中,系统的一个或多个启动子是真核活性启动子,例如哺乳动物启动子。
C.单链DNA病毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码单链DNA(ssDNA)病毒基因组。示例性ssDNA病毒包括细小病毒科(例如腺相关病毒)、指环病毒科(Anelloviridae)、二分DNA病毒科(Bidnaviridae)、圆环病毒科(Circoviridae)、双生病毒科(Geminiviridae)、类双生病毒科(Genomoviridae)、丝形病毒科(Inoviridae)、微小噬菌体科(Microviridae)、矮化病毒科(Nanoviridae)、丝马病毒科(Smacoviridae)和嗜热圈形病毒科(Spiraviridae)的成员。在一个实施方案中,自主复制型多核苷酸编码细小病毒。在一实施方案中,自主复制型多核苷酸编码腺相关病毒(AAV)。
D.双链DNA病毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码双链DNA(dsDNA)病毒基因组。示例性dsDNA病毒包括肌病毒科(Myoviridae)、足病毒科(Podoviridae)、长尾病毒科(Siphoviridae)、异名病毒科(Alloherpesviridae)、疱疹病毒科(例如,HSV-1、HSV-1、马疱疹病毒)、痘病毒科(例如,牛痘病毒和粘液瘤病毒)。在一实施方案中,自主复制型多核苷酸编码腺病毒。
E.miRNA减毒
在一些实施方案中,本文所述的自主复制型多核苷酸编码包含插入一个或多个必需病毒基因中的一个或多个微小RNA(miRNA)靶序列的具有复制能力的病毒基因组。miR调节编码多种蛋白质,包括那些参与细胞增殖和凋亡控制的蛋白质的许多转录物。由miR调节的示例性蛋白质包括常规的原癌蛋白和肿瘤抑制因子,如Ras、Myc、Bcl2、PTEN和p53。
miRNA与正常细胞过程密切相关,其失调导致多种疾病,包括癌症。重要的是,与正常组织相比,miRNA在癌症组织中差异表达,从而使它们能够在多种癌症中充当靶向机制。与致癌、恶性转化或转移相关(正或负)的miRNA被称为“oncomiR”。表2提供了特定癌症中的oncomiR及其相对表达的列表。
在某些方面,特定miRNA的表达与特定癌症的发展或维持和/或转移正相关。这类miR在本文中称为“致癌miRNA”或“oncomiR”。在一些实施方案中,致癌miRNA在癌细胞或组织中的表达与在非癌对照细胞(即,正常或健康对照)中观察到的表达水平相比增加,或与在源自不同癌症类型的癌细胞中观察到的表达水平相比增加。例如,致癌miRNA在癌细胞中的表达与致癌miRNA在非癌对照细胞或源自不同癌症类型的癌细胞中的表达相比可能至少增加5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、60%、70%、80%、90%、100%、150%、200%、300%、400%、500%、1000%或更多。在一些方面,癌细胞可能表达在非癌对照细胞中不表达的致癌miRNA。
在一些实施方案中,特定oncomiR的表达与特定癌症的发展或维持和/或转移负相关。这类oncomiR在本文中称为“肿瘤抑制miRNA”或“肿瘤抑制性miRNA”,因为它们的表达阻止或抑制了癌症的发展。在一些实施方案中,肿瘤抑制miRNA在癌细胞或组织中的表达与在非癌对照细胞(即,正常或健康对照)中观察到的表达水平相比降低,或与在源自不同癌症类型的癌细胞中观察到的肿瘤抑制miRNA的表达水平相比降低。例如,肿瘤抑制miRNA在癌细胞中的表达与肿瘤抑制miRNA在非癌对照细胞或源自不同癌症类型的癌细胞中的表达相比可能至少降低5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、60%、70%、80%、90%或100%。在一些方面,非癌对照细胞可能表达在癌细胞中不表达的肿瘤抑制miRNA。
通常,将特定的miRNA指定为致癌还是肿瘤抑制性miRNA将根据癌症的类型而变化。例如,一种miRNA的表达在特定癌症中可能增加并且与该癌症的发展相关,而同一miRNA的表达在不同癌症中可能降低并且与该癌症的发展的预防有关。但是,一些miRNA可能起致癌miRNA的作用,与癌症的类型无关。例如,一些miRNA靶向肿瘤抑制基因的mRNA转录物进行降解,从而减少肿瘤抑制蛋白的表达。表2提供了几种癌症以及在每种癌症类型中观察到的相应的“上调”的miRNA和“下调”的miRNA的列表。在表2中,上调的miRNA是在该特定癌症中可能致癌的miRNA,而下调的miRNA在该特定癌症中可能是肿瘤抑制性的。表3示出了其它肿瘤抑制性miRNA的列表。表1示出了12种精选oncomiR(9种肿瘤抑制miRNA和3种致癌miRNA)与多种癌症之间的关系。
在一些方面,通过在病毒基因组中一个或多个位置处掺入一种或多种miRNA靶序列,将由本文所述的多核苷酸产生的病毒的复制限于肿瘤细胞。在一些实施方案中,将一种或多种miRNA靶序列掺入具有复制能力的病毒基因组的5'UTR和/或3'UTR中。在一些实施方案中,将一种或多种miRNA靶序列掺入必需病毒基因的一个或多个基因座中。如本文所用,“必需病毒基因”是指病毒复制、病毒基因产物装配成感染性颗粒所必需或维持所装配的感染性颗粒的结构完整性所必需的病毒基因。在一些实施方案中,必需病毒基因可包括UL1、UL5、UL6、UL7、UL8、UL9、UL11、UL12、UL14、UL15、UL17、UL18、UL19、UL20、UL22、UL25、UL26、UL26.5、UL27、UL28、UL29、UL30、UL31、UL32、UL33、UL34、UL35、UL36、UL37、UL38、UL39、UL40、UL42、UL48、UL49、UL50、UL52、UL53、UL54、US1、US3、US4、US5、US6、US7、US8、US12、ICP0、ICP4、ICP22、ICP27、ICP47、PB、F、B5R、SERO-1、Cap、Rev、VP1-4、核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)、聚合酶(L)、E1、E2、E3、E4、VP1、VP2、VP3、VP4、2A、2B、2C、3A、3B、3C和3D。
在一些实施方案中,插入到必需病毒基因的一个或多个基因座中的miRNA靶序列对应于由正常的非癌细胞表达的并且在癌细胞中不表达或显示表达减少的miRNA。在正常(非癌)细胞中表达的miRNA将与多核苷酸中相应的靶序列结合,并抑制含有miRNA靶序列的病毒基因的表达,从而阻止病毒复制和/或结构装配成感染性颗粒。因此,miRNA靶序列的插入保护正常细胞免受编码病毒的溶解作用。在一些实施方案中,miRNA靶序列是肿瘤抑制性miRNA(例如,表3中列出的miRNA)的靶序列。在一些实施方案中,多核苷酸可包含被插入到至少一个、至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个、至少九个或至少十个必需病毒基因的基因座中的miRNA靶序列。在一些实施方案中,一种或多种miRNA靶序列掺入一个或多个必需病毒基因的5'非翻译区(UTR)和/或3'UTR中。在一些实施方案中,一种或多种miRNA靶序列掺入病毒基因组(例如γ34.5)中的非必需基因的3'或5'UTR中。
在一些实施方案中,本文所述的多核苷酸包含被掺入必需病毒基因的基因座中的miRNA靶序列。在一些方面,本文所述的自主复制型多核苷酸包含多个被掺入一个或多个必需病毒基因中的miRNA靶序列。在一些实施方案中,多核苷酸包含被掺入多个(例如2个或更多个)必需病毒基因中的miRNA靶序列。例如,本文所述的多核苷酸可以包含被插入到2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个必需病毒基因中的miRNA靶序列。在这样的实施方案中,每个必需病毒基因将包含一个miRNA靶序列,而多核苷酸整体上将包含多个miRNA靶序列。在这样的实施方案中,多个miRNA靶序列可以对应于相同的miRNA。举例来说,本文所述的多核苷酸可包含被插入到2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个必需病毒基因中的相同的miRNA靶序列。在这样的实施方案中,多个miRNA靶序列可以对应于两种或更多种不同的miRNA。例如,本文所述的多核苷酸可包含对应于被插入到第一必需病毒基因中的第一miRNA的miRNA靶序列、对应于被插入到第二必需病毒基因中的第二miRNA的miRNA靶序列、对应于被插入到第三必需病毒基因中的第三miRNA的miRNA靶序列等等。
在一些实施方案中,miRNA靶序列的多个拷贝掺入必需病毒基因的基因座中。例如,在一些实施方案中,可以将miRNA靶序列的2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个拷贝插入到必需病毒基因的基因座中。在一些实施方案中,插入到必需病毒基因的基因座中的多个miRNA靶序列中的每一个对应于相同的miRNA。在一些实施方案中,插入到必需病毒基因的基因座中的多个miRNA靶序列中的每一个对应于不同的miRNA。举例来说,对应于2种、3种、4种、5种、6种、7种、8种、9种、10种或更多种不同的miRNA的miRNA靶序列可插入到必需病毒基因的基因座中。
在一些实施方案中,miRNA靶序列的多个拷贝掺入多个必需病毒基因的基因座中。举例来说,在一些实施方案中,miRNA靶序列的2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个拷贝可插入到2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个必需病毒基因的基因座中。在一些实施方案中,插入到特定必需病毒基因中的多个miRNA靶序列可均对应于相同的miRNA。例如,在一些实施方案中,第一必需病毒基因可包含各自对应于第一miRNA的多个miRNA靶序列,而第二必需病毒基因可包含各自对应于第二miRNA的多个miRNA靶序列。在一些实施方案中,自主复制型多核苷酸可进一步包含第三个、第四个、第五个、第六个、第七个、第八个、第九个或第十个必需病毒基因,所述必需病毒基因包含各自分别对应于第三种、第四种、第五种、第六种、第七种、第八种、第九种或第十种miRNA的多个miRNA靶序列。
在一些实施方案中,对应于不同的miRNA的多个miRNA靶序列被插入到多个必需病毒基因基因座中。举例来说,在一些实施方案中,第一必需病毒基因可包含对应于两种或更多种不同的miRNA的多个miRNA靶序列,并且第二必需病毒基因可包含对应于两种或更多种不同的miRNA的多个miRNA靶序列。在这样的实施方案中,第一必需病毒基因中的miRNA靶序列可以与第二必需病毒基因中的miRNA靶序列相同或不同。在一些实施方案中,自主复制型多核苷酸还可包含第三个、第四个、第五个、第六个、第七个、第八个、第九个或第十个必需病毒基因,各自包含对应于不同的miRNA的多个miRNA靶序列。在一些实施方案中,第一个、第二个、第三个、第四个、第五个、第六个、第七个、第八个、第九个或第十个必需病毒基因中的任何一个中的miRNA靶序列可以与其它必需病毒基因中的任何一个中的miRNA靶序列相同。在一些实施方案中,第一个、第二个、第三个、第四个、第五个、第六个、第七个、第八个、第九个或第十个必需病毒基因中的任何一个中的miRNA靶序列可以与其它必需病毒基因中的任何一个中的miRNA靶序列不同。
在一些实施方案中,多个miRNA靶序列串联插入到一个或多个必需病毒基因的基因座中,并通过接头序列或间隔子序列彼此分开。在一些实施方案中,接头或间隔子间隔序列包含4个或更多个核苷酸。在一些实施方案中,接头或间隔子间隔序列包含5个、6个、7个、8个、9个、10个或更多个核苷酸。在一实施方案中,接头序列或间隔子序列包含至少4个至至少6个核苷酸。
在一些实施方案中,至少1个、2个、3个、4个、5个、6个、7个、8个、9个、10或更多个以下任一亚基串联插入到一个或多个必需病毒基因的基因座中:(a)第一miRNA的靶序列-接头或间隔子序列-第一miRNA的靶序列;或(b)第一个miRNA的靶序列-接头或间隔子序列-第二个miRNA的靶序列。在一些实施方案中,miRNA靶序列是表3中列出的任一个或多个miRNA的靶序列。
F.有效载荷分子
在一些实施方案中,本文所述的多核苷酸包含编码有效载荷分子的核酸序列。在一些实施方案中,编码有效载荷分子的核酸作为与编码具有复制能力的病毒基因组的重组核酸分子分开的第二多核苷酸存在。如本文所用,“有效载荷分子”(也称为“治疗性分子”)是指能够进一步增强由本文所述的自主复制型多核苷酸编码的病毒或其感染性颗粒的治疗功效的任何分子。适用于本公开的有效载荷分子包括蛋白质或肽,例如细胞毒性肽、免疫调节肽(例如,抗原结合分子如抗体或其抗原结合片段、细胞因子、趋化因子、可溶性受体、细胞表面受体配体、二分肽和酶。这类有效载荷分子还可包含核酸(例如,shRNA、siRNA、反义RNA、antagomir、核酶和适体)。有效载荷分子的性质将随疾病类型和所需治疗结果而变化。
在一些实施方案中,一种或多种miRNA靶序列掺入编码有效载荷分子的多核苷酸序列的3'或5'UTR中。在这样的实施方案中,有效载荷的翻译和随后的表达在表达相应miRNA的细胞中不发生或基本上不减少。在一些实施方案中,一种或多种miRNA靶序列插入到编码治疗性多肽的多核苷酸序列的3'和/或5'UTR中。
在一些实施方案中,治疗性分子的表达可以由转录控制元件进一步调节,所述转录控制元件驱动癌细胞中的治疗性分子的表达与非癌细胞相比增加(例如,源自hTERT、HE4、CEA、OC、ARF、CgA、GRP78、CXCR4、HMGB2、INSM1、间皮素、OPN、RAD51、TETP、H19、uPAR、ERBB2、MUC1、Frz1、IGF2-P4的启动子,或低氧(HRE)和辐射反应元件)。在一些实施方案中,有效载荷分子的表达在与自主复制型多核苷酸相同的转录控制元件的控制下。
在一些实施方案中,本文所述的重组核酸分子包含自主复制型多核苷酸,并且还包含编码细胞毒性肽的多核苷酸。如本文所用,“细胞毒性肽”是指当在宿主细胞中表达时能够诱导细胞死亡,和/或当宿主细胞分泌时,能够诱导邻近细胞的细胞死亡的蛋白质。在一些实施方案中,细胞毒性肽是胱天蛋白酶、p53、白喉毒素(DT)、假单胞菌外毒素A(PEA)、I型核糖体失活蛋白(RIP)(例如肥皂草素(saporin)和白树毒素(gelonin))、II型RIP(例如蓖麻毒素)、志贺样毒素1(Slt1)、光敏活性氧(例如杀手红)。在某些实施方案中,细胞毒性肽由通过细胞凋亡引起细胞死亡的自杀基因,例如胱天蛋白酶基因编码。
在一些实施方案中,有效载荷是免疫调节肽。如本文所用,“免疫调节肽”是能够调节(例如,激活或抑制)特定免疫受体和/或通路的肽。在一些实施方案中,免疫调节肽可作用于任何哺乳动物细胞,包括免疫细胞、组织细胞和基质细胞。在一个优选的实施方案中,免疫调节肽作用于免疫细胞,例如T细胞、NK细胞、NKT T细胞、B细胞、树突状细胞、巨噬细胞、嗜碱性粒细胞、肥大细胞或嗜酸性粒细胞。示例性免疫调节肽包括抗原结合分子如抗体或其抗原结合片段、细胞因子、趋化因子、可溶性受体、细胞表面受体配体、二分肽和酶。
在一些实施方案中,有效载荷是细胞因子,例如IL-1、IL-2、IL-12、IL-15、IL-18、IL-36、IL-36γ、LIGHT(TNFSF14/CD258)、TNFα、IFNα、IFNβ或IFNγ。在一些实施方案中,有效载荷是选自IL-2、IL-18、LIGHT和IL-36γ的细胞因子。在一些实施方案中,有效载荷是编码如CXCL10、CXCL9、CCL21、CCL4或CCL5的趋化因子的多核苷酸。在一些实施方案中,有效载荷是选自CCL21、CCL4和CCL5的趋化因子。在一些实施方案中,有效载荷是细胞表面受体的配体,例如NKG2D配体、神经纤毛蛋白配体、Flt3配体、CD47配体(例如SIRP1α)。在一些实施方案中,有效载荷是可溶性受体,例如可溶性细胞因子受体(例如IL-13R、TGFβR1、TGFβR2、IL-35R、IL-15R、IL-2R、IL-12R和干扰素受体)或可溶性先天免疫受体(例如toll样受体、补体受体等)。在一些实施方案中,有效载荷是参与细胞内RNA和/或DNA感应的蛋白质的显性激动剂突变体(例如STING、RIG-1或MDA-5的显性激动剂突变体)。
在一些实施方案中,有效载荷是抗原结合分子,例如抗体或其抗原结合片段(例如单链可变片段(scFv)、F(ab)等)。在一些实施方案中,抗原结合分子特异性结合细胞表面受体,例如免疫检查点受体(例如PD1、PDL1、CTLA4和CD47)或参与细胞生长和活化的其它细胞表面受体(例如OX40、CD200R、CSF1R、41BB、CD40和NKG2D)。
在一些实施方案中,有效载荷分子是蝎多肽,例如氯毒素(chlorotoxin)、BmKn-2、新普拉丁(neopladine)1、新普拉丁2和莫瑞泊林(mauriporin)。在一些实施方案中,治疗性分子是蛇多肽,例如蛇毒解聚素(contortrostatin)、载脂蛋白-I(apoxin-I)、矛头蝮蛇毒素(bothropstoxin)-I、BJcuL、OHAP-1、蛇毒蛋白(rhodostomin)、drCT-1、CTX-III、B1L和ACTX-6。在一些实施方案中,有效载荷分子是蜘蛛多肽,例如拉塔蛋白(latarcin)和透明质酸酶。在一些实施方案中,有效载荷分子是蜜蜂多肽,例如蜂毒素(melittin)和蜂毒明肽(apamin)。在一些实施方案中,有效载荷分子是蛙多肽,例如PsT-1、PdT-1和PdT-2。
在一些实施方案中,有效载荷是酶。在一些实施方案中,酶能够通过改变细胞外基质来调节肿瘤微环境。在这样的实施方案中,酶可以包括但不限于基质金属蛋白酶(例如MMP9)、胶原酶、透明质酸酶、明胶酶或弹性蛋白酶。在一些实施方案中,酶是基因导向性酶前药疗法(GDEPT)系统的一部分,例如单纯疱疹病毒胸苷激酶、胞嘧啶脱氨酶、硝基还原酶、羧肽酶G2、嘌呤核苷磷酸化酶或细胞色素P450。在一些实施方案中,酶能够诱导或激活靶细胞(例如,胱天蛋白酶)中的细胞死亡通路。
在一些实施方案中,有效载荷分子是二分肽。如本文所用,“二分肽”是指由能够结合在非癌性效应细胞上表达的细胞表面抗原的第一结构域和能够结合由靶细胞(例如癌细胞、肿瘤细胞或不同类型的效应细胞)表达的细胞表面抗原的第二结构域构成的多聚体蛋白。在一些实施方案中,二分多肽的单个多肽结构域可包含抗体或其结合片段(例如单链可变片段(scFv)或的F(ab))、蝎多肽、双功能抗体、柔性抗体、DOCK-AND-LOCK
表5:临床前和临床研究中使用的经过验证的BiTE
在一些实施方案中,在效应细胞上表达的细胞表面抗原选自下表6。在一些实施方案中,在肿瘤细胞或效应细胞上表达的细胞表面抗原选自下表7。在一些实施方案中,在肿瘤细胞上表达的细胞表面抗原是肿瘤抗原。在一些实施方案中,肿瘤抗原选自CD19、EpCAM、CEA、PSMA、CD33、EGFR、Her2、EphA2、MCSP、ADAM17、PSCA、17-A1、NKGD2配体、CSF1R、FAP、GD2、DLL3或神经纤毛蛋白(neuropilin)。在一些实施方案中,肿瘤抗原选自EpCam、DLL3和CEA。在一些实施方案中,肿瘤抗原选自表7中列出的那些。
表6:示例性效应细胞靶抗原
表7:示例性靶细胞抗原
III.产生包含自主复制型多核苷酸的重组核酸分子的方法
在一些实施方案中,使用一种或多种载体在体外产生本文所述的重组核酸分子。术语“载体”在本文中用以指能够转移或转运另一种核酸分子的核酸分子。所转移的核酸一般被插入载体核酸分子中。载体可以包括指导细胞中的自主复制的序列和/或可以包括足以允许整合至宿主细胞DNA中的序列。
在一些实施方案中,通过将本文所述的自主复制型多核苷酸插入到质粒主链中来产生本文所述的重组核酸分子。
在一些实施方案中,使用一种或多种病毒载体产生本文所述的重组核酸分子。病毒载体有时可称为“重组病毒”或“病毒”。在一些实施方案中,使用两载体系统。举例来说,在一些实施方案中,本文所述的自主复制型多核苷酸侧接AAV来源的ITR。然后侧接ITR的多核苷酸被插入到第一表达载体中,并且编码ITR介导的复制所必需的AAV蛋白(例如Rep78和Rep52)的多核苷酸被插入到第二表达载体中。在这样的实施方案中,第一载体和第二载体在细胞内递送(例如借助于转染、转导、电穿孔等)至合适的宿主细胞(例如昆虫细胞系),产生其中侧接ITR的多核苷酸稳定地整合至宿主细胞的基因组中的细胞。在一些实施方案中,第一载体和第二载体是疱疹病毒表达载体。在一些实施方案中,第一载体和第二载体是杆状病毒表达载体。这种表达系统描述于例如Li等人,Plos One,8:8,2013中。在一些实施方案中,宿主细胞产生的侧接ITR的自主复制型多核苷酸的量超过在缺乏ITR的情况下产生的量。在一些实施方案中,来自经侧接ITR的转基因转染的宿主细胞的侧接ITR的病毒基因组DNA可能比不含ITR的类似转染的转基因(例如经由重组杆状病毒感染)产生4至60倍更多的DNA(参见Li等人,PLoS One,2013)。
在一些实施方案中,使用单一载体表达系统在体外产生本文所述的多核苷酸。例如,在一些实施方案中,包含侧接AAV ITR的本文所述的自主复制型多核苷酸的表现盒被插入在重组HSV基因组主链的UL3与UL4基因之间(例如基因间基因座中)或ICP4基因座(参见例如图4B和图5B)。包含编码ITR介导的复制所必需的AAV蛋白(例如Rep78和Rep52)的多核苷酸的第二表现盒被插入到重组HSV基因组主链的ICP0或ICP4基因座中。Rep蛋白的表达使得侧接ITR的多核苷酸能够从单一载体有效复制。在一些实施方案中,编码Rep蛋白的多核苷酸可操作地连接于可调控型或诱导型启动子。
在一些实施方案中,本文所述的重组核酸分子通过细胞内(例如借助于转染、转导、电穿孔等)递送HSV载体至合适宿主细胞来产生,所述HSV载体包括包含侧接ITR的自主复制型多核苷酸的表现盒和包含编码ITR介导的复制的所必需的AAV蛋白的多核苷酸的表现盒。合适的宿主细胞包括昆虫和哺乳动物细胞系。将包含HSV载体的宿主细胞培养适当时间量,允许所插入的表现盒的表达和重组DNA分子的产生。然后从宿主细胞DNA分离重组DNA分子并且配制用于治疗用途(例如包封在颗粒中)。
在一些实施方案中,由上述AAV-ITR系统产生的重组DNA分子引起每端共价连接在一起的两个单链DNA分子的产生。例如,第一DNA分子的5'ITR共价连接于第二DNA分子的3'ITR并且第一DNA分子的3'ITR共价连接于所述第二DNA分子的5'ITR。在这样的实施方案中,共价连接的侧接ITR的多核苷酸形成末端封闭的线性双链体溶瘤病毒核酸分子,在本文中称为NanoV分子。在一些实施方案中,单链DNA分子中的每一个包含单一侧接ITR的多核苷酸。例如,在一些实施方案中,NanoV分子包含两个ssDNA分子,其中一个ssDNA分子包含以下结构:5'–ITR–[自主复制型多核苷酸的有义序列]–ITR–3';并且其中一个ssDNA分子包含以下结构:3'–ITR–[自主复制型多核苷酸的反义序列]–ITR–3'。在一些实施方案中,单链DNA分子中的每一个包含两个或更多个侧接ITR的多核苷酸(即侧接ITR的多核苷酸的串联体)。侧接ITR的多核苷酸的串联体可以具有多种取向。例如,在一些实施方案中,串联体以头接头取向或尾接尾取向形成。
IV.包含自主复制型多核苷酸的颗粒
在一些实施方案中,本文所述的多核苷酸被包封在“颗粒”中。如本文所用,颗粒是指物质的非组织来源的组合物,例如脂质体、脂质体复合物、纳米颗粒、纳米胶囊、微粒、微球体、脂质颗粒、外泌体、囊泡等。在某些实施方案中,颗粒是非蛋白质的和非免疫原性的。在这样的实施方案中,本文所述的多核苷酸的包封允许在不诱发全身性的抗病毒免疫应答下递送病毒有效载荷并且减轻中和抗病毒抗体的作用。此外,本文所述的多核苷酸的包封保护多核苷酸避免降解,并促进多核苷酸引入至靶宿主细胞中。
在一些实施方案中,颗粒在受试者中是生物可降解的。在这样的实施方案中,可以向受试者施用多剂颗粒,颗粒不会在受试者中累积。合适颗粒的实例包括聚苯乙烯颗粒、聚(乳酸-共-乙醇酸)PLGA颗粒、基于多肽的阳离子聚合物颗粒、环糊精颗粒、壳聚糖颗粒、基于脂质的颗粒、聚(β-氨基酯)颗粒、低分子量聚乙烯亚胺颗粒、聚磷酸酯颗粒、二硫化物交联的聚合物颗粒、聚酰胺胺颗粒、聚乙烯亚胺(PEI)颗粒和PLURIONICS稳定的聚硫化丙烯颗粒。
在一些实施方案中,本文所述的多核苷酸包封在无机颗粒中。在一些实施方案中,无机颗粒是金纳米颗粒(GNP)、金纳米棒(GNR)、磁性纳米颗粒(MNP)、磁性纳米管(MNT)、碳纳米角(CNH)、碳富勒烯、碳纳米管(CNT)、磷酸钙纳米颗粒(CPNP)、介孔二氧化硅纳米颗粒(MSN)、二氧化硅纳米管(SNT)或星形中空二氧化硅纳米颗粒(SHNP)。
A.外泌体
在一些实施方案中,本文所述的多核苷酸包封在外泌体中。外泌体是内吞起源的小膜囊泡,在多囊泡体与亲本细胞(例如,释放外泌体的细胞,在本文中也称为供体细胞)的质膜融合后释放到细胞外环境中。外泌体的表面包含源自亲本细胞的细胞膜的脂质双层,并且还可包含在亲本细胞表面表达的膜蛋白。在一些实施方案中,外泌体还可含有来自亲本细胞的胞液。外泌体由许多不同的细胞类型产生,包括上皮细胞、B和T淋巴细胞、肥大细胞(MC)和树突状细胞(DC),并已在血浆、尿液、支气管肺泡灌洗液、肠上皮细胞和肿瘤组织中鉴定出。由于外泌体的组成取决于其源自的亲本细胞类型,因此不存在“外泌体特异性”蛋白。但是,许多外泌体包含与亲本细胞中外泌体源自于的胞内囊泡相关的蛋白质(例如,与内体和溶酶体相关和/或由内体和溶酶体表达)。例如,外泌体可以富含抗原呈递分子,例如主要组织相容性复合物I和II(MHC-I和MHC-II)、四跨膜蛋白(例如CD63)、几种热休克蛋白、细胞骨架成分(例如肌动蛋白和微管蛋白)、参与细胞内膜融合的蛋白质、细胞间相互作用(例如CD54)、信号转导蛋白和胞浆酶。
外泌体可以通过外泌体膜与靶细胞的质膜融合来介导细胞蛋白从一个细胞(例如,亲本细胞)转移到靶细胞或受体细胞。这样,修饰被外泌体包封的物质提供了一种机制,通过该机制可以将外源性剂(例如本文所述的多核苷酸)引入靶细胞。已经被修饰成含有一种或多种外源剂的外泌体(例如,本文所述的多核苷酸)在本文中称为“修饰的外泌体”。在一些实施方案中,通过将外源剂(例如,本文所述的多核苷酸)引入亲本细胞中来产生修饰的外泌体。在这样的实施方案中,将外源核酸引入产生外泌体的亲本细胞中,从而将外源核酸本身或外源核酸的转录物掺入由亲本细胞产生的修饰的外泌体中。可以通过本领域已知的方法,例如转导、转染、转化和/或显微注射外源核酸,将外源核酸引入亲本细胞。
在一些实施方案中,通过直接将本文所述的多核苷酸引入外泌体中来产生修饰的外泌体。在一些实施方案中,本文所述的多核苷酸引入完整外泌体中。“完整外泌体”是指包含源自产生外泌体的亲本细胞的蛋白质和/或遗传物质的外泌体。获得完整外泌体的方法是本领域已知的(参见例如Alvarez-Erviti L.等人,Nat Biotechnol.2011年4月;29(4):34-5;Ohno S等人,Mol Ther 2013年1月;21(l):185-91;以及EP专利公布No.2010663)。
在特定实施方案中,将外源剂(例如,本文所述的多核苷酸)引入空外泌体中。“空外泌体”是指缺乏源自亲本细胞的蛋白质和/或遗传物质(例如DNA或RNA)的外泌体。产生空外泌体(例如,缺乏亲本细胞来源的遗传物质)的方法是本领域已知的,包括紫外线暴露、介导核酸负载到外泌体中的内源蛋白质的突变/缺失,以及对外泌体膜中的开孔进行电穿孔和化学处理,以使内源遗传物质通过开孔从外泌体中出来。在一些实施方案中,通过用pH为约9至约14的水溶液处理来打开外泌体以获得外泌体膜,除去囊泡内组分(例如,囊泡内蛋白质和/或核酸),并重新装配外泌体膜以形成空外泌体,从而产生空外泌体。在一些实施方案中,囊泡内组分(例如,囊泡内蛋白质和/或核酸)通过超速离心或密度梯度超速离心来除去。在一些实施方案中,通过超声处理、机械振动、通过多孔膜的挤出、电流或这些技术中的一种或多种的组合来重新装配膜。在特定实施方案中,通过超声处理将膜重新装配。
在一些实施方案中,可以使用常规的分子生物学技术,如体外转化、转染和/或显微注射,实现完整或空外泌体负载外源剂(例如,本文所述的多核苷酸)以产生修饰的外泌体。在一些实施方案中,外源剂(例如本文所述的多核苷酸)通过电穿孔直接引入至完整或空外泌体中。在一些实施方案中,外源剂(例如本文所述的多核苷酸)通过脂质体转染(例如转染)直接引入至完整或空外泌体中。适用于产生根据本公开的外泌体的脂质体转染试剂盒在本领域中是已知的并且是可商购(例如,来自Roche的
可以从许多不同的亲本细胞,包括细胞系、骨髓来源的细胞和源自初代患者样品的细胞中获得外泌体。可以通过本领域已知的方法从亲本细胞培养物的上清液中分离出从亲本细胞释放的外泌体。例如,外泌体的物理性质可用于将它们与介质或其它原材料分离,包括基于电荷(例如电泳分离)、尺寸(例如过滤、分子筛等)、密度(例如常规或梯度离心)和斯韦德贝里常数(Svedberg constant)(例如,在有或没有外力作用下的沉降等)分离。替代地或另外地,分离可以基于一种或多种生物学特性,并且包括可以采用表面标记的方法(例如,用于沉淀、与固相的可逆结合、FACS分离、特异性配体结合、非特异性配体结合等)。外泌体表面蛋白的分析可以通过流式细胞术,使用针对外泌体相关蛋白(例如CD63)的荧光标记的抗体来确定。用于表征外泌体的其它标记在国际PCT公布No.WO 2017/161010中进行了描述。在进一步预期的方法中,外泌体也可以使用化学方法和/或物理方法融合,包括PEG诱导的融合和/或超声融合。
在一些实施方案中,可以使用尺寸排阻色谱法分离外泌体。在一些实施方案中,如本领域通常已知的,外泌体可以在色谱法分离之后,通过离心技术分离(一种或多种色谱分离级分)进一步分离。在一些实施方案中,外泌体的分离可涉及方法的组合,所述方法包括但不限于如先前所述的差速离心(参见Raposo,G.等人,J.Exp.Med.183,1161-1172(1996))、超速离心、基于尺寸的膜过滤、浓缩和/或速率区带离心。
在一些实施方案中,外泌体膜包含磷脂、糖脂、脂肪酸、鞘脂、磷酸甘油酯、固醇、胆固醇和磷脂酰丝氨酸中的一种或多种。另外,膜可包含一种或多种多肽和一种或多种多糖,例如聚糖。示例性的外泌体膜组合物和用于改变一种或多种膜组分的相对量的方法描述于国际PCT公布No.WO 2018/039119。
优选地,本文所述的颗粒是纳米尺寸的,以提高溶解度,避免由体内聚集引起的可能的并发症并促进胞饮作用。在一些实施方案中,颗粒具有约小于约1000nm的平均直径。在一些实施方案中,颗粒具有小于约500nm的平均直径。在一些实施方案中,颗粒具有介于约30nm与约100nm之间、介于约50nm与约100nm之间或介于约75nm与约100nm之间的平均直径。在一些实施方案中,颗粒具有介于约30nm与约75nm之间或约30nm与约50nm之间的平均直径。在一些实施方案中,颗粒具有介于约100nm与约500nm之间的平均直径。在一些实施方案中,颗粒具有介于约200nm与400nm之间的平均直径。在一些实施方案中,颗粒具有约350nm的平均尺寸。
在一些实施方案中,颗粒是外泌体并且具有介于约30nm与约100nm之间、介于约30nm与约200nm之间或介于约30nm与约500nm之间的直径。在一些实施方案中,颗粒是外泌体并且具有介于约10nm与约100nm之间、介于约20nm与约100nm之间、介于约30nm与约100nm之间、介于约40nm与约100nm之间、介于约50nm与约100nm之间、介于约60nm与约100nm之间、介于约70nm与约100nm之间、介于约80nm与约100nm之间、介于约90nm与约100nm之间、介于约100nm与约200nm之间、介于约100nm与约150nm之间、介于约150nm与约200nm之间、介于约100nm与约250nm之间、介于约250nm与约500nm之间或介于约10nm与约1000nm之间的直径。在一些实施方案中,颗粒是外泌体并且具有介于约20nm与300nm之间、介于约40nm与200nm之间、介于约20nm与250nm之间、介于约30nm与150nm之间或介于约30nm与100nm之间的直径。
B.脂质纳米颗粒
在某些实施方案中,本文所述的重组DNA分子包封在脂质纳米颗粒(LNP)中。在某些实施方案中,LNP包含一种或多种脂质,例如甘油三酯(例如三硬脂酸甘油酯)、甘油二酯(例如山嵛酸甘油酯)、甘油单酯(例如单硬脂酸甘油酯)、脂肪酸(例如硬脂酸)、类固醇(例如胆固醇)和蜡(例如棕榈酸十六烷酯)。在一些实施方案中,LNP包含一种或多种阳离子型脂质和一种或多种辅助脂质。在一些实施方案中,LNP包含一种或多种阳离子型脂质、胆固醇和一种或多种中性脂质
阳离子型脂质是指在选定的pH值(例如生理pH值)下带有净正电荷的多种脂质中的任何一种。这类脂质包括但不限于1,2-二亚油基氧基-N,N-二甲基氨基丙烷(DLinDMA)、1,2-二亚麻基氧基-N,N-二甲基氨基丙烷(DLenDMA)、二-十八烷基二甲基铵(DODMA)、二硬脂基二甲基铵(DSDMA)、N,N-二油烯基-N,N-二甲基氯化铵(DODAC);N-(2,3-二油烯基氧基)丙基)-N,N,N-三甲基氯化铵(DOTMA);N,N-二硬脂基-N,N-二甲基溴化铵(DDAB);N-(2,3-二油酰氧基)丙基)-N,N,N-三甲基氯化铵(DOTAP);3-(N-(N’,N’-二甲基氨基乙烷)-氨基甲酰基)胆固醇(DC-Chol)和N-(1,2-二肉豆蔻基氧基丙-3-基)-N,N-二甲基-N-羟乙基溴化铵(DMRIE)。例如,在低于生理pH值的条件下具有正电荷的阳离子型脂质包括但不限于DODAP、DODMA和DMDMA。在一些实施方案中,阳离子型脂质包含C
在一些实施方案中,阳离子型脂质包含可质子化的叔胺头基。这样的脂质在本文中称为可电离的脂质。可电离的脂质是指包含可电离的胺头基且典型地包含小于约7的pKa的脂质种类。因此,在酸性pH的环境中,可电离的胺头基被质子化,使得可电离的脂质优先与带负电荷的分子(例如核酸,例如本文所述的重组多核苷酸)相互作用,从而促进纳米颗粒的装配和包封。因此,在一些实施方案中,可电离的脂质可以增加核酸在脂质纳米颗粒中的负载。在pH值大于约7(例如约7.4的生理pH值)的环境中,可电离的脂质包含中性电荷。当包含可离子的脂质的颗粒被吸收到内体的低pH环境(例如pH<7)时,可电离的脂质再次质子化并与阴离子内体膜缔合,从而促进了被颗粒包封的内容物的释放。在一些实施方案中,阳离子型脂质是选自DLinDMA、DLin-KC2-DMA和DLin-MC3-DMA的可电离的脂质。在一些实施方案中,阳离子型可电离的脂质是DLin-MC3-DMA(MC3)。
在一些实施方案中,LNP包含一种或多种非阳离子辅助脂质(中性脂质)。示例性的中性辅助脂质包括(1,2-二月桂酰基-sn-甘油基-3-磷酸乙醇胺)(DLPE)、1,2-二植烷酰基-sn-甘油基-3-磷酸乙醇胺(DiPPE)、1,2-二硬脂酰基-sn-甘油基-3-磷酸胆碱(DSPC)、1,2-二棕榈酰基-sn-甘油基-3-磷酸胆碱(DPPC)、1,2-二油酰基-sn-甘油基-3-磷酸乙醇胺(DOPE)、1,2-二棕榈酰基-sn-甘油基-3-磷酸乙醇胺(DPPE)、1,2-二肉豆蔻酰基-sn-甘油基-3-磷酸乙醇胺(DMPE)、(1,2-二油酰基-sn-甘油-3-磷酸-(l'-rac-甘油)(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)、神经酰胺、鞘磷脂和胆固醇。
还考虑本文所述的脂质体和药物组合物中聚乙二醇(PEG)修饰的磷脂和衍生的脂质,例如衍生的神经酰胺(PEG-CER)的使用和包括,包括N-辛酰基-鞘氨醇-1-[琥珀酰基(甲氧基聚乙二醇)-2000](C8PEG-2000神经酰胺),优选与本文公开的一种或多种化合物和脂质组合。
在一些实施方案中,脂质纳米颗粒可进一步包含一种或多种PEG修饰的脂质,所述脂质包含共价连接至包含一个或多个C6-C20烷基的脂质的长度高达5kDa的聚(乙)二醇链。在一些实施方案中,LNP还包含1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-聚(乙二醇)(DSPE-PEG)或1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-N-[氨基(聚乙二醇)](DSPE-PEG-胺)。在一些实施方案中,PEG修饰的脂质占脂质纳米颗粒中总脂质内含物的约0.1%至约1%。在一些实施方案中,PEG修饰的脂质占脂质纳米颗粒中总脂质内含物的约0.1%、约0.2%、约0.3%、约0.4%、约0.5%、约0.6%、约0.7%、约0.8%、约0.9%或约1.0%。
在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中阳离子型脂质是DOTAP。在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中阳离子型脂质是DLin-MC3-DMA(MC3)。在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中一种或多种辅助脂质包含胆固醇。在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中一种或多种辅助脂质包含DLPE。在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中一种或多种辅助脂质包含DSPC。在一些实施方案中,LNP包含阳离子型脂质和一种或多种辅助脂质,其中一种或多种辅助脂质包含DOPE。在一些实施方案中,LNP包含阳离子型脂质和至少两种辅助脂质,其中阳离子型脂质是DOTAP,并且至少两种辅助脂质包括胆固醇和DLPE。在一些实施方案中,LNP包含阳离子型脂质和至少两种辅助脂质,其中阳离子型脂质是MC3,并且至少两种辅助脂质包含胆固醇和DSPC。在一些实施方案中,至少两种辅助脂质包括胆固醇和DOPE。在一些实施方案中,至少两种辅助脂质包含胆固醇和DSPC。在一些实施方案中,LNP包含阳离子型脂质和至少三种辅助脂质,其中阳离子型脂质是DOTAP,并且至少三种辅助脂质包含胆固醇、DLPE和DSPE。在一些实施方案中,LNP包含阳离子型脂质和至少三种辅助脂质,其中阳离子型脂质是MC3,并且至少三种辅助脂质包含胆固醇、DSPC和DMG。在一些实施方案中,至少三种辅助脂质包含胆固醇、DOPE和DSPE。在一些实施方案中,至少三种辅助脂质包含胆固醇、DSPC和DMG。在一些实施方案中,LNP包含DOTAP、胆固醇和DLPE。在一些实施方案中,LNP包含MC3、胆固醇和DSPC。在一些实施方案中,LNP包含DOTAP、胆固醇和DOPE。在一些实施方案中,LNP包含DOTAP、胆固醇、DLPE和DSPE。在一些实施方案中,LNP包含MC3、胆固醇、DSPC和DMG。在一些实施方案中,LNP包含DOTAP、胆固醇、DLPE和DSPE-PEG。在一些实施方案中,LNP包含MC3、胆固醇、DSPC和DMG-PEG。在一些实施方案中,LNP包含DOTAP、胆固醇、DOPE和DSPE。在一些实施方案中,LNP包含DOTAP、胆固醇、DOPE和DSPE-PEG。
在一些实施方案中,LNP包括DOTAP、胆固醇(Chol)和DLPE,其中DOTAP:Chol:DLPE的比率(占总脂质内含物的百分比)约为50:35:15。在一些实施方案中,LNP包含DOTAP、胆固醇(Chol)和DLPE,其中DOTAP:Chol:DOPE的比率(占总脂质内含物的百分比)约为50:35:15。在一些实施方案中,LNP包含DOTAP、胆固醇(Chol)、DLPE、DSPE-PEG,其中DOTP:Chol:DLPE的比率(占总脂质内含物的百分比)约为50:35:15并且其中颗粒包含约0.2%DSPE-PEG。在一些实施方案中,LNP包含MC3、胆固醇(Chol)、DSPC和DMG-PEG,其中MC3:Chol:DSPC:DMG-PEG的比率(占总脂质内含物的百分比)约为49:38.5:11:1.5。
在一些实施方案中,LNP包含可电离的脂质,例如7.SS可裂解的和pH响应性脂质样物质(例如
在一些实施方案中,纳米颗粒用糖胺聚糖(GAG)包被,以调节或促进靶细胞对纳米颗粒的吸收(图2)。GAG可以是肝素/硫酸肝素、硫酸软骨素/硫酸皮肤素、硫酸角蛋白或透明质酸(HA)。在一个特定的实施方案中,纳米颗粒的表面用HA包被并且靶向该等颗粒以供肿瘤细胞吸收。在一些实施方案中,脂质纳米颗粒被精氨酸-甘氨酸-天冬氨酸三肽(RGD肽)包被(参见Ruoslahti,Advanced Materials,24,2012,3747-3756;及Bellis等人,Biomaterials,32(18),2011,4205-4210)。
在一些实施方案中,LNP的平均尺寸为约50nm至约500nm。举例来说,在一些实施方案中,LNP的平均尺寸为约50nm至约200nm、约100nm至约200nm、约150nm至约200nm、约50nm至约150nm、约100nm至约150nm、约150nm至约500nm、约200nm至约500nm、约300nm至约500nm、约350nm至约500nm、约400nm至约500nm、约425nm至约500nm、约450nm至约500nm或约475nm至约500nm。
在一些实施方案中,LNP的平均ζ电位小于约-20mV。举例来说,在一些实施方案中,LNP的平均ζ电位少于约少于约-30mV、少于约35mV或少于约-40mV。在一些实施方案中,LNP的平均ζ电位介于约-50mV至约-20mV、约-40mV至约-20mV或约-30mV至约-20mV之间。在一些实施方案中,LNP的平均ζ电位为约-30mV、约-31mV、约-32mV、约-33mV、约-34mV、约-35mV、约-36mV、约-37mV、约-38mV、约-39mV或约-40mV。
在一些实施方案中,脂质纳米颗粒包含本文所述的重组核酸分子,并且脂质(L)与核酸(N)的比率为约3:1(L:N)。在一些实施方案中,脂质纳米颗粒包含本文所述的重组核酸分子并且包含约4:1、约5:1、约6:1或约7:1的L:N比率。在一些实施方案中,脂质纳米颗粒包含本文所述的重组核酸分子并且包含约4.5:1、约4.6:1、约4.7:1、约4.8:1、约4.9:1、约5:1、约5.1:1、约5.2:1、约5.3:1、约5.4:1或约5.5:1的L:N比率。
V.治疗性组合物和使用方法
本公开的一个方面涉及包含本文所述的重组核酸分子的治疗性组合物或包含本文所述的重组核酸分子的颗粒,以及治疗癌症的方法。可以以适合所需递送途径的任何方式配制本文所述的组合物。通常,制剂包括所有生理上可接受的组合物,包括其衍生物或前药、溶剂化物、立体异构体、外消旋体或互变异构体,以及任何药学上可接受的载体、稀释剂、和/或赋形剂。
如本文所用,“药学上可接受的载体、稀释剂或赋形剂”包括但不限于已被美国食品药物管理局批准为可用于人或家畜的任何佐剂、载体、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增香剂、表面活性剂、润湿剂、分散剂、悬浮剂、稳定剂、等渗剂、溶剂、表面活性剂或乳化剂。示例性的药学上可接受的载体包括但不限于糖,例如乳糖、葡萄糖和蔗糖;淀粉,例如玉米淀粉和马铃薯淀粉;纤维素和其衍生物,例如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;黄蓍胶;麦芽;明胶;滑石;可可脂、蜡、动植物脂肪、石蜡、硅酮、膨润土、硅酸、氧化锌;油类,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇,例如丙二醇;多元醇,例如甘油、山梨糖醇、甘露糖醇和聚乙二醇;酯,例如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,例如氢氧化镁和氢氧化铝;海藻酸;无热原水;等渗盐水;林格氏溶液(Ringer’s solution);乙醇;磷酸盐缓冲溶液;以及药物制剂中使用的任何其它相容物质。
“药学上可接受的盐”包括酸加成盐和碱加成盐两者。药学上可接受的盐包括酸加成盐(与蛋白质的游离氨基一起形成),并用无机酸形成,例如盐酸、氢溴酸、硫酸、硝酸、磷酸等等;并且用有机酸形成,例如但不限于乙酸、2,2-二氯乙酸、己二酸、海藻酸、抗坏血酸、天冬氨酸、苯磺酸、苯甲酸、4-乙酰胺基苯甲酸、樟脑酸、樟脑-10-磺酸、癸酸、己酸、辛酸、碳酸、肉桂酸、柠檬酸、环己氨磺酸、十二烷基磺酸、乙-1,2-二磺酸、乙磺酸、2-羟基乙磺酸、甲酸、富马酸、半乳糖酸、龙胆酸、葡萄糖庚酸、葡萄糖酸、葡萄糖醛酸、谷氨酸、戊二酸、2-氧代-戊二酸、甘油磷酸、乙醇酸、马尿酸、异丁酸、乳酸、乳糖酸、月桂酸、马来酸、苹果酸、丙二酸、扁桃酸、甲磺酸、粘酸、萘-1,5-二磺酸、萘-2-磺酸、1-羟基-2-萘甲酸、烟酸、油酸、乳清酸、草酸、棕榈酸、双羟萘酸(pamoic acid)、丙酸、焦谷氨酸、丙酮酸、水杨酸、4-氨基水杨酸、癸二酸、硬脂酸、琥珀酸、酒石酸、硫氰酸、对甲苯磺酸、三氟乙酸、十一碳烯酸等。由游离羧基形成的盐也可以衍生自无机碱,例如钠、钾、锂、铵、钙、镁、铁、锌、铜、锰、铝盐等。衍生自有机碱的盐包括但不限于以下胺的盐:伯胺、仲胺和叔胺;取代胺,包括天然存在的取代胺;环胺和碱性离子交换树脂,例如氨、异丙胺、三甲胺、二乙胺、三乙胺、三丙胺、二乙醇胺、乙醇胺、地阿诺(deanol)、2-二甲基氨基乙醇、2-二乙基氨基乙醇、二环己胺、赖氨酸、精氨酸、组氨酸、咖啡因、普鲁卡因、海巴明(hydrabamine)、胆碱、甜菜碱、苯乙苄胺(benethamine)、苄星、乙二胺、葡糖胺、甲基葡糖胺、可可碱、三乙醇胺、缓血酸胺、嘌呤、哌嗪、哌啶、N-乙基哌啶、多胺树脂等。特别优选的有机碱是异丙胺、二乙胺、乙醇胺、三甲胺、二环己胺、胆碱和咖啡因。
本公开提供了杀死癌细胞或靶细胞的方法,该方法包括在足以将组合物经细胞内递送至癌细胞的条件下,将细胞暴露于本文所述的多核苷酸或颗粒或其组合物。如本文所用,“癌细胞”或“靶细胞”是指被选择用本文所述的多核苷酸或颗粒或本文所述的组合物治疗或施用的哺乳动物细胞。如本文所用,“杀死癌细胞”具体是指通过细胞凋亡或坏死引起的癌细胞死亡。癌细胞的杀伤可以通过本领域已知的方法来确定,所述方法包括但不限于肿瘤尺寸测量、细胞计数和流式细胞术,以检测细胞死亡标志物如膜联蛋白V和掺入碘化丙啶。
本公开还提供了一种在有需要的受试者中治疗或预防癌症的方法,其中将有效量的本文所述的治疗性组合物施用于该受试者。施用途径自然会随所治疗疾病的位置和性质而变化,并且可以包括例如皮内、透皮、皮下、肠胃外、经鼻、静脉内、肌内、鼻内、皮下、经皮、经气管内、腹膜内、肿瘤内、灌注、灌洗、直接注射和口服。包封的本文所述的多核苷酸组合物特别适用于治疗转移癌,其中可能需要全身性施用以递送组合物至多个器官和/或细胞类型。因此,在特定的实施方案中,本文所述的组合物是全身施用的。
本文可互换使用的“有效量”或“有效剂量”是指本文所述的组合物改善或补救疾病或病症的症状的量和/或剂量。改善是疾病或病症或者疾病或病症的症状的任何改善或补救。所述改善是可观察到的或可测量的改善,或者可以是受试者的总体幸福感的改善。因此,本领域技术人员意识到治疗可以改善疾病状况,但是可能不能完全治愈该疾病。受试者的改善可能包括但不限于减少肿瘤负担、减少肿瘤细胞增殖、增加肿瘤细胞死亡、激活免疫通路、增加肿瘤进展时间、减少癌症疼痛、增加生存率或改善生活质量。
在一些实施方案中,可以通过施用单剂量本文所述的组合物来实现有效剂量的施用。如本文所用,“剂量”是指一次递送的组合物的量。在一些实施方案中,可以通过给定体积中的颗粒数目来测量剂量(例如,颗粒/毫升)。在一些实施方案中,可以通过每个颗粒中存在的本文所述的多核苷酸的基因组拷贝数进一步细化剂量(例如,颗粒数目/毫升,其中每个颗粒包含多核苷酸的至少一个基因组拷贝)。在一些实施方案中,有效剂量的递送可能需要施用多剂本文所述的组合物。这样,有效剂量的施用可能需要施用至少2剂、3剂、4剂、5剂、6剂、7剂、8剂、9剂、10剂、20剂、30剂、40剂、50剂或更多剂的本文所述的组合物。
在施用多剂本文所述的组合物的实施方案中,每剂无需由相同的参与者施用和/或在相同的地理位置施用。此外,可以根据预定时间表来给药。例如,预定的给药方案可以包含每天、每隔一天、每周、每两周、每月、每两个月、每年、每半年一次等施用本文所述的组合物的剂量。可以根据给定患者的需要调整预定的给药方案(例如,可以增加或减少组合物的施用量)和/或可以增加或减少剂量的频率,和/或可以增加或减少总施用剂量次数)。
如本文所用,“预防(prevention)”或“预防(prophylaxis)”是指完全预防疾病症状、延迟疾病症状发作或减轻随后发展的疾病症状的严重性。
本文所用的术语“受试者”或“患者”是指根据本文所述的方法施用本文所述的组合物的任何哺乳动物受试者。在一个具体的实施方案中,本公开的方法用于治疗人类受试者。本公开的方法还可用于治疗非人灵长类动物(例如猴子、狒狒和黑猩猩)、小鼠、大鼠、牛、马、猫、狗、猪、兔子、山羊、鹿、绵羊、雪貂、沙鼠、豚鼠、仓鼠、蝙蝠、鸟类(例如鸡、火鸡和鸭)、鱼类和爬行动物。
本文中的“癌症”是指或描述哺乳动物中通常以细胞生长不受调控为特征的生理疾患。癌症的实例包括但不限于癌、淋巴瘤、母细胞瘤、肉瘤(包括脂肪肉瘤、成骨肉瘤、血管肉瘤、内皮细胞肉瘤、平滑肌肉肉瘤、脊索瘤、淋巴管肉瘤、淋巴管内膜上皮肉瘤、横纹肌肉瘤、纤维肉瘤、粘液肉瘤和软骨肉瘤)、神经内分泌瘤、间皮瘤、滑膜瘤、神经鞘瘤、脑膜瘤、腺癌、黑色素瘤和白血病或淋巴样恶性病。这类癌症的更具体的实例包括鳞状细胞癌(例如上皮鳞状细胞癌);肺癌,包括小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞癌、小细胞肺癌瘤;腹膜癌、肝细胞癌、胃癌或胃癌(包括胃肠道癌)、胰腺癌、胶质母细胞瘤、子宫颈癌、卵巢癌、肝癌、膀胱癌、肝细胞瘤、乳腺癌、结肠癌、直肠癌、结肠直肠癌、子宫内膜癌或子宫癌、唾液腺癌、肾癌或肾癌、前列腺癌、外阴癌、甲状腺癌、肝癌瘤、肛门癌、阴茎癌、睾丸癌、食道癌、胆道肿瘤、尤因氏肿瘤(Ewing’s tumor)、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、支气管癌、肾细胞癌、肝细胞瘤、胆管癌、绒毛膜癌、精原细胞瘤、胚胎癌、威尔姆斯瘤(Wilms’tumor)、睾丸肿瘤、肺癌瘤、膀胱癌瘤、上皮癌瘤、胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑膜瘤、黑色素瘤、神经母细胞瘤、视网膜母细胞瘤、白血病、淋巴瘤、多发性骨髓瘤、华氏巨球蛋白血症(Waldenstrom’smacroglobulinemia)、骨髓增生异常疾病、重链病、神经内分泌肿瘤、神经鞘瘤和其它癌以及头颈癌。此外,良性(即非癌性)过度增生性疾病、病症和疾患,包括良性前列腺肥大(BPH)、脑膜瘤、神经鞘瘤、神经纤维瘤病、瘢痕、肌瘤和子宫肌瘤等也可以使用本文公开的公开内容进行治疗。
VI.示例性自主复制型多核苷酸
本领域技术人员将理解,编码病毒的性质将变化并且将取决于待治疗的疾病适应症。例如,在一些实施方案中,脊髓灰质炎病毒可以用于治疗特定的癌症。脊髓灰质炎病毒基因组包含单链正义极性RNA分子,该分子编码单个多聚蛋白。5'非翻译区(UTR)包含两个功能域,三叶草和内部核糖体进入位点(IRES),并与病毒蛋白VPg共价连接。3'UTR被聚腺苷酸化(参见例如图6A)。在一些实施方案中,脊髓灰质炎病毒基因组在5'和3'末端侧接AAV来源的ITR(参见例如图6A)。
在一些实施方案中,一种或多种miRNA靶序列可操作地连接于病毒基因,例如必需病毒基因。例如,脊髓灰质炎病毒基因组包含几个适合于达成此目的的基因,包括但不限于:3D
在一些实施方案中,通过将含有四聚体miR-124、miR-145、miR-34a和let7靶位点的miRNA靶序列盒插入到3'UTR中以减毒一种或多种必需脊髓灰质炎病毒基因组来修饰野生型脊髓灰质炎病毒基因组(图8A)。在一些实施方案中,所述miRNA减毒的脊髓灰质炎病毒适合用于治疗非小细胞肺癌(图8A)。在一些实施方案中,通过将含有四聚体miR-122、miR-124、miR-34a和let7靶位点的miRNA靶序列盒插入到一种或多种必需脊髓灰质炎病毒基因的3'UTR中来修饰野生型PV基因组(图8B)。在一些实施方案中,所述miRNA减毒的脊髓灰质炎病毒适合用于治疗肝细胞癌(图8B)。在一些实施方案中,通过将含有四聚体miR-124、miR-143、miR-145和let7靶位点的miRNA靶序列盒插入到3'UTR中以减毒一种或多种必需脊髓灰质炎病毒基因来修饰野生型脊髓灰质炎病毒基因组(图8C)。在一些实施方案中,所述miRNA减毒的脊髓灰质炎病毒适合用于治疗前列腺癌(图8C)。
在一些实施方案中,VSV可用于治疗特定癌症。VSV基因组包含单链负义极性RNA分子,该分子编码五种主要蛋白质:核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)和聚合酶(L)。五种病毒编码蛋白中的每一种都有一个单顺反子mRNA。mRNA被加帽,甲基化和聚腺苷酸化。由于VSV是一种细胞质负义RNA病毒,因此用于mRNA合成和修饰的酶被包装在病毒体中(图9A)。在一些实施方案中,VSV基因组侧接AAV来源的ITR序列以帮助多核苷酸复制和核进入(图9A)。
在一些实施方案中,通过插入miRNA靶序列盒来修饰野生型VSV基因组,所述miRNA靶序列盒包含一种或多种miRNA靶序列,所述miRNA靶序列插入到VSV基因组的一种或多种必需病毒基因的基因座中(例如N、P、M、G或L基因中的一种或多种)(图9B)。在一些实施方案中,miRNA靶序列插入到基因的5'UTR或3'UTR中。在一些实施方案中,通过将包含四聚体miR-122、miR-124、miR-34a和let7靶位点的miRNA靶序列盒插入到五种病毒编码的转录物中的四种转录物的3'UTR中以减毒(例如N、P、M、G或L基因中的四种)来修饰野生型VSV基因组(图11A)。在一些实施方案中,所述miRNA减毒的VSV适合用于治疗肝细胞癌(图11A)。在一些实施方案中,通过将包含四聚体miR-124、miR-143、miR-145和let7靶位点的miRNA靶序列盒插入到五种病毒编码的转录物中的四种转录物的3'UTR中以减毒(例如N、P、M、G或L基因中的四种)来修饰野生型VSV基因组(图11B)。在一些实施方案中,所述miRNA减毒的VSV适合用于治疗前列腺癌(图11B)。在一些实施方案中,通过将包含四聚体miR-124、miR-145、miR-34a和let7靶位点的miRNA靶序列盒插入到五种病毒编码的转录物中的四种转录物的3'UTR中以减毒(例如N、P、M、G或L基因中的四种)来修饰野生型VSV基因组(图11C)。在一些实施方案中,所述miRNA减毒的VSV适合用于治疗非小细胞肺癌(图11C)。
在一些实施方案中,腺病毒可用于治疗特定癌症。AAV基因组包含双链DNA分子,该分子编码24-36种蛋白编码基因。E1A、E1B、E2A、E2B、E3和E4转录单元在病毒生殖周期的早期转录(图12A)。这些转录单元内的基因编码的蛋白质主要参与病毒转录的调控、病毒DNA的复制以及宿主对感染的反应的抑制。在一些实施方案中,腺病毒基因组侧接AAV来源的ITR序列以帮助多核苷酸复制和核进入(图12A)。
在一些实施方案中,通过插入miRNA靶序列盒来修饰野生型AAV基因组,所述miRNA靶序列盒包含一种或多种miRNA靶序列,所述miRNA靶序列插入到AAV基因组的一种或多种必需病毒基因(例如E1A、E1B、E2A、E2B、E3或E4中的一种或多种)中(图12B)。在一些实施方案中,通过将包含四聚体miR-122、miR-124、miR-34a和let7靶位点的miRNA靶序列盒插入到一种或多种必需基因(例如E1A、E1B、E2A、E2B、E3或E4中的一种或多种)的3'UTR中来修饰野生型AAV基因组(图13A)。在一些实施方案中,所述miRNA减毒的腺病毒适合用于治疗肝细胞癌(图13A)。在一些实施方案中,通过将包含四聚体miR-124、miR-143、miR-145和let7靶位点的miRNA靶序列盒插入到一种或多种必需基因(例如E1A、E1B、E2A、E2B、E3或E4中的一种或多种)的3'UTR中来修饰野生型AAV基因组(图13B)。在一些实施方案中,所述miRNA减毒的腺病毒适合用于治疗前列腺癌(图13B)。在一些实施方案中,通过将包含四聚体miR-124、miR-145、miR-34a和let7靶位点的miRNA靶序列盒插入到一种或多种必需基因(例如E1A、E1B、E2A、E2B、E3或E4中的一种或多种)的3'UTR中来修饰野生型AAV基因组(图13C)。在一些实施方案中,所述miRNA减毒的腺病毒适合用于治疗非小细胞肺癌(图13C)。
实施例
给出以下实施例是为了说明本公开的各种实施方案,并不意味着以任何方式限制本公开。本实施例;目前与本文所述的方法一起代表了优选的实施方案;是示例性的;并且不意图限制本公开的范围。本领域技术人员将想到其中的改变和包含在由权利要求书的范围所限定的本公开的精神内的其它用途。
实施例1:编码具有复制能力的病毒基因组的多核苷酸构建体的工程化
本文所述的自主复制型多核苷酸构建体是使用标准的分子生物学和遗传学技术工程化和产生的。编码特定病毒的示例性构建体以及用这些构建体治疗的相应癌症在以下表13、14和15中进行了描述。但是,可以基于病毒的期望特性和要治疗的癌症的特性来选择适当的病毒。类似地,可以将miRNA靶序列盒(miR TS)插入病毒基因组中的一个或多个位置,以控制编码的病毒基因组在正常非癌细胞中的复制,同时允许在癌细胞中复制。在整个本公开中描述了示例性构建体。下表8中总结了已制成的构建体。
表8:编码具有复制能力的病毒基因组的多核苷酸构建体
在设计自主复制型多核苷酸之后,通过插入质粒主链或通过添加源自腺相关病毒(AAV)的末端反向重复序列(ITR),对构建体进行工程化以进行递送。已经开发出用于设计这两种特定类型的递送机制的方案和方法,即质粒基因组构建体和侧接ITR的纳米病毒(NanoV)构建体,并在下面进行描述。
实施例2:包含编码具有复制能力的病毒基因组的多核苷酸构建体的质粒的设计和产生
在Genscript合成SVV病毒DNA,并在利用Gibson装配插入到基础载体中后,通过融合PCR添加多聚(A)、5'锤头状核酶和3'δ肝炎核酶。所述基础载体的长度为2.4kb,并且包含最小的复制起点和已经被优化用于哺乳动物细胞的卡那霉素(kanamycin)抗性盒(图31A)。所述表达盒公开为SEQ ID NO:1。针对柯萨奇病毒(CVA21)构建了类似的载体,并且在图31B中示出。CVA21表达盒公开为SEQ ID NO:2。
实施例3:侧接ITR的NanoV构建体的设计和产生
为了产生侧接ITR的NanoV构建体,在四环素(Tet)应答型启动子的控制下,将自主复制型多核苷酸构建体插入侧接AAV来源的ITR的表达盒中。图17提供了模型NanoV构建体的示意图。四环素应答型启动子(TRE紧密)驱动mCherry的表达,mCherry用作占位子,并且可以用适当的病毒基因组构建体代替(图17中示为OV)。四环素控制的反式激活因子(tTA)的表达由组成型启动子控制,在图17中显示为UbCP。使用允许快速插入不同的NanoV盒的Gateway克隆系统(Thermo Fisher)将所述NanoV构建体插入到HSV-1的UL3/4基因间区域中。在培养基中添加四环素会导致Tet与tTA结合,从而阻止mCherry构建体的表达。因此,从培养基中除去Tet可以诱导mCherry表达。此外,在第二种组成型启动子(例如CMV)的控制下,将iDimerize盒(Takara)插入HSV-1BAC内的UL50/51基因间基因座中。iDimerize盒包含两个可调控异二聚体诱导性Rep78/52表达的异源二聚结构域(DmrA和DmrC)。将A/C异二聚体AP21967添加至培养基会激活iDimerize盒并引起Rep78/52表达,这驱动侧接ITR的NanoV构建体的复制。
为证明iDimerize盒对Rep 78/52表达的调控,在AP21967存在下在0.5nm、5nm、50nm或500nm下用iDimerize-Rep盒转染Vero细胞。编码Rep蛋白的质粒(pCDNA-Rep)用作阳性对照物。转染后24小时从细胞中提取蛋白质,然后使用α-Rep或α-肌动蛋白抗体进行SDS-PAGE/蛋白质印迹(Western blot)分析。如图18所示,异二聚体浓度≥50nM诱导Rep78/52从iDimerize盒表达,而添加异二聚体对pCDNA-Rep转染的细胞中Rep表达水平没有影响。
为了证明NanoV构建体的产生,用图17所示的重组HSV-1载体感染U2OS细胞。
为了确定NanoV串联体的方向,将从3.7kb单体和7.4kb二聚体中提取的DNA用AflII消化,并通过非还原琼脂糖凝胶电泳进行分析。AflII的预期裂解位点是在UbC启动子中,从而在单体中产生预期大小为1.2kb和2.5kb的裂解产物,如图20A所示。来自串联体的预期产物尺寸将根据二聚体的取向而变化(例如,头对头、尾对尾或头对尾,如图20B所示)。从图18B的3.7kb片段中提取的DNA的AflII裂解产生了预期的1.2kb和2.5kb片段(图20C,条带的存在由白条指示)。从图19B的7.4kb片段中提取的DNA的AflII裂解产生了1.2kb和5kb的片段尺寸,这指示串联体的尾对尾取向,而2.5kb和2.4kb指示串联体的头对头取向。
实施例4:从质粒基因组产生感染性小核糖核酸病毒需要3'和5'核酶
进行实验以评估由实施例2中产生的质粒产生感染性SVV病毒的能力,所述质粒包含在哺乳动物Pol II启动子控制下的编码SVV的多核苷酸。正义单链RNA病毒(例如SVV和柯萨奇病毒)需要病毒固有的离散5'和3'末端才能正确复制,而含有哺乳动物5'和3'UTR的哺乳动物RNA Pol II转录物不会产生。因此,产生感染性+义ssRNA病毒需要包括5'和3'核酶序列,以催化从Pol II编码的SVV转录物中去除非病毒RNA,并能够表达具有复制能力和感染性的SVV(参见图22和23A的一般示意图)。
简单地说,在有(SVV w/R)和未(SVV w/o R)插入5'和3'核酶编码序列下产生编码SVV病毒基因组的DNA多核苷酸(图23A)。如实施例2中所述,将这些构建体插入DNA质粒中。为了测试具有和不具有末端核酶序列的编码SVV的质粒产生感染性病毒的能力,将293T细胞以1×10
实施例5:包含编码SVV的多核苷酸的DNA质粒能够体外表达有效载荷蛋白
进行实验以评估实施例2中描述的SVV质粒从掺入到编码SVV的多核苷酸中的有效载荷编码序列表达有效载荷蛋白的能力。测试了三种有效载荷:mCherry报告基因、纳米荧光素酶蛋白和CXCL10。包含末端核酶序列的编码SVV的质粒能够表达mCherry蛋白,而没有末端核酶序列的编码SVV的质粒则不能表达(图25A)。此外,编码SVV的质粒能够表达纳米荧光素酶(图25B)。更进一步地,编码SVV的质粒能够表达CXCL10(图25C)。这些数据表明,除了产生感染性SVV,这些质粒构建体还能够表达多种不同类型的有效载荷蛋白,包括荧光蛋白(以mCherry为例)、酶蛋白(以纳米荧光素酶为例)和重组趋化因子(以CXCL10为例)。
实施例6:编码SVV的自主复制型多核苷酸的miRNA减毒
进行实验以确定实施例2中描述的编码SVV的多核苷酸是否可以进行miRNA减毒。如图26所示,将带有miR-1和miR-122靶序列的miRNA靶盒(miR-T)与SVV病毒多聚蛋白一起同框插入内源病毒2A与合成T2A序列之间(又见图16)。预期miR-1靶序列可控制肌肉细胞中的病毒复制,而预期miR-122靶序列可控制肝细胞中的病毒复制。如实施例4中所述,通过从用编码SVV的质粒转染的293T细胞的上清液中分离病毒来产生miRNA减毒的SVV和WT(对照)SVV病毒。该病毒用于感染表达miR-1和miR-122模拟物的允许H1299细胞。48小时后,收集感染细胞的上清液,并用结晶紫将细胞染色。SVV-miRT复制与SVV WT相当,并且miRNA减毒有效,如结晶紫染色所见(图26B)。通过用Cell Titer Glo测定法评估H446细胞上被感染的H1299细胞上清液的病毒滴度来确定与WT SVV相比SVV miR-T构建体的miRNA减毒。如以下表9左列中所示,阴性对照模拟物、miR-1和miR-122TCID
表9:miRNA模拟物预处理后的TCID
实施例7:包含编码SVV的多核苷酸的质粒在体内产生感染性病毒
使用H1299异种移植模型进行实验以确定包含编码SVV的多核苷酸的质粒在体内产生感染性病毒的能力。简单地说,将5×10
包含图22中例示的编码SVV的启用核酶的表达盒(SVV w/R)和未启用核酶(SVV w/o R)的盒的质粒用Lipofectamine 3000配制。简单地说,将14μg每种构建体与Lipofectamine 3000以1:1比率混合并涡旋,然后在注射前孵育10分钟。两剂质粒DNA以每剂14μg在接种后第18天和第20天肿瘤内施用。每周使用电子卡尺测量3次肿瘤体积。在第20天、第22天和第23天,收获肿瘤用于评估感染性病毒。
如图27A所示,与经未启用核酶的编码SVV的质粒处理的小鼠相比,经启用核酶的编码SVV的质粒处理的小鼠展现肿瘤生长的显著抑制。从每组收获的肿瘤中分离病毒,并滴定到H1299细胞上,并通过结晶紫染色评估病毒溶解。如图27B所示,与从SVV w/o R组分离的病毒(左图,图27B)相比,来自从经SVV w/R质粒处理的小鼠获得的肿瘤的分离物含有活性溶解病毒,通过结晶紫染色的不透明性降低证明(右图,图27B)。这些数据表明,包含编码SVV的启用核酶的多核苷酸的质粒在体内产生感染性溶解病毒,并在肿瘤内递送时抑制肿瘤生长。
实施例8:包含编码SVV的多核苷酸的质粒在体内表达有效载荷
进行另外的实验以评估当体内施用时,包含编码SVV的多核苷酸的质粒表达各种有效载荷的能力。如实施例7中所述,配制启用核酶的质粒DNA构建体,并经肿瘤内注射到H1299异种移植模型中。除了编码SVV的多核苷酸序列之外,将编码纳米荧光素酶(图28A)或CXCL10(图28B)的序列掺入质粒插入物中。在第2天(纳米荧光素酶)或第6天(CXCL10),收获肿瘤并评估相应有效载荷蛋白的表达。如图28A-图28B所示,在肿瘤内施用带有编码荧光素酶的多核苷酸的SVV质粒或带有编码CXCL10的多核苷酸的SVV质粒使得在分离出的肿瘤中检测出每种有效载荷(图28A显示增强的发光,并且图28B显示CXCL10水平升高)。这些数据表明,除了产生感染性病毒之外,编码SVV的质粒还能够在体内表达外源酶和细胞因子有效载荷。
实施例9:用于静脉内递送编码SVV的质粒的脂质纳米颗粒的配制
编码SVV的质粒被配制成脂质纳米颗粒中以静脉内递送质粒。
(a)N-[1-(2,3-二油酰基氧基)丙基]-N,N,N-三甲基铵(DOTAP);
(b)胆固醇;
(c)1,2-二月桂酰基-sn-甘油基-3-磷酸乙醇胺(DLPE);
(d)1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-N-[氨基(聚乙二醇)(PEG-DSPE胺)
(e)1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-(聚乙二醇)(PEG-DSPE)。
表10:包封制剂参数
表11:包封制剂的Zetasizer数据
表12:包封制剂的体外活性
如表12所示,质粒DNA的脂质颗粒制剂能够将质粒DNA递送至细胞并产生感染性病毒,因为不同制剂的TCID
实施例10:静脉内注射质粒DNA使得其可递送至肿瘤部位并抑制肿瘤生长
进行实验以确定当全身施用时,编码SVV的质粒DNA的脂质颗粒制剂是否可以将pDNA递送至肿瘤。选择实施例9和表10中所述的制剂52021-4D,并用PBS配制颗粒,达到约95%活性DNA回收率和脂质包封效率。当肿瘤体积达到约150mm
如图30所示,与在PBS对照物中观察到的生长相比,在LNP中配制的质粒DNA的静脉内递送随着时间的推移显著抑制肿瘤的生长(图30,****p<0.0001,双向ANOVA与邦费罗尼校正(Bonferroni correction))。这些结果证明,编码感染性病毒的质粒DNA可以在非病毒媒介物中静脉内递送,并且可以显著抑制体内肿瘤的生长。
实施例11:用编码病毒基因组的LNP包封的自主复制型多核苷酸治疗患有癌症的患者
可以进行实验以评估本文所述的自主复制型病毒基因组治疗患有癌症的患者的能力。在这样的实验中,一般如实施例1中所述,对编码病毒基因组的自主复制型多核苷酸进行工程化。
这些自主复制型多核苷酸可以被进一步工程化以掺入质粒主链中。或者,对于自主复制型多核苷酸的大规模体外繁殖,可将AAV-ITR序列掺入以侧接整个病毒基因组,以产生NanoV构建体,从而帮助多核苷酸复制和核进入。将整个侧接ITR的基因组插入重组HSV基因组主链的基因间位点(图4B、图7B)或可替代地ICP4位点(图5B、图10B,ICP4由ICP4补体细胞系反式提供)。将AAV rep基因插入到ICP0中以使得能够有效复制侧接ITR的病毒基因组DNA(参见实施例3)。
使用标准分子生物学技术(例如Maxi-prep)从培养物中纯化质粒基因组或NanoV基因组,然后包封到冻干的透明质酸(HA)表面修饰的脂质纳米颗粒(LNP)中(参见实施例9)。通过超速离心去除未包封的病毒基因组DNA,并通过qPCR定量纳米颗粒包封的病毒基因组。为了向患有癌症的患者体内施用,在磷酸盐缓冲溶液(PBS)中制备LNP以及药学上可接受的稳定剂。在第一天,通过静脉内输注用体积10mL药学上可接受的载体中的10
实施例12:用编码病毒基因组的LNP包封的自主复制型多核苷酸治疗患有肺癌的患者
可以根据实施例11进行实验以评估本文所述的自主复制型病毒基因组治疗患有非小细胞肺癌(NSCLC)的患者或患有小细胞肺癌(SCLC)的患者的能力。下表13概述了可包封在LNP中并用于治疗NSCLC和SCLC的示例性自主复制型多核苷酸。
表13:用于治疗NSCLC和SCLC的自主复制型载体的概述
实施例13:患有肝细胞癌的患者的治疗
可以根据实施例11进行实验以评估本文所述的自主复制型病毒基因组治疗患有肝细胞癌的患者的能力。下表14概述了可包封在LNP中并用于治疗肝细胞癌的示例性自主复制型多核苷酸。
表14:用于治疗肝细胞癌的自主复制型载体的概述
实施例14:患有前列腺癌的患者的治疗
可以根据实施例11进行实验以评估本文所述的自主复制型病毒基因组治疗患有前列腺癌的患者的能力。下表15概述了可包封在LNP中并用于治疗前列腺癌的示例性自主复制型多核苷酸。
表15:用于治疗前列腺癌的自主复制型载体的概述
实施例15:从具有3’核酶和5’siRNA靶序列的质粒基因组产生感染性小核糖核酸病毒
进行实验以评估由以下质粒产生感染性SVV病毒的能力,所述质粒包含在哺乳动物Pol II启动子控制下并且具有3'核酶序列和5'siRNA靶序列以产生病毒基因组的3'和5'末端的编码SVV的多核苷酸(参见图33中的一般示意图)。
简单地说,在5'和3'核酶(SVV WT-R,实施例2和4中所述)以及3'核酶和5'siRNA靶序列(5p siRNA)下产生编码SVV病毒基因组的DNA多核苷酸。如实施例2中所述,将这些构建体插入DNA质粒中。为了测试具有对称末端(3'和5'核酶)和不对称末端(3'核酶和5'siRNA靶序列)的编码SVV的质粒产生感染性病毒的能力,将293T细胞以1×10
实施例16:从具有3'和5'AmiR靶序列的质粒基因组产生感染性小核糖核酸病毒
进行实验以评估由以下质粒产生感染性SVV病毒的能力,所述质粒包含在哺乳动物Pol II启动子控制下并且具有5'amiRNA靶序列以产生病毒基因组的5'末端和3'HDV核酶的编码SVV的多核苷酸。
简单地说,在5'和3'核酶(WT-R,实施例2和4中所述)以及5'和3'AmiR靶序列(5p3pAmi)下产生编码SVV病毒基因组的DNA多核苷酸。如实施例2中所述,将这些构建体插入DNA质粒中。为了测试这些编码SVV的质粒产生感染性病毒的能力,将293T细胞以1×10
如下表16所示,与在5'和3'核酶下所观察到相比,从包含不5'amiRNA靶序列的构建体观察到活性溶解SVV的产量增加。
表16
实施例17:肿瘤内注射质粒AmiR-SVV DNA增强对肿瘤生长的抑制
进行另外的实验以确定如图35中所述的具有5'AmiR靶序列和3'核酶的编码SVV的质粒DNA的脂质颗粒制剂当在H446异种移植模型中经肿瘤内施用时,是否会影响肿瘤生长。还施用了具有5'和3'核酶序列的编码SVV的质粒DNA,并将PBS用作媒介物对照。如图27所述,用Lipofectamine 3000配制pDNA构建体。当肿瘤体积达到约150mm
实施例18:用于静脉内递送编码SVV的质粒的脂质纳米颗粒的配制
编码SVV阴性、SVV-WT和Ami-SVV的质粒被配制成脂质纳米颗粒以静脉内递送。
(a)D-Lin-MC3-DMA(MC3);
(b)胆固醇;
(c)1,2-二硬脂酰基-sn-甘油基-3-磷酸胆碱(DSPC);
(d)1,2-二肉豆蔻酰基-rac-甘油基-3-甲氧基聚乙二醇-2000(DMG-PEG 2000)。
表17:包封制剂的Zetasizer数据
其它编号的实施方案
本公开的其它编号实施例如下:
实施方案1.一种脂质纳米颗粒(LNP),所述脂质纳米颗粒包含重组DNA分子,所述重组DNA分子包含编码具有复制能力的病毒基因组的多核苷酸序列,其中所述多核苷酸序列可操作地连接于能够结合哺乳动物RNA聚合酶II(Pol II)的启动子序列并且侧接3'接合裂解序列和5'接合裂解序列,其中所述3'接合裂解序列和所述5'接合裂解序列属于不同类型,并且其中编码所述具有复制能力的病毒基因组的所述多核苷酸序列是非病毒来源的。
实施方案2.实施方案1的LNP,其中所述3'接合裂解序列是核酶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案3.实施方案2的LNP,其中所述3'接合裂解序列是核酶序列并且所述5'接合裂解序列是人工miR(AmiR)靶序列。
实施方案4.实施方案1的LNP,其中所述3'接合裂解序列是微小RNA(miR)靶序列并且所述5'接合裂解序列选自核酶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案5.实施方案1的LNP,其中所述3'接合裂解序列是人工miR(AmiR)靶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、核酶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案6.实施方案1的LNP,其中所述3'接合裂解序列是向导RNA(gRNA)靶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、核酶序列、pri-miR序列和适体酶序列。
实施方案7.实施方案1的LNP,其中所述3'接合裂解序列是pri-miR序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、核酶序列和适体酶序列。
实施方案8.实施方案1的LNP,其中所述3'接合裂解序列是适体酶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和核酶序列。
实施方案9.实施方案1-8中的任一项的LNP,其中所述具有复制能力的病毒基因组是单链RNA(ssRNA)病毒。
实施方案10.实施方案9的LNP,其中所述单链RNA(ssRNA)病毒是正义((+)-义)或负义((-)-义)ssRNA病毒。
实施方案11.实施方案10的LNP,其中所述具有复制能力的病毒基因组是(+)-义ssRNA病毒并且所述(+)-义ssRNA病毒是小核糖核酸病毒。
实施方案12.实施方案11的LNP,其中所述小核糖核酸病毒是塞内加谷病毒(SVV)或柯萨奇病毒。
实施方案13.实施方案1-12中的任一项的LNP,其中所述LNP与细胞接触引起所述细胞产生病毒颗粒,并且其中所述病毒颗粒是感染性的和溶解性的。
实施方案14.实施方案1-13中的任一项的LNP,其中所述重组DNA分子还包含编码外源有效载荷蛋白的多核苷酸序列。
实施方案15.实施方案1-13中的任一项的LNP,其中所述LNP还包含编码外源有效载荷蛋白的第二多核苷酸序列。
实施方案16.实施方案14或15的LNP,其中所述外源有效载荷蛋白是荧光蛋白、酶蛋白、细胞因子、趋化因子、细胞表面受体的配体或能够结合于细胞表面受体的抗原结合分子。
实施方案17.实施方案16的LNP,其中所述细胞因子选自Flt3配体和IL-18、IL-18γ和IL-2。
实施方案17A.实施方案16的LNP,其中所述细胞表面受体的配体是Flt3配体。
实施方案18.实施方案16的LNP,其中所述趋化因子选自CCL21、CCL5、CXCL10和CCL4。
实施方案19.实施方案16的LNP,其中所述抗原结合分子能够结合和抑制免疫检查点受体。
实施方案20.实施方案19的LNP,其中所述免疫检查点受体是PD1。
实施方案21.实施方案16的LNP,其中所述抗原结合分子能够结合于选自DLL3、EpCam和CEA的肿瘤相关抗原。
实施方案21A.实施方案16-21中的任一项的LNP,其中所述抗原结合分子是包含对肿瘤抗原具有特异性的第一结构域和对T细胞表面分子具有特异性的第二结构域的双特异性T细胞衔接分子。
实施方案21B.实施方案21A的LNP,其中所述T细胞表面分子是CD3。
实施方案22.实施方案1-21中的任一项的LNP,其中微小RNA(miRNA)靶序列(miR-TS)盒被插入编码所述具有复制能力的病毒基因组的核酸序列中,其中所述miR-TS盒包含一种或多种miRNA靶序列,并且其中细胞中一种或多种相应miRNA的表达抑制所述具有复制能力的病毒基因组在所述细胞中的复制。
实施方案23.实施方案22的LNP,其中所述一种或多种miRNA选自miR-124、miR-1、miR-143、miR-128、miR-219、miR-219a、miR-122、miR-204、miR-217、miR-137和miR-126。
实施方案24.实施方案23的LNP,其中所述miR-TS盒包含miR-124靶序列的一个或多个拷贝、miR-1靶序列的一个或多个拷贝和miR-143靶序列的一个或多个拷贝。
实施方案25.实施方案23的LNP,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-219a靶序列的一个或多个拷贝和miR-122靶序列的一个或多个拷贝。
实施方案26.实施方案23的LNP,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-204靶序列的一个或多个拷贝和miR-219靶序列的一个或多个拷贝。
实施方案27.实施方案23的LNP,其中所述miR-TS盒包含miR-217靶序列的一个或多个拷贝、miR-137靶序列的一个或多个拷贝和miR-126靶序列的一个或多个拷贝。
实施方案28.实施方案1-27中的任一项的LNP,其中所述重组DNA分子是包含所述编码具有复制能力的病毒基因组的多核苷酸序列的质粒。
实施方案29.实施方案1-28中的任一项的LNP,其中所述LNP包含阳离子型脂质、胆固醇和中性脂质。
实施方案30.实施方案29的LNP,其中所述阳离子型脂质是1,2-二油酰基-3-三甲基铵-丙烷(DOTAP),并且其中所述中性脂质是1,2-二月桂酰基-sn-甘油基-3-磷酸乙醇胺(DLPE)或1,2-二油酰基-sn-甘油基-3-磷酸乙醇胺(DOPE)。
实施方案31.实施方案29或30的LNP,所述LNP还包含磷脂-聚合物缀合物,其中所述磷脂-聚合物缀合物是1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-聚(乙二醇)(DSPE-PEG)或1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-N-[氨基(聚乙二醇)](DSPE-PEG-胺)。
实施方案31A.实施方案29的LNP,其中所述阳离子型脂质是D-Lin-MC3-DMA(MC3)并且其中所述中性脂质是1,2-二硬脂酰基-sn-甘油基-3-磷酸胆碱(DSPC)。
实施方案31B.实施方案31A的LNP,其中还包含1,2-二肉豆蔻酰基-rac-甘油基-3-甲氧基聚乙二醇(DMG-PEG)的磷脂-聚合物缀合物。
实施方案32.实施方案1-31B中的任一项的LNP,其中透明质酸缀合于所述LNP的表面。
实施方案32A.实施方案1-31B中的任一项的LNP,其中RGD肽缀合于所述LNP的表面。
实施方案33.一种治疗性组合物,所述治疗性组合物包含多个根据实施方案1-32中的任一项的脂质纳米颗粒,其中所述多个LNP具有约150nm至约500nm的平均尺寸。
实施方案34.实施方案33的治疗性组合物,其中所述多个LNP具有约50nm至约200nm、约100nm至约200nm、约150nm至约200nm、约50nm至约150nm、约100nm至约150nm、约200nm至约500nm、约300nm至约500nm、约350nm至约500nm、约400nm至约500nm、约425nm至约500nm、约450nm至约500nm或约475nm至约500nm的平均尺寸。
实施方案35.实施方案33或34的治疗性组合物,其中所述多个LNP具有小于约-20mV、小于约-30mV、小于约35mV或小于约-40mV的平均ζ-电位。
实施方案36.实施方案35的治疗性组合物,其中所述多个LNP具有介于约-50mV至约-20mV、约-40mV至约-20mV或约-30mV至约-20mV之间的平均ζ-电位。
实施方案37.实施方案35或36的治疗性组合物,其中所述多个LNP具有约-30mV、约-31mV、约-32mV、约-33mV、约-34mV、约-35mV、约-36mV、约-37mV、约-38mV、约-39mV或约-40mV的平均ζ-电位。
实施方案38.实施方案33-37中的任一项的治疗性组合物,其中施用所述治疗性组合物至受试者将所述重组DNA多核苷酸递送至所述受试者的靶细胞,并且其中所述重组DNA多核苷酸产生能够溶解所述受试者的所述靶细胞的感染性病毒。
实施方案39.实施方案38的治疗性组合物,其中所述组合物经静脉内或经肿瘤内递送。
实施方案40.实施方案38的治疗性组合物,其中所述靶细胞是癌细胞。
实施方案41.一种抑制有需要的受试者中癌性肿瘤的生长的方法,所述方法包括施用根据实施方案33-40中的任一项的治疗性组合物至所述有需要的受试者,其中所述组合物的施用抑制所述肿瘤的生长。
实施方案42.实施方案41的方法,其中所述施用是肿瘤内或静脉内的。
实施方案43.实施方案41或42的方法,其中所述癌症是肺癌或肝癌。
实施方案44.一种重组DNA分子,所述重组DNA分子包含编码具有复制能力的病毒基因组的多核苷酸序列,其中所述多核苷酸序列可操作地连接于能够结合哺乳动物RNA聚合酶II(Pol II)的启动子序列并且侧接3'接合裂解序列和5'接合裂解序列,其中所述3'接合裂解序列和所述5'接合裂解序列属于不同类型,并且其中编码所述具有复制能力的病毒基因组的所述多核苷酸序列是非病毒来源的。
实施方案45.实施方案44的重组DNA分子,其中所述3'接合裂解序列是核酶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案46.实施方案45的重组DNA分子,其中所述3'接合裂解序列是核酶序列并且所述5'接合裂解序列是人工miR(AmiR)靶序列。
实施方案47.实施方案44的重组DNA分子,其中所述3'接合裂解序列是微小RNA(miR)靶序列并且所述5'接合裂解序列选自核酶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案48.实施方案44的重组DNA分子,其中所述3'接合裂解序列是人工miR(AmiR)靶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、核酶序列、向导RNA(gRNA)靶序列、pri-miR序列和适体酶序列。
实施方案49.实施方案44的重组DNA分子,其中所述3'接合裂解序列是向导RNA(gRNA)靶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、核酶序列、pri-miR序列和适体酶序列。
实施方案50.实施方案44的重组DNA分子,其中所述3'接合裂解序列是pri-miR序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、核酶序列和适体酶序列。
实施方案51.实施方案44的重组DNA分子,其中所述3'接合裂解序列是适体酶序列并且所述5'接合裂解序列选自微小RNA(miR)靶序列、人工miR(AmiR)靶序列、向导RNA(gRNA)靶序列、pri-miR序列和核酶序列。
实施方案52.实施方案44-51中的任一项的重组DNA分子,其中所述编码病毒是单链RNA(ssRNA)病毒
实施方案53.实施方案52的重组DNA分子,其中所述ssRNA病毒是正义((+)-义)或负义((-)-义)ssRNA病毒。
实施方案54.实施方案53的重组DNA分子,其中所述(+)-义ssRNA病毒是小核糖核酸病毒。
实施方案55.实施方案54的重组DNA分子,其中所述小核糖核酸病毒是塞内加谷病毒(SVV)或柯萨奇病毒。
实施方案56.实施方案44-55中的任一项的重组DNA分子,其中所述重组DNA分子在通过非病毒性递送媒介物引入细胞中时能够产生感染性的溶解性病毒。
实施方案57.实施方案44-56中的任一项的重组DNA分子,其中所述重组DNA分子还包含编码外源有效载荷蛋白的多核苷酸序列。
实施方案58.实施方案57的重组DNA分子,其中所述外源有效载荷蛋白是荧光蛋白、酶蛋白、细胞因子、趋化因子或能够结合于细胞表面受体的抗原结合分子。
实施方案59.实施方案58的重组DNA分子,其中所述细胞因子是Flt3配体、IL-18、IL-18γ和IL-2。
实施方案60.实施方案58的重组DNA分子,其中所述趋化因子选自CCL21、CCL5、CXCL10和CCL4。
实施方案61.实施方案58的重组DNA分子,其中所述抗原结合分子能够结合和抑制免疫检查点受体。
实施方案62.实施方案62的重组DNA分子,其中所述免疫检查点受体是PD1。
实施方案63.实施方案58的重组DNA分子,其中所述抗原结合分子能够结合于选自DLL3、EpCam和CEA的肿瘤相关抗原。
实施方案63A.实施方案58或实施方案63的重组DNA分子,其中所述抗原结合分子是包含对肿瘤抗原具有特异性的第一结构域和对T细胞表面分子具有特异性的第二结构域的双特异性T细胞衔接分子。
实施方案63B.实施方案63A的重组DNA分子,其中所述T细胞表面分子是CD3。
实施方案64.实施方案44-63中的任一项的重组DNA分子,其中微小RNA(miRNA)靶序列(miR-TS)盒被插入编码所述具有复制能力的病毒基因组的核酸序列中,其中所述miR-TS盒包含一种或多种miRNA靶序列,并且其中细胞中一种或多种相应miRNA的表达抑制所述细胞中所述编码病毒的复制。
实施方案65.实施方案64的重组DNA分子,其中所述一种或多种miRNA选自miR-124、miR-1、miR-143、miR-128、miR-219、miR-219a、miR-122、miR-204、miR-217、miR-137和miR-126。
实施方案66.实施方案64的重组DNA分子,其中所述miR-TS盒包含miR-124靶序列的一个或多个拷贝、miR-1靶序列的一个或多个拷贝和miR-143靶序列的一个或多个拷贝。
实施方案67.实施方案64的重组DNA分子,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-219a靶序列的一个或多个拷贝和miR-122靶序列的一个或多个拷贝。
实施方案68.实施方案64的重组DNA分子,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-204靶序列的一个或多个拷贝和miR-219靶序列的一个或多个拷贝。
实施方案69.实施方案64的重组DNA分子,其中所述miR-TS盒包含miR-217靶序列的一个或多个拷贝、miR-137靶序列的一个或多个拷贝和miR-126靶序列的一个或多个拷贝。
实施方案70.实施方案44-69中的任一项的重组DNA分子,其中所述重组DNA分子是包含所述编码具有复制能力的病毒基因组的多核苷酸序列的质粒或NanoV。
实施方案71.一种重组DNA分子,所述重组DNA分子包含编码具有复制能力的病毒基因组的多核苷酸序列,其中编码所述具有复制能力的病毒的所述多核苷酸序列是非病毒来源的,并且其中所述重组DNA分子在通过非病毒性递送媒介物引入细胞中时能够产生具有复制能力的病毒。
实施方案72.实施方案71的重组DNA分子,其中所述具有复制能力的病毒基因组是DNA病毒的基因组或RNA病毒的基因组。
实施方案73.实施方案5672的重组DNA分子,其中所述DNA基因组或RNA基因组是双链或单链病毒。
实施方案74.实施方案73的重组DNA分子,其中所述单链基因组是正义((+)-义)或负义((-)-义)基因组。
实施方案75.实施方案71的重组DNA分子,其中所述细胞是哺乳动物细胞。
实施方案76.实施方案75的重组DNA分子,其中所述细胞是哺乳动物受试者中存在的哺乳动物细胞。
实施方案77.实施方案71的重组DNA分子,其中所述具有复制能力的病毒选自由以下组成的组:腺病毒、柯萨奇病毒、脊髓灰质炎病毒、塞内加谷病毒、马疱疹病毒、单纯疱疹病毒1型(HSV-1)、拉沙病毒、鼠白血病病毒、甲型流感病毒、乙型流感病毒、新城鸡瘟病毒、麻疹病毒、细小病毒、呼肠孤病毒、辛德毕斯病毒、牛痘病毒、粘液瘤病毒、水疱性口腔炎病毒(VSV)、马拉巴病毒。
实施方案78.实施方案71-77中的任一项的重组DNA分子,所述重组DNA分子还包含一个或多个被插入编码所述具有复制能力的病毒基因组的所述多核苷酸中的微小RNA(miRNA)靶序列(miR-TS)盒,其中所述miR-TS盒包含一种或多种miRNA靶序列,并且其中细胞中对应miRNA中的一个或多个的表达抑制所述细胞中编码病毒的复制。
实施方案79.实施方案78的重组DNA分子,其中所述一个或多个miR-TS盒并入一种或多种必需病毒基因的5'非翻译区(UTR)或3'UTR中。
实施方案80.实施方案79的重组DNA分子,其中所述一种或多种必需病毒基因选自由以下组成的组:UL1、UL5、UL6、UL7、UL8、UL9、UL11、UL12、UL14、UL15、UL17、UL18、UL19、UL20、UL22、UL25、UL26、UL26.5、UL27、UL28、UL29、UL30、UL31、UL32、UL33、UL34、UL35、UL36、UL37、UL38、UL39、UL40、UL42、UL48、UL49、UL50、UL52、UL53、UL54、US1、US3、US4、US5、US6、US7、US8、US12、ICP0、ICP4、ICP22、ICP27、ICP47、PB、F、B5R、SERO-1、Cap、Rev、VP1-4、核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)、聚合酶(L)、E1、E2、E3、E3、VP1、VP2、VP3、VP4、2A、2B、2C、3A、3B、3C和3D。
实施方案81.实施方案78的重组DNA分子,其中所述一个或多个miR-TS盒并入一种或多种非必需基因的5'非翻译区(UTR)或3'UTR中。
实施方案82.实施方案71-81中的任一项的重组DNA分子,其中所述多核苷酸被插入选自以下的核酸载体中:复制子、质粒、粘粒、噬菌粒、转座子、细菌人工染色体、酵母人工染色体或末端封闭的线性双链溶瘤病毒(Ov)DNA分子。
实施方案83.实施方案71的重组DNA分子,其中所述多核苷酸是DNA多核苷酸并且还包含编码所述具有复制能力的病毒基因组的所述核酸序列的5'末端上的第一AAV来源的反向末端重复序列(ITR)和编码所述具有复制能力的病毒基因组的所述核酸序列的3'末端上的第二AAV来源的ITR。
实施方案84.实施方案71的重组DNA分子,其中所述多核苷酸是DNA多核苷酸并且还包含紧靠编码所述具有复制能力的病毒基因组的所述核酸序列3'的第一核酶编码序列和紧靠编码所述具有复制能力的病毒基因组的所述核酸序列5'的第二核酶编码序列。
实施方案85.实施方案84的重组DNA分子,其中所述第一核酶编码序列和所述第二核酶编码序列编码锤头核酶或肝炎δ病毒核酶。
实施方案86.实施方案71的重组DNA分子,其中所述启动子序列能够结合真核RNA聚合酶。
实施方案87.实施方案71的重组DNA分子,其中所述启动子序列能够结合哺乳动物RNA聚合酶。
实施方案88.实施方案71的重组DNA分子,其中所述多核苷酸是DNA多核苷酸并且所述哺乳动物聚合酶驱动感染性的具有复制能力的RNA病毒转录。
实施方案89.实施方案71的重组DNA分子,其中所述多核苷酸是DNA多核苷酸并且所述哺乳动物聚合酶驱动感染性的具有复制能力的DNA病毒转录。
实施方案90.实施方案71的重组DNA分子,其中所述启动子序列选择性地驱动癌细胞中所述多核苷酸的转录。
实施方案91.实施方案71-90中的任一项的重组DNA分子,其中所述启动子序列源自于选自由以下组成的组的基因:hTERT、HE4、CEA、OC、ARF、CgA、GRP78、CXCR4、HMGB2、INSM1、间皮素、OPN、RAD51、TETP、H19、uPAR、ERBB2、MUC1、Frz1或IGF2-P4。
实施方案92.实施方案71-91中的任一项的重组DNA分子,所述重组DNA分子还包含编码选自由以下组成的组的有效载荷分子的核酸序列:细胞毒性多肽、细胞因子、趋化因子、抗原结合分子、细胞表面受体的配体、可溶性受体、酶、蝎多肽、蛇多肽、蜘蛛多肽、蜜蜂多肽、蛙多肽和治疗性核酸。
实施方案93.实施方案92的重组DNA分子,其中所述一个或多个miR-TS盒并入编码所述有效载荷分子的所述核酸序列的5'非翻译区(UTR)或3'UTR中。
实施方案94.实施方案92的重组DNA分子,其中所述细胞毒性多肽选自p53、白喉毒素(DT)、假单胞菌外毒素A(Pseudomonas Exotoxin A,PEA)、I型核糖体失活蛋白(RIP)、II型RIP或志贺样毒素1(Shiga-like toxin 1,Slt1)。
实施方案95.实施方案92的重组DNA分子,其中所述酶选自金属蛋白酶、胶原酶、弹性蛋白酶、透明质酸酶、胱天蛋白酶、明胶酶或作为选自以下的基因导向性酶前药疗法(GDEPT)系统的一部分的酶:单纯疱疹病毒胸苷激酶、胞嘧啶脱氨酶、硝基还原酶、羧肽酶G2、嘌呤核苷磷酸化酶或细胞色素P450。
实施方案96.实施方案95的重组DNA分子,其中所述明胶酶是成纤维细胞激活蛋白(FAP)。
实施方案97.实施方案95的重组DNA分子,其中所述金属蛋白酶是基质金属蛋白酶(例如MMP9)或ADAM17。
实施方案98.实施方案92的重组DNA分子,其中所述细胞因子选自由以下组成的组:骨桥蛋白、IL-13、TGFβ、IL-35、IL-18、IL-15、IL-2、IL-12、IFNα、IFNβ、IFNγ。
实施方案99.实施方案92的重组DNA分子,其中所述趋化因子选自CXCL10、CCL4、CCL5、CXCL9和CCL21。
实施方案100.实施方案92的重组DNA分子,其中所述细胞表面受体的配体是NKG2D配体、神经纤毛蛋白配体、Flt3配体或CD47配体。
实施方案101.实施方案92的重组DNA分子,其中所述抗原结合分子结合于选自由以下组成的组的细胞表面抗原:PD-1、PDL-1、CTLA4、CCR4、OX40、CD200R、CD47、CSF1R、EphA2、CD19、EpCAM、CEA、PSMA、CD33、EGFR、CD200、CD40、HER2、DLL3、4-1BB、17-1A、GD2和表7中列出的肿瘤抗原中的任一种或多种。
实施方案102.实施方案92的重组DNA分子,其中所述蝎多肽选自由以下组成的组:氯毒素、BmKn-2、新普拉丁1、新普拉丁2和莫瑞泊林。
实施方案103.实施方案92的重组DNA分子,其中所述蛇多肽选自由以下组成的组:蛇毒解聚素、载脂蛋白-I、矛头蝮蛇毒素-I、BJcuL、OHAP-1、马来亚蝮蛇蛇毒蛋白、drCT-I、CTX-III、B1L以及ACTX-6。
实施方案104.实施方案92的重组DNA分子,其中所述蜘蛛多肽选自由拉塔蛋白和透明质酸酶组成的组。
实施方案105.实施方案92的重组DNA分子,其中所述蜜蜂多肽选自由蜂毒素和蜂毒明肽组成的组。
实施方案106.实施方案92的重组DNA分子,其中所述蛙多肽选自由PsT-1、PdT-1和PdT-2组成的组。
实施方案107.实施方案92-106中的任一项的重组DNA分子,其中所述有效载荷蛋白作用于免疫细胞。
实施方案108.实施方案107的重组DNA分子,其中所述免疫细胞选自由以下组成的组:T细胞、B细胞、自然杀伤(NK)细胞、NKT细胞、巨噬细胞和/或树突状细胞。
实施方案109.实施方案92的重组DNA分子,其中所述有效载荷多肽是包含能够结合人细胞表面抗原的第一结构域和能够结合人肿瘤细胞抗原的第二结构域的双向多肽。
实施方案110.实施方案109的重组DNA分子,其中所述双向多肽的一个或两个结构域是选自由以下组成的组的抗原结合分子:抗体、单链可变片段(scFv)、F(ab)、免疫球蛋白重链可变结构域、双功能抗体、柔性抗体、DOCK-AND-LOCK
实施方案111.实施方案110的重组DNA分子,其中所述双向多肽是双重可变结构域抗体(DVD-Ig
实施方案112.实施方案110的重组DNA分子,其中所述抗体是具有工程化Fc结构域的IgG抗体。
实施方案113.实施方案92的重组DNA分子,其中所述治疗性核酸是antagomir、短发夹RNA(shRNA)、核酶或适体。
实施方案114.实施方案72-113中的任一项的重组DNA分子,其中所述多核苷酸在表达结合于所述miR-TS盒中所包含的miRNA靶序列的miRNA的细胞中不复制或最低限度地复制。
实施方案115.实施方案114的重组DNA分子,其中所述miRNA选自表3。
实施方案116.实施方案114的重组DNA分子,其中所述一种或多种miRNA选自miR-124、miR-1、miR-143、miR-128、miR-219、miR-219a、miR-122、miR-204、miR-217、miR-137和miR-126。
实施方案117.实施方案116的重组DNA分子,其中所述miR-TS盒包含miR-124靶序列的一个或多个拷贝、miR-1靶序列的一个或多个拷贝和miR-143靶序列的一个或多个拷贝。
实施方案118.实施方案116的重组DNA分子,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-219a靶序列的一个或多个拷贝和miR-122靶序列的一个或多个拷贝。
实施方案119.实施方案116的重组DNA分子,其中所述miR-TS盒包含miR-128靶序列的一个或多个拷贝、miR-204靶序列的一个或多个拷贝和miR-219靶序列的一个或多个拷贝。
实施方案120.实施方案116的重组DNA分子,其中所述miR-TS盒包含miR-217靶序列的一个或多个拷贝、miR-137靶序列的一个或多个拷贝和miR-126靶序列的一个或多个拷贝。
实施方案121.实施方案71-120中的任一项的重组DNA分子,其中所述重组DNA分子是包含所述自主复制型多核苷酸的质粒。
实施方案122.一种重组DNA分子,所述重组DNA分子包含:(i)第一单链DNA(ssDNA)分子,所述第一ssDNA分子包含病毒基因组的有义序列;和(ii)第二ssDNA分子,所述第二ssDNA分子包含所述病毒基因组的反义序列,其中所述第一ssDNA分子和所述第二ssDNA分子中的每一个包含3'反向末端重复序列和5'反向末端重复序列并且其中所述有义ssDNA分子的3'末端共价连接于所述反义ssDNA分子的5'末端,并且所述有义ssDNA分子的5'末端共价连接于所述反义ssDNA分子的3'末端,以形成末端封闭的线性双链溶瘤病毒(Ov)DNA分子。
实施方案123.实施方案122的重组DNA分子,其中所述编码病毒是负义或正义单链(ss)RNA病毒。
实施方案124.实施方案123的重组DNA分子,其中所述正义ssRNA病毒是脊髓灰质炎病毒(PV)。
实施方案125.实施方案123的重组DNA分子,其中所述负义ssRNA病毒是水疱性口腔炎病毒(VSV)基因组。
实施方案126.实施方案122的重组DNA分子,其中所述第一ssDNA分子和所述第二ssDNA分子中的每一个还包含紧靠所述病毒基因组序列5'的核酶编码序列和紧靠所述病毒基因组序列3'的核酶编码序列。
实施方案127.实施方案122-126中的任一项的重组DNA分子,其中所述病毒基因组包含一个或多个被插入一种或多种必需病毒基因中的微小RNA(miRNA)靶序列。
实施方案128.实施方案127的重组DNA分子,其中所述一种或多种miRNA靶序列被插入所述一种或多种必需病毒基因的3'非翻译区(UTR)和/或5'UTR中。
实施方案129.实施方案127或128的重组DNA分子,其中所述一种或多种miRNA靶序列被插入至少2种、至少3种、至少4种或更多种必需病毒基因中。
实施方案130.实施方案127-129中的任一项的重组DNA分子,其中至少2个、至少3个或至少4个miRNA靶序列被插入一种或多种必需病毒基因中。
实施方案131.实施方案130的重组DNA分子,其中所述至少2个、至少3个或至少4个miRNA靶序列包含一种miRNA的靶序列。
实施方案132.实施方案130的重组DNA分子,其中所述至少2个、至少3个或至少4个miRNA靶序列包含至少2种、至少3种或至少4种不同miRNA的靶序列。
实施方案133.实施方案122的重组DNA分子,其中所述病毒基因组是VSV基因组,并且其中所述一种或多种miRNA靶序列被插入编码核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)和/或聚合酶(L)蛋白的基因中的一种或多种中。
实施方案134.实施方案122的重组DNA分子,其中所述病毒基因组是PV基因组,并且其中所述一种或多种miRNA靶序列被插入编码VP1、VP2、VP3、VP4、2A、2B、2C、3A、3B(VPg)、3C或3D蛋白的基因中的一种或多种中。
实施方案135.实施方案122-134中的任一项的重组DNA分子,其中3'和5'ITR源自于AAV。
实施方案136.实施方案135的重组DNA分子,其中所述AAV是AAV2。
实施方案137.一种组合物,所述组合物包含有效量的实施方案44-136中的任一项的重组DNA分子和适合于施用于哺乳动物受试者的载体。
实施方案138.一种颗粒,所述颗粒包含实施方案44-136中的任一项的重组DNA分子。
实施方案139.实施方案138的颗粒,其中所述颗粒是生物可降解的。
实施方案140.实施方案139的颗粒,其中所述颗粒选自由纳米颗粒、外泌体、脂质体和脂质体复合物(lipoplex)组成的组。
实施方案141.实施方案140的颗粒,其中所述外泌体是源自于完整外泌体或空外泌体的修饰外泌体。
实施方案142.实施方案140的颗粒,其中所述纳米颗粒是包含阳离子型脂质、胆固醇和中性脂质的脂质纳米颗粒(LNP)。
实施方案143.实施方案142的LNP,其中所述阳离子型脂质是1,2-二油酰基-3-三甲基铵-丙烷(DOTAP),并且其中所述中性脂质是1,2-二月桂酰基-sn-甘油基-3-磷酸乙醇胺(DLPE)或1,2-二油酰基-sn-甘油基-3-磷酸乙醇胺(DOPE)。
实施方案144.实施方案142或143的LNP,所述LNP还包含磷脂-聚合物缀合物,其中所述磷脂-聚合物缀合物是1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-聚(乙二醇)(DSPE-PEG)或1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-N-[氨基(聚乙二醇)](DSPE-PEG-胺)。
实施方案145.实施方案142-144中的任一项的LNP,其中透明质酸缀合于所述LNP的表面。
实施方案146.一种治疗性组合物,所述治疗性组合物包含多个根据实施方案142-145中的任一项的脂质纳米颗粒,其中所述多个LNP具有约150nm至约500nm的平均尺寸。
实施方案147.实施方案146的治疗性组合物,其中所述多个LNP具有约200nm至约500nm、约300nm至约500nm、约350nm至约500nm、约400nm至约500nm、约425nm至约500nm、约450nm至约500nm或约475nm至约500nm的平均尺寸。
实施方案148.实施方案146或147的治疗性组合物,其中所述多个LNP具有小于约-20mV、小于约-30mV、小于约35mV或小于约-40mV的平均ζ-电位。
实施方案149.实施方案148的治疗性组合物,其中所述多个LNP具有介于约-50mV至约-20mV、约-40mV至约-20mV或约-30mV至约-20mV之间的平均ζ-电位。
实施方案150.实施方案147或148的治疗性组合物,其中所述多个LNP具有约-30mV、约-31mV、约-32mV、约-33mV、约-34mV、约-35mV、约-36mV、约-37mV、约-38mV、约-39mV或约-40mV的平均ζ-电位。
实施方案151.实施方案146-150中的任一项的治疗性组合物,其中所述组合物递送至受试者将所述包封的DNA表达盒递送至靶细胞,并且其中所述包封的DNA表达盒产生能够溶解所述靶细胞的感染性病毒。
实施方案152.实施方案151的治疗性组合物,其中所述组合物经静脉内或经肿瘤内递送。
实施方案153.实施方案152的治疗性组合物,其中所述靶细胞是癌细胞。
实施方案154.一种无机颗粒,所述无机颗粒包含实施方案44-136中的任一项的多核苷酸。
实施方案155.实施方案154的颗粒,其中所述无机颗粒选自由以下组成的组:金纳米颗粒(GNP)、金纳米棒(GNR)、磁性纳米颗粒(MNP)、磁性纳米管(MNT)、碳纳米角(CNH)、碳富勒烯、碳纳米管(CNT)、磷酸钙纳米颗粒(CPNP)、介孔二氧化硅纳米颗粒(MSN)、二氧化硅纳米管(SNT)或星形中空二氧化硅纳米颗粒(SHNP)。
实施方案156.一种组合物,所述组合物包含实施方案154或155的颗粒,其中所述颗粒的平均直径小于约500nm,介于约250nm与约500nm之间,或为约350nm。
实施方案157.一种杀死癌细胞的方法,所述方法包括在足以将颗粒经细胞内递送至所述癌细胞的条件下使所述癌细胞暴露于实施方案137-156中的任一项的颗粒或组合物,或其组合物,其中由包封的多核苷酸产生的具有复制能力的病毒导致所述癌细胞的杀死。
实施方案158.实施方案157的方法,其中所述具有复制能力的病毒不在非癌细胞中产生。
实施方案159.实施方案157或158的方法,其中所述方法在体内、体外或离体进行。
实施方案160.一种治疗受试者的癌症的方法,所述方法包括向罹患所述癌症的受试者施用有效量的实施方案137-156中的任一项的颗粒或组合物,或其组合物。
实施方案161.实施方案160的方法,其中所述颗粒或其组合物经静脉内、鼻内、呈吸入剂施用,或直接注射至肿瘤中。
实施方案162.实施方案160或161的方法,其中所述颗粒或其组合物重复施用于所述受试者。
实施方案163.实施方案160-162中的任一项的方法,其中所述受试者是小鼠、大鼠、兔、猫、狗、马、非人灵长类动物或人。
实施方案164.实施方案160-163中的任一项的方法,其中所述癌症选自肺癌、乳腺癌、卵巢癌、宫颈癌、前列腺癌、睾丸癌、结肠直肠癌、结肠癌、胰腺癌、肝癌、胃癌、头颈癌、甲状腺癌、恶性胶质瘤、胶质母细胞瘤、黑色素瘤、B细胞慢性淋巴细胞性白血病、弥漫性大B细胞淋巴瘤(DLBCL)和边缘区淋巴瘤(MZL)。
实施方案165.实施方案164的方法,其中所述肺癌是小细胞肺癌或非小细胞肺癌。
实施方案166.实施方案164的方法,其中所述肝癌是肝细胞癌(HCC)。
实施方案167.一种产生前述实施方案中的任一项的重组DNA分子的方法,所述方法包括:a.将所述重组DNA分子插入第一病毒表达载体中,其中所述重组DNA分子包含多核苷酸的5'腺相关病毒(AAV)来源的反向末端重复序列(ITR)和3'AAV来源的ITR末端;b.将编码ITR介导的复制所需的AAV蛋白的多核苷酸插入第二病毒表达载体中;以及c.将所述第一病毒表达载体和所述第二病毒表达载体经细胞内递送至细胞,其中所述重组DNA分子稳定地整合至基因组中,其中所述细胞产生的侧接ITR的多核苷酸的量大于在不存在ITR的情况下将产生的量。
实施方案168.实施方案167的方法,其中所述病毒表达载体是疱疹病毒或杆状病毒。
以引用的方式并入
本文中引用的所有参考文献、文章、公布、专利、专利公布和专利申请均以引用的方式整体并入本文中以达成所有目的。然而,对本文中引用的任何参考文献、文章、公布、专利、专利公布和专利申请的提及,并不也不应被视为承认或任何形式的建议,它们构成有效的现有技术或形成世界上任何国家的公知常识的一部分。
尽管本文已经示出并描述了本公开的优选实施方案;但是本领域的技术人员显而易见的是,只是以示例的方式提供这类实施方案。在不脱离本公开的情况下,本领域的技术人员现在将想到许多变化、改变和替代。应当理解,在实践本公开中可以采用本文所述的本公开的实施方案的各种替代方案。意图以下权利要求书界定本公开的范围,并且由此涵盖在这些权利要求书范围内的方法和结构和它们的等同物。
表1:12种精选oncomiR(9种肿瘤抑制物和3种致癌miRNA)与多种癌症之间的关系的概述
表2:oncomiR和癌症概述
表3:示例性的肿瘤抑制性miR
参考文献
1.Loffler A et al.,Blood.2000;95:2098-2103
2.Bargou R et al.,Science.2008;321:974-977
3.Klinger M et al.,Blood.2012;119:6226-6233
4.Topp MS et al.,J Clin Oncol.2011;29:2493-2498.
5.Loffler A et al.,Leukemia.2003;17:900-909
6.Topp MS et al.,Blood.2012;120:5185-5187
7.Brischwein K et al.,Mol Immunol.2006;43:1129-1143
8.Herrmann I et al.,PLoS ONE.2010;5:e13474.
9.Cioffi M et al.,Clin Cancer Res.2012;18:465-474
10.Witthauer J et al.,2009;117:471-481
11.Osada T et al.,Br J Cancer.2010;102:124-133
12.Lutterbuese R et al.,J Immunother.2009;32:341-352.
13.Friedrich M et al.,Molecular Cancer Therapeutics.2012;11:2664-2673
14.Laszlo GS et al.,Blood.2014;123:554-561
15.Friedrich M et al.,Mol Cancer Ther.2014;13:1549-1557
16.Lutterbuese R et al.,PNAS,2010;107:12605-12610
17.Wuellner U et al.,Antibodies 2015,4,426-440
18.Lopez-Albaitero A,Xu H,Guo H,et al.Oncoimmunology,2017;6(3):el267891
19.Hammond SA et al.,Cancer Research.2007;67:3927-3935
20.Torisu-Itakura Het al.,J Immunother.2011;34:597-605
21.YamamotoK etal.,Biochem J.2012;445:135-144
22.Feldmann A et al.,The Journal of Immunology.2012;189:3249-3259
23.Mack M et al.,PNAS.1995;92:7021-7025
24.Zhang T et al.,Cancer Research.2011;71:2066-2076
25.Godbersen C et al.,Mol Cancer Ther.2017Jul;16(7):1335-1346
26Ross SL et al.,PLoS One,2017;eO183390
序列表
<110> 昂克诺斯公司(Oncorus, Inc.)
米切尔·H·菲尼尔(Finer, Mitchell H)
爱德华·肯尼迪(Kennedy, Edward)
洛伦娜·勒纳(Lerner, Lorena)
<120> 包封多核苷酸及使用方法
<130> ONCR-014/01WO 324865-2142
<150> 62/760,422
<151> 2018-11-13
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 8385
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 实验室制造-SVV表达盒
<400> 1
acattgatta ttgactagtt attaatagta atcaattacg gggtcattag ttcatagccc 60
atatatggag ttccgcgtta cataacttac ggtaaatggc ccgcctggct gaccgcccaa 120
cgacccccgc ccattgacgt caataatgac gtatgttccc atagtaacgc caatagggac 180
tttccattga cgtcaatggg tggagtattt acggtaaact gcccacttgg cagtacatca 240
agtgtatcat atgccaagta cgccccctat tgacgtcaat gacggtaaat ggcccgcctg 300
gcattatgcc cagtacatga ccttatggga ctttcctact tggcagtaca tctacgtatt 360
agtcatcgct attaccatgg tgatgcggtt ttggcagtac atcaatgggc gtggatagcg 420
gtttgactca cggggatttc caagtctcca ccccattgac gtcaatggga gtttgttttg 480
gcaccaaaat caacgggact ttccaaaatg tcgtaacaac tccgccccat tgacgcaaat 540
gggcggtagg cgtgtacggt gggaggtcta tataagcaga gctctctggc taactagaga 600
acccactgct tactggctta tcgaaattaa tacgactcac tatagggaga cccaagctgg 660
ctagcgttta aacttaagct tggtacctta tcaaactgat gagtccgtga ggacgaaacg 720
agtaagctcg tctttgaaat ggggggctgg gccctgatgc ccagtccttc ctttcccctt 780
ccggggggtt aaccggctgt gtttgctaga ggcacagagg ggcaacatcc aacctgcttt 840
tgcggggaac ggtgcggctc cgattcctgc gtcgccaaag gtgttagcgc acccaaacgg 900
cgcacctacc aatgttattg gtgtggtctg cgagttctag cctactcgtt tctcccccga 960
ccattcactc acccacgaaa agtgtgttgt aaccataaga tttaaccccc gcacgggatg 1020
tgcgataacc gtaagactgg ctcaagcgcg gaaagcgctg taaccacatg ctgttagtcc 1080
ctttatggct gcaagatggc tacccacctc ggatcactga actggagctc gaccctcctt 1140
agtaagggaa ccgagaggcc ttcgtgcaac aagctccgac acagagtcca cgtgactgct 1200
accaccatga gtacatggtt ctcccctctc gacccaggac ttctttttga atatccacgg 1260
ctcgatccag agggtggggc atgaccccta gcatagcgag ctacagcggg aactgtagct 1320
aggccttagc gtgccttgga tactgcctga tagggcgacg gcctagtcgt gtcggttcta 1380
taggtagcac atacaaatat gcagaactct catttttctt tcgatacagc ctctggcacc 1440
tttgaagatg taaccggaac aaaagtcaag atcgttgaat accccagatc ggtgaacaat 1500
ggtgtttacg attcgtctac tcatttggag atactgaacc tacagggtga aattgaaatt 1560
ttaaggtctt tcaatgaata ccaaattcgc gccgccaaac aacaactcgg actggacatc 1620
gtgtacgaac tacagggtaa tgttcagaca acgtcaaaga atgattttga ttcccgtggc 1680
aataatggta acatgacctt caattactac gcaaacactt atcagaattc agtagacttc 1740
tcgacctcct cgtcggcgtc aggcgccgga cctgggaact ctcggggcgg attagcgggt 1800
ctcctcacaa atttcagtgg aatcttgaac cctcttggct acctcaaaga tcacaacacc 1860
gaagaaatgg aaaactctgc tgatcgagtc acaacgcaaa cggcgggcaa cactgccata 1920
aacacgcaat catcattggg tgtgttgtgt gcctacgttg aagacccgac caaatctgat 1980
cctccgtcca gcagcacaga tcaacccacc accactttca ctgccatcga caggtggtac 2040
actggacgtc tcaattcttg gacaaaagct gtaaaaacct tctcttttca ggccgtcccg 2100
cttcccggtg cctttctgtc taggcaggga ggcctcaacg gaggggcctt cacagctacc 2160
ctacatagac actttttgat gaagtgcggg tggcaggtgc aggtccaatg taatttgaca 2220
caattccacc aaggcgctct tcttgttgcc atggttcctg aaaccaccct tgatgtcaag 2280
cccgacggta aggcaaagag cttacaggag ctgaatgaag aacagtgggt ggaaatgtct 2340
gacgattacc ggaccgggaa aaacatgcct tttcagtctc ttggcacata ctatcggccc 2400
cctaactgga cttggggtcc caatttcatc aacccctatc aagtaacggt tttcccacac 2460
caaattctga acgcgagaac ctctacctcg gtagacataa acgtcccata catcggggag 2520
acccccacgc aatcctcaga gacacagaac tcctggaccc tcctcgttat ggtgctcgtt 2580
cccctagact ataaggaagg agccacaact gacccagaaa ttacattttc tgtaaggcct 2640
acaagtccct acttcaatgg gcttcgcaac cgctacacgg ccgggacgga cgaagaacag 2700
gggcccattc ctacggcacc cagagaaaat tcgcttatgt ttctctcaac cctccctgac 2760
gacactgtcc ctgcttacgg gaatgtgcgt acccctcctg tcaattacct ccctggtgaa 2820
ataaccgacc ttttgcaact ggcccgcata cccactctca tggcatttga gcgggtgcct 2880
gaacccgtgc ctgcctcaga cacatatgtg ccctacgttg ccgttcccac ccagttcgat 2940
gacaggcctc tcatctcctt cccgatcacc ctttcagatc ccgtctatca gaacaccctg 3000
gttggcgcca tcagttcaaa tttcgccaat taccgtgggt gtatccaaat cactctgaca 3060
ttttgtggac ccatgatggc gagagggaaa ttcctgctct cgtattctcc cccaaatgga 3120
acgcaaccac agactctttc cgaagctatg cagtgcacat actctatttg ggacataggc 3180
ttgaactcta gttggacctt cgtcgtcccc tacatctcgc ccagtgacta ccgtgaaact 3240
cgagccatta ccaactcggt ttactccgct gatggttggt ttagcctgca caagttgacc 3300
aaaattactc taccacctga ctgtccgcaa agtccctgca ttctcttttt cgcttctgct 3360
ggtgaggatt acactctccg tctccccgtt gattgtaatc cttcctatgt gttccactcc 3420
accgacaacg ccgagaccgg ggttattgag gcgggtaaca ctgacaccga tttctctggt 3480
gaactggcgg ctcctggctc taaccacact aatgtcaagt tcctgtttga tcgatctcga 3540
ttattgaatg taatcaaggt actggagaag gacgccgttt tcccccgccc tttccctaca 3600
caagaaggtg cgcagcagga tgatggttac ttttgtcttc tgaccccccg cccaacagtc 3660
gcttcccgac ccgccactcg tttcggcctg tacgccaatc cgtccggcag tggtgttctt 3720
gctaacactt cactggactt caatttttat agcttggcct gtttcactta ctttagatcg 3780
gaccttgagg ttacggtggt ctcactagag ccggatctgg aatttgctgt agggtggttt 3840
ccttctggca gtgaatacca ggcttccagc tttgtctacg accagctgca tgtgcccttc 3900
cactttactg ggcgcactcc ccgcgctttc gctagcaagg gtgggaaggt atctttcgtg 3960
ctcccttgga actctgtctc gtctgtgctc cccgtgcgct gggggggggc ttccaagctc 4020
tcttctgcta cgcggggtct accggcgcat gctgattggg ggactattta cgcctttgtc 4080
ccccgtccta atgagaagaa aagcaccgct gtaaaacacg tggccgtgta cattcggtac 4140
aagaacgcac gtgcctggtg ccccagcatg cttccctttc gcagctacaa gcagaagatg 4200
ctgatgcaat ctggcgatat cgagaccaat cccgggcctg cttctgacaa cccaattttg 4260
gagtttcttg aagcagaaaa tgatctagtc actctggcct ctctctggaa gatggtgcac 4320
tctgttcaac agacctggag aaagtatgtg aagaacgatg atttttggcc caatttactc 4380
agcgagctag tgggggaagg ctctgtcgcc ttggccgcca cgctatccaa ccaagcttca 4440
gtaaaggctc ttttgggcct gcactttctc tctcgggggc tcaattacac tgacttttac 4500
tctttactga tagagaaatg ctctagtttc tttaccgtag aaccacctcc tccaccagct 4560
gaaaacctga tgaccaagcc ctcagtgaag tcgaaattcc gaaaactgtt taagatgcaa 4620
ggacccatgg acaaagtcaa agactggaac caaatagctg ccggcttgaa gaattttcaa 4680
tttgttcgtg acctagtcaa agaggtggtc gattggctgc aggcctggat caacaaagag 4740
aaagccagcc ctgtcctcca gtaccagttg gagatgaaga agctcgggcc tgtggccttg 4800
gctcatgacg ctttcatggc tggttccggg ccccctctta gcgacgacca gattgaatac 4860
ctccagaacc tcaaatctct tgccctaaca ctggggaaga ctaatttggc ccaaagtctc 4920
accactatga tcaatgccaa acaaagttca gcccaacgag ttgaacccgt tgtggtggtc 4980
cttagaggca agccgggatg cggcaagagc ttggcctcta cgttgattgc ccaggctgtg 5040
tccaagcgcc tctatggctc ccaaagtgta tattctcttc ccccagatcc agatttcttc 5100
gatggataca aaggacagtt cgtgaccttg atggatgatt tgggacaaaa cccggatgga 5160
caagatttct ccaccttttg tcagatggtg tcgaccgccc aatttctccc caacatggcg 5220
gaccttgcag agaaagggcg tccctttacc tccaatctca tcattgcaac tacaaatctc 5280
ccccacttca gtcctgtcac cattgctgat ccttctgcag tctctcgccg tatcaactac 5340
gatctgactc tagaagtatc tgaggcctac aagaaacaca cacggctgaa ttttgacttg 5400
gctttcaggc gcacagacgc cccccccatt tatccttttg ctgcccatgt gccctttgtg 5460
gacgtagctg tgcgcttcaa aaatggtcac cagaatttta atctcctaga gttggtcgat 5520
tccatttgta cagacattcg agccaagcaa caaggtgccc gaaacatgca gactctggtt 5580
ctacagagcc ccaacgagaa tgatgacacc cccgtcgacg aggcgttggg tagagttctc 5640
tcccccgctg cggtcgatga ggcgcttgtc gacctcactc cagaggccga cccggttggc 5700
cgtttggcta ttcttgccaa gctaggtctt gccctagctg cggtcacccc tggtctgata 5760
atcttggcag tgggactcta caggtacttc tctggctctg atgcagacca agaagaaaca 5820
gaaagtgagg gatctgtcaa ggcacccagg agcgaaaatg cttatgacgg cccgaagaaa 5880
aactctaagc cccctggagc actctctctc atggaaatgc aacagcccaa cgtggacatg 5940
ggctttgagg ctgcggtcgc taagaaagtg gtcgtcccca ttaccttcat ggttcccaac 6000
agaccttctg ggcttacaca gtccgctctt ctggtgaccg gccggacctt cctaatcaat 6060
gaacatacat ggtccaatcc ctcctggacc agcttcacaa tccgcggtga ggtacacact 6120
cgtgatgagc ccttccaaac ggttcatttc actcaccacg gtattcccac agatctgatg 6180
atggtacgtc tcggaccggg caattctttc cctaacaatc tagacaagtt tggacttgac 6240
cagatgccgg cacgcaactc ccgtgtggtt ggcgtttcgt ccagttacgg aaacttcttc 6300
ttctctggaa atttcctcgg atttgttgat tccatcacct ctgaacaagg aacttacgca 6360
agactcttta ggtacagggt gacgacctac aaaggatggt gcggctcggc cctggtctgt 6420
gaggccggtg gcgtccgacg catcattggc ctgcattctg ctggcgccgc cggtatcggc 6480
gccgggacct atatctcaaa attaggacta atcaaagccc tgaaacacct cggtgaacct 6540
ttggccacaa tgcaaggact gatgactgaa ttagagcctg gaatcaccgt acatgtaccc 6600
cggaaatcca aattgagaaa gacgaccgca cacgcggtgt acaaaccgga gtttgagcct 6660
gctgtgttgt caaaatttga tcccagactg aacaaggatg ttgacttgga tgaagtaatt 6720
tggtctaaac acactgccaa tgtcccttac caacctcctt tgttctacac atacatgtca 6780
gagtacgctc atcgagtctt ctccttcttg gggaaagaca atgacattct gaccgtcaaa 6840
gaagcaattc tgggcatccc cggactagac cccatggatc cccacacagc tccgggtctg 6900
ccttacgcca tcaacggcct tcgacgtact gatctcgtcg attttgtgaa cggtacagta 6960
gatgcggcgc tggctgtaca aatccagaaa ttcttagacg gtgactactc tgaccatgtc 7020
ttccaaactt ttctgaaaga tgagatcaga ccctcagaga aagtccgagc gggaaaaacc 7080
cgcattgttg atgtgccctc cctggcgcat tgcattgtgg gcagaatgtt gcttgggcgc 7140
tttgctgcca agtttcaatc ccatcctggc tttctcctcg gctctgctat cgggtctgac 7200
cctgatgttt tctggaccgt cataggggct caactcgagg ggagaaagaa cacgtatgac 7260
gtggactaca gtgcctttga ctcttcacac ggcactggct ccttcgaggc tctcatctct 7320
cactttttca ccgtggacaa tggttttagc cctgcgctgg gaccgtatct cagatccctg 7380
gctgtctcgg tgcacgctta cggcgagcgt cgcatcaaga ttaccggtgg cctcccctcc 7440
ggttgtgccg cgaccagcct gctgaacaca gtgctcaaca atgtgatcat caggactgct 7500
ctggcattga cttacaagga atttgaatat gacatggttg atatcatcgc ctacggtgac 7560
gaccttctgg ttggcacgga ttacgatctg gacttcaatg aggtggcacg acgcgctgcc 7620
aagttggggt ataagatgac tcctgccaac aagggttctg tcttccctcc gacttcctct 7680
ctttccgatg ctgtttttct aaagcgcaaa ttcgtccaaa acaacgacgg cttatacaaa 7740
ccagttatgg atttaaagaa tttggaagcc atgctctcct acttcaaacc aggaacacta 7800
ctcgagaagc tgcaatctgt ttctatgttg gctcaacatt ctggaaaaga agaatatgat 7860
agattgatgc accccttcgc tgactacggt gccgtaccga gtcacgagta cctgcaggca 7920
agatggaggg ccttgttcga ctgacccaga tagcccaagg cgcttcggtg ctgccggcga 7980
ttctgggaga actcagtcgg aacagaaaag ggaaaaaaaa aaaaaaaaaa aaaaaaaaaa 8040
aaggccggca tggtcccagc ctcctcgctg gcgccggctg ggcaacatgc ttcggcatgg 8100
cgaatgggac gcggccgctc gagtctagag ggcccgttta aacccgctga tcagcctcga 8160
ctgtgccttc tagttgccag ccatctgttg tttgcccctc ccccgtgcct tccttgaccc 8220
tggaaggtgc cactcccact gtcctttcct aataaaatga ggaaattgca tcgcattgtc 8280
tgagtaggtg tcattctatt ctggggggtg gggtggggca ggacagcaag ggggaggatt 8340
gggaagacaa tagcaggcat gctggggatg cggtgggctc tatgg 8385
<210> 2
<211> 8523
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 实验室制造-CVA21表达盒
<400> 2
acattgatta ttgactagtt attaatagta atcaattacg gggtcattag ttcatagccc 60
atatatggag ttccgcgtta cataacttac ggtaaatggc ccgcctggct gaccgcccaa 120
cgacccccgc ccattgacgt caataatgac gtatgttccc atagtaacgc caatagggac 180
tttccattga cgtcaatggg tggagtattt acggtaaact gcccacttgg cagtacatca 240
agtgtatcat atgccaagta cgccccctat tgacgtcaat gacggtaaat ggcccgcctg 300
gcattatgcc cagtacatga ccttatggga ctttcctact tggcagtaca tctacgtatt 360
agtcatcgct attaccatgg tgatgcggtt ttggcagtac atcaatgggc gtggatagcg 420
gtttgactca cggggatttc caagtctcca ccccattgac gtcaatggga gtttgttttg 480
gcaccaaaat caacgggact ttccaaaatg tcgtaacaac tccgccccat tgacgcaaat 540
gggcggtagg cgtgtacggt gggaggtcta tataagcaga gctctctggc taactagaga 600
acccactgct tactggctta tcgaaattaa tacgactcac tatagggaga cccaagctgg 660
ctagcgttta aacttaagct tggtaccgtt taaacttaag cttgtttaac tgatgagtcc 720
gtgaggacga aacgagtaag ctcgtcttaa aacagcctgt gggttgttcc caccccagag 780
gcccacgtgg cggctagtac tctggtatta cggtaccttt gtacgcctgt tttgtatccc 840
ttcccccgta actttagaag cttatcaaaa gttcaatagc aggggtacaa accagtacct 900
ctacgaacaa gcacttctgt ttccccggtg atatcacata gactgtaccc acggtcaaaa 960
gtgattgatc cgttatccgc ttgagtactt cgagaagcct agtatcacct tggaatcttc 1020
gatgcgttgc gctcaacact ctgccccgag tgtagcttag gctgatgagt ctgggcactc 1080
cccaccggcg acggtggccc aggctgcgtt ggcggcctac ccatggctga tgccgtggga 1140
cgctagttgt gaacaaggtg tgaagagcct attgagctac tcaagagtcc tccggcccct 1200
gaatgcggct aatcctaacc acggagcaac cgctcacaac ccagtgagta ggttgtcgta 1260
atgcgtaagt ctgtggcgga accgactact ttgggtgtcc gtgtttccct ttatattcat 1320
actggctgct tatggtgaca atttacaaat tgttaccata tagctattgg attggccacc 1380
cagtattgtg caatatattt gagtgtttct ttcataagcc ttattaacat cacattttta 1440
atcacaataa acagtgcaaa tgggggctca agtttcaacg caaaagaccg gtgcgcacga 1500
gaatcaaaac gtggcagcca atggatccac cattaattac actactatca actattacaa 1560
agacagtgcg agtaattccg ctactagaca agacctctcc caagatccat caaaattcac 1620
agaaccggtt aaggacttaa tgttgaaaac agcaccagct ctaaactcgc ctaacgtgga 1680
agcatgtggg tacagtgacc gtgtgaggca aatcacttta ggcaactcga ctattactac 1740
acaagaagca gccaatgcta ttgttgctta cggtgaatgg cccacttaca taaatgattc 1800
agaagctaat ccggtagatg cacccactga gccagacgtt agtagcaacc ggttttacac 1860
cctagaatcg gtgtcttgga agaccacttc aaggggatgg tggtggaagt taccagattg 1920
tttgaaggac atgggaatgt ttggtcagaa tatgtactat cactacttgg ggcgctctgg 1980
ttacaccatt catgtccagt gcaacgcttc aaaatttcac caaggggcgt taggagtttt 2040
tctgatacca gagtttgtca tggcttgcaa cactgagagt aaaacgtcat acgtttcata 2100
catcaatgca aatcctggtg agagaggcgg tgagtttacg aacacctaca atccgtcaaa 2160
tacagacgcc agtgagggca gaaagtttgc agcattggat tatttgctgg gttctggtgt 2220
tctagcagga aacgcctttg tgtacccgca ccagatcatc aacctacgta ccaacaacag 2280
tgcaacaatt gtggtgccat acgtaaactc acttgtgatt gattgtatgg caaaacacaa 2340
taactggggc attgtcatat taccactggc acccttggcc tttgccgcaa catcgtcacc 2400
acaggtgcct attacagtga ccattgcacc catgtgtaca gaattcaatg ggttgagaaa 2460
catcaccgtc ccagtacatc aagggttgcc gacaatgaac acacctggtt ccaatcaatt 2520
ccttacatct gatgacttcc agtcgccctg tgccttacct aattttgatg ttactccacc 2580
aatacacata cccggggaag taaagaatat gatggaacta gctgaaattg acacattgat 2640
cccaatgaac gcagtggacg ggaaggtgaa cacaatggag atgtatcaaa taccattgaa 2700
tgacaatttg agcaaggcac ctatattctg tttatcccta tcacctgctt ctgataaacg 2760
actgagccgc accatgttgg gtgaaatcct aaattattac acccattgga cggggtccat 2820
caggttcacc tttctatttt gtggtagtat gatggccact ggtaaactgc tcctcagcta 2880
ttccccaccg ggagctaaac caccaaccaa tcgcaaggat gcaatgctag gcacacacat 2940
catctgggac ctagggttac aatccagttg ttccatggtt gcaccgtgga tctccaacac 3000
agtgtacaga cggtgtgcac gtgatgactt cactgagggc ggatttataa cttgcttcta 3060
tcaaactaga attgtggtac ctgcttcaac ccctaccagt atgttcatgt taggctttgt 3120
tagtgcgtgt ccagacttca gtgtcagact gcttagggac actccccata ttagtcaatc 3180
gaaactaata ggacgtacac aaggcattga agacctcatt gacacagcga taaagaatgc 3240
cttaagagtg tcccaaccac cctcgaccca gtcaactgaa gcaactagtg gagtgaatag 3300
ccaggaggtg ccagctctaa ctgctgtgga aacaggagca tctggtcaag caatccccag 3360
tgatgtggtg gaaactaggc acgtggtaaa ttacaaaacc aggtctgaat cgtgtcttga 3420
gtcattcttt gggagagctg cgtgtgtcac aatcctatcc ttgaccaact cctccaagag 3480
cggagaggag aaaaagcatt tcaacatatg gaatattaca tacaccgaca ctgtccagtt 3540
acgcagaaaa ttagagtttt tcacgtattc caggtttgat cttgaaatga cttttgtatt 3600
cacagagaac tatcctagta cagccagtgg agaagtgcga aaccaggtgt accagatcat 3660
gtatattcca ccaggggcac cccgcccatc atcctgggat gactacacat ggcaatcctc 3720
ttcaaaccct tccatcttct acatgtatgg aaatgcacct ccacggatgt caattcctta 3780
cgtagggatt gccaatgcct attcacactt ctacgatggc tttgcacggg tgccacttga 3840
gggtgagaac accgatgctg gcgacacgtt ttacggttta gtgtccataa atgattttgg 3900
agttttagca gttagagcag taaaccgcag taatccacat acaatacaca catctgtgag 3960
agtgtacatg aaaccaaaac acattcggtg ttggtgcccc agacctcctc gagctgtatt 4020
atacagggga gagggagtgg acatgatatc cagtgcaatt ctacctctga ccaaggtaga 4080
ctcaattacc acttttgggt ttggtcatca gaacaaagca gtgtacgttg ccggttacaa 4140
gatttgcaac taccacctag caaccccaag tgatcacttg aatgcaatta gtatgttatg 4200
ggacagggat ttaatggtgg tggaatctag agcccaggga actgatacca tcgccagatg 4260
tagttgcagg tgtggagttt actattgtga atctaggagg aagtactacc ctgtcacttt 4320
tactggccca acgtttcgat tcatggaagc aaacgactac tatccagcaa gataccagtc 4380
tcacatgctg atagggtgcg gatttgcaga acccggggac tgcggtggga tactgaggtg 4440
cactcatggg gtaattggta tcattactgc aggaggtgaa ggggtagtag cctttgctga 4500
cattagagac ctctgggtgt atgaagagga ggccatggaa cagggaataa caagctacat 4560
cgaatctctc ggcacagcct ttggcgcagg gttcacccac acaatcagtg agaaagtgac 4620
tgaattgaca acaatggtta ccagcactat cacagaaaaa ctactgaaaa acttggtgaa 4680
aatagtgtcg gctctagtga ttgttgtgag aaattatgag gacactacca cgatccttgc 4740
aacactagca ctactcgggt gtgatatatc tccttggcaa tggttgaaga agaaggcatg 4800
tgacttacta gagattcctt atgtgatgcg ccaaggtgat gggtggatga agaaattcac 4860
agaggcgtgc aatgcagcta aaggcttaga gtggattagc aacaaaattt ccaagtttat 4920
agattggttg aagtgtaaaa ttatcccaga cgctaaggac aaggtggaat ttctcaccaa 4980
gttgaaacag ctagacatgt tggaaaatca aattgcaacc atccaccaat cttgccccag 5040
ccaagaacaa caagagattc ttttcaacaa tgtgagatgg ctagcagtcc agtcccgtcg 5100
gtttgcacca ttatacgctg tggaggcacg ccgaattaac aaaatggaga gcacaataaa 5160
caattatata cagttcaaga gcaaacaccg tattgaacca gtatgtatgc tcattcatgg 5220
gtcaccaggg acgggtaaat ctatagctac ttcattaata ggtagagcaa tagcagagaa 5280
ggaaagcaca tcagtctatt caatgccacc tgacccatct cactttgatg gctataaaca 5340
acaaggggta gtgattatgg acgacctaaa ccaaaacccc gatggtatgg acatgaaact 5400
gttttgccaa atggtatcaa cagtggagtt tattcctcca atggcctcat tagaggagaa 5460
gggcattttg tttacatctg attatgtcct ggcttctacc aactctcatt caattgtacc 5520
acccacagtg gctcacagtg atgccttaac cagacgattt gcatttgatg tggaggttta 5580
cacgatgtct gaacattcag tcaaaggcaa actgaatatg gccacggcca ctcaattgtg 5640
taaggattgt ccaacacctg caaattttaa aaagtgttgc cctctcgttt gtggaaaggc 5700
cttgcaatta atggacaggt acaccagaca aaggttcact gtagatgaga ttaccacatt 5760
aatcatgaat gagaaaaaca gaagggccaa tatcggcaat tgcatggaag ccttgtttca 5820
aggaccatta aggtataaag atttgaagat cgatgtgaag acagttcccc cccctgagtg 5880
catcagtgat ttgttacaag cagtggattc tcaagaggtt agggattact gtgagaagaa 5940
aggctggatc gttaacgtta ctagccagat tcaactagaa aggaacatca atagggccat 6000
gactatactc caagctgtta ccacattcgc agcagtcgca ggagtagtgt atgtaatgta 6060
caaactcttc gccggtcaac agggtgcata cactggcttg ccaaacaaaa aacccaatgt 6120
ccctactatc agagtcgcta aagtccaggg gccaggattt gactacgcag tggcaatggc 6180
aaaaagaaac atagttactg caaccaccac caagggtgaa tttaccatgc taggggtgca 6240
tgataatgta gcaatattgc caacccatgc cgctccagga gaaaccatta ttattgatgg 6300
gaaagaagta gagatcctag atgccagagc cttagaagat caagcgggaa ccaatcttga 6360
gatcaccatt attactctaa aaagaaatga gaagtttaga gacatcagat cacatattcc 6420
cacccaaatt actgaaacta acgatggagt gttgatcgtg aacactagca agtaccccaa 6480
tatgtatgtc cccgttggtg ctgtgaccga acagggatat cttaatctca gtggacgtca 6540
aactgctcgc actttaatgt acaactttcc aacaagggca ggccagtgcg gaggaatcat 6600
cacttgtact ggcaaagtca ttgggatgca tgttggcggg aacggttcac atgggtttgc 6660
agcagccctc aagcgatcat acttcactca aaatcagggc gaaatccagt ggatgaggtc 6720
atcaaaagaa gtggggtacc ccattataaa tgccccatcc aagacaaagt tagaacccag 6780
tgctttccac tatgtttttg aaggtgttaa ggaaccagct gtactcacta agaatgaccc 6840
cagactaaaa acagattttg aagaagccat cttttctaaa tatgtgggga acaaaattac 6900
tgaagtggac gagtacatga aagaagcagt ggatcactat gcaggacagt taatgtcact 6960
ggatatcaac acagaacaga tgtgcctgga ggatgccatg tacggcaccg atggtcttga 7020
ggccctggat cttagcacta gtgctggata tccttatgtt gcaatgggga aaaagaaaag 7080
agacattcta gataaacaga ccagagatac taaggagatg cagagacttt tagataccta 7140
tggaatcaat ctaccattag tcacgtacgt gaaagatgaa ctcaggtcaa agactaaagt 7200
ggaacaagga aagtcaagat tgattgaagc ttccagcctt aatgattcag ttgcaatgag 7260
aatggccttt ggcaatcttt acgcagcttt ccacaagaat ccaggtgtgg tgacaggatc 7320
agcagttggt tgtgacccag atttgttttg gagtaagata ccagtgctaa tggaagaaaa 7380
actcttcgct tttgactaca cagggtatga tgcctcactc agccctgctt ggtttgaagc 7440
tcttaaaatg gtgttagaaa aaattggatt tggcagtaga gtagactata tagactacct 7500
gaaccactct caccaccttt acaaaaacaa gacttattgt gtcaaaggcg gcatgccatc 7560
cggctgctct ggcacctcaa ttttcaactc aatgattaac aacctgatca ttaggacgct 7620
tttactgaga acctacaagg gcatagactt ggaccattta aaaatgattg cctatggtga 7680
tgacgtgata gcttcctacc cccatgaggt tgacgctagt ctcctagccc aatcaggaaa 7740
agactatgga ctaaccatga ctccagcaga taaatcagta acctttgaaa cagtcacatg 7800
ggagaatgta acatttctga aaagattttt cagagcagat gagaagtatc cattcctggt 7860
gcatccagtg atgccaatga aagaaattca cgaatcaatc agatggacca aggaccctag 7920
aaacacacag gatcacgtac gctcgttgtg cctattagct tggcacaacg gtgaagaaga 7980
atacaataaa tttttagcta aaatcagaag tgtgccaatc ggaagagctt tattgctccc 8040
agagtactct acattgtacc gccgatggct cgactcattt tagtaaccct acctcagtcg 8100
gattggattg ggttatactg ttgtaggggt aaatttttct ttaattcgga gaaaaaaaaa 8160
aaaaaaaaaa aaaaaaaaaa aggccggcat ggtcccagcc tcctcgctgg cgccggctgg 8220
gcaacatgct tcggcatggc gaatgggacg ctcgagtcta gagggcaggg cccgtttaaa 8280
cccgctgatc agcctcgact gtgccttcta gttgccagcc atctgttgtt tgcccctccc 8340
ccgtgccttc cttgaccctg gaaggtgcca ctcccactgt cctttcctaa taaaatgagg 8400
aaattgcatc gcattgtctg agtaggtgtc attctattct ggggggtggg gtggggcagg 8460
acagcaaggg ggaggattgg gaagacaata gcaggcatgc tggggatgcg gtgggctcta 8520
tgg 8523
- 包封多核苷酸及使用方法
- 包封的多核苷酸和使用方法
