一种厌氧菌床旁培养检测系统
文献发布时间:2023-06-19 13:48:08
技术领域
本发明涉及医疗器械技术领域,特别涉及一种厌氧菌床旁培养检测系统。
背景技术
厌氧菌是许多临床标本中最容易被忽视的微生物,在临床实践中,每当高度怀疑厌氧菌病因时,仅依赖于经验性抗生素治疗,主要原因是,厌氧培养技术繁琐,运输、培养需要维持厌氧环境,厌氧菌鉴定费时费力费钱,更重要的是,将厌氧培养报告告知临床医生需要更长的周转时间,仅培养基孵育时间就需要2-5天不等,某些特殊菌属,需要长达14天。
目前常见的厌氧菌鉴定方法如下:
1、经典的PRAS试管进行生化测试
根据菌种生长速率的不同鉴定时间在1-6天不等,菌落培养的选择依赖主观判读,缺乏客观标准。
2、自动化诱导酶检测系统
该技术利用单位时间内厌氧菌对碳水化合物及其它底物分解的能力进行厌氧菌的检测,优点是操作及时,无需厌氧环境,缺点是需要特殊设备,对生长缓慢菌落数量较小的厌氧菌来说难以实现较高的接种量,且许多厌氧菌诱导酶反应为阴性而难以检出。
3、24小时孵育的手工鉴定试剂盒
结合快速生化斑点试验和对特殊抗生素(如万古霉素、卡那霉素)的敏感性,确定临床相关的主要厌氧菌种,此技术简单可操作,缺点是需要厌氧环境。
4、MALDI-TOF质谱仪
基于分离蛋白质、肽类、脂类、糖和DNA等大分子物质的质谱技术可用于厌氧菌的鉴定,所需接种量小,检测快速,然而成本较高。
5、基因测序技术
可用于厌氧菌新物种鉴定和描述,缺点是需要特殊的设备,且需要生物信息学知识储备。
由于上述方法存在的缺乏客观性、灵敏度低、厌氧生长环境不佳、成本高、需要特殊设备等问题,难以在临床感染标本检测中普及厌氧菌检测。
发明内容
未解决上述问题,本发明实施例提供一种厌氧菌床旁培养检测系统。
本发明实施例提供的一种厌氧菌床旁培养检测系统,所述系统包括:样本收集装置,用于在患者床旁收集所述患者的用于检测厌氧菌的样本;厌氧菌培养装置,用于在所述患者床旁将收集的所述样本涂布在第一培养基上,并置于厌氧环境中进行厌氧培养;厌氧菌鉴定装置,用于对所述厌氧菌培养装置培养出的所述第一培养基中的菌落进行鉴定,得到鉴定结果。
优选地,所述样本收集装置包括:无菌容器,用于收集所述患者的痰液或非痰液,其中,所述非痰液包括以下之一:血、胸水、腹水、肺泡灌洗液、胆汁、脓肿穿刺液。
优选地,所述厌氧菌培养装置包括:第一接种环,用于将在所述患者床旁将所述样本涂布在所述第一培养基上;第一厌氧产气袋,用于为所述第一培养基提供密封的厌氧环境;二氧化碳孵箱,用于为所述厌氧产气袋中的所述第一培养基提供厌氧环境以进行厌氧培养。
优选地,所述系统还包括:需氧菌培养装置,用于在所述患者床旁将收集的所述样本涂布在第二培养基上,并置于普通气体环境中。
优选地,所述需氧菌培养装置包括:第二接种环,用于将在所述患者床旁将所述样本涂布在所述第二培养基上;普通气袋,用于为所述第二培养基提供普通气体环境;温箱,用于为所述普通气袋中的所述第二培养基提供普通气体环境以进行需氧培养。
优选地,所述系统还包括:兼性厌氧菌鉴定装置,用于在厌氧培养期间,对所述需氧菌培养装置培养出的所述第二培养基中的菌落进行鉴定,得到鉴定结果;厌氧培养控制装置,用于在所述兼性厌氧菌鉴定装置鉴定出所述第二培养基中存在兼性厌氧菌时,控制所述厌氧菌鉴定装置中止厌氧培养,在所述兼性厌氧菌鉴定装置未鉴定出所述第二培养基中存在兼性厌氧菌时,控制所述厌氧菌鉴定装置继续进行厌氧培养,以供所述厌氧菌鉴定装置进行鉴定。
优选地,所述样本是痰液,所述系统还包括:第一样本检验装置,用于检验床旁涂片的样本是否合格,以便在检验所述样本合格时进行相应培养以及在检验所述样本不合格时不进行相应培养。
优选地,所述样本检验装置包括:已在所述患者床旁涂抹所述样本的第一玻片;第二厌氧产气袋,用于在所述第一玻片上的所述样本自然干燥后,为所述第一玻片上的所述样本提供密封的厌氧环境;第一染色镜检设备,用于对从所述第二厌氧产气袋中取出的所述第一玻片上涂抹的所述样本进行染色镜检,以确定所述样本是否合格。
优选地,所述样本是非痰液,所述系统还包括:第二样本检验装置,用于检验床旁涂片的样本中是否存在细菌。
优选地,所述第二样本检验装置包括:已在所述患者床旁涂抹所述样本的第二玻片;第三厌氧产气袋,用于在所述第二玻片上的所述样本自然干燥后,为所述第二玻片上的所述样本提供密封的厌氧环境;第二染色镜检设备,用于对从所述第三厌氧产气袋中取出的所述第二玻片上涂抹的所述样本进行染色镜检,确定所述样本中是否存在细菌,以便在所述第二染色镜检设备确定所述第二玻片上的所述样本中存在细菌且所述厌氧菌鉴定装置确定所述第一培养基中不存在厌氧菌时,通过基因组测序进一步确定所述样本中是否存在厌氧菌。
本发明实施例提供一种厌氧菌床旁培养检测系统,能够以更客观、更准确地检测厌氧菌感染,可相对降低检测成本,且不需要特殊设备。
附图说明
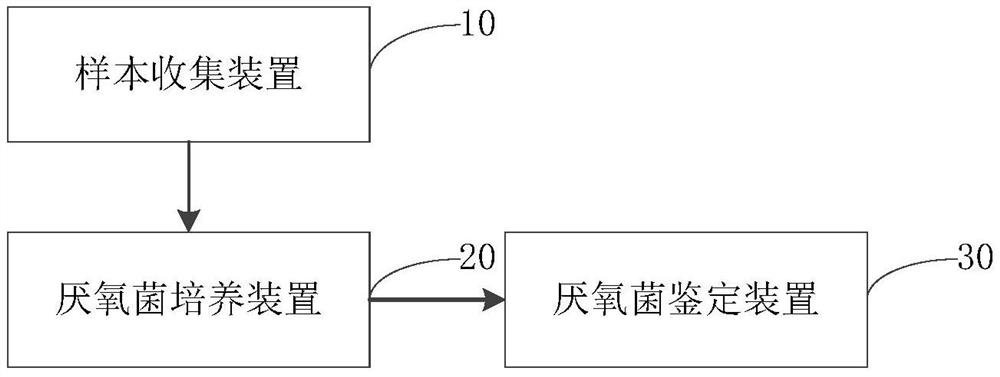
图1是本发明第一实施例提供的一种厌氧菌床旁培养检测系统的结构框图;
图2是图1所示系统的厌氧菌床旁培养检测流程图;
图3是本发明第二实施例提供的一种厌氧菌床旁培养检测系统的结构框图;
图4是图3所示系统的厌氧菌床旁培养检测流程图;
图5是本发明第三实施例提供的一种厌氧菌床旁培养检测系统的结构框图;
图6是图5所示系统的厌氧菌床旁培养检测流程图;
图7是本发明第四实施例提供的一种厌氧菌床旁培养检测系统的结构框图;
图8是图7所示系统的厌氧菌床旁培养检测流程图。
具体实施方式
以下结合附图对本发明的优选实施例进行详细说明,应当理解,以下所说明的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
图1是本发明第一实施例提供的一种厌氧菌床旁培养检测系统的结构框图,如图1所示,所述系统可以包括:样本收集装置10、厌氧菌培养装置20、厌氧菌鉴定装置。
所述样本收集装置10,用于在患者床旁收集所述患者的用于检测厌氧菌的样本;
厌氧菌培养装置20,用于在所述患者床旁将收集的所述样本涂布在第一培养基上,并置于厌氧环境中进行厌氧培养;
厌氧菌鉴定装置30,用于对所述厌氧菌培养装置培养出的所述第一培养基中的菌落进行鉴定,得到鉴定结果。
其中,所述样本收集装置10可以包括:无菌容器,用于收集所述患者的痰液或非痰液,其中,所述非痰液包括以下之一:血、胸水、腹水、肺泡灌洗液、胆汁、脓肿穿刺液。
其中,所述厌氧菌培养装置20可以包括:第一接种环,用于将在所述患者床旁将所述样本涂布在所述第一培养基上;第一厌氧产气袋,用于为所述第一培养基提供密封的厌氧环境;二氧化碳孵箱,用于为所述厌氧产气袋中的所述第一培养基提供厌氧环境以进行厌氧培养。
图2是图1所示系统的厌氧菌床旁培养检测流程图,如图2所示,可以包括如下步骤:
步骤1:确定进行厌氧检测的患者。
当存在以下情况中的至少一个时,临床高度怀疑患者发生厌氧菌感染:1)腐臭味的分泌液;2)感染涉及邻近粘膜表面的正常菌群,例如上呼吸道,胃肠道和女性生殖道;3)以脓肿形成为特征的感染;4)渗出液革兰氏染色呈现具有厌氧菌形态特征的多种菌群或生物;5)感染部位有气体形成;6)怀疑组织中毒性梭菌综合征,如破伤风、肉毒杆菌中毒、产气荚膜梭菌食物中毒、气性坏疽、艰难梭菌(曾称为梭菌)引起的腹泻或结肠炎、坏死性肠炎。7)临床常规需要进行厌氧血培养。
步骤2:准备
器材包,包括:玻片、一次性接种环、增菌培养基、厌氧产气袋、塑封袋、黄色垃圾袋、便签、马克笔;
防护用品包,包括:白大褂、帽子、口罩、无菌手套、知情同意书、笔。
步骤3:床旁接种
研究人员提前30分钟到达取样地点,签署知情同意书;穿戴好防护用具,包括:白大褂、帽子、口罩(如涉及呼吸道标本,戴N95口罩)、无菌手套;由标本采集人员采集患者的标本(或称样本),并保存于无菌容器中。
研究人员立即使用10uL一次性接种环将标本以分区划线法涂在增菌培养基上,使用马克笔在培养基底面标记时间(精确到分钟)、患者姓名、标本类型、厌氧培养,将培养基放入厌氧产气袋中密封。
需要说明的是,所有进行涂板操作的人员,例如前述研究人员,需进行过无菌操作、平板划线的培训。另外,从标本离开人体到接种完毕放入厌氧产气袋的时间需不可超过5分钟。
步骤4:送检
2小时内将密封有培养基的厌氧产气袋送至分中心检验科指定接收标本处,并将厌氧产气袋中的培养基送入36℃二氧化碳孵箱进行无菌培养。
另外,使用便签记录以下内容:科室、送检时间(精确到分钟)、送检人、联系电话,记录后将便签一起放置在孵箱中。
步骤5:结果输出及反馈
检验科工作人员利用厌氧菌鉴定装置30对培养基中培养出的菌落进行鉴定后将鉴定结果反馈给研究人员,由研究人员第一时间反馈给临床医生。
若鉴定结果为阴性则考虑无厌氧菌检出,若鉴定结果为阳性则考虑有厌氧菌检出。
本发明基于床旁接种的方式进行厌氧菌检测,克服了传统痰培养厌氧菌生长环境不佳致鉴定困难的问题,能够更客观、更准确地检测厌氧菌,且检测成本低,不需要特殊设备。
图3是本发明第二实施例提供的一种厌氧菌床旁培养检测系统的结构框图,如图3所示,在图1所示的第一实施例的基础上,所述系统还可以包括:需氧菌培养装置40、兼性厌氧菌鉴定装置50、厌氧培养控制装置60。
所述需氧菌培养装置40,用于在所述患者床旁将收集的所述样本涂布在第二培养基上,并置于普通气体环境中;
所述兼性厌氧菌鉴定装置50,用于在厌氧培养期间,对所述需氧菌培养装置培养出的所述第二培养基中的菌落进行鉴定,得到鉴定结果;
所述厌氧培养控制装置60,用于在所述兼性厌氧菌鉴定装置鉴定出所述第二培养基中存在兼性厌氧菌时,控制所述厌氧菌鉴定装置中止厌氧培养,在所述兼性厌氧菌鉴定装置未鉴定出所述第二培养基中存在兼性厌氧菌时,控制所述厌氧菌鉴定装置继续进行厌氧培养,以供所述厌氧菌鉴定装置进行鉴定。
其中,所述需氧菌培养装置40可以包括:第二接种环,用于将在所述患者床旁将所述样本涂布在所述第二培养基上;普通气袋,用于为所述第二培养基提供普通气体环境;温箱,用于为所述普通气袋中的所述第二培养基提供普通气体环境以进行需氧培养。所述普通气体为空气。
其中,所述厌氧菌鉴定装置30和所述兼性厌氧菌鉴定装置50可以是相同的鉴定装置,也可以是不同的鉴定装置。
图4是图3所示系统的厌氧菌床旁培养检测流程图,如图4所示,可以包括如下步骤:
步骤1:确定进行厌氧检测的患者。
当存在以下情况中的至少一个时,临床高度怀疑患者发生厌氧菌感染:1)腐臭味的分泌液;2)感染涉及邻近粘膜表面的正常菌群,例如上呼吸道,胃肠道和女性生殖道;3)以脓肿形成为特征的感染;4)渗出液革兰氏染色呈现具有厌氧菌形态特征的多种菌群或生物;5)感染部位有气体形成;6)怀疑组织中毒性梭菌综合征,如破伤风、肉毒杆菌中毒、产气荚膜梭菌食物中毒、气性坏疽、艰难梭菌(曾称为梭菌)引起的腹泻或结肠炎、坏死性肠炎。7)临床常规需要进行厌氧血培养。
步骤2:准备
器材包,包括:玻片、一次性接种环、增菌培养基、厌氧产气袋、塑封袋、黄色垃圾袋、便签、马克笔;
防护用品包,包括:白大褂、帽子、口罩、无菌手套、知情同意书、笔。
步骤3:床旁接种
研究人员提前30分钟到达取样地点,签署知情同意书;穿戴好防护用具,包括:白大褂、帽子、口罩(如涉及呼吸道标本,戴N95口罩)、无菌手套;由标本采集人员采集患者的标本(或称样本),并保存于无菌容器中。
研究人员立即使用10uL一次性接种环将标本以分区划线法涂在一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、厌氧培养,将该培养基放入厌氧产气袋中密封。
同样地,研究人员使用另一10uL一次性接种环将标本以分区划线法涂在另一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、需氧培养,将该培养基放入普通袋子中。也就是说,更换一次性接种环,再次进行一次涂板,将培养基放入普通袋子进行需氧条件涂板做对比。
需要说明的是,所有进行涂板操作的人员,例如前述研究人员,需进行过无菌操作、平板划线的培训。另外,从标本离开人体到接种完毕放入厌氧产气袋的时间需不可超过5分钟。
步骤4:送检
2小时内将密封有培养基的厌氧产气袋和装有培养基的普通袋子送至分中心检验科指定接收标本处,并将厌氧产气袋中的培养基送入36℃二氧化碳孵箱进行无菌培养,将普通袋子中的培养基送入35℃温箱中进行无菌培养。
另外,使用便签记录以下内容:科室、送检时间(精确到分钟)、送检人、联系电话,记录后将便签分别放置在孵箱和温箱中。
步骤5:结果输出及反馈
检验科工作人员将鉴定结果反馈给研究人员,由研究人员第一时间反馈给临床医生。具体包括以下几种情况:
1、对于需氧培养的培养基,在鉴定结果为A.0培养阴性或者A.1培养出需氧菌时,继续进行厌氧培养满5天。5天后,对于厌氧培养的培养基,若鉴定结果为B.0培养阴性,则考虑无厌氧菌检出,若鉴定结果为B.1培养阳性,则考虑有厌氧菌检出,并鉴定出厌氧菌的菌种。
2、对于需氧培养的培养基,在鉴定结果为A.2存在兼性厌氧菌时,因兼性厌氧菌会明显掩盖专性厌氧菌生长,此时中止厌氧培养,鉴定结果为:NA,即,无法确定是否存在专性厌氧菌。
在第一实施例的基础上,第二实施例通过配合需氧培养,能够在鉴定出兼性厌氧菌的情况下,及时中止无效的厌氧培养,提高检验效率和准确率,降低检验成本。
图5是本发明第三实施例提供的一种厌氧菌床旁培养检测系统的结构框图,如图5所示,在图3所示的第二实施例的基础上,所述系统还可以包括:第一样本检验装置11。
所述第一样本检验装置11,用于检验床旁涂片的样本是否合格,以便在检验所述样本合格时进行相应培养以及在检验所述样本不合格时不进行相应培养。
其中,所述第一样本检验装置11应用于所述样本是痰液的情况下,所述第一样本检验装置11可以包括:已在所述患者床旁涂抹所述样本的第一玻片;第二厌氧产气袋,用于在所述第一玻片上的所述样本自然干燥后,为所述第一玻片上的所述样本提供密封的厌氧环境;第一染色镜检设备,用于对从所述第二厌氧产气袋中取出的所述第一玻片上涂抹的所述样本进行染色镜检,以确定所述样本是否合格。
图6是图5所示系统的厌氧菌床旁培养检测流程图,如图6所示,可以包括如下步骤:
步骤1:确定进行厌氧检测的患者。
当存在以下情况中的至少一个时,临床高度怀疑患者发生厌氧菌感染:1)腐臭味的分泌液;2)感染涉及邻近粘膜表面的正常菌群,例如上呼吸道,胃肠道和女性生殖道;3)以脓肿形成为特征的感染;4)渗出液革兰氏染色呈现具有厌氧菌形态特征的多种菌群或生物;5)感染部位有气体形成;6)怀疑组织中毒性梭菌综合征,如破伤风、肉毒杆菌中毒、产气荚膜梭菌食物中毒、气性坏疽、艰难梭菌(曾称为梭菌)引起的腹泻或结肠炎、坏死性肠炎。7)临床常规需要进行厌氧血培养。
步骤2:准备
器材包,包括:玻片、一次性接种环、增菌培养基、厌氧产气袋、塑封袋、黄色垃圾袋、便签、马克笔;
防护用品包,包括:白大褂、帽子、口罩、无菌手套、知情同意书、笔。
步骤3:床旁涂片和床旁接种
研究人员提前30分钟到达取样地点,签署知情同意书;穿戴好防护用具,包括:白大褂、帽子、口罩(如涉及呼吸道标本,戴N95口罩)、无菌手套;由标本采集人员采集患者的标本(或称样本),并保存于无菌容器中。
床旁涂片:进行床旁痰涂片。具体地说,取经过95%的乙醇擦拭脱脂,干燥清洁、无划痕、无油污的合格的玻片,在玻片背面左端1/3处注明编号;小心打开痰标本盒,使用折断的竹签茬端,挑取痰标本中干酪样、脓样或可疑部分约0.05-0.1ml,于玻片正面右侧2/3处,均匀涂抹成10*20mm的卵圆形痰膜;痰膜朝上静置自然干燥,然后将该玻片放入厌氧产气袋中送至分中心检验科接收标本处进行染色镜检。若痰标本合格(即,满足低倍镜下鳞状细胞小于10个,白细胞>25个,或者鳞/白比例<1:2.5,则进行床旁接种;若痰标本不合格,则床旁接种及后续培养对判断致病菌感染意义有限,不再进行床旁接种和培养。
床旁接种:研究人员立即使用10uL一次性接种环将标本以分区划线法涂在一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、厌氧培养,将该培养基放入厌氧产气袋中密封。同样地,研究人员使用另一10uL一次性接种环将标本以分区划线法涂在另一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、需氧培养,将该培养基放入普通袋子中。也就是说,更换一次性接种环,再次进行一次涂板,将培养基放入普通袋子进行需氧条件涂板做对比。需要说明的是,所有进行涂板操作的人员,例如前述研究人员,需进行过无菌操作、平板划线的培训。另外,为了保证从标本离开人体到接种完毕放入厌氧产气袋的时间需不可超过5分钟,也可以同时进行床旁涂片和床旁接种。
步骤4:送检
2小时内将密封有培养基的厌氧产气袋和装有培养基的普通袋子送至分中心检验科指定接收标本处,并将厌氧产气袋中的培养基送入36℃二氧化碳孵箱进行无菌培养,将普通袋子中的培养基送入35℃温箱中进行无菌培养。
另外,使用便签记录以下内容:科室、送检时间(精确到分钟)、送检人、联系电话,记录后将便签分别放置在孵箱和温箱中。
步骤5:结果输出及反馈
检验科工作人员将鉴定结果反馈给研究人员,由研究人员第一时间反馈给临床医生。具体包括以下几种情况:
1、对于需氧培养的培养基,在鉴定结果为A.0培养阴性或者A.1培养出需氧菌时,继续进行厌氧培养满5天。5天后,对于厌氧培养的培养基,若鉴定结果为B.0培养阴性,则考虑无厌氧菌检出,若鉴定结果为B.1培养阳性,则考虑有厌氧菌检出,并鉴定出厌氧菌的菌种。
2、对于需氧培养的培养基,在鉴定结果为A.2存在兼性厌氧菌时,因兼性厌氧菌会明显掩盖专性厌氧菌生长,此时中止厌氧培养,鉴定结果为:NA,即,无法确定是否存在专性厌氧菌。
在第一和第二实施例的基础上,第三实施例在样本为痰液的情况下,通过床旁涂片预先判断痰液样本是否合格,从而在判断痰液样本不合格时,及时中止第一实施例的厌氧培养或中止第二实施例的需氧培养和厌氧培养,也就是说,仅在痰液样本合格时进行相应培养,有助于提高检验效率和准确率,降低检验成本。
图7是本发明第四实施例提供的一种厌氧菌床旁培养检测系统的结构框图,如图7所示,在在图3所示的第二实施例的基础上,所述系统还可以包括:第二样本检验装置70。
所述第二样本检验装置70,用于检验床旁涂片的样本中是否存在细菌。
其中,所述第二样本检验装置70应用于所述样本是非痰液的情况下,所述第二样本检验装置70可以包括:已在所述患者床旁涂抹所述样本的第二玻片;第三厌氧产气袋,用于在所述第二玻片上的所述样本自然干燥后,为所述第二玻片上的所述样本提供密封的厌氧环境;第二染色镜检设备,用于对从所述第三厌氧产气袋中取出的所述第二玻片上涂抹的所述样本进行染色镜检,确定所述样本中是否存在细菌,以便在所述第二染色镜检设备确定所述第二玻片上的所述样本中存在细菌且所述厌氧菌鉴定装置确定所述第一培养基中不存在厌氧菌时,通过基因组测序进一步确定所述样本中是否存在厌氧菌。
所述第一染色镜检设备和所述第二染色镜检设备可以是相同设备,也可以是不同设备。
图8是图7所示系统的厌氧菌床旁培养检测流程图,如图8所示,可以包括如下步骤:
步骤1:确定进行厌氧检测的患者。
当存在以下情况中的至少一个时,临床高度怀疑患者发生厌氧菌感染:1)腐臭味的分泌液;2)感染涉及邻近粘膜表面的正常菌群,例如上呼吸道,胃肠道和女性生殖道;3)以脓肿形成为特征的感染;4)渗出液革兰氏染色呈现具有厌氧菌形态特征的多种菌群或生物;5)感染部位有气体形成;6)怀疑组织中毒性梭菌综合征,如破伤风、肉毒杆菌中毒、产气荚膜梭菌食物中毒、气性坏疽、艰难梭菌(曾称为梭菌)引起的腹泻或结肠炎、坏死性肠炎。7)临床常规需要进行厌氧血培养。
步骤2:准备
器材包,包括:玻片、一次性接种环、增菌培养基、厌氧产气袋、塑封袋、黄色垃圾袋、便签、马克笔;
防护用品包,包括:白大褂、帽子、口罩、无菌手套、知情同意书、笔。
步骤3:床旁涂片和床旁接种
研究人员提前30分钟到达取样地点,签署知情同意书;穿戴好防护用具,包括:白大褂、帽子、口罩(如涉及呼吸道标本,戴N95口罩)、无菌手套;由标本采集人员采集患者的标本(或称样本),并保存于无菌容器中。
床旁涂片:进行床旁非痰涂片。标本为其它类型的标本,例如,血、胸水、腹水、肺泡灌洗液、胆汁、脓肿穿刺液等较稀薄的标本,采用推片法,取一小滴标本滴在玻片偏右侧端,用推片用30度夹角将玻片上液体轻轻向左推;玻片朝上静置自然干燥,将玻片放入厌氧产气袋中送至分中心检验科接收标本处进行染色镜检。
床旁接种:研究人员立即使用10uL一次性接种环将标本以分区划线法涂在一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、厌氧培养,将该培养基放入厌氧产气袋中密封。同样地,研究人员使用另一10uL一次性接种环将标本以分区划线法涂在另一增菌培养基上,使用马克笔在该培养基底面标记时间(精确到分钟)、患者姓名、标本类型、需氧培养,将该培养基放入普通袋子中。也就是说,更换一次性接种环,再次进行一次涂板,将培养基放入普通袋子进行需氧条件涂板做对比。需要说明的是,所有进行涂板操作的人员,例如前述研究人员,需进行过无菌操作、平板划线的培训。另外,为了保证从标本离开人体到接种完毕放入厌氧产气袋的时间需不可超过5分钟,也可以同时进行床旁涂片和床旁接种。
步骤4:送检
2小时内将密封有培养基的厌氧产气袋和装有培养基的普通袋子送至分中心检验科指定接收标本处,并将厌氧产气袋中的培养基送入36℃二氧化碳孵箱进行无菌培养,将普通袋子中的培养基送入35℃温箱中进行无菌培养。
另外,使用便签记录以下内容:科室、送检时间(精确到分钟)、送检人、联系电话,记录后将便签分别放置在孵箱和温箱中。
步骤5:结果输出及反馈
检验科工作人员将鉴定结果反馈给研究人员,由研究人员第一时间反馈给临床医生。具体包括以下几种情况:
1、对于需氧培养的培养基,在鉴定结果为A.0培养阴性或者A.1培养出需氧菌时,继续进行厌氧培养满5天。5天后,对于厌氧培养的培养基,若鉴定结果为B.0培养阴性,若鉴定结果为B.1培养阳性,则考虑有厌氧菌检出,并鉴定出厌氧菌的菌种。
2、对于需氧培养的培养基,在鉴定结果为A.2存在兼性厌氧菌时,因兼性厌氧菌会明显掩盖专性厌氧菌生长,此时中止厌氧培养,鉴定结果为:NA,即,无法确定是否存在专性厌氧菌。
3、在非痰液标本的床旁涂片的鉴定结果为C.1阳性(即染色镜检可见细菌),而厌氧培养的鉴定结果为B.0阴性时,可能说明细菌活力较弱,难以培养,此时无法判定是否存在厌氧菌感染,需通过基因组测序进一步确定D.0阴性(即非痰液标本存在厌氧菌)或D.1阳性(即非痰液标本不存在厌氧菌)。
4、在非痰液标本的床旁涂片的鉴定结果为C.0阴性(即染色镜检未见细菌),而厌氧培养的鉴定结果为B.1阳性时,以涂板结果(即厌氧培养的鉴定结果)为准。
在第一和第二实施例的基础上,第四实施例在样本为非痰液的情况下,如果床旁涂片的鉴定结果为C.1阳性且厌氧培养的鉴定结果为B.0阴性,则通过基因组测序进行厌氧菌检测,有利于检测出活力较弱难以培养的厌氧菌,提高检测准确率。
综上所述,本发明可以规范临床感染标本厌氧感染检测,优化检测流程,提高检验的灵敏度和效率,降低检验成本。一方面,本发明通过床旁涂片及接种的方式纳入痰标本进行厌氧菌检测,克服传统痰培养厌氧菌生长环境不佳而导致的鉴定困难的问题,可系统地判断痰标本微生物检测结果,及时中止无效的厌氧培养,提高检验效率,理论上可缩短检验成本。另一方面,对于非痰标本,本发明通过结合床旁涂片及接种,综合判断是否有厌氧菌感染可能,是否有进行基因组测序的必要性,理论上可以提高厌氧菌检出的灵敏度。
尽管上文对本发明进行了详细说明,但是本发明不限于此,本技术领域技术人员可以根据本发明的原理进行各种修改。因此,凡按照本发明原理所作的修改,都应当理解为落入本发明的保护范围。
- 一种厌氧菌床旁培养检测系统
- 一种食气厌氧菌利用合成气发酵产醇的培养体系和培养方法
