一种5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的检测方法
文献发布时间:2023-06-19 19:27:02
技术领域
本发明属于抗氧剂检测分析技术领域。更具体地,涉及一种5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的检测方法。
背景技术
塑料作为日常生活中的材料,其应用领域十分广泛,其中,由于阻隔性好、强度高、透明、质轻等优点,塑料成为主要的包装材料。但高分子材料易发生氧化反应,使材料发生褪色、泛黄、龟裂、硬化、丧失光泽或透明等现象,进而导致抗冲击强度、抗绕曲强度、抗张强度和伸长率等物理性能的大幅下降,影响塑料制品的正常使用。目前延缓高聚物氧化作用的措施较为适宜的有改进高聚物的化学结构、对活泼端基进行消活稳定处理和添加抗氧剂等。其中,添加抗氧剂是高聚物稳定化处理最简单通用的方法。抗氧剂是抑制或延缓高聚物受大气中氧或臭氧作用而降解的添加剂,是塑料中应用最广泛的助剂。抗氧剂虽可阻缓材料老化,但过量加入会对人体产生危害。有毒理实验表明,合成抗氧化剂(最常用的有BHA、BHT)毒副作用较大,对人体肝、脾、肺等均有不利影响。世界各国相继颁布了针对直接接触食品包装材料的标准要求,迫切需要建立一种快速测定包装材料里的抗氧剂含量的检测方法。
目前,为了控制抗氧剂的添加量,抗氧剂常用的检测方法主要包括:液相色谱法、气相色谱法、气相色谱-质谱联用法和红外光谱法等。5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮(抗氧剂HP-136)常作为抗氧剂添加到塑料包装材料中,也需要严格监控,但是迄今为止,关于5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮(抗氧剂HP-136)的研究主要集中在合成及应用领域,关于其在塑料包装材料中含量的检测罕见报道。王勇等公开了一种通过液相色谱-PDA检测法测定复合塑料中的抗氧剂HP-136成分,但所述方法的分析成本、仪器价格及日常维护费用都较高(王勇,胡翠兰.复合塑料添加剂(9M)中有效成分的测定[C]//.第十五次全国色谱学术报告会文集(下册).,2005:99-100.)。
发明内容
本发明要解决的技术问题是克服现有技术测定5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮方法的缺陷和不足,提供一种灵敏度高、检测速度快、检测准确度和精密度高以及操作简单的检测方法。
本发明上述目的通过以下技术方案实现:
一种5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的检测方法,包括以下步骤:
S1.制备标准溶液和供试品溶液,其中,供试品溶液的制备方法为:将样品破碎,加入有机溶剂,于25~40℃充分萃取,对萃取液进行过滤,所得滤液待测;
S2.采用气相色谱-质谱联用仪进行检测分析,其中,气相色谱条件为:采用DB-5HT或DB-5MS;设置进样口温度:240~300℃;进样模式为不分流;色谱柱流量为0.8~1.5mL/min;气相色谱的升温程序为:设置初始温度为80~120℃,以20~30℃/min升温至310~320℃,保持3~5min;
质谱条件为:离子源:EI源;电离能量:70ev;离子源温度:220~240℃;四级杆温度:140~160℃;溶剂延迟:3~5min;采集模式:sim和扫描;定量离子(m/z):307,定性离子(m/z):308,350,335;其中,所述m/z是质子数与电荷数的比值。
进一步地,所述检测方法,还包括以下步骤:
(1)绘制标准曲线:以浓度为横坐标X,峰面积为纵坐标Y,绘制标准工作曲线;
(2)求目标物质的含量:将测试所得的5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的峰面积代入标准工作曲线,得到供试品溶液中5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的浓度,然后根据供试品溶液所对应的样品质量计算得到样品中5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的残留量。
优选地,所述气相色谱条件为:色谱柱:DB-5HT(长度15m,内径0.25mm,膜厚0.1μm),进样口温度:290℃,进样模式:不分流,色谱柱流量:1.2mL/min,升温程序:初始温度100℃,保持0min,以30℃/min升温至320℃,保持3min。
优选地,所述质谱条件为:离子源:EI源,电离能量:70ev,离子源温度:230℃,四级杆温度:150℃,溶剂延迟:3min,采集模式:sim和扫描,定量离子(m/z):307,定性离子(m/z):308,350,335。
优选地,所述有机溶剂为甲醇或甲苯。
最优选地,所述有机溶剂为甲苯。采用甲苯作为溶剂,得到的目标物响应值较高。
优选地,所述样品与有机溶剂的用量比为1g:10~50mL。
优选地,所述充分萃取的方式为超声。
优选地,所述充分萃取的时间为30~50min。
优选地,所述对萃取液进行过滤的滤膜孔径为0.45μm。
进一步地,所述检测方法的检测限为0.0061mg/L。
进一步地,所述检测方法的定量限为0.0204mg/L。
本发明具有以下有益效果:
(1)本发明建立了一种全新的5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的检测方法,通过仪器分析参数的优化设定,目标化合物5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮可在6min内得到对称的色谱峰。
(2)该分析测试方法测定的目标化合物在一定范围内呈现良好的线性关系;检出限和定量限值都较低,灵敏度高;相对标准偏差和加标回收率均在测试要求范围内,精密度和准确度较高;并且该方法操作简单高效,可以为塑料包装材料的安全使用以及厂家对产品的质量管控提供技术和数据支持。
附图说明
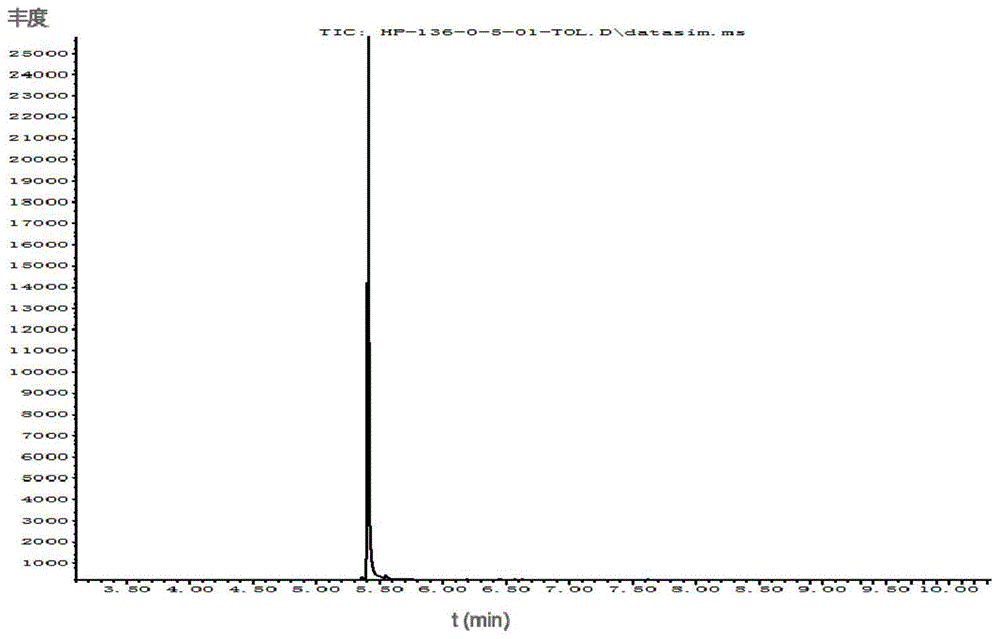
图1为以甲苯为溶剂配制的5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准溶液的色谱图。
图2为以甲苯为溶剂配制的5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准溶液的质谱图。
图3为不同溶剂对应的同一浓度标准溶液的叠加色谱图。
图4为不同萃取温度对应的加标回收率的数据说图。
图5为不同萃取时间对应的加标回收率的数据图。
图6为以甲苯为溶剂配制的5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的标准工作曲线图。
具体实施方式
以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
除非特别说明,以下实施例所用试剂和材料均为市购。
5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的信息如表1所示:
表1 5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的基本信息
实施例1 5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的色谱图和质谱图的测定
一种5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的检测方法,具体包括以下步骤:
1、实验方法
S1.标准溶液的配制
(1)标准储备液:用十万分级分析天平准确称取5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准品10mg,用甲苯溶解并定容至10mL容量瓶中,得到标准物质1000mg/L储备液,于4℃冰箱中避光保存。
(2)标准工作溶液:用甲苯逐级稀释标准储备液,得到0.1mg/L、0.5mg/L、1.0mg/L、2.0mg/L、5.0mg/L、10.0mg/L系列混合标准工作溶液。
S2.检测分析采用GC-MS联用仪对步骤S1所得浓度为0.5mg/mL的标准工作溶液进行测定;
(1)气相色谱条件:
色谱柱:DB-5HT(长度15m,内径0.25mm,膜厚0.1μm),进样口温度:290℃,进样模式:不分流,色谱柱流量:1.2mL/min,升温程序:初始温度100℃,以30℃/min升温至320℃,保持3min。
(2)质谱条件:
离子源:EI源,电离能量:70ev,离子源温度:230℃,四级杆温度:150℃,溶剂延迟:3min,采集模式:选择全扫描模式定性,选择SIM模式定量,定量离子(m/z):307,定性离子(m/z):308,350,335。
2、实验结果。
根据上述条件,对标准溶液进行分析,记录色谱图和质谱图,得到5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的色谱图和质谱图,结果分别如图1和图2所示。由图1可知,5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的色谱峰的峰形较尖锐对称,在5.5min内出峰;由图2可知,选择离子308、335和350为5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的定性离子;其中离子307的响应值最高,选择其作为5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的定量离子。
实施例2溶剂的选择
1、实验方法
S1.标准溶液的配制
(1)标准储备液:用十万分级分析天平准确称取5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准品10mg,分别用甲苯、甲醇和丙酮作为有机溶剂溶解并定容至10mL容量瓶中,得到标准物质1000mg/L储备液,于4℃冰箱中避光保存。
(2)标准工作溶液:采用对应的有机溶剂逐级稀释标准储备液,得到0.1mg/L、0.5mg/L、1.0mg/L、2.0mg/L、5.0mg/L、10.0mg/L系列混合标准工作溶液。
S2.检测分析
采用GC-MS联用仪对步骤S1所得浓度为0.5mg/mL的标准工作溶液进行测定;
(1)气相色谱条件:
色谱柱:DB-5HT(长度15m,内径0.25mm,膜厚0.1μm),进样口温度:290℃,进样模式:不分流,色谱柱流量:1.2mL/min,升温程序:初始温度100℃,以30℃/min升温至320℃,保持3min。
(2)质谱条件:
离子源:EI源,电离能量:70ev,离子源温度:230℃,四级杆温度:150℃,溶剂延迟:3min,采集模式:选择全扫描模式定性,选择SIM模式定量,定量离子(m/z):307,定性离子(m/z):308,350,335。
2、实验结果
根据上述条件进行检测,记录不同溶剂配制的标准工作溶液的色谱图,结果如图3所示,丙酮对应的目标物响应很低,而甲苯对应的目标物响应值最高,应该是由于5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮中含有两个苯环以及烷烃结构,物质本身的极性较小,导致它在甲苯中的溶解度较好。根据响应值对比结果,因此选择甲苯作为萃取溶剂。
实施例3萃取温度的优化
1、实验方法
S1.标准溶液的配制
(1)标准储备液:用十万分级分析天平准确称取5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准品10mg,用甲苯溶解并定容至10mL容量瓶中,得到标准物质1000mg/L储备液,于4℃冰箱中避光保存。
(2)标准工作溶液:用甲苯逐级稀释标准储备液,得到0.1mg/L、0.5mg/L、1.0mg/L、2.0mg/L、5.0mg/L、10.0mg/L系列混合标准工作溶液。
S2.供试液和加标溶液的制备
(1)供试液的配制:称取不含有目标产物的塑料薄膜样品1g(精确至0.1mg),剪碎至2mm×2mm,置于样品瓶中,加入10mL有机溶剂。
(2)加标溶液的配制:称取不含有目标产物的塑料薄膜样品1g(精确至0.1mg),剪碎至2mm×2mm,置于样品瓶中,加入9mL有机溶剂,再加入浓度为20mg/mL的标准工作溶液1mL。
(3)依次设定萃取温度为25℃、40℃及60℃,分别在不同温度条件下对样品(供试液或加标溶液)溶液超声50min进行萃取,取萃取后的溶液经0.45μm滤膜过滤后得到待测溶液。
S3.检测分析
采用GC-MS联用仪对步骤S1和步骤S2所得溶液进行测定;
(1)气相色谱条件:
色谱柱:DB-5HT(长度15m,内径0.25mm,膜厚0.1μm),进样口温度:290℃,进样模式:不分流,色谱柱流量:1.2mL/min,升温程序:初始温度100℃,以30℃/min升温至320℃,保持3min。
(2)质谱条件:
离子源:EI源,电离能量:70ev,离子源温度:230℃,四级杆温度:150℃,溶剂延迟:3min,采集模式:选择全扫描模式定性,选择SIM模式定量,定量离子(m/z):307,定性离子(m/z):308,350,335。
(3)绘制标准曲线:以浓度为横坐标X,峰面积为纵坐标Y,绘制标准工作曲线。
(4)加标回收率计算公式
P=(c
式中,P为加标回收率;
c
c
c
2、实验结果
将测试所得数据得到各条件下目标产物的浓度,再利用上述计算公式得到加标回收率的测试结果(以平行测定3次结果的平均值作为测试结果),结果如图4所示,当萃取温度为25℃时,5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮的平均回收率最高,高于95%。当温度为40℃时,其回收率相对25℃的略有下降,但仍高于95%,而当升温至60℃时,回收率急剧下降,平均回收率降至约86%,可能是由于温度升高,增强了基质干扰,破坏了萃取平衡。综合萃取因素及回收率结果,因此选择优化的萃取温度为40℃。
实施例4萃取时间的优化
1、实验方法
S1.标准溶液的配制
(1)标准储备液:用十万分级分析天平准确称取5,7-二叔丁基-3-(3,4-二甲苯基)苯并呋喃-2(3H)-酮标准品10mg,用甲苯溶解并定容至10mL容量瓶中,得到标准物质1000mg/L储备液,于4℃冰箱中避光保存。
(2)标准工作溶液:用甲苯逐级稀释标准储备液,得到0.1mg/L、0.5mg/L、1.0mg/L、2.0mg/L、5.0mg/L、10.0mg/L系列混合标准工作溶液。S2.供试液和加标溶液的制备
(1)供试液的配制:称取不含有目标产物的塑料薄膜样品1g(精确至0.1mg),剪碎至2mm×2mm,置于样品瓶中,加入10mL有机溶剂。
(2)加标溶液的配制:称取不含有目标产物的塑料薄膜样品1g(精确至0.1mg),剪碎至2mm×2mm,置于样品瓶中,加入9mL有机溶剂,再加入浓度为20mg/mL的标准工作溶液1mL。
(3)依次设定萃取时间为30min,50min,70min,90min,110min,萃取温度均设置为40℃,分别在不同时间条件下对样品溶液(供试液或加标溶液)进行超声萃取,取萃取后的溶液经0.45μm滤膜过滤后得到待测溶液。
S3.检测分析
采用GC-MS联用仪对步骤S1和步骤S2所得溶液进行测定;
(1)气相色谱条件:
色谱柱:DB-5HT(长度15m,内径0.25mm,膜厚0.1μm),进样口温度:290℃,进样模式:不分流,色谱柱流量:1.2mL/min,升温程序:初始温度100℃,以30℃/min升温至320℃,保持3min。
(2)质谱条件:
离子源:EI源,电离能量:70ev,离子源温度:230℃,四级杆温度:150℃,溶剂延迟:3min,采集模式:选择全扫描模式定性,选择SIM模式定量,定量离子(m/z):307,定性离子(m/z):308,350,335。
2、实验结果
记录色谱图,参照实施例3的计算方法得到不同萃取时间的加标回收率数据结果,结果如图5所示,当萃取时间从30min增加至50min时,目标物的平均回收率几乎不变,当萃取时间从50min增至70min、90min和110min时,目标物的回收率均有所下降。综合萃取因素和回收率结果,因此选择优化的萃取时间为50min。
实施例5线性方程和检出限的测定
1、实验方法
参照实施例1标准溶液的配置方法,得到不同浓度的标准工作溶液,参照实施例1的GC-MS条件,分别进样,进样量1uL,每个浓度进样次数3次(最后取平均值),求得每个浓度的平均峰面积,以质量浓度X(mg/L)为横坐标,峰面积Y为纵坐标绘制标准工作曲线(如图6所示)。
2、实验结果
所得待测物的线性回归方程及其他参数见表2。
表2目标化合物回归方程及其他参数
结合表2中数据和图6可看出,在0.1mg/L~10.0mg/L的线性范围内,目标化合物呈现出很好的线性关系,其检出限和定量限都较低,分别为0.0061mg/L和0.0204mg/L。
实施例6精密度与准确度考察
1、实验方法
选择不含有目标产物的塑料薄膜样品,设定萃取温度为40℃,分别制备了3个不同的加标浓度水平(0.1mg/L、2.0mg/L、10.0mg/L)的加标溶液进行精密度与准确度实验,每个水平平行测定3次,计算平均加标回收率和精密度,其余操作参见实施例3。
2、实验结果
测定结果见表3。
表3精密度与准确度试验结果
结果表明,相对标准偏差<3.4%,说明该测试方法重复性好,精密性高;在3种不同加标水平下,目标物的加标回收率在95.3%~105.0%区间内,表明该方法准确度较高,可以满足测试要求。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 一种采用HPLC测定3-丁基-1(3H)-异苯并呋喃酮有关物质的检测方法
- 一种3-丁基-1(3H)-异苯并呋喃酮磺丁基-β-环糊精包合物及其制备方法和应用
