丹莪妇康煎膏中三七含量的检测方法
文献发布时间:2023-06-19 19:28:50
技术领域
本发明属于质量检测技术领域,具体涉及丹莪妇康煎膏中三七含量的检测方法。
背景技术
丹莪妇康煎膏属于传统中药制剂中的膏滋剂,具有活血化瘀、疏肝理气、调经止痛、软坚化积等功效,是临床上治疗子宫内膜异位症的常用药。丹莪妇康煎膏呈黑褐色粘稠的半流体状态,全方由紫丹参、莪术、滇柴胡、三七、赤芍、当归、三棱、香附、延胡索和甘草10味药组成。
在国家食品药品监督管理总局国家药品标准中,采用高效液相色谱法检测丹莪妇康煎膏中三七皂苷R
因此,需要对丹莪妇康煎膏供试品溶液的制备方法和检测的色谱条件进行优化,建立一个准确、稳定、易操作的检测丹莪妇康煎膏中三七含量的方法。
发明内容
本发明的目的在于提供一种丹莪妇康煎膏中三七含量的检测方法,以解决现有技术中存在的供试品溶液的制备方法过于复杂,耗时耗力;检测目标峰不能完全分离,分析时间较长的问题。
本发明为解决上述技术问题采用的技术方案是提供了丹莪妇康煎膏中三七含量的检测方法。该检测方法为:以水作为溶剂制备供试品溶液,注入超高效液相色谱仪测定含量;色谱条件为:以十八烷基硅烷键合硅胶为填充剂;以乙腈和水为流动相进行梯度洗脱;检测波长为203nm,柱温为20~35℃;流速为0.4~0.6mL/min;理论塔板数按人参皂苷Rb1峰计算应不低于700000。
其中,上述丹莪妇康煎膏中三七含量的检测方法中,所述供试品溶液的制备是取丹莪妇康煎膏2~5g置于50mL容量瓶中,加水超声30~90分钟后,再加入水定容,摇匀,滤过。
优选地,取丹莪妇康煎膏2g置于50mL容量瓶中,加水超声30分钟后,再加入水定容,摇匀,滤过。
为了使供试品的制备方法更加简便、省时,同时能保证丹莪妇康煎膏中三七的有效成分有效提取,发明人通过大量试验研究,发现采用水作为溶剂结合超声处理,可以在短时间内将三七中的有效成分提取出来,并且,以水作为溶剂,既可以减少有机溶剂的污染及对人体健康的危害,又可以节约成本,简化步骤。
进一步地,所述超声的功率为480~520W;超声的频率为35~45kHz。
优选地,所述超声的功率为500W;超声的频率为40Hz。
进一步地,以乙腈和水为流动相的梯度洗脱条件为:
时间为0~11min,流动相乙腈为16%,流动相水为84%;
时间为11~15min,流动相乙腈为16~21%,流动相水为84~79%;
时间为15~24min,流动相乙腈为21~31%,流动相水为79~69%;
时间为24~26min,流动相乙腈为31~40%,流动相水为69~60%;
时间为26~29min,流动相乙腈为40%,流动相水为60%;
时间为29~30min,流动相乙腈为40~16%,流动相水为60~84%;
时间为30~33min,流动相乙腈为16%,流动相水为84%。
发明人考察了多种流动相梯度洗脱条件,发现在本发明所述的梯度洗脱的条件下,三七皂苷R
进一步地,柱温为25℃;流速为0.4mL/min。
本发明的有益效果是:
本发明方法采用超高效液相色谱仪,通过优化供试品的制备方法和检测色谱条件测定丹莪妇康煎膏中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量,具有良好的线性、重复性、稳定性和回收率,能很好的控制丹莪妇康煎膏的质量。本发明方法简化了供试品的制备工序,采用水作为溶剂结合超声处理,可以在短时间内将三七中的有效成分提取出来,省时省力,并且更加环保,节约成本;本发明方法优化了流动相洗脱程序,既能使目标峰完全分离,又节约了分析时间。
附图说明
图1为实施例1测得的丹莪妇康煎膏中三七皂苷R
图2为对比例1测得的丹莪妇康煎膏中三七皂苷R
图3为对比例1测得的丹莪妇康煎膏中人参皂苷Rg
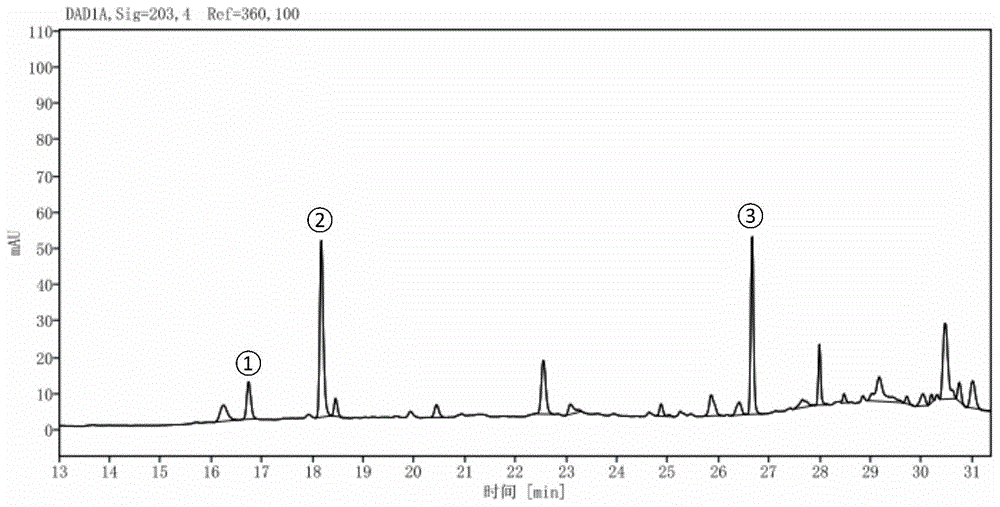
图4为对比例2测得的三七皂苷混合对照品的色谱图(①为三七皂苷R
图5为对比例2测得丹莪妇康煎膏样品中三七皂苷R
图6为不同流动相分离三七皂苷R
图7为不同柱温分离三七皂苷R
图8为线性关系考察三七皂苷R
图9为线性关系考察三七皂苷Rg
图10为线性关系考察三七皂苷Rb
图11为专属性考察测得的色谱图(由上至下分别为丹莪妇康煎膏阴性样品(缺三七)、丹莪妇康煎膏样品、三七皂苷混合对照品)。
具体实施方式
下面将通过具体的实施例对本发明作进一步地详细阐述。
实施例1
对照品溶液的制备:精密称取三七皂苷R
供试品溶液的制备:取丹莪妇康煎膏2g,精密称定,置50mL量瓶中,加水适量,密塞,超声处理30分钟,超声功率为500W,超声频率为40kHz,取出,放冷至室温,加水定容至刻度,摇匀,滤过,取续滤液即得。
色谱条件及系统适用性试验:以十八烷基硅烷键合硅胶为填充剂(2.1×100m,1.9μm);以乙腈和水为流动相,按表1进行梯度洗脱;检测波长为203nm,柱温为25℃。理论塔板数按人参皂苷Rb1峰计算应不低于700000。
测定法:分别精密吸取对照品溶液与供试品溶液各2μL,注入超高效液相色谱仪,测定,即得。结果见图1。
本品每1g含三七以三七皂苷R
表1实施例1采用的流动相梯度条件
对比例1采用国家药品标准WS-10227(ZD-0227)2002-2012Z-2016方法检测
对照品溶液的制备:精密称取人参皂苷Rg
供试品溶液的制备:取本品7.5g,精密称定,置100mL量瓶中,加入甲醇约90mL,超声处理(功率500W,频率59kHz)30分钟,静置过夜,超声处理(功率500W,频率59kHz)10分钟,放冷,用甲醇稀释至刻度,摇匀,滤过,精密量取续滤液50mL,置100mL量瓶中,加入5%醋酸铅溶液40mL超声处理(功率500W,频率59kHz)20分钟,放冷,用水稀释至刻度,摇匀,滤过,精密量取续滤液40mL,蒸干,加水25mL使溶解,转移至分液漏斗中,用三氯甲烷洗涤3次,每次25mL,弃去三氯甲烷液,水液用水饱和的正丁醇振摇提取5次(30mL、25mL、15mL、15mL、15mL),合并正丁醇液,浓缩约至25mL,转移至分液漏斗中,趁热用氨试液洗涤2次,每次25mL,弃去氨液,正丁醇液蒸干,残渣加甲醇使溶解,转移至10mL量瓶中,并加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
色谱条件及系统适用性试验:以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以0.45%磷酸二氢钠溶液为流动相B,按表2中规定的梯度进行洗脱,检测波长为203nm。理论板数按人参皂苷Rg1峰计算应不低于10000。
分别精密吸取对照品溶液与供试品溶液各5μL,注入液相色谱仪进行测定。
表2对比例1采用的流动相梯度条件
对比例2
采用本发明实施例1制备的供试品溶液和对照品溶液按照如下条件进行检测:
色谱柱(Ultimate XB-C18柱,2.1mm×50.0mm,1.8μm);检测波长为203nm;柱温25℃;流速0.6mL/min;进样量2μL;以水和乙腈为流动相按表3中的规定进行梯度洗脱。测得三七皂苷混合对照品和丹莪妇康煎膏供试品的色谱图见图3和图4。
表3对比例2采用的流动相梯度条件
试验例1色谱条件的选择
1.1流动相的选择
分别以乙腈-0.1%的磷酸溶液和乙腈-水为流动相,按照本发明流动相梯度条件进行考察,试验结果表明,采用乙腈-水作为流动相能使各目标峰分离完全,无干扰,故流动相选择乙腈-水。见图5。
1.2柱温的选择
考察了20℃、25℃、30℃、35℃不同柱温,结果在柱温25℃条件下分离最佳,各目标峰与邻峰能达到完全分离,故柱温选择25℃。见图6。
1.3提取方法的选择
取6份丹莪妇康煎膏,每份精密称取2g,其中3份置50mL容量瓶中,加水适量,密塞,超声处理(功率500W,频率40KHz)提取60分钟,取出,放冷至室温,加水定容至刻度,摇匀;另取3份置具塞锥形瓶中,精密加入50mL水,称定重量,加热回流提取60分钟,取出,放冷,称重,用水补足减失的重量,摇匀。将两种提取样品滤过,取续滤液测定,结果见表4。
表4提取方法考察(n=3)
结果表明,采用超声提取方法提取效率较高,并且超声处理方法更简便,故选择超声(功率500W,频率40KHz)作为本品的提取方法。
试验例2方法学验证
制备对照品溶液:称取三七皂苷R
2.1系统适用性试验
取混合对照品溶液注入超高效液相色谱仪,连续进样5针,记录峰面积,计算RSD值,结果见表5,进样精密度较好,人参皂苷Rb
表5进样精密度考察结果(n=5)
2.2线性
对照品贮备液的制备:取三七皂苷R
精密量取以上三种对照品溶液各2mL,置10mL量瓶中,加甲醇稀释至刻度,摇匀,即得三七皂苷混合对照品贮备液。
分别精密量取三七皂苷混合对照品贮备液1mL、1mL、1mL、1mL、2mL,分别置于100mL、50mL、10mL、5mL、5mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,分别吸取甲醇(空白)和上述对照品溶液2μL注入超高效液相色谱仪,记录色谱图,测定峰面积,以对照品浓度作为横坐标,峰面积作为纵坐标,绘制各对照品标准曲线,并计算线性回归方程、相关系数及线性范围。结果见表6、表7、表8和图7、图8、图9。
表6三七皂苷R
线性回归方程为:y=1621.7x+0.7261,相关系数r=0.99991。
表7人参皂苷Rg
线性回归方程为:y=1928.9x+2.2495,相关系数r=0.99990。
表8人参皂苷Rb
线性回归方程为:y=1293.9x+1.5639,相关系数r=0.99991。
试验结果表明,在浓度为0~0.2152mg/mL范围内,进样量为2μL时,三七皂苷R
2.3专属性考察
取本品阴性样品(缺三七)按照供试品溶液的制备方法制备阴性样品溶液并测定,结果在与对照品色谱峰相应保留时间位置,无干扰峰,表明本发明方法专属性较好。见图10。
2.4供试品溶液稳定性
取本品按照供试品溶液制备方法制备样品,分别在0h、4h、8h、12h、16h、20h、24h、36h测定,计算三七皂苷总量及RSD值,结果见表9。结果表明供试品溶液在36h内较为稳定。
表9供试品溶液稳定性考察
2.5重复性
取本品分别制备6份供试品溶液,按本发明方法测定,计算三七皂苷总量及RSD值,结果见表10。结果表明本发明方法重复性较好。
表10供试品溶液稳定性考察(n=6)
2.6回收率
取本品1g(共6份),精密称定,分别置50mL量瓶中,加入三七皂苷R
表11三七皂苷R
/>
表12人参皂苷Rg
表13人参皂苷Rb
2.7中间精密度考察
考察不同分析人员在不同时间,采用不同仪器对同一供试品进行测定。结果见表14,含量结果无明显差异,表明本发明方法中间精密度较好。
表14中间精密度结果
2.8含量限度
按照本发明方法,对19批丹莪妇康煎膏成品进行测定,结果三七皂苷R
表15 19批丹莪妇康煎膏三七皂苷含量测定结果(n=3)
试验结果表明,本发明采用超高效液相色谱仪,通过优化供试品的制备方法和检测色谱条件测定丹莪妇康煎膏中三七的含量,能够很好地将三七皂苷R
- 丹莪妇康煎膏的特征图谱建立和检测方法
- 丹莪妇康煎膏的指纹图谱建立方法及其标准指纹图谱和应用
