一种基于微生物矿化技术的包膜型缓释材料、及其制备方法
文献发布时间:2024-01-17 01:26:37
技术领域
本发明属于重金属污染治理技术领域,具体来讲,涉及一种能够实现尿素缓释的基于微生物矿化技术的包膜型缓释材料及其制备方法。
背景技术
微生物矿化是自然界中普遍存在的一种现象,是指某些微生物能够利用自身的新陈代谢活动生成多种矿物结晶的过程。微生物矿化技术由于其过程中无需添加大剂量的沉淀剂,同时伴有生物体代谢、细胞、有机质的参与,和传统化学胶结矿化技术相比,其具有绿色无污染、生态相容性好等优点。
随着微生物矿化技术的兴起,近年来该技术已被提出应用于处理重金属污染废水,称为微生物诱导碳酸钙沉淀技术(MICP)。该技术是指在微生物参与下,重金属离子从环境中选择性地沉淀在特定有机质上,在生物大分子的调控和诱导作用下,形成矿物的过程。该过程依靠胞外聚合物(EPS)与金属离子之间的静电作用,将金属离子固定,并最终在生物控制、影响下完成重金属离子向固相矿物的转变。如目前有相关研究中报道了利用一种产脲酶菌(巴氏芽孢八叠球菌)来分解尿素产生碳酸根,通过产生的碳酸根与重金属离子形成不可溶的碳酸盐沉淀,从而达到去除中金属的效果。
以往MICP技术应用固定重金属过程中,选取MICP所需的微生物菌种进行活性培养;将菌液与胶结液(由氯化钙和尿素组成)均匀混合,将其作用在待处理的重金属污水中,检测去除重金属效果。但是,当前这种MICP技术通常是基于过量尿素溶解在污水中,这就会导致在将菌种与尿素混合物添加到待处理污水之前,尿素在脲酶作用下已经开始提前水解,造成固定重金属效果变低,也即存在尿素过度浪费、尿素在环境中被提前水解的问题。
发明内容
为了解决目前MICP技术应用于水体中重金属污染治理时所存在的尿素因直接投放污水而提前分解、造成过度浪费的问题,本发明的发明人在对MICP技术长期研究的基础之上对该类材料的结构进行了改进,提供了一种包膜型缓释材料。该包膜型缓释材料能够在重金属污水中应用时才缓释出尿素,避免直接投放尿素而造成的尿素提前水解的问题,避免尿素浪费,提升治理效率。
具体地,本发明提供了下述技术方案:
一种基于微生物矿化技术的包膜型缓释材料,其包括以尿素颗粒为材料的芯部、包覆在该芯部外表的以脲酶微生物-多糖聚合物复合物为材料的内包膜层、以及包覆在该内包膜层外表的以碳酸钙为材料的外包膜层。
具体地,在该包膜型缓释材料中,芯部材料除了尿素颗粒外,会存在少许因尿素与脲酶微生物接触而被分解产生的碳酸根,但是,因该部分结构几乎为无水环境,上述因二者接触而被分解的尿素的量是极少的。
与此同时,作为外包膜层的材料的碳酸钙,也主要是由上述因部分尿素被分解产生的碳酸根而形成的,该形成的碳酸钙即以包覆有芯部的内包膜层颗粒物作为成核位点,而覆盖沉积在该内包膜层外表,形成了外包膜层。
如此,易于分解的尿素颗粒即被双层包膜包覆在内部,即便与具有脲酶微生物的内包膜层相接触,几乎无水的环境也不会导致其过早被大量分解;同时最外层通过致密坚硬的碳酸钙外包膜层进行包覆,可以使MICP技术中发挥作用的几种有效成分(尿素、脲酶微生物)均保持原始状态而不被分解。而当该包膜型缓释材料应用至含有重金属的污水中时,通常呈酸性的重金属污水可破坏上述外包膜层的碳酸钙结构,而将内部的尿素颗粒及脲酶微生物进行缓慢释放。此时,脲酶微生物代谢产生脲酶,而尿素在水性环境中即在脲酶的作用下首先水解成氨及氨基甲酸,氨基甲酸再自发水解成氨及碳酸,污水中的重金属离子与尿素水解后产生的碳酸根离子反应生成碳酸盐沉淀,从而降低重金属离子的迁移性,完成重金属固定过程。
进一步地,上述尿素颗粒呈粒径为2mm~5mm的球状。
进一步地,上述脲酶微生物是具有高脲酶活性的巴氏芽孢杆菌,当然,也可以是任意目前已知可应用至MICP技术中的其他脲酶微生物;上述多糖聚合物选自海藻酸钠、纳米纤维素、琼脂、黄原胶中的至少一种。
进一步地,在上述包膜型缓释材料中,芯材的质量占比为80%~95%,而内包膜层和外包膜层的总质量占比为5%~20%。
本发明提供的上述包膜型缓释材料,采用下述方法来制备获得:
步骤S1、将脲酶微生物溶液加入多糖聚合物溶液中,制备脲酶微生物-多糖聚合物混合液;
步骤S2、将尿素颗粒和脲酶微生物-多糖聚合物混合液进行包衣处理,并进行干燥,形成由以尿素颗粒为材料的芯材、和包覆在芯材外表面的以脲酶微生物-多糖聚合物复合物为材料的内包膜层组成的单层包膜中间体;
步骤S3、将上述单层包膜中间体置于含钙矿化液中进行矿化反应,在内包膜层的外表面形成以碳酸钙为材料的外包膜层,获得包膜型缓释材料。
具体地,在上述步骤S1中,脲酶微生物溶液与多糖聚合物溶液的体积比为1:20~20:1。
进一步地,脲酶微生物溶液的脲酶活性为2U/mL~20U/mL(1U表示1min内该溶液中脲酶分解尿素释放的氨基氮的量)。
具体地,在上述步骤S2中,可基于包衣机并采用下述方式来进行包衣处理:选用工业用球状颗粒尿素置于包衣机的包衣锅中,将脲酶微生物-多糖聚合物混合液置于包衣机的加料桶中,打开喷枪喷射脲酶微生物-多糖聚合物混合液,当球状尿素表面附着一层溶胶状液体时,停止喷射直至球状尿素表面干燥为止,即获得上述单层包膜中间体。
进一步地,在上述步骤S2中,尿素颗粒与脲酶微生物-多糖聚合物混合液的用量比例为每kg尿素颗粒对应100mL~300mL脲酶微生物-多糖聚合物混合液。
具体地,在上述步骤S3形成外包膜层的过程中,一方面,将上述单层包膜中间体放置于含钙矿化液中进行矿化反应,含钙矿化液中含有的钙离子同包衣(即内包膜层)中的多糖聚合物发生交联反应,形成凝胶将脲酶微生物固定在包衣中,防止流失;另一方面,包衣中含有的脲酶微生物产生的具有脲酶活性的脲酶菌水解芯部的尿素产生碳酸根,同含钙矿化液中的钙离子反应形成不溶的碳酸钙附着在该单层薄膜中间体外表,形成外包膜层。
进一步地,上述含钙矿化液可以是氯化钙溶液、硝酸钙溶液、醋酸钙溶液等水溶性含钙溶液中的任意一种、或至少两种的混合液;其中,钙离子的浓度为0.1mol/L~2mol/L。
进一步地,上述含钙矿化液的用量为其与尿素颗粒的体积之比为1:1~10:1。
本发明通过简单的包衣技术,即实现了对尿素颗粒的第一次包覆,并借助第一次包覆过程中生成的碳酸根进行矿化处理,即实现了第二次包覆,仅在将获得的包膜型缓释材料应用至酸性含重金属污水中时,才得以破坏包膜层而缓释其内部的尿素,继而发生微生物诱导碳酸钙沉淀反应,而避免现有技术中直投的尿素颗粒被过早分解而造成浪费。
另外,上述第二次包覆形成的以碳酸钙为材料的外包膜层还对其内部的脲酶微生物起到保护作用,防止其在应用过程中直接与酸性的重金属污水接触而活性降低。而外包膜层在逐渐被溶解的过程中,也调整了重金属污水的pH,降低了酸度,不仅起到缓释尿素的作用,而且也保护了脲酶微生物。
具有上述结构的新型包膜型缓释材料结构新颖、应用性能好;且上述制备方法简单,易于制备,保证了该包膜型缓释材料能够以较低成本来制备,具有很好的应用价值和使用前景。
附图说明
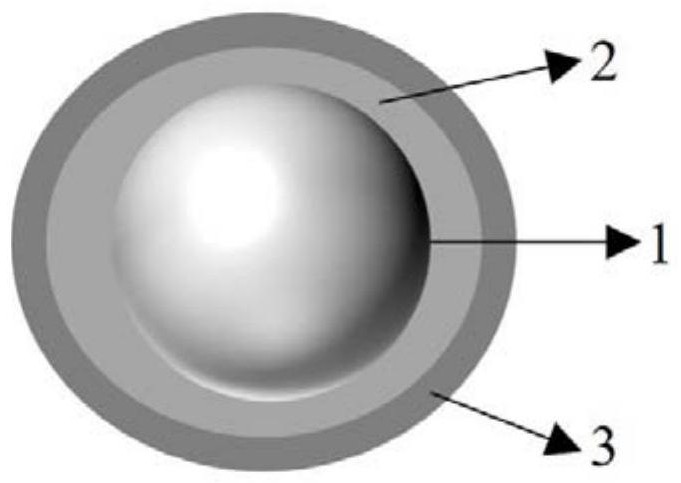
图1是根据本发明的实施例1的包膜型缓释材料的结构示意图;
图2是根据本发明的实施例1的包膜型缓释材料的SEM图片;
图3是根据本发明的实施例1的包膜型缓释材料的XRD图片;
图4是根据本发明的实施例及对比例提供的各材料的固定重金属去除率对比图。
具体实施方式
下面将结合实施例对本发明加以详细说明,需要指出的是,所描述的实施例仅旨在于对本发明的理解,而对其不起任何限制作用。
本发明下述各实施例中采用的脲酶微生物具体为巴氏芽孢杆菌,为市售巴氏芽孢杆菌ATCC11859,为本领域常规菌株。
巴氏芽孢杆菌菌液是通过如下方法获得的:将巴氏芽孢杆菌接种于培养基中,28℃条件下振荡培养2d,培养完成后使用分光光度计测量菌液吸光值,通过离心浓缩或加入生理盐水调节菌液浓度至OD
其中,培养基配方为:将20g酵母粉、15g NH
当然,上述脲酶微生物可以是其他本领域常规的任意可产脲酶的微生物,并不限制于此。
实施例1
本实施例提供了一种包膜型缓释材料,其具有如图1所示的结构。
如图1所示,该包膜型缓释材料以粒径为4mm左右的尿素颗粒为芯材1,其外表包覆有一层以巴氏芽孢杆菌-海藻酸钠为材料的内包膜层2,最外表又包覆有一层以碳酸钙为材料的外包膜层3。
本实施例提供的上述包膜型缓释材料,其通过下述方法制备获得:
首先,将高脲酶活性的巴氏芽孢杆菌溶液加入至海藻酸钠溶液中,制备巴氏芽孢杆菌-海藻酸钠溶液。
具体地,该巴氏芽孢杆菌-海藻酸钠溶液中,巴氏芽孢杆菌溶液与海藻酸钠溶液的体积比为1:10;所用的巴氏芽孢杆菌溶液的脲酶活性为10U/mL,海藻酸钠溶液的浓度为5g/L。
其次,选用颗粒直径大小为4mm的工业用球状颗粒尿素做球状尿素包衣,将其置于包衣机的包衣锅中,将已经配制完成的巴氏芽孢杆菌-海藻酸钠溶液置于包衣机的加料桶中,打开喷枪喷射巴氏芽孢杆菌-海藻酸钠溶液,当球状尿素表面附着一层溶胶状液体时,停止喷射直至球状尿素表面干燥为止,获得单层包膜中间体。
具体地,利用2mL该巴氏芽孢杆菌-海藻酸钠溶液和10g尿素来制备该包膜型缓释材料,也即控制巴氏芽孢杆菌-海藻酸钠溶液的用量为200mL/kg尿素。
最后,将单层包膜中间体放置于1mol/L氯化钙溶液中进行矿化反应,在单层包膜中间体的表面上沉积碳酸钙作为外包膜层,获得包膜型缓释材料。
对本实施例获得的包膜型缓释材料分别进行了SEM测试和XRD测试,其SEM图片和XRD结果分别如图2和图3所示。
结合图2和图3的结果,可以看出,该包膜型缓释材料的最外表层是致密的碳酸钙层。
实施例2
在本实施例中,其提供的包膜型缓释材料的结构在此不再赘述,其具有与实施例1中包膜型缓释材料相似的结构。
以下对本实施例的包膜型缓释材料的制备方法进行说明,其与实施例1中的制备方法的相同之处在此不再赘述,仅描述与实施例1中的制备方法的不同之处。
本实施例的制备方法与实施例1的制备方法的不同之处在于,在步骤一中,在巴氏芽孢杆菌-琼脂溶液中,巴氏芽孢杆菌溶液与琼脂溶液的体积比为1:20;所用的巴氏芽孢杆菌溶液的脲酶活性为2U/mL,琼脂溶液的浓度为0.1g/L。
在步骤二中,利用1mL该巴氏芽孢杆菌-琼脂溶液和10g尿素来制备该包膜型缓释材料,也即控制巴氏芽孢杆菌-琼脂溶液的用量为100mL/kg尿素。
在步骤三中,含钙矿化液具体为0.1mol/L氯化钙溶液。
实施例3
在本实施例中,其提供的包膜型缓释材料的结构在此不再赘述,其具有与实施例1中包膜型缓释材料相似的结构。
以下对本实施例的包膜型缓释材料的制备方法进行说明,其与实施例1中的制备方法的相同之处在此不再赘述,仅描述与实施例1中的制备方法的不同之处。
本实施例的制备方法与实施例1的制备方法的不同之处在于,在步骤一中,在巴氏芽孢杆菌-黄原胶溶液中,巴氏芽孢杆菌溶液与黄原胶溶液的体积比为20:1;所用的巴氏芽孢杆菌溶液的脲酶活性为20U/mL,黄原胶溶液的浓度为5g/L。
在步骤二中,利用3mL该巴氏芽孢杆菌-黄原胶溶液和10g尿素来制备该包膜型缓释材料,也即控制巴氏芽孢杆菌-黄原胶溶液的用量为300mL/kg尿素。所使用的尿素颗粒的粒径为5mm左右。
在步骤三中,含钙矿化液具体为2mol/L醋酸钙溶液。
为了体现本发明上述包膜型缓释材料结构对其性能的必要性,进行了下述诸多对比实验。
对比例1
本对比例的目的在于体现以碳酸钙为材料的外包膜层对尿素保护及缓释的重要性,为此,提供了下述第一对比包膜型缓释材料。
在本对比例的该第一对比包膜型缓释材料的制备过程中,与实施例1的相同之处在此不再赘述,只描述与实施例1中的不同之处。本对比例与实施例1中制备方法的不同之处在于,缺少其第三步对单层包膜中间体进行矿化反应从而形成外包膜层的步骤;也即,第二步获得的单层薄膜中间体即为该第一对比包膜型缓释材料。
对比例2
本对比例的目的在于体现含有脲酶微生物的内包膜层对应用效果的重要性,为此,提供了下述第二对比包膜型缓释材料。
在本对比例的该第二对比包膜型缓释材料的制备过程中,与实施例1的相同之处在此不再赘述,只描述与实施例1中的不同之处。本对比例与实施例1中制备方法的不同之处在于,缺少第一步中巴氏芽孢杆菌-海藻酸钠溶液的配制,第二步中仅以海藻酸钠溶液加入至包衣机的加料桶中并对尿素颗粒进行喷射包衣处理;也即,第二步获得的单层薄膜中间体中,内包膜层的材料相较实施例1缺少脲酶微生物。
需要说明的是,在本对比例中,虽然内包膜层的材料中缺少了脲酶微生物,但尿素颗粒仍可通过在少水环境中的水解而产生部分碳酸根,从而在第三步中发生矿化而形成以碳酸钙为材料的外包膜层。
对比例3
本对比例仅提供一种与实施例1中巴氏芽孢杆菌-海藻酸钠溶液相同的胶凝材料作为第三对比材料。
对比例4
本对比例仅提供一种与实施例1中巴氏芽孢杆菌溶液相同的液体作为第四对比材料。
为了验证上述各材料的应用效果,将各材料应用至10L含Cd
实施例和对比例提供的各材料设置三组平行样品,检测结果取平均值。
需要说明的是,在对上述各对比例提供的材料进行测试时,为了保持其与实施例结构中涉及的有效材料一致,采用外加的方式补齐其本身材料缺少的等量有效组分。如对比例2提供的第二对比包膜型缓释材料缺少脲酶微生物,那么将与实施例1中制备时等量的巴氏芽孢杆菌直接投放至上述重金属污水中;同样,对比例3的材料测试中直接投放了等量的尿素,而对比例4的材料测试中直接投放了等量的尿素和海藻酸钠。
各实施例及对比例提供的材料的去除重金属Cd
从图4中可以看出,实施例提供的各包膜型缓释材料均具有良好的重金属Cd
- 一种高肥效缓释型生态水泥材料的制备方法
- 一种高含蜡高温高矿化油井微生物清防蜡剂及其制备方法
- 利用微生物矿化制备不同晶型碳酸钙的方法
- 一种包膜缓释材料及其制备方法和由其制得的包膜缓释肥
- 一种疏水性材料包膜的环境友好型包膜缓释肥及其制备方法
