一种犬八联抗体快速检测卡及试剂盒
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于抗体检测技术领域,尤其涉及一种犬八联抗体快速检测卡及试剂盒。
背景技术
抗体是机体由于抗原(如细菌、病毒等)刺激而产生的具有保护作用的蛋白质,对抗病原的并不是疫苗本身,而是疫苗刺激机体产生的抗体。抗体能够帮助机体清除细菌、病毒和抵抗疾病,但是抗体必须达到一定的量才有足够的保护力。从疫苗的注射到抗体的产生是一个复杂的生理过程,打了疫苗并不意味着免疫成功,所以需要通过检测抗体来判断免疫是否成功。
临床上,免疫失败的情况时有发生,常见的原因有:①母源抗体过高,中和了疫苗抗原;②疫苗本身原因,任何疫苗都无法达到100%的免疫效果,再者疫苗批间稳定性、冷链异常对疫苗品质的影响无法用肉眼辨别;③在非健康状态下接种,比如常见的营养不良,感染疾病或者使用免疫抑制性药物等;④免疫诱导期内发生感染,比如在疫苗注射后产生保护力之前感染,仍可能导致疾病爆发;⑤免疫系统问题,天生免疫系统缺陷,或感染了猫艾滋、猫白血病等免疫抑制性疾病,免疫系统无法发挥正常作用;⑥遗传因素,有研究表明,博美、雪纳瑞、藏獒、罗威纳等个别犬种对疫苗的免疫反应较弱,免疫失败的机率较高。所以,通过抗体检测来判断免疫是否成功就显得尤为重要。
抗体检测的应用场景主要包含以下几个方面:①新宠到家。幼宠首次免疫前检测母源抗体,若母源抗体过高则不能立即进行免疫,需等母源抗体降到一个很低的浓度后再行免疫。研究表明,犬母源抗体代谢周期为8周,猫为12周甚至更长。②爱宠免疫完2~3周后,及时检测抗体水平,明确疫苗的免疫效果。如果抗体滴度不够,则需加强免疫或更换疫苗免疫。③爱宠首次免疫接种超过6针抗体仍不达标的,建议不再免疫,避免出现免疫麻痹。④爱宠每年加强免疫前测抗体,如果抗体滴度足够即可跳过此次加强周期,降低疫苗副反应对爱宠的应激及注射部位肉瘤等疾病发生率。⑤对于领养或抱养宠物,如其免疫史未知,需通过抗体检测确认免疫效果。⑥对于寄养、旅游外出、住院治疗的宠物,需综合评估爱宠的免疫机能,减少感染风险。⑦当进行非紧急性手术(如绝育),可以先补免,待抗体足量后再安排手术。
目前确定接种犬疫苗后产生的犬抗体的方法,常见的有酶联免疫吸附实验、荧光定量免疫层析实验、胶体金或乳胶免疫层析实验等。市面上犬的抗体检测产品,常见有犬二联(犬瘟/犬细小)抗体检测、犬三联(犬瘟/犬细小/犬传染性肝炎)抗体检测、犬三联(犬瘟/犬细小/犬腺病毒)抗体检测、狂犬抗体检测,但是针对接种率比较高的梅里亚六联(犬瘟热、犬细小、犬副流感、犬钩端螺旋体、犬腺病毒)疫苗或者卫佳捌联(犬瘟热、犬腺病毒2型、犬副流感、犬细小、犬钩端螺旋体、犬冠状病毒)疫苗的免疫效果,市面上缺乏一个全面的检测试剂进行有效评估,普遍表现在检测指标过于单一,如仅仅只检测人畜共患的犬钩端螺旋体抗体或只检测犬冠状抗体,或表现在检测手段过于复杂,需要配备专门的仪器设备。
目前市面上的产品常只针对1-3个具体指标检测,想要得到一个全面的评估结果,常常面临操作麻烦和体验感差的问题,主要表现在:不同厂家的产品在检测同一份样本时,不同指标呈现的结果不同;不同厂家的产品对样本要求不同,部分取全血即可测试,部分需要血清血浆才能检测,部分因其只能适配某种特定抗凝剂,甚至需要要求制备血浆的抗凝管;因此,常常导致临床检测中重复多次取样,采用多种抗凝管盛样,效率低下、操作繁琐,容易出错。
开发一款能同时检测犬瘟热、犬腺病毒、犬传染性肝炎、犬副流感、犬细小病毒、犬钩端螺旋体、黄疸出血型钩端螺旋体和犬冠状病毒抗体的检测试剂,可以全面获知不同项目抗体水平,特别是大家关注的人畜共患的犬钩端螺旋体和致死率高的黄疸型钩端螺旋体,如果再配上简单的操作程序以及对检测结果的快捷直观地读取,必将能快速解决临床痛点,做到精准防控,避免常见传染病或寄生虫的感染,有着巨大的临床应用价值。
发明内容
本发明的第一个目的是针对现有技术的不足,提供一种犬八联抗体快速检测卡,该卡检测指标覆盖了全部的疫苗项目,特别涵盖了人畜共患的犬钩端螺旋体和致死率高的黄疸型钩端螺旋体,上样量少,一次取样即可同时获得8个指标总抗体检测结果,无需配备读卡机器,操作简单便捷,结果获取快速有效,能有效降低检测成本,同时较低的取样量能减少被测宠物伤害,可静脉采血也可牙龈取血,满足宠物医院和居家自测等多种临床场景的使用,具有广阔的应用前景。
为了实现上述目的,本发明采用以下技术方案:
一种犬八联抗体快速检测卡,包括犬瘟(CDV)+犬腺病毒(CAV-II)二合一试剂条、犬传染性肝炎(CAV-I)+犬副流感(CPIV)二合一试剂条、犬细小(CPV)+犬钩端螺旋体(cLep)二合一试剂条和黄疸出血型钩端螺旋体(JLep)+犬冠状(CCV)二合一试剂条;
所述犬瘟(CDV)+犬腺病毒(CAV-II)二合一试剂条包括样品垫、乳胶垫和硝酸纤维素膜;所述样品垫经处理液1处理,所述处理液1组分包括30-50g/L硼砂、5-15g/L PVP-10、5-15ml/L Tween20、5-15g/L EDTA和20-30ml/L抗RBC抗体;所述乳胶垫上包被有兔IgG、犬瘟抗原和犬腺病毒抗原的红乳胶标记物;
所述犬传染性肝炎(CAV-I)+犬副流感(CPIV)二合一试剂条包括样品垫、乳胶垫和硝酸纤维素膜;所述样品垫经处理液2处理,所述处理液2组分包括0.5-1L/L Tris-Casein-PVP10母液、0.5-1.5g/L无水碳酸钠、5-15g/L TritonX-405和20-30ml/L抗RBC抗体;所述乳胶垫上包被有鼠IgG、犬传染性肝炎抗原和犬副流感抗原的红乳胶标记物;
所述犬细小(CPV)+犬钩端螺旋体(cLep)二合一试剂条包括样品垫、乳胶垫和硝酸纤维素膜;所述样品垫经处理液3处理,所述处理液3组分包括5-15g/L季酮酸、40-60ml/L抗RBC抗体、5-15g/L Tris、5-15g/L Casein、5-15g/L PVP-10和0.02%Proclin300;所述乳胶垫上包被有鼠IgG、犬细小抗原和犬钩端螺旋体抗原的蓝乳胶标记混合物。
所述黄疸出血型钩端螺旋体(JLep)+犬冠状(CCV)二合一试剂条包括样品垫、乳胶垫和硝酸纤维素膜;所述样品垫经处理液4处理,所述处理液4组分包括10-20g/L Tris、5-15g/LBSA、5-15g/LPVP-10、5-15g/L季酮酸、10-20g/L Casein、5-15g/L Tween20和0.02%Proclin 300;所述乳胶垫上包被有兔IgG、黄疸出血型钩端螺旋体抗原、犬冠状抗原的蓝乳胶标记混合物。
作为优选,所述犬瘟(CDV)+犬腺病毒(CAV-II)二合一试剂条的硝酸纤维素膜上包被羊抗兔IgG、犬瘟抗原和犬腺病毒抗原,形成质控线C1和两条检测线T2、T1;
所述犬传染性肝炎(CAV-I)+犬副流感(CPIV)二合一试剂条的硝酸纤维素膜上依次包被有羊抗鼠IgG、犬传染性肝炎抗原和犬副流感抗原,形成质控线C2和两条检测线T4、T3;
所述犬细小(CPV)+犬钩端螺旋体(cLep)二合一试剂条的硝酸纤维素膜上依次包被有羊抗鼠IgG、犬细小抗原和犬钩端螺旋体抗原,形成质控线C3和两条检测线T6、T5;
所述黄疸出血型钩端螺旋体(JLep)+犬冠状(CCV)二合一试剂条的硝酸纤维素膜上依次包被有羊抗兔IgG、黄疸出血型钩端螺旋体抗原、犬冠状抗原,形成质控线C4和两条检测线T8、T7。
作为优选,所述犬瘟(CDV)+犬腺病毒(CAV-II)二合一试剂条、犬传染性肝炎(CAV-I)+犬副流感(CPIV)二合一试剂条、犬细小(CPV)+犬钩端螺旋体(cLep)二合一试剂条和黄疸出血型钩端螺旋体(JLep)+犬冠状(CCV)二合一试剂条均还包括吸水垫和底板;底板的中间位置粘贴硝酸纤维素膜,上方粘贴吸水垫,下方粘贴乳胶垫和样品垫。
作为优选,所述底板为PVC底板。
本发明的第二个目的是提供一种犬八联抗体快速检测试剂盒,包括上述检测卡和缓冲液。
作为优选,所述缓冲液包括浓度为0.5-1.5g/L的NaCl、浓度为2-10g/L的EDTA和体积分数为0.02%的Proclin300,所述缓冲液的pH为10.7±0.2。
本发明采用双抗原夹心法进行半定量抗体检测,配备专门的半定量乳胶比色卡,通过检测线显色的颜色深浅来反应犬体内的抗体水平,结果读取简单易操作。所述试剂条间配备不同配方的溶液处理的玻纤,并有不同的质控系统(兔IgG-羊抗兔IgG;鼠IgG-羊抗鼠IgG),配备不同的乳胶颗粒来显色,来满足多指标产品联合检测的性能要求。
考虑到检测的样本类型为犬血,为了操作的方便性,将8个不同检测指标对应的缓冲液优化为同一种配方,期间需兼顾到不同指标的灵敏度和特异性要求,其开发难度远超于常规的单指标检测产品和三指标检测产品。优化后的缓冲液组分包括0.5-1.5g/L NaCl、2-10g/L EDTA、0.02%Proclin 300,将以上组分混合于水溶液中,调节混合液最终pH为10.7±0.2。缓冲液中氯化钠可提供一个稳定的离子检测环境;EDTA可用于去除重金属离子对酶的抑制作用,提高临床检出率;Proclin 300是一种生物防腐剂,可有效控制试剂中微生物的生长。
本发明具有以下有益效果:
(1)本发明将不同检测指标处理在同一试剂条的不同检测区域,提高了检测的准确性,降低了检测的成本,克服了检测试剂开发的难点,利用不同原料的交叉反应性不同,将无交叉反应性或交叉反应性弱的原料两两组合后处理在试剂条上,同时对处理液1、2、3、4的组分和缓冲液的组分进行了优化创新,不同于市面上产品的单一示踪物标记或单一的C线显色体系或常规的缓冲液pH值7.0-8.0,本发明采用双色示踪物标记,两套C线显色体系,红蓝线双色显色结果,同时调整缓冲液的pH值到一个强碱性范围(10.7±0.2),可以将8个指标性能难统一的问题得到很好的解决,极大地减少了检测时的交叉反应。本发明中的四张试剂条采用同一配方缓冲液进行检测,极大提高了操作的简便性,有较好的用户体验。同时一个试剂条上检测两个生物指标,节省了样本使用量,简化了操作步骤,提升了检测效率。
(2)本发明抗体检测项目全,涵盖了现有的商业化疫苗等常见评价指标,能全面评估疫苗免疫效果;目前针对高端市场,国内外并没有能检测梅里亚六联疫苗和卫佳捌联疫苗的抗体产品,本发明能够很好地填补这一检测试剂的市场空白。
(3)本发明能够同时完成对高度传染性的呼吸道疾病-犬副流感病毒抗体和极其重要的人畜共患的犬钩端螺旋体抗体以及致死率高的黄疸型钩端螺旋体抗体的检测,克服了现有的检测产品无法同时检测这三种抗体的缺陷。
(4)本发明所需上样量少,一次取样即可同时获得8个指标总抗体检测结果,无需配备读卡机器,操作简单便捷,结果获取快速有效,能有效降低检测成本,同时较低的取样量能减少被测宠物伤害。
(5)本发明的检测样本采集可选用静脉采血,也可牙龈取血,满足宠物医院和宠主居家自测等多种临床场景的使用,具有广阔的应用前景。
附图说明
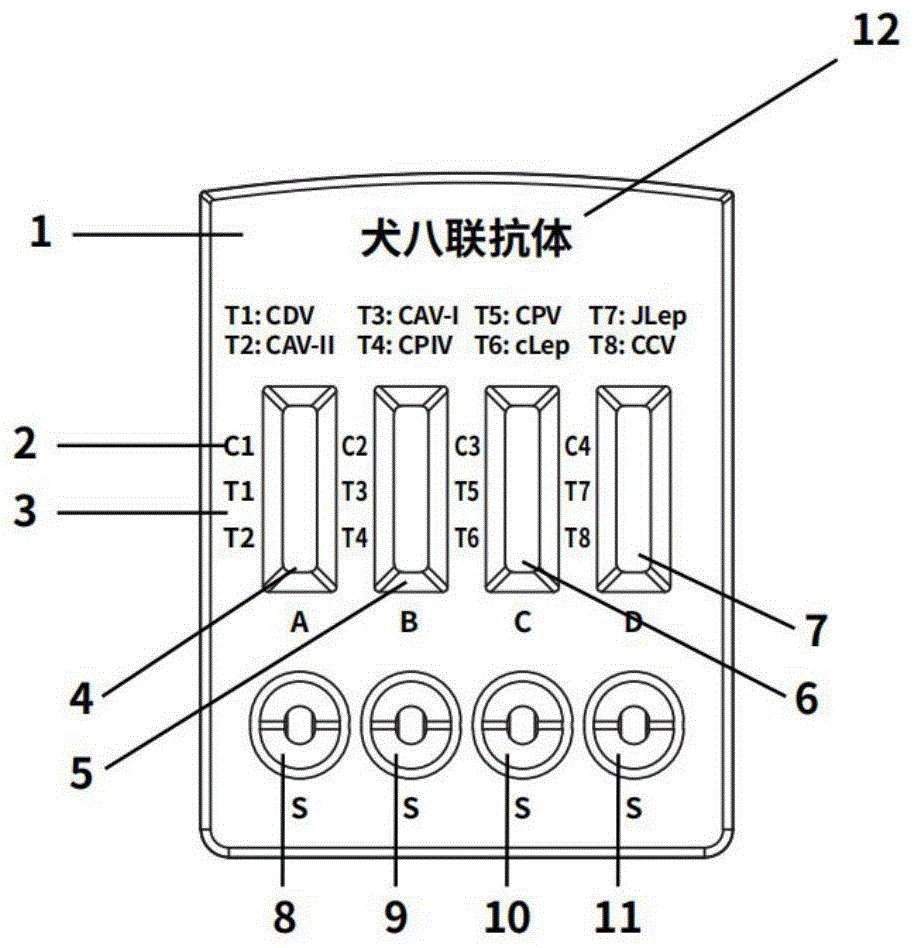
图1为本发明犬八联抗体快速检测卡中上壳结构的俯视图。
图2为本发明犬八联抗体快速检测卡中上壳内侧结构示意图。
图3为本发明犬八联抗体快速检测卡中下壳内侧结构示意图。
图4为本发明犬八联抗体快速检测卡检测过程图。
其中,1-上壳,2-质控线标识,3-检测线标识,4-A窗口(CDV/CAV-II结果读取窗口),5-B窗口(CAV-I/CPIV结果读取窗口),6-C窗口(CPV/cLep结果读取窗口),7-D窗口(JLep/CCV结果读取窗口),8-A窗口对应样品孔S,9-B窗口对应样品孔S,10-C窗口对应样品孔S,11-D窗口对应样品孔S,12-检测指标,13-上下盖卡钉,14-试剂条上卡钉,15-试剂条长挡板,16-试剂条短挡板,17-试剂条下卡钉,18-样品孔S,19-上下盖卡钉扣,20-试剂条上卡槽,21-CDV/CAV-II二合一试剂条,22-CAV-I/CPIV二合一试剂条,23-JLep/CCV二合一试剂条,24-CPV/cLep二合一试剂条,25-试剂条下卡槽,26-试剂条中卡钉,27-下壳。
具体实施方式
下面结合附图与具体实施方法对本发明做进一步的描述。
实施例1
一种犬八联抗体快速检测卡,其结构如图1、图2和图3所示,包括上壳1和下壳27,上壳1和下壳27的材质均为塑料,上壳1和下壳27的边缘结构设有可将上壳1和下壳27结合固定的卡扣结构13、14、17和19。上壳1的上方印刷有检测指标12“犬八联抗体”字样,上壳1的中间部分从左至右依次设有A窗口4、B窗口5和C窗口6和D窗口7,A观察窗口边上印刷有相应的字母C1和检测指标缩写T1(CDV)、T2(CAV-II);B观察窗口边上印刷有相应的字母C2和检测指标缩写T3(CAV-I)、T4(CPIV);C观察窗口边上印刷有相应的字母C3和检测指标缩写T5(CPV)、T6(cLep);D观察窗口边上印刷有相应的字母C4和检测指标缩写T7(JLep)、T8(CCV);在A窗口4、B窗口5、C窗口6和D窗口7的下方分别设有缓冲液孔8、9、10、11。下壳27内侧最上端设有四个试剂条上卡槽20,试剂条上卡槽20从左至右依次固定CDV/CAV-II二合一试剂条21、CAV-I/CPIV二合一试剂条22、CPV/cLep二合一试剂条23、JLep/CCV二合一试剂条24;所述A窗口4与所述CDV/CAV-II二合一试剂条21对应,所述B窗口5与所述CAV-I/CPIV二合一试剂条22对应,所述C窗口6与所述CPV/cLep二合一试剂条23对应,所述D窗口7与所述JLep/CCV二合一试剂条24对应;所述下壳27在各试剂条的两侧设置了1对中卡钉26,各试剂条下端固定在试剂条下卡槽25内,下板上的上下盖卡钉扣19与上板上的卡钉13形成紧配,加上试剂条长挡板15和试剂条短挡板16、试剂条上卡钉14、试剂条下卡钉17共同作用,固定各试剂条。
该犬八联抗体快速检测卡由如下步骤制备得到:
(1)CDV/CAV-II试剂样品垫I制备:取38.1g/L硼砂、10g/L PVP-10、10ml/LTween20、10g/L EDTA、25ml/L抗RBC抗体溶解于纯化水中,调节pH为8.0,喷洒在Millpore8964#玻璃纤维膜上,37℃烘干12-24h制得。
(2)CAV-I/CPIV试剂样品垫II制备:取0.7L/L Tris-Casein-PVP10母液、1.1g/L无水碳酸钠、10g/L TritonX-405、25ml/L抗RBC抗体溶解于纯化水中,调节pH为8.0,喷洒在Millpore 8964#玻璃纤维膜上,37℃烘干12-24h制得。
(3)CPV/cLep试剂样品垫III制备:取10g/L季酮酸、50ml/L抗RBC抗体、6g/L Tris、5g/L Casein、10g/LPVP-10、0.02%Proclin 300溶解于纯化水中,调节pH为8.0,喷洒在Millpore 8964#玻璃纤维膜上,37℃烘干12-24h制得。
(4)JLep/CCV试剂样品垫IIII制备:取12.114g/LTris、10g/LBSA、10g/LPVP-10、8g/L季酮酸、15g/L Casein、5g/L Tween20、0.02%Proclin 300溶解于纯化水中,调节pH为8.0,喷洒在Millpore 8964#玻璃纤维膜上,37℃烘干12-24h制得。
(5)乳胶标记液制备:在pH=6.0的2-(N-吗啉代)乙磺酸溶液中依次加入乳胶微球、10mg/mLNHS、5mg/mLEDC溶液进行微球的活化,20min后置于13000rpm离心机中离心30min,弃上清。加入适量体积的2-(N-吗啉代)乙磺酸,超声混匀,加入适量的原料至0.2mg/ml,在旋转架上反应1.5-2h,再加入适量封闭剂BSA,在旋转架上反应1.0-1.5h。再在13000rpm离心机中离心30min,弃掉上清,加入计划量体积的PBS混匀后,进行超声涡旋混匀;超声完成后,在13000rpm离心机中离心30min,弃上清。再加入计划量体积的pH=8.0Tris,超声混匀后制备得到所需的乳胶标记液。
(6)CDV/CAV-II试剂乳胶垫I制备:取CDV、CAV-II和兔IgG乳胶标记液,原始浓度分别为1.01%、0.98%、1.0%,用含酪蛋白的Tris溶液分别稀释成0.2%、0.22%和0.35%,混匀成一管溶液后,按2.5ul/cm处理在聚酯膜上,37℃干燥12h。
(7)CAV-I/CPIV试剂乳胶垫II制备:取CAV-I、CPIV和鼠IgG乳胶标记液,原始浓度分别为0.98%、0.86%、1.12%,用含酪蛋白的Tris溶液分别稀释成0.22%、0.25%和0.35%,混匀成一管溶液后,按2.5ul/cm处理在聚酯膜上,37℃干燥12h。
(8)CPV/cLep试剂乳胶垫III制备:取CPV、cLep和鼠IgG乳胶标记液,原始浓度分别为1.0%、0.89%、1.12%,用含酪蛋白的Tris溶液分别稀释成0.4%、0.35%和0.35%,混匀成一管溶液后,按2.5ul/cm处理在聚酯膜上,37℃干燥12h。
(9)JLep/CCV试剂乳胶垫IIII制备:取JLep、CCV和兔IgG乳胶标记液,原始浓度分别为0.89%、0.98%、1.0%,用含酪蛋白的Tris溶液分别稀释成0.35%、0.4%和0.35%,混匀成一管溶液后,按2.5μL/cm处理在聚酯膜上,37℃干燥12h。
(10)CDV/CAV-II硝酸纤维素膜I的制备:用1x PBS将1.97mg/ml的CAV-II抗原稀释成0.5mg/ml,将1mg/ml的CDV抗原稀释成0.5mg/ml,将8.3mg/ml的羊抗兔IgG抗体稀释成1.0mg/ml后,按0.9μL/cm喷量喷点在硝酸纤维素膜上分别做检测线T1、T2和质控线C1,55℃±2℃烘干12h制得CDV/CAV-II硝酸纤维素膜;
(11)CAV-I/CPIV硝酸纤维素膜II的制备:用1x PBS将1.22mg/ml的CPIV抗原稀释成1mg/ml,将1.97mg/ml的CAV-I抗原稀释成0.5mg/ml,将5mg/ml的羊抗鼠IgG抗体稀释成1.2mg/ml后,按0.9μL/cm喷量喷点在硝酸纤维素膜上分别做检测线T3、T4和质控线C2,55℃±2℃烘干2h制得CAV-I/CPIV硝酸纤维素膜;
(12)CPV/cLep硝酸纤维素膜III的制备:用1x PBS将0.9mg/ml的cLep抗原稀释成0.8mg/ml,将1.0mg/ml的CPV抗原稀释成0.9mg/ml,将5mg/ml的羊抗鼠IgG抗体稀释成1.2mg/ml后,按0.9μL/cm喷量喷点在硝酸纤维素膜上分别做检测线T5、T6和质控线C3,37℃±2℃烘干12-24h制得CPV/cLep硝酸纤维素膜;
(13)JLep/CCV硝酸纤维素膜IIII的制备:用1x PBS将0.8mg/ml的CCV抗原稀释成0.5mg/ml,将0.9mg/ml的JLep抗原稀释成0.8mg/ml,将8.3mg/ml的羊抗兔IgG抗体稀释成1.0mg/ml后,按0.9μL/cm喷量喷点在硝酸纤维素膜上分别做检测线T7、T8和质控线C4,55℃±2℃烘干12h制得JLep/CCV硝酸纤维素膜;
(14)犬八联抗体试剂制备:将样品垫I、乳胶垫I、硝酸纤维素膜I、吸水垫依次按顺序在PVC底板上进行连接组装、切割,即得CDV/CAV-II二合一试剂条;将样品垫II、乳胶垫II、硝酸纤维素膜II、吸水垫依次按顺序在PVC底板上进行连接组装、切割,即得CAV-I/CPIV二合一试剂条;将样品垫III、乳胶垫III、硝酸纤维素膜III、吸水垫依次按顺序在PVC底板上进行连接组装、切割,即得CPV/cLep二合一试剂条;将样品垫IIII、乳胶垫IIII、硝酸纤维素膜IIII、吸水垫依次按顺序在PVC底板上进行连接组装、切割,即得JLep/CCV二合一试剂条。
(15)犬八联抗体快速检测卡制备:将CDV/CAV-II二合一试剂条、CAV-I/CPIV二合一试剂条、CPV/cLep二合一试剂条和JLep/CCV二合一试剂条依次组装在犬八联抗体的塑料模具里即得。
如图4所示,使用该犬八联抗体快速检测卡的检测步骤为:
(1)在各样品孔中分别加入1滴犬血清血浆样本或者2滴犬全血样本;
(2)在各样品孔加入2滴缓冲液,15-20min读取实验结果。
其中缓冲液的制备过程为将0.9g/L NaCl、5g/L EDTA、0.02%Proclin 300混合于水溶液中,调节混合液最终pH为10.7±0.2,得到碱性缓冲液,由于碱性溶液中的标记物颗粒表面带有负电荷,可与靶蛋白分子的正电荷基团形成牢固的结合,降低与非靶蛋白的非特异性结合,提高免疫层析过程中试剂的准确度。
对比例1
一种犬三联抗体快速检测卡,与实施例1的不同之处在于,只含CDV/CPV/CAV-II试剂条。
对比例2
一种犬八联抗体快速检测卡,与实施例1的不同之处在于,其样品垫I组分为水、38.1g/L硼砂、10g/LPVP-10、1ml/L Tween20、1g/L EDTA、25ml/L抗RBC抗体,pH为8.0;其样品垫II组分为水、0.7L/L Tris-Casein-PVP10母液、1.1g/L无水碳酸钠、1g/L TritonX-405、25ml/L抗RBC抗体,pH为8.0;其样品垫III组分为水、10g/L季酮酸,50ml/L抗RBC抗体、6g/LTris、1g/L Casein,1g/L PVP-10,0.02%Proclin 300,pH为8.0;其样品垫IIII组分为水、12.114g/LTris,1g/L BSA、1g/LPVP-10、8g/L季酮酸,15g/L Casein,5g/L Tween20,0.02%Proclin 300,调节pH为8.0。
在不同样品垫配方中,我们主要对Tween20、EDTA、TritonX-405、Casein、PVP-10、BSA浓度进行了调整,以观察这些常见的表面活性剂、封闭剂及离子螯合剂对试剂性能的影响。
Tween20是一大类优良的油/水型乳化剂,当样品垫I中Tween20浓度由10ml/L降低为1ml/L时,可引起CAV-II试剂条特异性变差,产生一些非特异性结合;合适的浓度范围常控制在5-15ml/L,过高浓度(>15ml/L)常导致颗粒过于分散和释放,反而起不到提高灵敏度的效果,过低浓度(<5ml/L)常导致增溶乳化效果不好,假阳性增多。
EDTA作为一种优越的螯合剂,可与二价金属离子如Ca2+形成稳定的螯合物,这些离子可能作为某些酶类的辅基(微活剂或稳定剂),这些离子的存在状态的改变使得酶的活性发生改变。当样品垫I中EDTA浓度由10g/L降低为1g/L时,可引起CAV-II试剂条特异性变差,产生一些非特异性结合;合适的浓度范围常控制在5-15g/L,过高浓度(>15g/L)常导致样品垫中离子成分发生改变,影响抗原抗体结合的亲和性,过低浓度(<5g/L)常导致离子螯合不够彻底,干扰层析反应,特异性变差。
TritonX-405是种水溶性的非离子表面活性剂,作为优越的乳化剂和润湿剂,对改善体系稳定性十分有效。当样品垫II中将TritonX-405添加浓度由10g/L降低为1g/L时,体系由于乳化润湿不够导致免疫反应不彻底,进而影响CAV-1/CPIV的结合,导致灵敏度下降;合适的浓度范围常控制在5-15g/L,过高浓度(>15g/L)常导致溶颗粒增大,试剂常以油的形式进入水溶液中,引起胶团结构过多,灵敏度下降,过低浓度(<5g/L)常导致非互溶体的形成难度增大,结合及反应的不够充分,检出率降低。
Casein酪蛋白是免疫检测系统中常用的封闭剂,与BSA、明胶、脱脂奶粉等相比,酪蛋白在降低非特异性本底信号方面通常更为有效。当样品垫III中将Casein添加浓度由5g/L降低为1g/L时,体系由于封闭不彻底,进而影响cLep的结合,导致特异性变差;合适的浓度范围常控制在5-15g/L,过高浓度(>15g/L)常导致封闭过度影响抗原抗体的结合,降低灵敏度。过低浓度(<5g/L)常导致封闭不够彻底,非特异性结合增强。
PVP-10在免疫层析中可增加反应的粘附性,当样品垫III和IIII中PVP-10浓度由10g/L降低为1g/L时,可引起cLep、JLep和CCV试剂条特异性变差,产生一些非特异性结合。合适的浓度范围常控制在5-15g/L,过高浓度(>15g/L)常导致分子之间相互吸引力增大,朝向不同表面的引力增加,灵敏度增大的同时特异性也变差。过低浓度(<5g/L)常导致分子结合力变弱,反应的稳定性变差,产生特异性结合。
牛血清白蛋白BSA作为封闭剂,可防止抗体和非特异性蛋白结合。当样品垫IIII中将BSA添加浓度由10g/L降低为1g/L时,体系由于封闭不彻底,进而影响JLep和CCV的结合,导致特异性变差。合适的浓度范围常控制在5-15g/L,过高浓度(>15g/L)常常导致封闭过度影响抗原抗体的结合,降低灵敏度。过低浓度(<5g/L)常导致封闭不够彻底,非特异性结合增强。浓度调整后,对试纸结果的影响见下表2。
对比例3
一种犬八联抗体快速检测卡,与实施例1的不同之处在于,其缓冲液组分包括0.9g/L NaCl、1g/L EDTA和0.02%Proclin 300,调节缓冲液PH=10.7±0.2。
对比例4
一种犬八联抗体快速检测卡,与实施例1的不同之处在于,其缓冲液组分包括0.9g/L NaCl、5g/L EDTA和0.02%Proclin 300,分别调节缓冲液pH=7.5、pH=8.5、pH=9.5、pH=10.5。
使用实施例1和对比例1-4所得犬八联抗体快速检测卡检测犬临床样本以验证本发明检测卡的准确性,待测样品情况如表1所示:
表1待测样品情况一览
表2.实施例1和对比例1-3对不同临床样本检测结果
*注:“+”代表检测结果为阳性;“-”代表检测结果为阴性;10(+)代表10个检测结果均为阳性;10(-)代表10个检测结果均为阴性;表中粗斜体标注代表检测结果为假阴或假阳。
表3.实施例1和对比例4对犬2联、犬8联和未免疫犬不同临床样本检测结果
/>
*注:“+”代表检测结果为阳性;“-”代表检测结果为阴性;10(+)代表10个检测结果均为阳性;10(-)代表10个检测结果均为阴性;7(+)代表7个检测结果均为阳性;3(-)代表3个检测结果均为阴性,以此类推;表中粗斜体标注代表检测结果为假阴或假阳。
结果表明,本发明所述的犬八联抗体快速检测卡具有较高的准确度,对于正常犬血样本,实施例1的准确率达到100%;对比例1仅能检测到犬三联CDV/CPV/CAV-II抗体;对比例2A、C和D窗口试剂条易产生假阳性结果,B窗口试剂条易产生假阴性结果;对比例3试剂条易产生假阳性结果。在对比例4中,当缓冲液的pH从10.7逐渐降低到7.5时,CPIV和CCV假阳性风险逐渐升高,当pH=7.5时,CPIV全部假阳。
对比例1与实施例1的对比结果表明,仅测三项指标不能满足临床需求,很多多联疫苗的免疫效果不能有效得到检测;对比例2与实施例1的对比结果表明,在样品垫I上减少Tween20和EDTA的浓度至1,可能导致假阳的发生,在样品垫II上减少Triton X-405的浓度至1,可能导致漏检的发生,在样品垫III上减少PVP-10和Cassein的浓度至1可能导致假阳的发生,在样品垫IIII上减少PVP-10和BSA的浓度至1可能导致假阳的发生;对比例3与实施例1的对比结果表明,降低缓冲液中EDTA的浓度至1可能增加假阳的风险,显示出错误的结果;对比例4与实施例1的对比结果表明,从pH=10.7逐渐下调缓冲液的pH至pH=7.5,CPIV和CCV假阳性风险逐渐升高,显示错误的结果。
- 一种莲藕潜隐病毒双抗体夹心酶联免疫检测试剂盒及制备与检测方法
- 一种犬细小病毒抗体化学发光定量检测试剂盒
- 一种寨卡病毒抗原抗体检测试剂盒
- 一种猪瘟病毒抗体的可视化快速检测试剂盒及其应用
- 一种犬三联抗体检测试剂盒
- 犬瘟热病毒抗体、犬细小病毒抗体和犬冠状病毒抗体联合检测卡
