芴基功能化4,4'-双(N-咔唑)苯乙烯联苯的激光材料及其制备方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料及其制备方法,属于有机激光材料技术领域。
背景技术
目前,激光材料是一种具有广泛应用前景的高科技材料。它们可以被应用于显示器、照明、传感器、光通信和光谱分析等多个领域。相对于无机半导体激光器而言,有机半导体激光器具有成本低、重量轻、机械柔韧性高、超短脉冲工作和波长可调谐高等优点。这些特点使得有机半导体激光器成为无机半导体激光器的潜在替代品。然而,有机半导体激光器仍需克服一些挑战,例如难以实现连续波(CW)激光。据观察,有机半导体激光器的发射线宽比无机半导体激光器至少窄一个数量级。因此,有机半导体激光器在激光材料领域具有潜在的应用前景,但是需要在合成新材料、了解其受激发射特性以及开发新的器件结构等方面投入更多的研究力量,以提高有机半导体激光器的性能。
然而,尽管连续波有机激光器在实际应用中具有重要的意义,但是与脉冲有机激光器相比,关于连续波有机激光器的研究报道却相对较少。在连续波有机激光器中,长寿命三重态猝灭单态的问题,即所谓的单态-三态湮灭(STA)问题,是有机激光器的一个严重挑战。避免STA问题的一种方法是设计一种有机激光染料,其激光发射光谱和激发态吸收光谱(如单态、三态或极化子吸收)之间不存在或很少重叠,但是,目前具有较少光谱重叠的有机材料非常罕见和有限。进一步的,即使完全排除STA问题,三重态在发射体分子上的积累也可能导致另一种有害的现象,即化学降解,从而影响激光器件的稳定性。
有鉴于此,确有必要提出一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料及其制备方法,以解决上述问题。
发明内容
本发明的目的在于提供一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料及其制备方法,以解决现有有机激光材料中激光增益介质的稳定性低、阈值低、加工方法复杂中的至少一个问题。
为实现上述目的,本发明提供一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料,所述激光材料的结构通式为式I和/或式II:
其中,X为单键、-CR
q为0或1,n1和n2为0至10中的任意一个整数;
均各自独立的选自C
R
为以下结构中的任意一种:
R
作为本发明的进一步改进,
其中,L
为实现上述目的,本发明提供一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料的制备方法,包括:
S1、将咔唑苯甲醛和三氟化硼乙醚加入烧瓶中并加入二氯甲烷搅拌溶解;
S2、将用于制备式Ⅰ或式Ⅱ所需的化合物单体溶解于二氯甲烷,并缓慢滴加到溶解有咔唑苯甲醛和三氟化硼乙醚的烧瓶中,进行搅拌反应;
S3、向反应液中加水进行淬灭,随后用二氯甲烷萃取,干燥后得到中间体;
S4、将所述中间体、4,4′-双(二乙氧基膦酰甲基)联苯和叔丁醇钾加入烧瓶中,在惰性气体的保护下加入四氢呋喃,搅拌反应;
S5、反应完成后进行旋干,并使用二氯甲烷进行萃取,旋干后进行重结晶,过滤干燥后得到芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料。
作为本发明的进一步改进,S2中:所述咔唑苯甲醛、化合物单体和所述三氟化硼乙醚的摩尔比为1:1:1~5,反应温度为25℃,反应时间为1小时。
作为本发明的进一步改进,S4中:中间体、4,4′-双(二乙氧基膦酰甲基)联苯和叔丁醇钾的摩尔比为2:1:2.8~3.2,反应温度为25℃,反应时间为4小时。
作为本发明的进一步改进,S4中:惰性气体为氮气、氩气、氦气、氖气、氪气、氙气中的任意一种。
作为本发明的进一步改进,S5中:旋干后用四氢呋喃和乙醇进行重结晶,随后用乙醇淋洗三次,最后用滤纸进行过滤。
本发明的有益效果是:本发明通过将芴基功能化处理,使得材料的溶解度得到大幅提升,进一步降低了合成的工艺成本和难度;通过超位阻功能化与4,4′-双[(N-咔唑)苯乙烯]联苯刚性骨架的协同作用,使得材料的放大受激发射光谱稳定性得到大幅提高,在不影响激光特性的前提下降低了增益介质的膜厚依赖性和温度依赖性。
附图说明
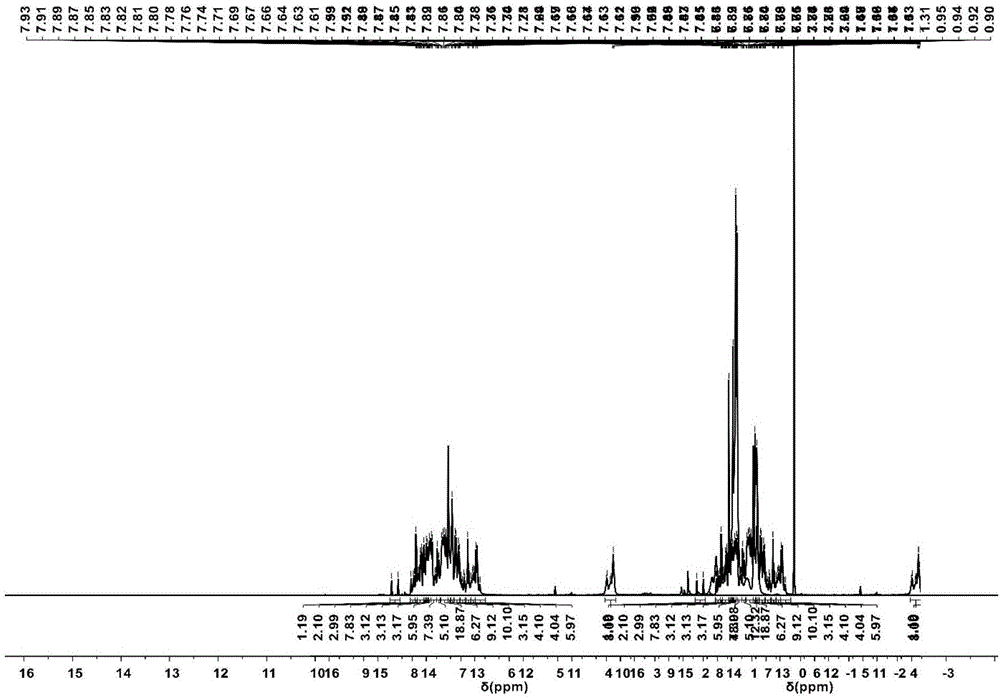
图1是本发明实施例7的核磁共振氢谱图。
图2是本发明实施例22的核磁共振氢谱图。
图3是实施例7和实施例22的荧光衰减曲线图。
图4是实施例7(a)和实施例22(b)在ASE光谱的FWHM和发射强度与泵浦能量的关系图。
图5是实施例7(a)和实施例22(b)在不同温度下的ASE光谱。
具体实施方式
为了使本发明的目的、技术方案和优点更加清楚,下面结合附图和具体实施例对本发明进行详细描述。
本发明提供了一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料,激光材料的结构通式为式I和/或式II:
其中,X为单键、-CR
q为0或1,n1和n2为0至10中的任意一个整数。
均各自独立的选自C
具体的:
L
R
为以下结构中的任意一种:
R
本发明还提供了一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料的制备方法,包括:
S1、将咔唑苯甲醛和三氟化硼乙醚加入烧瓶中并加入二氯甲烷搅拌溶解。
S2、将用于制备式Ⅰ或式Ⅱ所需的化合物单体溶解于二氯甲烷,并缓慢滴加到溶解有咔唑苯甲醛和三氟化硼乙醚的烧瓶中,进行搅拌反应。
其中,咔唑苯甲醛、化合物单体和三氟化硼乙醚的摩尔比为1:1:1~5,反应温度为25℃,反应时间为1小时。优选的,咔唑苯甲醛、化合物单体和三氟化硼乙醚的摩尔比为1:1:1。
S3、向反应液中加水进行淬灭,随后用二氯甲烷萃取,干燥后得到中间体。
S4、将中间体、4,4′-双(二乙氧基膦酰甲基)联苯和叔丁醇钾加入烧瓶中,在惰性气体的保护下加入四氢呋喃,搅拌反应。
其中,惰性气体为氮气、氩气、氦气、氖气、氪气、氙气中的任意一种,本实施例中使用的是氮气,但是在其它实施例中,可以选用上述惰性气体中的任意一种或几种的组合,此处不做限制。
中间体、4,4′-双(二乙氧基膦酰甲基)联苯和叔丁醇钾的摩尔比为2:1:2.8~3.2,反应温度为25℃,反应时间为4小时。优选的,中间体、4,4′-双(二乙氧基膦酰甲基)联苯和叔丁醇钾的摩尔比为2:1:2.8。
S5、反应完成后进行旋干,并使用二氯甲烷进行萃取,旋干后进行重结晶,过滤干燥后得到芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料。
具体的,旋干后用四氢呋喃和乙醇进行重结晶,随后用乙醇淋洗三次,最后用滤纸进行过滤,以得到目标产物。
实施例1
反应路线为:
将咔唑苯甲醛(0.702mmol)、三氟化硼乙醚(0.733mmol)加入烧瓶中,加入20ml二氯甲烷(DCM)进行溶解,将MD1溶解于60ml DCM,并通过恒压滴液漏斗滴加入烧瓶中,室温搅拌一小时。向反应液中缓慢加入水进行猝灭反应,随后用DCM萃取,将萃取溶液进行旋干得到粗中间产物。将粗中间产物利用柱层析法过柱,得到中间产物MA1。
将中间产物MA1(0.1mmol)、4,4′-双(二乙氧基膦酰甲基)联苯(0.05mmol)和叔丁醇钾(0.16mmol)加入50ml烧瓶,封口,抽真空鼓氮气三次,插上氮气球保护。转移装置到搅拌台,用针管抽取超干四氢呋喃(2.6ml)注入,搅拌,在室温下反应四小时。将反应液倒入茄形瓶中旋干,以除去反应液中的THF,随后用DCM萃取,旋干,随后用四氢呋喃和乙醇进行重结晶,用乙醇淋洗三遍,再用滤纸进行过滤,烘干后得到目标产物P1。
经检测实施例1中得到的产物P1的均分子量为1657g/mol。
实施例2
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD2,得到的中间产物为MA2,目标产物为P2,其中,MD2与MD1在结构上不同。
经检测实施例2中得到的产物P2的均分子量为1649g/mol。
实施例3
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD3,得到的中间产物为MA3,目标产物为P3。
经检测实施例3中得到的产物P3的均分子量为1713g/mol。
实施例4
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD4,得到的中间产物为MA4,目标产物为P4。
经检测实施例4中得到的产物P4的均分子量为1882g/mol。
实施例5
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD5,得到的中间产物为MA5,目标产物为P5。
经检测实施例5中得到的产物P5的均分子量为1862g/mol。
实施例6
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD6,得到的中间产物为MA6,目标产物为P6。
经检测实施例6中得到的产物P6的均分子量为1862g/mol。
实施例7
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD7,得到的中间产物为MA7,目标产物为P7。
本实施例中的核磁测试数据为:1H NMR(400MHz,Chloroform-d)δ7.87–7.83(s,4H),7.79–7.74(d,J=7.6Hz,8H),7.70–7.59(m,12H),7.49–7.40(dd,J=10.8,8.0Hz,12H),7.37–7.31(t,J=7.4Hz,8H),7.25–7.22(d,J=8.7Hz,8H),7.21–7.16(m,6H),7.16–7.11(d,J=8.6Hz,8H),3.95–3.80(t,J=6.4Hz,8H),1.39–1.13(m,48H),0.96–0.76(t,J=6.7Hz,12H)。
经检测实施例7中得到的产物P7的均分子量为2162g/mol。
实施例8
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD8,得到的中间产物为MA8,目标产物为P8。
经检测实施例8中得到的产物P8的均分子量为1874g/mol。
实施例9
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD9,得到的中间产物为MA9,目标产物为P9。
经检测实施例9中得到的产物P9的均分子量为1874g/mol。
实施例10
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD10,得到的中间产物为MA10,目标产物为P10。
经检测实施例10中得到的产物P10的均分子量为1938g/mol。
实施例11
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD11,得到的中间产物为MA11,目标产物为P11。
经检测实施例11中得到的产物P11的均分子量为1718g/mol。
实施例12
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD12,得到的中间产物为MA12,目标产物为P12。
经检测实施例12中得到的产物P12的均分子量为1926g/mol。
实施例13
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD13,得到的中间产物为MA13,目标产物为P13。
经检测实施例13中得到的产物P13的均分子量为2319g/mol。
实施例14
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD14,得到的中间产物为MA14,目标产物为P14。
经检测实施例14中得到的产物P14的均分子量为1938g/mol。
实施例15
反应路线为:
本实施例中的反应步骤以及反应条件与实施例1中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD15,得到的中间产物为MA15,目标产物为P15。
经检测实施例15中得到的产物P15的均分子量为2359g/mol。
实施例16
反应路线为:
将咔唑苯甲醛(0.46mmol)、三氟化硼乙醚(163.25mmol)加入烧瓶中,加入250ml二氯甲烷(DCM)进行溶解,将MD16溶解于250ml DCM,并通过恒压滴液漏斗滴加入烧瓶中,室温搅拌一小时。向反应液中缓慢加入水进行猝灭反应,随后用DCM萃取,将萃取溶液进行旋干得到粗中间产物。将粗中间产物利用柱层析法过柱,得到中间产物MA16。
将中间产物MA16(0.076mmol)、4,4′-双(二乙氧基膦酰甲基)联苯(BDTPMBP)(0.152mmol)和叔丁醇钾(0.152mmol)加入烧瓶,封口,抽真空鼓氮气三次,插上氮气球保护。转移装置到搅拌台,用针管抽取超干四氢呋喃(3ml)注入,搅拌,在室温下反应四小时。将反应液倒入茄形瓶中旋干,以除去反应液中的四氢呋喃,随后用DCM萃取,旋干,随后用四氢呋喃和乙醇进行重结晶,用乙醇淋洗三遍,再用滤纸进行过滤,烘干后得到目标产物P16。
经检测实施例16中得到的产物P16的均分子量为2283g/mol。
实施例17
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD17,得到的中间产物为MA17,目标产物为P17。
经检测实施例17中得到的产物P17的均分子量为2274g/mol。
实施例18
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD18,得到的中间产物为MA18,目标产物为P18。
经检测实施例18中得到的产物P18的均分子量为2338g/mol。
实施例19
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD19,得到的中间产物为MA19,目标产物为P19。
经检测实施例19中得到的产物P19的均分子量为2307g/mol。
实施例20
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD20,得到的中间产物为MA20,目标产物为P20。
经检测实施例20中得到的产物P20的均分子量为2307g/mol。
实施例21
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD21,得到的中间产物为MA21,目标产物为P21。
经检测实施例21中得到的产物P21的均分子量为2242g/mol。
实施例22
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD22,得到的中间产物为MA22,目标产物为P22。
请参阅图2所示,本实施例中的核磁测试数据为:1H NMR(400MHz,Chloroform-d)δ8.46–8.25(1H),8.04–7.95(2H),7.94–7.90(3H),7.89–7.77(8H),7.77–7.73(3H),7.73–7.70(3H),7.70–7.67(3H),7.66–7.62(6H),7.62–7.50(7H),7.50–7.42(5H),7.41–7.27(19H),7.26–7.21(6H),7.20–7.14(9H),7.13–7.02(10H),7.01–6.91(3H),6.89–6.79(4H),6.79–6.70(4H),6.70–6.49(6H),4.02–3.80(8H),1.44–1.22(48H),1.00–0.74(12H)。
经检测实施例22中得到的产物P22的均分子量为2787g/mol。
实施例23
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD23,得到的中间产物为MA23,目标产物为P23。
经检测实施例23中得到的产物P23的均分子量为2555g/mol。
实施例24
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD24,得到的中间产物为MA24,目标产物为P24。
经检测实施例24中得到的产物P24的均分子量为2499g/mol。
实施例25
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD25,得到的中间产物为MA25,目标产物为P25。
经检测实施例25中得到的产物P25的均分子量为2619g/mol。
实施例26
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD26,得到的中间产物为MA26,目标产物为P26。
经检测实施例26中得到的产物P26的均分子量为2563g/mol。
实施例27
反应路线为:
本实施例中的反应步骤以及反应条件与实施例16中相同,此处不再赘述,其中,区别点在于:本实施例中使用的原料为MD27,得到的中间产物为MA27,目标产物为P27。
经检测实施例27中得到的产物P27的均分子量为2563g/mol。
分别对实施例1至27制备得到的目标产物P1至P27进行测试,测试结果如下表所示:
对两个通式,以实施例7和实施例22为例,分别提供具体测试情况与原材料进行对比分析如下文。
现有的激光材料4,4′-双[(N-咔唑)苯乙烯]联苯的合成路线如下:
将咔唑苯甲醛(0.076mmol)、4,4′-双(二乙氧基膦酰甲基)联苯(BDTPMBP)(0.152mmol)和叔丁醇钾(0.152mmol)加入烧瓶,封口,抽真空鼓氮气三次,插上氮气球保护。转移装置到搅拌台,用针管抽取超干四氢呋喃(3ml)注入,搅拌,在室温下反应四小时。将反应液倒入茄形瓶中旋干,以除去反应液中的四氢呋喃,随后用DCM萃取,旋干,随后用四氢呋喃和乙醇进行重结晶,用乙醇淋洗三遍,再用滤纸进行过滤,烘干后得到4,4′-双[(N-咔唑)苯乙烯]联苯,下文分析中用B分子指代。
请参阅图3所示,通过测试材料的荧光衰减曲线,利用origin对该数据进行拟合得到两者的瞬态寿命分别为0.59ns和0.63ns,B分子根据文献可知瞬态寿命为0.59ns,均属于短寿命荧光发光分子。而原材料B分子由于溶解度较差,溶液加工制备出的薄膜成膜较差以至无法测试其溶液加工薄膜的荧光量子效率。根据实施例7和实施例22的荧光量子效率(47%和71%),我们可以计算得到两者的辐射衰减速率分别为0.80和1.13ns
请参阅图4所示,对实施例7和实施例22进行了ASE现象的测试,在泵浦能量低时,CCD光谱仪接收的光信号强度缓慢增加、半峰宽缓慢减小,当泵浦能量超过阈值点时,光信号强度增强的幅度加大。对输出强度进行分段线性拟合,交点即材料的ASE阈值。实施例7和实施例22的阈值分别取得6.79和1.95μJ/cm
请参阅图5所示,为了对比其稳定性的变化,我们测试了实施例7和实施例22在不同温度下的ASE光谱,可以发现随着温度的提升材料的光谱红移并不明显,且始终保持的较小的半峰宽。这一点极大的改善了B分子容易光热降解的缺点,提升了材料的稳定性。
综上所述,本发明提供了一种芴基功能化4,4′-双[(N-咔唑)苯乙烯]联苯的激光材料及其制备方法,通过将芴基功能化处理,使得材料的溶解度得到大幅提升,使其更易于溶液加工,降低了合成的工艺成本和难度;通过超位阻功能化与4,4′-双[(N-咔唑)苯乙烯]联苯刚性骨架的协同作用,使得材料的放大受激发射光谱稳定性得到大幅提高,在不影响激光特性的前提下降低了增益介质的膜厚依赖性和温度依赖性,使得该激光材料在有机激光领域既有广泛的应用前景。
以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围。
- 4,4-双(2-磺酸基苯乙烯基)-1,1-联苯的制备方法
- 4,4-双(2-磺酸基苯乙烯基)-1,1-联苯的制备方法
