一种应用笼式镧系超分子标记体系的均相免疫检测方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及免疫检测领域,特别涉及一种应用笼式镧系超分子标记体系的均相免疫检测方法。
背景技术
免疫标记技术是目前诊断领域应用最广的技术之一,通常指用荧光物质、放射性同位素、酶、胶体金及化学发光剂等作为追踪物,标记抗原或抗体进行免疫反应,并用荧光显微镜、放射线测定仪、酶标仪、电子显微镜和发光免疫测定仪等仪器,对实验结果直接镜检观察或自动化测定。
有些免疫分析技术在标记和免疫反应结束后,需要清除体系中未结合的游离物或干扰物质才能进行下一步检测。为使清除效果更加彻底,反应体系中被引入固相载体,也就是非均相免疫分析技术。常见的固相载体有磁微粒、微孔板等,可以将抗体或抗原结合到固相载体表面。免疫反应发生时,溶液中形成“固相载体-抗体-抗原-抗体-标记物”免疫复合物;接着用特殊方法吸附固相载体及整个免疫复合物(例如磁微粒依靠磁场的变化被吸附),将溶液排空并注入新的缓冲液,混匀重悬后再进行检测。但往往吸附/洗脱步骤需要重复若干次,繁琐又耗时,而且容易导致固相载体的破裂或丢失,影响检测结果。此外,昂贵的固相载体拉高成本、可能会发生的固相非特异性吸附干扰结果等等,都在一定程度上限制了非均相免疫分析技术的应用。
近年来均相免疫分析技术一直是研究热点。本发明基于一对笼式镧系超分子和有机小分子作为标记物,开发了一种均相免疫检测方法。其具体表现为:将笼式镧系超分子和有机小分子作为供体和受体分别与单克隆抗体进行共价交联,反应时与待测样本中的抗原形成“供体-抗体-抗原-抗体-受体”免疫复合物;用激发光照射反应液溶液,供体接收激发光并将能量传递给受体,受体发生发光反应。上述反应需要满足供体-受体距离在2-10nm之间的条件时才会发生,即必须形成免疫复合物且结合位点合宜。因此体系中游离或结合位点错误的供体受体均不能产生能量传递和发光反应,无需清洗分离即可识别待测物的免疫结合体。
笼式镧系超分子和有机小分子除了交联抗原抗体外,还可以结合到不同的生物分子上,如蛋白二聚体、DNA互补链等等,应用市场与前景广泛。
本发明的均相免疫分析技术有效避免了洗脱、分离等繁琐步骤,极大提高了分析效率和性价比,准确度和灵敏度更高,具有取代传统非均相免疫分析的潜力。
发明内容
本发明的目的旨在至少解决非均相免疫分析技术的缺陷之一。
为此,本发明的一个目的在于提出一种应用笼式镧系超分子标记体系的均相免疫检测方法,按照先后顺序包括以下步骤:
步骤S1:采用带有羧基和氨基的笼式镧系超分子作为供体,与抗体1进行共价交联,作为试剂1;
步骤S2:采用有机小分子作为受体,与抗体2进行共价交联,作为试剂2;
步骤S3:取待测样本,向其中加入试剂1和试剂2;
步骤S4:混匀以上混合物,37℃孵育T时间;
步骤S5:用激发光照射待测混合物,记录其在两种检测波长下的发光强度,并对照标准曲线计算测量结果。
具体而言,步骤S1中所述的供体为笼式镧系超分子,优选的是穴状三价铕螯合物,更优选的是三联吡啶铕衍生物;步骤S2中所述的受体为有机小分子,分子量不超过2000,优选的是AlexaFlour系列,更优选的是AlexaFlour647。
在上述任一方案中优选的是,步骤S1、S2、S3中所述的试剂1和试剂2,既可以独立作为双试剂存在,也可以混合为单试剂使用。
在上述任一方案中优选的是,步骤S4中所述的孵育T时间,优选的是8-20分钟。
在上述任一方案中优选的是,步骤S5中所述的激发光,波长在280-380nm;所述的两种检测光,波长在580-680nm。
在上述任一方案中优选的是,步骤S3至S5在专用的配套全自动化学发光分析仪中完成。
在上述任一方案中优选的是,步骤S5中所述的标准曲线,其横坐标为样本浓度,纵坐标为该样本在两种检测波长下发光强度的比值。
与现有技术相比,本发明的有益效果是:基于笼式镧系超分子和有机小分子的标记免疫技术,搭建了全均相免清洗的反应体系,在摒弃常规固相载体降低试剂成本的同时,还能避免因固相载体丢失或破裂而导致的误差、多次洗脱带来的污染和耗时等问题,提升检测的准确度和灵敏度。此外本发明的检测过程全部在专用的配套全自动化学发光分析仪上完成,大幅提高检测效率,使临床检验工作更高效便捷。
本发明附加的方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
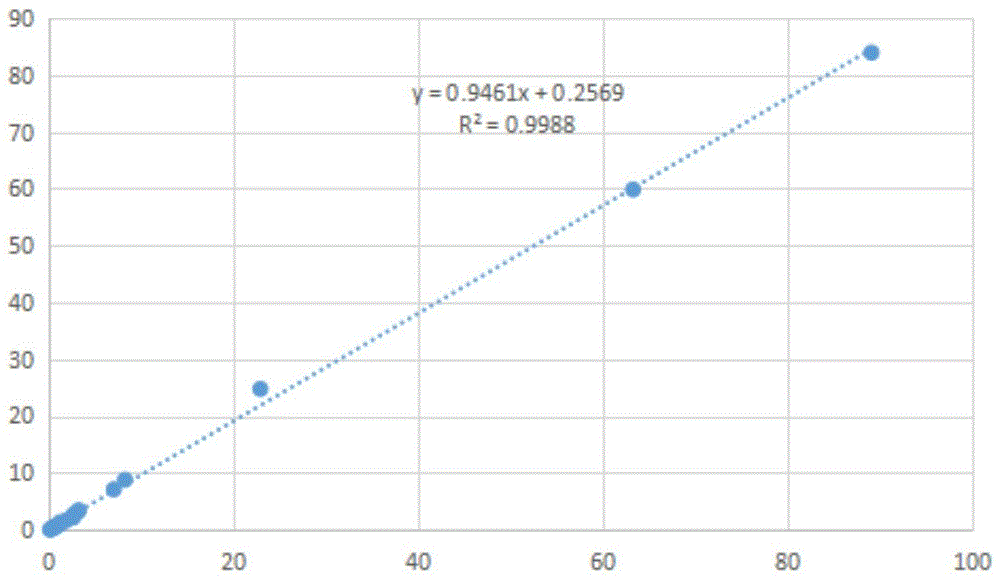
图1为降钙素原(PCT)的检测结果的“样本浓度-信号值”标准曲线。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
实施例一
降钙素原(PCT)检测流程
试剂1:将笼式镧系超分子与抗体1交联,加入保存缓冲液配制成试剂1。
试剂2:将AlexaFlour647与抗体2交联,加入保存缓冲液配制成试剂2。
检测体系:时间T为1080s,激发波长为320nm,检测波长为665nm和620nm。
定标过程:将已知浓度样本、试剂1、试剂2放入全自动化学发光分析仪的相应位置,设置好测量参数和流程,开始检测。以样本在665nm和620nm波长下发光强度的比值为信号值,建立的“样本浓度-信号值”标准曲线。
检测过程:将待测样本、试剂1、试剂2放入全自动化学发光分析仪的相应位置,设置好测量参数和流程,开始检测。对照标准曲线的信号值,计算输出待测样本的浓度。
对比检测结果:
数据显示,本发明与罗氏的检测结果相比,R2=0.9988大于0.990,本发明所述的均相检测方法临床一致性良好。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在不脱离本发明的原理和宗旨的情况下在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。本发明的范围由所附权利要求及其等同限定。
- 一种金属氧化物标记的免疫复合物及其制备方法和其在均相电化学免疫分析中的应用
- 一种生物素标记聚合物纳米颗粒模拟抗体及其在Bt蛋白酶联免疫检测中的应用
- 一种水溶性烷基镧系超分子聚集体及其制备和应用
- 一种水溶性烷基镧系超分子聚集体及其制备和应用
