用于乳腺癌患者鉴定的设备及其制备用途
文献发布时间:2024-04-18 20:01:23
技术领域
本发明属于生物技术领域,具体涉及一种替代FISH对HER2表达IHC2+(阳性不确定)乳腺癌患者准确快速鉴定的新方法。本发明通过 SRM-MS 靶向蛋白质组学方法,能够准确地直接定量乳腺癌中肿瘤细胞HER2蛋白表达(异常)的含量,能够准确地识别从抗HER2治疗中获益的乳腺癌患者,改善临床治疗和结果。本发明可作为指南标准IHC法的一种补充方法。
背景技术
在乳腺癌患者中HER2蛋白异常表达约占乳腺癌患者的20%左右,临床上发现HER2阳性乳腺癌患者术后易复发、转移,临床治疗和预后不良。
评估HER2状态的标准方法是免疫组织化学(IHC)和荧光原位杂交(FISH)试验,由美国FDA批准。IHC也是美国FDA批准的第一个伴随诊断产品。曲妥珠单抗是FDA第一个批准的癌症靶向治疗的抗体药物。随着曲妥珠单抗靶向药物的上市和临床推广应用,对于HER2阳性乳腺癌和胃癌患者来说,其单抗的治疗意味着生存率的显著提高和癌症复发的持续减少,使得部分患者获益。这表明IHC对曲妥珠单抗药物的发展十分重要。
目前FISH是检测HER2状态的金标准,但其费用高,耗时较长。IHC具有费用低,快捷、无需昂贵设备的优点,目前是大多数病理学实验室常规方法。尽管IHC是评估HER2的指南标准方法,但因自身的方法学问题存有一定的局限性,其结果假阳性和假阴性的问题常引起临床医生的质疑。据报道,IHC判断为HER2阳性患者,存在高达20%的假阳性,而判断为HER2阴性的患者,假阴性比例为1.1%~11.5%。IHC为抗原抗体法,属于半定量方法,结果需要人为主观判读,检测通量低。更重要的一点是不能准确的定量。HER2过表达肿瘤IHC评分将其分为3类:阴性(0+或1+),不明确(2+),阳性(3+)。对于IHC2+不明确的结果,推荐FISH/ISH方法来确认HER2阳性。目前,指南将FISH/ISH阳性定义为HER2信号与着丝粒CEP17信号≥2.0的比值。有研究报道指出最佳临界值为4.0。尽管IHC和FISH的结果具有良好的相关性,但一些研究表明存在差异和不一致性的问题。
FISH法属于基因方法亦不可避免地存在检测壁垒,例如:1)检测价格较免疫组化昂贵;2)信号强度随时间衰减,检测方法存在不稳定性;3)较难鉴定乳腺癌微小浸润灶,不能同时观察细胞形态;4)需要病理医师及技术员接受专业的培训,否则会出现主观判断的偏差;5)该检测方法属于半定量方法,无法检测肿瘤细胞中HER2表达量的真实数值。由于FISH检测的种种局限性或不足,HER2诊断方法的改进应受到鼓励。
临床质谱学的出现促进了分子诊断技术的进步与发展。靶向蛋白质谱是一种新颖的方法,与传统的IHC诊断方法相比,靶向质谱法具有独特的优势,克服了IHC和FISH方法学的局限性,可实现肿瘤细胞内5个数量级以上蛋白表达的绝对线性定量,可以在整个护理过程中同时定量多种特异性蛋白生物标志物。选择反应监测(selective-response-monitoring, SRM-MS)靶向蛋白质组学技术是美国CAP/CLIA实验室推荐的方法,已被广泛接受,用于定量特定蛋白靶点的水平。一些国家的相关研究已见报道,但在中国地区报道少见。
发明内容
本发明提供一种替代FISH方法对HER2表达IHC2+的乳腺癌患者进行精准鉴定的新方法。
一方面,本发明提供了一种对HER2表达为IHC2+的乳腺癌患者进行鉴定的方法,包括以下步骤:
1)在所述患者的样本中,通过选择反应监测靶向蛋白质组学技术确定HER2的蛋白表达水平;
2)将所述HER2的蛋白表达水平与阈值比较,如果HER2的蛋白表达水平高于阈值,判断该IHC2+的乳腺癌患者为HER2阳性患者;如果HER2的蛋白表达水平低于阈值,判断该IHC2+的乳腺癌患者为HER2阴性患者。
另一方面,本发明提供了一种包括HER2的生物标志物,或者针对HER2的检测试剂在制备用于对HER2表达为IHC2+的乳腺癌患者进行鉴定的设备中的用途,所述鉴定包括:
1)在所述患者的样本中,通过选择反应监测靶向蛋白质组学技术确定HER2的蛋白表达水平;
2)将所述HER2的蛋白表达水平与阈值比较,如果HER2的蛋白表达水平高于阈值,判断该IHC2+的乳腺癌患者为HER2阳性患者;如果HER2的蛋白表达水平低于阈值,判断该IHC2+的乳腺癌患者为HER2阴性患者。
另一方面,本发明提供了一种对HER2表达为IHC2+的乳腺癌患者进行鉴定的设备,其包括:
1)分析单元,适合于通过选择反应监测靶向蛋白质组学技术确定患者样品中HER2的蛋白表达水平;和
2)含数据处理器的评估单元,将所述HER2的蛋白表达水平与阈值比较,如果HER2的蛋白表达水平高于阈值,判断该IHC2+的乳腺癌患者为HER2阳性患者;如果HER2的蛋白表达水平低于阈值,判断该IHC2+的乳腺癌患者为HER2阴性患者。
在一些实施方案中,所述阈值是700 amol/μg。
在一些实施方案中,对于IHC2+的乳腺癌患者为HER2阳性患者,建议临床给予抗HER2靶向治疗;对于IHC2+的乳腺癌患者为HER2阴性患者,建议临床不给予抗HER2靶向治疗。
在一些实施方案中,所述样本是IHC2+的乳腺癌患者的石蜡包埋肿瘤组织样本或者新鲜的乳腺癌患者肿瘤组织样本。
与现有技术相比,本发明具有如下有益效果:
本发明技术方案通过建立一种替代FISH方法对HER2表达IHC2+的乳腺癌患者进行精准鉴定的新方法,具有以下优点:
1)可以精准的将肿瘤细胞与非肿瘤组织分离;避免了非肿瘤组织对HER2检测结果的干扰;
2)灵敏度高,特异性高,检测灵敏度可以到10
3)可以实现客观定量,通过在样本中加入已知含量的同位素标记肽段作为内标,实现对目标蛋白HER2的绝对定量。
在描述本发明的产品和方法之前,应理解本发明不限于所述的特定产品或方法,因而当然可改变。还应理解,本文所用的术语仅用于描述特定实施方案的目的,而不欲具限制性,因为本发明的范围将仅由所附权利要求书限制。
在提供数值范围时,应理解,除非上下文另有明确说明,否则还特定公开介于所述范围的上限和下限之间的每一中间值。介于所述范围中的任何所述值或中间值与所述范围中的任何其它所述值或中间值之间的每一较小范围涵盖在本发明内。这些较小范围的上限和下限可独立地包括在范围中或排除在范围外,并且其中任一界限、无一界限或两个界限包括在较小范围内的每一范围也涵盖在本发明内,受制于所述范围中任何明确排除的界限。在所述范围包括一个或两个界限时,排除那些所包括界限的任一个或两个的范围也包括在本发明中。
除非另外定义,否则本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常所理解相同的含义。虽然与本文所述类似或等效的任何方法和材料可以用于实施或测试本发明,但现在描述一些潜在和优选的方法和材料。本文所提及的所有公开案通过引用的方式并入本文中以结合所引用的公开案来公开和描述方法和/或材料。应理解,在存在冲突的程度上,本公开取代所并入的公开案的任何公开内容。
本领域技术人员在阅读本公开内容后将显而易见,本文所描述和说明的每一单独的实施方案具有分立成分和特征,在不偏离本发明的范围或精神的情况下,其可容易地与任何其它若干个实施方案的特征分离或组合。可以所述事件的顺序或以逻辑上可能的任何其它顺序进行任何所述方法。
人表皮生长因子受体2 (HER2),又称为 CD340(分化簇340)、原癌基因Neu、Erbb2(啮齿动物)或ERBB2(人),是由erbB2基因编码的蛋白。该癌基因扩增或过度表达在侵袭性类型的乳腺癌进展进程中起着重要作用。大家还认识到erbB2基因的过度表达亦发生在卵巢癌、胃癌、肺腺癌、侵袭性子宫癌及30%涎腺导管癌中。
免疫组织化学或免疫组化(IHC),是应用抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂(荧光素、酶、金属离子)显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及相对定量的检测。
荧光原位杂交(FISH),是利用报告分子(如生物素、地高辛等)标记核酸探针,然后将探针与染色体或DNA纤维切片上的靶DNA杂交,若两者同源互补,即可形成靶DNA与核酸探针的杂交体。此时可利用该报告分子与荧光素标记的特异亲和素之间的免疫化学反应,经荧光检测系统在镜下对待DNA进行定性、定量或相对定位分析。
术语“受试者”、“个体”或“患者”在本文中可互换使用。“受试者”可以是含有表达的遗传物质的生物实体。受试者可以为哺乳动物。该哺乳动物可以为人类。受试者可被诊断出疾病或怀疑处于疾病的高风险下。该疾病可为癌症。该癌症可为乳腺癌。在一些情况下,受试者不一定被诊断出疾病或怀疑处于疾病的高风险下。
术语“样品”指体液样品,分离的细胞样品,或来自组织或器官的样品。可由任意的组织或器官,通过例如活体组织检查(活检)或者手术切取或切除,获取组织或器官样品。
福尔马林固定和石蜡包埋后的组织切片(FFPE),是为了维持细胞核蛋白结构,先用福尔马林固定然后固体石蜡包埋,以便使用超薄切片机切成5-10微米厚的薄片的组织样品(通常是疑似肿瘤组织)。福尔马林与蛋白氨基发生了不可逆交联,保护细胞结构完整性,染色显示组织中肿瘤带来的畸形结构。
术语“表达水平”指生物标志物的蛋白或核酸表达水平,优选指生物标志物的蛋白表达水平。
本发明的选择反应监测(selective - response -monitoring, SRM-MS)靶向蛋白质组学技术,又称为多重反应监测质谱法(MRM-MS)。SRM-MS技术可使用三重四极杆(QQQ,triple quadrupole)质谱仪来从感兴趣的肽中选择带正电荷的离子,使带正电荷的离子片段化,随后测量所选带正电荷的片段离子的丰度。该测量通常可被称为过渡和/或过渡离子。
在一些应用中,SRM-MS与高压液相色谱法(HPLC)和最近的超高压液相色谱法(UHPLC)耦合。在其他应用中,SRM-MS与采用QQQ质谱仪的UHPLC耦合,以对所有感兴趣的肽和蛋白质进行所需的LC-MS过渡测量。
在一些应用中,可使用四极杆飞行时间(qTOF)质谱仪、飞行时间-飞行时间(TOF-TOF)质谱仪、轨道阱质谱仪、四极杆轨道阱质谱仪或任何四极杆离子阱质谱仪从一种或多种感兴趣的肽中选择带正电荷的离子。然后,可测量片段化的带正电荷的离子来确定带正电荷的离子的丰度以用于量化感兴趣的肽或蛋白质。
在一些应用中,可使用飞行时间(TOF)、四极杆飞行时间(qTOF)质谱仪、飞行时间-飞行时间(TOF-TOF)质谱仪、轨道阱质谱仪或四极杆轨道阱质谱仪来测量来自未片段化的感兴趣的蛋白质的带正电荷的肽离子的质量和丰度,以供定量。在本申请中,分析物质量测量的准确度可用作测定的选择标准。具有已知组成和浓度的同位素标记的内标物可用作质谱定量方法的一部分。
在一些应用中,可使用飞行时间(TOF)、四极杆飞行时间(qTOF)质谱仪、飞行时间-飞行时间(TOF-TOF)质谱仪、轨道阱质谱仪或四极杆轨道阱质谱仪来测量感兴趣的蛋白质的质量和丰度以供定量。在本申请中,分析物质量测量的准确度可用作测定的选择标准。任选地,本申请在通过质谱法分析之前,可使用蛋白质的蛋白水解消化。具有已知组成和浓度的同位素标记的内标物可用作质谱定量方法的一部分。
在一些应用中,各种电离技术可与本文提供的质谱仪耦合,以产生所需的信息。可与本公开一起使用的非限制性的示例性电离技术包括但不限于:基质辅助激光解吸电离(MALDI)、解吸电喷雾电离(DESI)、直接辅助实时(DART)、表面辅助激光解吸电离(SALDI)或电喷雾电离(ESI)。
在一些应用中,HPLC和UHPLC可与质谱仪耦合。在质谱分析前,可进行多种其他肽和蛋白质分离技术。可用于从基质背景中分离所需分析物(例如,肽或蛋白质)的一些示例性分离技术包括但不限于,蛋白质或肽的反相液相色谱法(RP-LC)、MALDI前的离线液相色谱法(LC)、一维凝胶分离、二维凝胶分离、强阳离子交换(SCX)色谱法、强阴离子交换(SAX)色谱法、弱阳离子交换(WCX)和弱阴离子交换(WAX)。在质谱分析前可使用上述技术中的一种或多种。
术语“预测”涉及判断受试者是否有患病的风险。
术语“评估”是指确定受试者患病的风险的高低。优选的,应该确定较之对象人群的平均风险,受试者风险是否处于升高的风险或降低的风险。
术语“诊断”在本文中用于指对分子或病理学状态、疾病或疾患(例如乳腺癌)的鉴定或分类。例如,“诊断”可以指特定乳腺癌类型的鉴定。
本发明的方法可以诊断受试者是否患有乳腺癌,具体包括在所述受试者的样品中,通过选择反应监测靶向蛋白质组学技术确定HER2的蛋白表达水平;将所述的蛋白表达水平与阈值比较,如果乳腺癌IHC 2+的患者检测值高于阈值,可诊断为该患者HER2表达阳性;如果检测值低于阈值,考虑该患者HER2表达阴性。
如本领域技术人员将理解的,这种预测、评估、诊断型虽然是优选的,但可能不会对100%被检测(研究)的受试者都是正确的。然而,该术语要求能够正确地评估具有统计学意义的部分的受试者,从而将乳腺癌HER2 IHC 2+的患者判定为阳性,还是阴性。
本发明中临床性能分为:灵敏度,特异性,阳性预测值(PPV),阴性预测值(NPV)。
“灵敏度”可用来衡量某种试验检测出有病者的能力,灵敏度是将实际有病的人正确地判定为真阳性的比例。灵敏度=真阳性人数/(真阳性人数+假阴性人数)*100%。
“特异性”是衡量试验正确地判定无病者的能力,特异性是将实际无病的人正确地判定为真阴性的比例。特异性=真阴性人数/(真阴性人数+假阳性人数)*100%。
阳性预测值(PPV)=真阳性人数/(真阳性人数+假阳性人数)*100%。
阴性预测值(NPV)=真阴性人数/(真阴性人数+假阴性人数)*100%。
本发明以所述的方法对乳腺癌进行诊断。例如,本文提供的设备可以以至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或约100%的灵敏度对乳腺癌进行诊断。
本发明所述的方法可以以至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或约100%的特异性对乳腺癌进行诊断。
在一些情况下,本发明所述的方法以至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或约100%的灵敏度和特异性对乳腺癌进行诊断。
术语“治疗”或“处理”在本文中可互换使用。这些术语可指用于获得有益或所需结果的方法,该有益或所需结果包括但不限于治疗益处和/或预防益处。治疗益处可指正在治疗的潜在病症的根除或减轻。另外,治疗益处也可如下实现:与该潜在病症有关的一种或多种生理学症状得到根除或减轻,使得在受试者中观察到改善,尽管该受试者可能仍患有该潜在病症。预防益处包括延缓、防止或消除疾病或状况的出现,延缓或消除疾病或状况的症状的发作,减慢、中止或逆转疾病或状况的进展,或上述的任意组合。为了获得预防益处,处于发展成特定疾病的风险下的受试者或报告有疾病的一种或多种生理学症状的受试者可接受治疗,即使可能尚未作出该疾病的诊断。
本发明的方法可以辅助乳腺癌患者治疗,具体包括在受试者的样本中,通过选择反应监测靶向蛋白质组学技术确定HER2的蛋白表达水平;将所述HER2的蛋白表达水平与阈值比较,如果高于阈值,可诊断乳腺癌受试者HER2蛋白表达阳性;如果低于下限阈值,可诊断为阴性。高于阈值的乳腺癌患者被认为将从抗HER2治疗中获益。
目前大家普遍认同的动态靶向蛋白的检测较相对静态的基因检测更接近临床的表型。在过去的十年里,人们越来越认识到许多看似相同的肿瘤患者对相同的治疗亦有不同的反应,还意识到没有两位患者的癌症是完全相同的。因此,每一种癌症患者接受常规治疗方法,如化疗、放疗或靶向治疗时就可能有不同的反应。基于精准肿瘤学研究策略与方法,深入探究肿瘤不同的基因改变和不同的分子表型表征,阐明个体患者肿瘤的分子属性,客观地制定患者整体临床治疗方案,客观地评估在特定临床治疗与干预中哪些人群可能获益,哪些存在毒性的可能性。依据个体肿瘤患者中的分子靶点状况与分子药物相匹配,将改善临床治疗和结果,将有助于提高癌症治疗水平。本专利推断,此类例样本为HER2表达阴性或呈极低表达,对抗HER2 靶向药的响应可能不佳,不宜抗HER2 靶向治疗。如果推断被得到证实,进一步说明基于HER2-SRM-MS靶向蛋白定量检测方法较传统方法优势明显,能够从特定的患病人群中准确地遴选出哪些将是从中获益的人群,哪些将是从中非获益的人群。还有HER2-SRM方法不依赖于IHC的病理诊断,独立地对肿瘤细胞内的靶蛋白直接进行绝对定量,其具有良好的临床应用价值与前景。
本发明中使用的术语“设备”可包括一个或以上的用于实践本发明的主题的分析单元,优选反应监测靶向蛋白质组学技术相关的分析单元。分析单元可以包括较大设备中用于预测目的的样品检测,例如定性和/或定量评估之一或两者的独立的装置或元件。例如,分析单元可以执行或辅助样品和/或试剂的移液,计量,混合。分析单元可包括用来夹持试剂以进行测定的试剂夹持单元。试剂的安排可以是,例如在盛有单独的试剂或一组试剂的容器或匣子里,置于储藏室或输送器中合适的托座或位置之中。检测试剂还可以固定在与样品相接触的固体支持物上。分析单元还可以包括对于特定的分析最优化的处理和/或检测组件。
本发明的分析单元还可以包含检测器,其用于确定与所述生物标志物特异性结合的检测试剂的量。本发明测定获得的值可手动计算并存储。或者,本发明的步骤可完全或部分地由计算机程序产品进行。本发明的分析单元可通过已知的任何连接方式与本发明所公开的含数据处理器的评估单元可操作地通讯,将经确定的量转移到所述评估单元。所述评估单元包括带有执行算法的数据处理元件,例如计算机,所述数据处理元件通过执行基于计算机的算法,与符合分析目的的阈值进行比较并得出比较结果。
因此,本发明提供了包括计算机可读存储介质的计算机程序产品,该计算机可读存储介质具有存储在其上的计算机程序。该程序在被计算机读取时,可基于从来自个体的一个或多个生物样品的分析获得的值(例如,基因或蛋白质表达水平、归一化、标准化、取阈和从测定的值到临床结果得分和/或临床状态或阶段的文本或图形描述的转换以及相关信息)来执行相关计算。该计算机程序产品在其中存储用于执行计算的计算机程序。
本发明提供了用于执行数据采集和处理或计算上述软件程序的系统,该系统通常包括:a)中央计算环境;b)输入设备,其可操作地连接到所述计算环境,以接收患者数据,其中所述患者数据可以包括,例如基因或蛋白质表达水平或从使用来自患者的生物样品的测定获得的其他值,或质谱数据或由本公开提供的任何测定的数据;c)输出设备,其连接至所述计算环境,以向用户(例如,医务人员)提供信息;以及d)由中央计算环境(例如,处理器)执行的算法,其中该算法基于由所述输入设备接收的数据来执行,并且其中所述算法计算表达得分、取阈或本文描述的其他功能。本公开提供的方法也可以是整体或部分自动化的。
本发明的比较结果可作为参数化的预测原始数据输出而给出。可以理解这些数据通常需要经过医生的解读。但是也可以预计专家系统设备,其中上述的输出包含无需专业医生进行解读的、经处理的预测原始数据。
当本发明的方法用于商业诊断目的,例如用于医疗领域中时,通常将生成从该方法获得的信息的报告或汇总。该方法的报告或汇总可包含关于一种或多种基因或蛋白质的表达水平、息肉或肿瘤的分类、患者的风险水平(如高、中或低)、患者的预后、治疗选择、治疗建议、生物标志物表达以及如何确定生物标志物水平、生物标志物谱、临床和病理因素的信息和/或与患者疾病状态相关的患者或群组的其他标准临床信息。
所述方法和报告可存储在数据库中。该方法可以在数据库中创建受试者的记录并将数据填入该记录。该报告可以是纸质报告、音频报告或电子记录。该报告可以显示和/或存储在计算设备(例如,手持设备、台式计算机、智能设备、网站等)上。可以预期,报告将提供给医师和/或患者。报告的接收可进一步包括建立与包含所述数据和报告的服务器计算机的网络连接,并从该服务器计算机请求该数据和报告。
本发明中使用的术语“试剂盒”指本发明所述组件的集合,优选地,其单独地或在单一的容器内提供。所述的容器内还包括实施本发明的方法的操作指南。这些操作指南可以是使用手册的形式,也可以通过计算机程序代码提供,当在计算机或数据处理设备上运行所述计算机程序代码时,其能够执行本发明的方法中的计算和比较,并相应地建立预测。所述的计算机程序代码可以是在数据存储介质或设备上,例如光学存储介质(例如光盘),或者直接在计算机或数据处理设备上提供。
本发明的SRM-MS 靶向蛋白质组学方法可作为指南标准IHC法的一种补充方法,能够准确地直接定量乳腺癌中肿瘤细胞HER2蛋白表达(异常)的含量,并能够准确地识别从抗HER2治疗中获益的乳腺癌患者,改善临床治疗和结果。该技术已针对中国北方地区人群得到了验证,对临床应用有一定的指导意义,能够促进在中国地区的临床应用与推广。
附图说明
图1:ELVSEFSR与ELVSEFSR [13C6,15N4] 的质谱二级裂解子离子图谱;
图2:ELVSEFSR与ELVSEFSR [13C6,15N4] 的质谱总离子流图(TIC);
图3:IHC2+中FISH检测阳性与阴性组的HER2蛋白表达量比较;
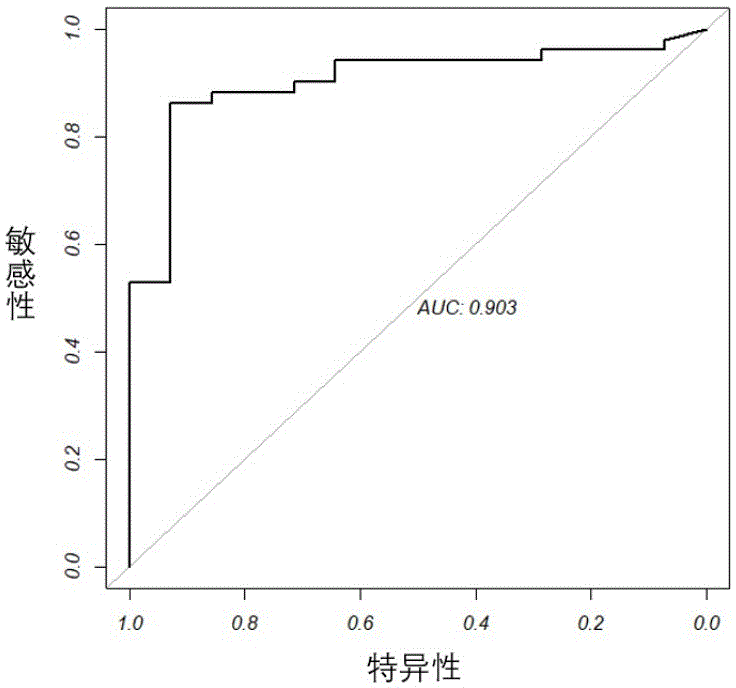
图4:显示以FISH 结果作为实际类别的HER2-SRM ROC曲线,受试者工作特征曲线(receiver operating characteristic curve,简称ROC曲线)。
具体实施方式
下面将结合本发明实施例,对本发明技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例
以下详细介绍一种替代FISH方法对HER2表达IHC2+的乳腺癌患者进行精准诊断的新方法。
为实现上述目的,本发明提出了一种用于肿瘤内HER2蛋白绝对定量的质谱检测方法,可定量HER2的表达量;具体实施如下。
1. 样本信息
样本为HER2检测为IHC2+的乳腺癌手术肿瘤组织的FFPE切片,样本由天津肿瘤医院收集;共65例,其中IHC2+/FISH-的样本14例;IHC2+/FISH+的样本51例。
2. 样本FFPE切片中肿瘤细胞的收集
每个样本分别取4 µm和10µm厚的FFPE切片,行苏木精和伊红染色,脱蜡处理。数字病理扫描系统(3DHistech,MIDI)将4 µm H&E切片和10µm切片扫描成像,并由病理专家在图像上对特定的肿瘤细胞区域进行标记,要保证单片肿瘤细胞标记区域面积大于8 mm
3. 肿瘤细胞的裂解与肽的提取
切割后的肿瘤细胞干燥,加入一定量的组织裂解液(Ammonium BicarbonateBuffer,Sigma Aldrich,S2454-200ML),孵育1.5小时,加入胰蛋白酶(Sequencing GradeModified Trypsin,Promega, V5111),过夜酶解后,终止酶解反应。采用微量BCA方法(Micro BCA, Thermo Fisher Scientific, 23231)检测酶解液中肽段的浓度。
4. 质谱检测
每个样品加入已知浓度的同位素标记的重肽作为内标,用于定量内源蛋白质的内标,将1µg样品注入连接三重四极杆质谱仪(Thermo,TSQ-Altis)的液相色谱仪(Waters,ACQUITY UPLC M-Class System),用于HER2-SRM质谱检测。
液相分离方法
液相色谱仪型号为 Waters ACQUITY UPLC M-Class System;采用梯度洗脱。流动相A为含0.1%甲酸的水溶液(Thermo Scientific,LS118),流动相B为含0.1%甲酸的乙腈溶液(Thermo Scientific,LS120)。色谱柱为捕集柱(nanoEase MZ Symmetry C18 TrapColumn, 100A, 5 um 180 um x 20mm)和分析柱(nanoEase MZ HSS T3 Column, 100Å,1.8 µm, 100 µm x 100 mm)。液相分离梯度见下表:
质谱方法
选用HER2的特异性肽段“ELVSEFSR”(轻肽)和同位素标记肽 ELVSEFSR [13C6,15N4] (重肽)作为内标,进行HER2-SRM的质谱定量检测;两者的离子对,见图1;洗脱曲线、保留时间和离子强度,见图2。质谱仪型号为Thermo TSQ-Altis,正极NSI模式下运行,质谱仪参数设置如下:
质谱数据处理
HER2-SRM质谱数据通过使用Pinnacle Production软件进行数据处理(版本号:V1.0.83.0),定量原理:根据内源HER2多肽和合成重肽的峰面积,绝对定量肿瘤细胞表达的HER2蛋白的量。
HER2的含量(amol)= 轻肽的峰面积/重肽的峰面积×5000amol。
统计学分析以及诊断最佳阈值预测
研究对象基线资料统计使用R 1.3.1093版本对数据进行分析;我们绘制了IHC2+样本以FISH检测阳性与阴性为假设的实际分组以HER2-SRM蛋白表达量为模型的线性预测的ROC曲线,ROC 曲线表明(如图4):HER2-SRM表达量在IHC2+/FISH-和IHC2+/FISH+两组之间的AUC大于0.9(AUC=0.903),具有良好的线性区分性,HER2蛋白可以作为区分两个组别的生物标志物。
在 FISH 判读结果视为正确的基础上,HER2-SRM 蛋白表达水平在 700 amol/µg阈值处具有高特异性 (85.7%) 和 高敏感性(88.2% )。因此,本专利在应用质谱定量值来诊断IHC2+乳腺癌患者为HER2阳性患者时,将700 amol/µg作为判读阈值;即,样本的HER2质谱检测值大于或等于700amol/µg时,判断该IHC2+的乳腺癌患者为HER2阳性患者,建议临床给予抗HER2靶向治疗;样本的HER2质谱检测值小于700amol/µg时,判断该IHC2+的乳腺癌患者为HER2阴性患者,不建议临床给予抗HER2靶向治疗。
