用于检测他克莫司个体化用药基因多态性的探针、引物及试剂盒
文献发布时间:2023-06-19 09:44:49
技术领域
本发明涉及分子生物学领域,具体的说涉及用于检测他克莫司个体化用药基因多态性的探针、引物及试剂盒。
背景技术
他克莫司(tacrolimus,FK506)为大环内酯类免疫抑制剂,临床上广泛用于肝、肾、心、肺、胰等器官移植患者的免疫抑制治疗,其主要不良反应包括继发性感染、肾毒性、神经毒性、胃肠反应、代谢障碍以及淋巴增生性疾病和肿瘤等。器官移植患者应用他克莫司后血药浓度偏低可导致急性排斥反应和药物敏感性降低;血药浓度偏高则容易发生肾毒性、神经毒性、糖尿病、高血脂症、高血压和胃肠道紊乱等不良反应。导致他克莫司毒副作用的发生。CYP3A5在他克莫司的代谢中起重要作用,其活性降低可导致他克莫司的血药浓度升高,不良反应增加。CPIC指南建议携带CYP3A5*3/*3基因型的移植患者减少他克莫司的用药剂量,以避免发生药物不良反应
CYP3A5参与他克莫司、咪达唑仑、氨苯砜、可的松、尼菲地平等多种药物的代谢。CYP3A5基因第3内含子内22893位存在6986A>G的突变(rs776746,CYP3A5*3),该SNP可导致CYP3A5mRNA异常剪接,引起终止密码子过早剪切CYP3A5蛋白,从而使其失去酶的活性,因此CYP3A5*3纯合子个体肝脏和肠道CYP3A5蛋白表达和活性显著下降。CYP3A5*1等位基因频率存在显著种族差异,白种人群中为10%--15%,中国人群中为28%,而黑种人群则高达60%--80%。
目前普遍应用的突变检测方法为DNA直接测序法,PCR产物直接进行DNA序列分析,可以明确突变位点,但存在费时费力,成本较昂贵,不适用于对大量样本进行检测等缺点。因此,需要开发一种适合大批量样本检测的方法。
发明内容
本发明的目的首先在于提供一种用于检测他克莫司个体化用药基因多态性的探针,该探针的序列如SEQ ID NO.:1所示,或者在SEQ ID NO.:1的序列两端加以基团修饰;
其中修饰基团为:5′的修饰基团为荧光基团,如HEX;3′的修饰基团为淬灭基团,如BHQ1;
具体的说,本发明提供的用于检测他克莫司个体化用药基因多态性的探针为:5’-HEX-CGGGGTGTCTTTCANTATCTCTTCCCCG-BHQ1-3’BHQ1;
其中N为变异碱基,具体为A>G;
所述的探针包括环序列和茎序列,其中环序列为第5~23bp(5′-TGTCTTTCANTATCTCTT-3′),其两侧是两个反向互补的茎序列,茎序列为(5′-CGGGG……CCCCG-3)。
该探针的设计原理为:根据CYP3A5基因多态性rs776746,设计探针和引物,需要保证在退火温度下DNA模板不存在时,探针呈茎环状态。探针所采用的淬灭基团为BHQ1,其淬灭空间范围很小,搭配短发射波长的荧光基团,如HEX,只有当分子信标呈茎环结构时,荧光才会被很好地淬灭。环序列与靶DNA序列互补时,确定最佳PCR引物为40-45bp大小,PCR产物长度100-180bp。
本发明还提供了一种用于检测他克莫司个体化用药基因多态性的引物,该引物的序列如SEQ ID NO.:2(引物1)和SEQ ID NO.:3(引物2)所示:
引物1 5’-AGGTGACACTATAGAATAACCACCCAGCTTAACGAATG-3’
引物2 5’-GCAAGCCCTCACGTAGCGAACAGCAAGAGTCTCACACAGGA-3’。
本发明还提供了一种用于检测他克莫司个体化用药基因多态性的试剂盒,该试剂盒包含如上所述的探针和/或引物;
该试剂盒还包含还有Taq酶、dNTP、和/或Mg
本发明还提供一种了用于检测他克莫司个体化用药基因多态性的方法该方法包括如下步骤:
(1)采集样本,抽提DNA;
(2)应用上述探针和引物进行荧光定量PCR反应;
(3)应用PCR仪配套软件分析结果,根据扩增曲线,规定合适基线和阈值,基于形成的杂交峰所显示的Tm值差异展现不同的基因型;
其中Tm值58℃时为野生型,Tm值66℃时为突变型。
其中PCR反应的总体系为15ul(包括PCR Mix 7.5ul、正向引物溶液0.5ul及反向引物溶液0.5ul,探针0.1ul,样本DNA 2ul,灭菌重蒸馏水4.4ul);在荧光定量PCR仪上进行反应,PCR反应条件为92-97℃预变性5-15分钟;92-97℃变性10-30秒,57-65℃退火10-30秒,70-75℃延伸10-30秒,40-50个循环;62℃延伸10分钟;92-97℃变性1分钟,40℃复性1分钟,熔解温度45-80℃过程中实时监测荧光信号,每升温1℃记录5次。
本发明对CYP3A5基因多态性进行检测,可实现对CYP3A5基因多态性的快速筛查,有利于建立对个体叶酸代谢能力进行评估,辅助临床对患者进行危险分层和指导叶酸的个体化服用。
本发明利用一种可以特异识别核酸序列的荧光探针,通过与靶序列进行杂交后发生构象的变化而释放荧光染料,根据杂交后产生不同温度的峰图判定分型结果。在没有靶DNA存在的情况下,荧光基团与淬灭基团可以稳定地结合在一起,检测不到荧光信号;当有靶DNA存在时,荧光标记探针结构被破坏,荧光基团与淬灭基团相互分离,即可检测到荧光信号。该方法与其他遗传分型技术相比,操作简单,2-3小时可以完成96例检测,具有灵敏度高、特异性好、快速、高通量检测等优点,通过直接探测PCR过程中荧光信号获得检测结果,基因分型清晰,不需要PCR后处理或电泳检测,可实现真正的闭管操作。
附图说明
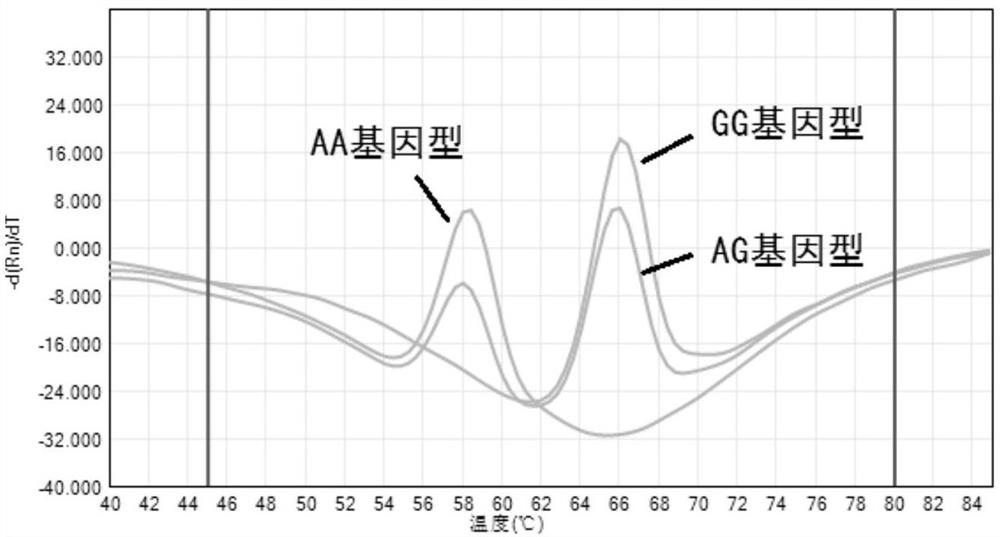
图1、rs776746位点的三种峰型(AA型、GG型、AG型)
图2、精密度实验结果(其中两个峰的为AG型,单峰的为AA型)
图3、多样本的熔解曲线图
具体实施方式
实施例1:探针及引物设计
本发明是针对CYP3A5 677A>G SNP位点设计探针及引物序列。具体原理是利用荧光探针与靶序列进行杂交后发生构象的变化而释放荧光染料,根据杂交后产生不同温度的峰图及Tm值判断基因分型结果。在没有靶DNA存在的情况下,荧光基团与淬灭基团可以稳定地结合在一起,检测不到荧光信号;当有靶DNA存在时,荧光标记探针结构被破坏,荧光基团与淬灭基团相互分离,即可检测到荧光信号。
设计探针和引物,实现在退火温度下模板不存在时,探针呈茎环状态,包括环序列及其两侧呈反向互补的茎序列,总长度为28bp,其中环序列为18bp(5′-TGTCTTTCA
引物和探针序列如下:
引物1的序列:5’-AGGTGACACTATAGAATA ACCACCCAGCTTAACGAATG-3’;
引物2的序列:5’-GCAAGCCCTCACGTAGCGAA CAGCAAGAGTCTCACACAGGA-3’;
探针的序列:5’-HEX-CGGGGTGTCTTTCANTATCTCTTCCCCG-BHQ1-3’。
其中N为变异碱基,具体为A>G;
上述探针和引物由生工生物工程(上海)股份有限公司合成。
实施例2:检测不同基因型标准品
1、用质粒CYP3A5 6986构建并制备含有目的基因rs776746位点的野生型标准品质粒和突变型标准品质粒(质粒来源,以及含目的基因质粒的合成由生工生物工程(上海)股份有限公司合成。通过sanger测序确定序列的准确性,野生型标准品质粒rs776746基因型为AA;突变型标准品质粒rs776746基因型为GG。标准品质粒DNA浓度标化到10ng/ul。
2、采用实施例1中的探针及引物。
3、PCR反应体系:
1)在每一个PCR反应孔中依次加入PCR Mix 7.5ul,引物1溶液0.5uM及引物2溶液0.5uM,探针0.1uM,然后在3个不同的PCR反应孔中分别加入野生型标准品质粒DNA、突变型标准品质粒DNA、混合型DNA(野生型标准品质粒和突变型标准品质粒按照1:1比例混合)各2ul,用灭菌重蒸馏水补足15ul;
2)在荧光定量PCR仪上进行反应,PCR反应条件为95℃预变性5分钟;95℃变性30秒,60℃退火30秒,62℃延伸30秒,45个循环;62℃延伸10分钟;95℃变性1分钟,40℃复性1分钟,熔解温度45-80℃过程中实时监测荧光信号,每升温1℃记录5次。
4、应用PCR仪配套软件SLAN分析结果,基于形成的杂交峰所显示的Tm值差异展现不同的基因型。rs776746位点峰出现在58℃为AA基因型,出现在66℃为GG基因型,两个位置都有峰为AG基因型(图1)。
实施例3:检测方法性能分析实验
1、精密度实验
取野生型标准品质粒DNA和混合型DNA(野生型标准品质粒和突变型标准品质粒按照1:1比例混合)各一份,每天检测3次,连续检测5天,扩增反应程序采用实施例2中方法,结果见图2。表明本发明的荧光PCR扩增反应重复性好(符合率大于95%,检测结果AG值变异系数CV小于5%)。
2、符合率实验
选取20例上海地区健康志愿者DNA样本,应用实施例2的方法进行rs776746位点检测,同时应用sanger测序法进行验证,比较两种方法检测结果的一致性,结果表明实施例2方法的分型结果与sanger测序法的符合率实验一致程度百分比为100%,一致性优秀。
3、检出限实验
取已知浓度的混合型DNA(野生型标准品质粒和突变型标准品质粒按照1:1比例混合)一份,稀释至10ng/ul、5ng/ul、2ng/ul、1ng/ul四个浓度,每个浓度平行检测3管。结果表明样本浓度为10ng/ul、5ng/ul、2ng/ul、1ng/ul时均可检出对应基因型,即最低可检出浓度为1ng/ul。
实施例4:口腔上皮细胞样本DNA的检测
1、采用硅胶吸附法抽提92例上海地区健康志愿者口腔上皮细胞基因组DNA,电泳凝胶成像法对DNA的浓度和纯度作检测,待测样本DNA浓度标化到10ng/ul。
2、检测方法如下:在每一个PCR反应孔中依次加入PCR Mix 7.5ul,正向引物溶液0.5uM及反向引物溶液0.5uM,探针0.1uM,同时进行弱阳性对照(基因型为AG)、阴性对照(基因型为AA)和待测样本的检测,每个反应孔加入DNA 2ul,用灭菌重蒸馏水补足15ul;在荧光定量PCR检测仪上进行反应,PCR反应条件为95℃预变性5分钟;95℃变性30秒,60℃退火30秒,62℃延伸30秒,45个循环;62℃延伸10分钟;95℃变性1分钟,40℃复性1分钟,熔解温度45-80℃过程中实时监测荧光信号,每升温1℃记录5次。
3、应用配套软件分析结果,基于形成的杂交峰所显示的Tm值差异展现不同的基因型。rs776746位点峰出现在58℃为AA基因型,出现在66℃为GG基因型,两个位置都有峰为AG基因型。如图3所示为多样本的熔解曲线图,分型成功率达到100%。
4、将92例口腔上皮细胞基因组DNA同时进行sanger测序,结果与本发明的检测结果完全一致,说明本发明方法用于检测他克莫司个体化用药基因多态性结果准确度高。
序列表
<110> 上海中优精准医疗科技股份有限公司
<120> 用于检测他克莫司个体化用药基因多态性的探针、引物及试剂盒
<160> 3
<170> SIPOSequenceListing 1.0
<210> 1
<211> 28
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<221> misc_feature
<222> (15)..(15)
<223> n=a或g
<400> 1
cggggtgtct ttcantatct cttccccg 28
<210> 2
<211> 38
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
aggtgacact atagaataac cacccagctt aacgaatg 38
<210> 3
<211> 41
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
gcaagccctc acgtagcgaa cagcaagagt ctcacacagg a 41
- 用于检测他克莫司个体化用药基因多态性的探针、引物及试剂盒
- 用于指导格列苯脲药物个体化用药相关基因检测的引物探针组合及试剂盒及应用
