含有间充质干细胞的液体医用生物功能敷料及其制备方法
文献发布时间:2023-06-19 11:17:41
技术领域
本发明属于医用生物敷料技术领域,涉及一种含有间充质干细胞的液体医用生物功能敷料及其制备方法。
背景技术
间充质干细胞(Mesenchymal Stem Cells,MSCs)是一群具有多向分化潜能和自我更新能力的前体细胞,存在于多种组织中,在组织损伤时,迁移至受损部位参与组织的损伤修复。研究发现在炎症的发生、发展过程中,MSCs能抑制炎性因子的表达,调节多种免疫细胞的数量和比例,进而影响炎症周围细胞的生长与代谢及功能的发挥和损伤修复,并对局部微环境进行调节。同时MSCs还可以通过诱导血管生成和组织形成来加速创面闭合、减少瘢痕形成来促进创面修复,在治疗皮肤组织再生中具有巨大的临床应用前景。
科技的不断进步加深了人们对伤口愈合过程和伤口护理过程的理解,功能性医用敷料是针对伤口的实际情况,为伤口愈合提供的特殊功能性的敷料。新型液体敷料是在伤口湿性愈合理念下应运而生的,湿性愈合理念由Winter博士等在1962年提出,具体指在无菌条件下,运用密闭性敷料或药液,保持伤口适度湿润的环境和适宜的温度,有利于创面上皮细胞的形成,促进肉芽组织生长和创面愈合。
由于伤口的种类繁多,且每一个伤口在其愈合的不同阶段对敷料的要求也不同。而目前现有的新型敷料主要具备的功能是抑菌、保湿、加快伤口愈合等。缺乏对损伤局部创面的调节和功能性的修复。因此,发明具有此类功能的医用生物功能敷料具有重要的意义。
发明内容
本发明的目的在于提供一种含有间充质干细胞的液体医用生物功能敷料及其制备方法。该液体医用生物功能敷料,一方面负载间充质干细胞作为损伤修复的基质,具备调节创面微环境,改善损伤及炎症环境的作用。同时该功能敷料为液体形态,有利于进入腔体或者损伤狭窄的区域,不但具有传统固体敷料(如纱布、创可贴)覆盖创面、隔绝异物的效果,而且还具有加速创面的愈合,屏蔽致病微生物、有害病原体的良好效果。
本发明的上述目的是通过以下技术方案实现的:
本发明提供了一种含有间充质干细胞的液体医用生物功能敷料,由间充质干细胞、人血白蛋白、羧甲基壳聚糖、羧甲基纤维素钠、透明质酸钠、溶剂组成。
进一步地,所述溶剂为生理盐水。
进一步地,所述液体医用生物功能敷料是通过将间充质干细胞、人血白蛋白与羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液混悬制得。
优选地,所述羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液的pH值为7.4。
优选地,所述液体医用生物功能敷料的混悬液中,间充质干细胞的含量为2×10
更优选地,所述间充质干细胞采用脐带华氏胶来源的P3-P5代间充质干细胞。
优选地,所述液体医用生物功能敷料的混悬液中,人血白蛋白的含量为10~20ng/ml。
优选地,所述液体医用生物功能敷料的混悬液中,羧甲基壳聚糖的含量为5~30mg/ml,羧甲基纤维素钠的含量为5~10mg/ml,透明质酸钠的含量为1~2mg/ml。
本发明还提供了上述含有间充质干细胞的液体医用生物功能敷料的制备方法,包括以下步骤:
1)将羧甲基壳聚糖、羧甲基纤维素钠、透明质酸钠与一定量的溶剂混合均匀,并调节pH值为7.4,得到羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液;
2)将间充质干细胞、人血白蛋白溶液、羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液混合均匀,生理盐水进行定容,即得到含有间充质干细胞的液体医用生物功能敷料。
优选地,间充质干细胞经脐带华氏胶分离、原代细胞培养、传代细胞培养、离心分离获得;所述人血白蛋白溶液通过用生理盐水溶解人血白蛋白得到。
与现有技术相比,本发明开拓性的将间充质干细胞应用在液体医用生物功能敷料中,利用其不仅能促进损伤组织的再生与修复,还拥有良好的免疫调节能力,通过调控免疫细胞的增殖、分化和功能状态,调节炎症因子水平,以应对各种炎症相关疾病。本发明采用羧甲基壳聚糖作为重要的成分之一,主要考虑其具有抗菌抗感染的功能,在干细胞的基础上进一步增强敷料的安全抗菌性能。本发明的医用生物功能敷料为液体形态,有利于进入腔体或者损伤狭窄的区域,不仅可以修复损伤、改善创面愈合,还可以调节局部微环境,改善其功能。
附图说明
图1为本发明获得脐带华氏胶间充质干细胞P3代(100×)细胞形态学观察结果。
图2为本发明获得脐带华氏胶间充质干细胞P4代(100×)细胞形态学观察结果。
图3为本发明获得脐带华氏胶间充质干细胞P4代细胞流式检测检测图。
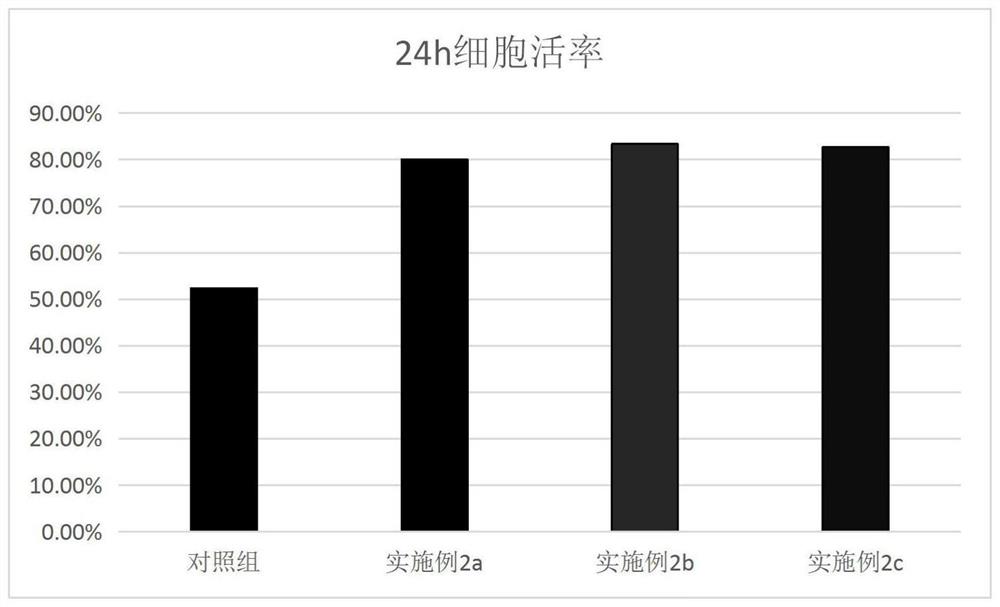
图4为存储条件下,液体医用生物功能敷料中间充质干细胞的活率检测结果。
图5为CCK-8法检测细胞活性实验结果图。
具体实施方式
为了更清楚地说明本发明的技术方案,通过以下实施例对本发明作进一步的描述,以便本领域的技术人员进一步本发明,但以下实施例不对本发明构成任何形式限制。
本申请中,“生理盐水”即0.9%氯化钠水溶液。在配制时,其用量根据需要制备的液体医用生物功能敷料的总体积以及其中各组分的终浓度确定及调整。如未有特殊说明,本申请采用的材料均为现有的材料,可从市面上直接购买得到。
实施例1 P4代间充质干细胞的获得
1、间充质干细胞的原代分离提取培养
1)将装有脐带(脐带组织来源为临床健康婴儿娩出后的废弃物,采集之前与产妇及其家属均签署知情同意书,方案经相关流程批准使用)的采集管用酒精喷壶喷淋并移入生物安全柜内。
2)准备五个100mm的培养皿,编号为1、2、3、4、5。1、3、4培养皿中加入30ml生理盐水,2号培养皿加入30ml 75%乙醇,5号培养皿中加入20ml基础培养基。
3)用止血钳将脐带取出放入1号皿中,润洗脐带,尽量将脐带表面附着的血块以及血管里的血块除掉,用剪刀剪掉头尾各1.5cm。
4)将清洗好的脐带转移至2号皿中杀菌60s后,及时转入到3号皿中,润洗除去酒精。在3号皿中将脐带剪为1.5cm长,转移至4号皿中。
5)华氏胶的剥离在一个皿盖中进行;利用齿摄剔除脐带表皮及其血管,将剥离的华氏胶置于5号皿中。
6)取一支50ml离心管置于离心管架上,将华氏胶置于50ml离心管中,利用剪刀剪碎至大小为2mm左右,利用移液器吸取1ml至于培养瓶中,将脐带碎块均匀铺满培养瓶,加入适量培养基,将培养瓶放入二氧化碳培养箱。
7)分离后第2天(添加培养基24小时后)观察培养液颜色,未变浑浊、颜色正常即可继续培养。
8)待培养瓶中细胞汇合度达到90%后进行细胞传代操作。
2、间充质干细胞的传代培养及收集
1)将培养瓶取出置于生物安全柜中,弃掉培养瓶内的组织块及其液体,吸取10~15ml生理盐水润洗瓶底,尽量去除组织块及其残留液体。
2)加入重组胰蛋白酶平铺浸润整个瓶底,震荡培养瓶。
3)观察到细胞从培养瓶底部脱落,加入胰蛋白酶液量2~3倍的培养基进行稀释。
4)吹打细胞,使贴壁细胞全部悬浮,转移至50ml离心管中,400g离心5min。
5)弃上清,加入10ml生理盐水重悬细胞,取20μl悬液检测细胞数、细胞活率。离心管内补加生理盐水至50ml,400g离心5min。
6)培养瓶放入5%二氧化碳培养箱继续培养。
7)收集传代至P4代间充质干细胞,以用于制备医用生物功能敷料。
实施例2a 含有间充质干细胞的液体医用生物功能敷料a的制备
1、成分配比
2、制备过程
1)羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液的制备:将羧甲基壳聚糖、羧甲基纤维素钠、透明质酸钠与一定量的生理盐水混合均匀,并调节pH至7.4,得到羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液。
2)人血白蛋白溶液的制备:用一定量的生理盐水溶解人血白蛋白,即得到人血白蛋白溶液。
3)间充质干细胞的医用生物功能敷料的制备:将间充质干细胞、人血白蛋白、羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液(pH=7.4)、剩余生理盐水混合均匀,即得到含有间充质干细胞的医用生物功能敷料。
4)将上述医用生物功能敷料置于无菌离心管,或者无菌密闭注射器中,置于4℃下保存。
实施例2b 含有间充质干细胞的液体医用生物功能敷料b的制备
1、成分配比
2、制备过程
1)羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液的制备:将羧甲基壳聚糖、羧甲基纤维素钠、透明质酸钠与一定量的生理盐水混合均匀,并调节pH至7.4,得到羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液。
2)人血白蛋白溶液的制备:用一定量的生理盐水溶解人血白蛋白,即得到人血白蛋白溶液。
3)间充质干细胞的医用生物功能敷料的制备:将间充质干细胞、人血白蛋白、羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液(pH=7.4)、剩余生理盐水混合均匀,即得到含有间充质干细胞的医用生物功能敷料。
4)将上述医用生物功能敷料置于无菌离心管,或者无菌密闭注射器中,置于4℃下保存。
实施例2c 含有间充质干细胞的液体医用生物功能敷料c的制备
1、成分配比
2、制备过程
1)羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液的制备:将羧甲基壳聚糖、羧甲基纤维素钠、透明质酸钠与一定量的生理盐水混合均匀,并调节pH至7.4,得到羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液。
2)人血白蛋白溶液的制备:用一定量的生理盐水溶解人血白蛋白,即得到人血白蛋白溶液。
3)间充质干细胞的医用生物功能敷料的制备:将间充质干细胞、人血白蛋白、羧甲基壳聚糖-羧甲基纤维素钠-透明质酸钠溶液(pH=7.4)、剩余生理盐水混合均匀,即得到含有间充质干细胞的医用生物功能敷料。
4)将上述医用生物功能敷料置于无菌离心管,或者无菌密闭注射器中,置于4℃下保存。
测试例1 间充质干细胞的质量检测
对实施例1获得的P4代间充质干细胞进行形态学观察和流式检测。形态学观察显示,P3代(100×)细胞形态学观察发现多数细胞呈梭形、多角形,符合间充质干细胞的形态特征,如图1所示。经过传代培养至P4代,细胞形态变为相对均一的梭形细胞,表明获得的干细胞为纯度高的间充质干细胞,如图2所示。流式检测结果表明所获的干细胞阳性表达CD73、CD90、CD105,其中CD73阳性表达99.98%,CD90阳性表达100%,CD105阳性表达100%;阴性表达(0%)HLA-DR、CD34、CD45、CD11b、CD19,表明获得干细胞为间充质干细胞,如图3所示。
测试例2 含有间充质干细胞的液体医用生物功能敷料的无菌和内毒素检测
对实施例2a-2c制得的医用生物功能敷料进行微生物检测和内毒素检测,其中微生物检测(细菌、真菌)根据2020年版中华人民共和国药典第4部通则1101进行检测;内毒素检测根据2020年版中华人民共和国药典第4部通则1143进行检测。
检测结果为实施例2a-2c制得医用生物功能敷料在细菌、真菌及内毒素的检测中,均呈阴性。说明该医用生物功能敷料的质量合格,可用于损伤及病源处的修复治疗。
测试例3 CCK-8法检测间充质干细胞的液体医用生物功能敷料的细胞毒性
通过CCK-8法对实施例2a-2c制得的医用生物功能敷料进行细胞毒性的检测,具体的检测过程如下:
1、取实施例1获得的P4代间充质干细胞,用完全培养基重悬细胞,按2×10
2、2h后取出细胞培养板,显微镜下观察细胞生长状况良好。其中医用生物功能敷料组细胞中各加入100μl新型液体功能敷料,最后5孔对照组加入100μl培养液。细胞培养板放回细胞培养箱中继续孵育。
3、24h后取出培养板并换液,然后每孔中加入100μl CCK8试剂,再次孵育2h直到培养液由淡红色逐渐变黄。
4、用移液器小心吸出200μl混匀后的培养液,放入96孔板中,同时在96孔板中选择5孔各加入200μl细胞培养液来测量背景值。多功能酶标仪测量450nm处吸光光度值(OD值),通过公式:细胞活性=(实验组OD值-背景OD值)/(空白对照组OD值-背景OD值)×100%,计算细胞生长活性。
5、根据表1和图5检测结果所示,实施例2a-2c制得的医用生物功能敷料检测值相比于对照组略低,但是细胞与功能敷料共孵育24h后,细胞活率仍保持90%以上,表明功能敷料对细胞生长活性影响较小,根据ISO10093-5医疗器械生物学评价之体外细胞毒性试验的标准,细胞活性高于70%的要求,我们发明的新型液体医用生物功能敷料的细胞毒性在标准范围内,敷料的细胞毒性满足国际标准的要求。
表1.本发明实施例2a-2c及对照组CCK8细胞毒性检测结果
测试例4 存储条件下,液体医用生物功能敷料中间充质干细胞的活率检测
对实施例2a-2c制得的医用生物功能敷料进行间充质干细胞的活率检测,具体的检测过程如下:
1、取实施例2a-2c中,4℃存储24h的医用生物功能敷料(对照组:同时间用生理盐水作为介质存储的间充质干细胞),37℃水浴锅中孵育5分钟;
2、采用生理盐水重悬敷料及对照组中的间充质干细胞于50ml离心管中,400g离心5min;
3、收集细胞沉淀,用10ml生理盐水重悬细胞;
4、分别取敷料、对照组的细胞,采用台盼蓝染色,进行活细胞计数。
5、活细胞计数结果表明,实施例2a-2c制得的医用生物功能敷料相比于对照组要高,其中实施例2a-2c的敷料中间充质干细胞的活率分别为80.1%、83.4%、82.7%,明显高于对照组的52.4%,表明本发明的该医用生物功能敷料在4℃条件下,存储24h仍保持较高的活率,如图4和表2所示。
表2.本发明实施例2a-2c及对照组4℃条件下,存储24h细胞活率
- 含有间充质干细胞的液体医用生物功能敷料及其制备方法
- 一种可被人体吸收的多功能液体医用水凝胶敷料及其制备方法
