结直肠肿瘤性病变血液tRF标志物及其应用
文献发布时间:2023-06-19 13:48:08
技术领域
本发明属于基因工程及肿瘤学领域,涉及一种新的结直肠肿瘤性病变(包括腺瘤和结直肠癌)血液tRF标志物及其应用。
背景技术
根据最新的全球癌症统计数据,结直肠癌(CRC)是全球第三大常见癌症,也是第二常见的致死癌症。2015年中国结直肠癌的新增病例和死亡人数分别为39万和19万。此外,未来数年,这一数字将继续呈上升趋势。最近的一项研究表明,约85%的CRCs可能由腺瘤转化而来。此外,在不同类型的腺瘤中,进展期腺瘤已被证明是CRC更明显的危险因素。因此,在临床应用中,早期筛查和诊断结直肠肿瘤性病变,包括腺瘤和CRC,对后续的治疗至关重要。
结肠镜检查被认为是结直肠肿瘤性病变筛查的金标准。然而,结肠镜检查存在漏检率以及覆盖不全等缺点。此外,在中国城市,大肠癌高危人群的结肠镜检查符合率仅约为15%。所有这些负担都干扰了结直肠肿瘤性病变的早期筛查及诊断。尽管已发现一些肿瘤标志物,如癌胚抗原(CEA)和糖类抗原(如CA19-9、CA74-2等)等,但对结直肠肿瘤性病变(包括腺瘤和结直肠癌)诊断的敏感度和特异度均有限,尤其在发现早期结直肠肿瘤性病变和鉴别侵袭性无痛性肿瘤方面。因此,寻找新的特异性高和敏感性好的标志物越来越受到国内外的重视。因此,迫切需要建立一种新的结直肠肿瘤病变筛选技术,该技术应简单易行,以提高符合率。
转移RNA(Transfer RNA,tRNA)是一种重要的调节性非编码RNA,参与疾病的各个过程。tRNAs被特异性酶裂解后可产生多种tRNA来源的片段(tRFs)。越来越多的证据表明,tRFs参与各种疾病的发生和发展,包括癌症。因此,tRFs可以作为结直肠肿瘤性病变的生物标志物。
目前还没有用于结直肠肿瘤性病变(包括腺瘤和结直肠癌)诊断的较为稳定的生物标志物的报道,若能筛选出结直肠肿瘤性病变(包括腺瘤和结直肠癌)异常表达的全血(包含血清或血浆)tRFs作为生物标志物,并开发出相应的诊断试剂盒,将会有力的推动我国结直肠肿瘤性病变(包括腺瘤和结直肠癌)的筛查及诊断。
发明内容
针对现有技术存在的问题和不足,发明人希望通过分离和研究结直肠肿瘤性病变(包括腺瘤和结直肠癌)患者以及与肿瘤性病变(包括腺瘤和结直肠癌)患者年龄、性别匹配的健康人对照全血(包含血清或血浆)中tRFs,寻找一组与结直肠肿瘤性病变(包括腺瘤和结直肠癌)高度相关的高特异性和敏感性的tRFs,并研制出可便于临床应用的结直肠肿瘤性病变(包括腺瘤和结直肠癌)诊断试剂盒,为结直肠肿瘤性病变(包括腺瘤和结直肠癌)的筛查和诊断提供数据支持,为发现具有潜在治疗价值的新型小分子药物提供数据支持。
为实现发明目的,本发明采用的技术方案如下:
本发明提供了一种用于结直肠肿瘤性病变(包括腺瘤和结直肠癌)辅助诊断的血液tRFs标志物,所述血液tRFs标志物为tRF-Tyr-GTA-081和tRF-Ala-AGC-060的组合,所述tRF-Tyr-GTA-081的扩增引物为Forward:5'GAGTTCTACAGTCCGACGATCT3’;Reverse:5’CTCTTCCGATCTAGATTTA CAGTC 3’。用于检测tRF-Ala-AGC-060的扩增引物为Forward:5'GTCCGACGATCTCCCCAGTA3’;Reverse:5’TGTGCTCTTCCGATCTTGGT 3’。
本发明还提供了一种上述血液tRFs标志物在制备结直肠肿瘤性病变(包括腺瘤和结直肠癌)辅助诊断试剂盒或试剂中的应用。
根据上述的应用,优选地,所述试剂盒包含检测tRF-Tyr-GTA-081和tRF-Ala-AGC-060的检测试剂。
根据上述的应用,优选地,所述检测试剂包括RNA反转录引物和/或DNA扩增引物。
本发明还提供了一种用于结直肠肿瘤性病变(包括腺瘤和结直肠癌)辅助诊断的试剂盒,所述试剂盒用于检测血液中的tRF-Tyr-GTA-081和tRF-Ala-AGC-060。
根据上述的试剂盒,优选地,所述试剂盒包含检测tRF-Tyr-GTA-081和tRF-Ala-AGC-060的检测试剂。
根据上述的试剂盒,优选地,所述检测试剂包括QPCR实验中使用的RNA反转录引物和/或DNA扩增引物,所述RNA反转录引物为Oligo(dt)引物;所述tRF-Tyr-GTA-081的扩增引物为Forward:5'GAGTTCTACAGTCCGACGATCT3’;Reverse:5’CTCTTCCGATCTAGATTTA CAGTC3’,亦即,如SEQ ID NO.1和SEQ ID NO.2所示。用于检测tRF-Ala-AGC-060的扩增引物为Forward:5'GTCCGACGATCTCCCCAGTA3’;Reverse:5’TGTGCTCTTCCGATCTTGGT 3’,亦即如SEQID NO.3和SEQ ID NO.4所示。
根据上述的试剂盒,优选地,所述试剂盒还包含检测内参基因的检测试剂;所述内参基因为SnRNA U6,所述内参基因的检测试剂包括QPCR实验中使用的RNA反转录引物和/或DNA扩增引物,所述RNA反转录引物为Oligo(dt)引物,用于检测SnRNA U6的DNA扩增引物的核苷酸序列为Forward:5’GCTTCGGCAGCACATATACTAAAAT 3’;Reverse:5’CGCTTCACGAATTTGCGTGTCAT 3’,亦即,如SEQ ID NO.5和SEQ ID NO.6所示。
根据上述的试剂盒,优选地,所述试剂盒还包含反转录反应试剂和PCR扩增试剂,如反转录酶、缓冲液、dNTPs,MgCl2,DEPC水和Taq酶等;还可以含有标准品和/或对照品。
具体地说,本发明解决问题的技术方案包括:
(1)建立统一标准的标本库和数据库:以标准操作程序(SOP)采集符合标准的血液样本,系统收集完整的人口学资料和临床资料。
(2)tRFs差异表达谱分析:选择结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例组织及对应结直肠癌癌旁组织样本,检测其组织样本tRFs表达谱及含量,分析结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例组织及对应结直肠癌癌旁组织tRFs的共性和特性,筛选差异表达tRFs;采用筛选的差异表达tRFs在组织和全血中进行进一步大样本验证,确定结直肠肿瘤性病变(包括腺瘤和结直肠癌)发病相关全血(包含血清和血浆)tRFs。
(3)全血(包含血清和血浆)tRFs筛查和诊断试剂盒的研制:根据结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例和健康人对照的特异全血(包含血清和血浆)tRFs开发tRFs诊断试剂盒。
上述步骤(2)中全血(包含血清和血浆)tRFs定量分析可以采用RT-PCR、QPCR、Solexa测序技术、Tapman low densityarray(TLDA)芯片检测等来完成。在本发明的具体的实施方案中,采用QPCR进行验证。
采用QPCR进行差异表达tRFs的验证,具体的操作步骤为:
(1)提取样本总RNA;
(2)将步骤(1)获得的RNA前处理,并逆转录成cDNA;
(3)在荧光实时定量PCR仪上将tRFs和参照基因进行扩增检测;
(4)通过融解曲线分析目的条带,ΔΔCT法进行相对定量。
与现有技术相比,本发明取得的积极有益效果为:
(1)本发明采用tRFs测序对结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例和癌旁组织样本tRFs表达谱进行检测分析,获取在结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例和癌旁组织中差异表达tRFs,并将这些差异表达tRFs在大样本人群的全血中进行验证,筛选得到了与结直肠肿瘤性病变(包括腺瘤和结直肠癌)稳定关联的血液tRFs标志物组合(tRF-Tyr-GTA-081和tRF-Ala-AGC-060的组合),该血液tRFs标志物组合对结直肠肿瘤性病变(包括腺瘤和结直肠癌)的AUC=0.801,sensitivity=73.13%,因此,本发明的血液tRFs标志物组合可用于结直肠肿瘤性病变(包括腺瘤和结直肠癌)的临床筛查诊断,有助于反映结直肠肿瘤性病变(包括腺瘤和结直肠癌)无症状高危人群的疾病状态,为临床医生快速准确掌握患者病情、及时采取更具个性化的防治方案提供支持。
(2)血液tRFs是一种新型生物标志物,不仅稳定、微创、易于检测,且定量精确,因此,本发明通过检测血清/血浆中tRF-Tyr-GTA-081和tRF-Ala-AGC-060表达将大大提高结直肠肿瘤性病变(包括腺瘤和结直肠癌)诊断的敏感性,为结直肠肿瘤性病变(包括腺瘤和结直肠癌)的诊断和治疗开创全新局面,同时为其他疾病生物标志物的研制提供借鉴。
(3)本发明以检测与结直肠肿瘤性病变(包括腺瘤和结直肠癌)辅助诊断相关的血液tRFs标志物组合(tRF-Tyr-GTA-081和tRF-Ala-AGC-060的组合)的RNA反转录引物和DNA扩增引物来制备试剂盒,该试剂盒的灵敏度高,特异性强,操作简单,使用方便,可用于结直肠肿瘤性病变(包括腺瘤和结直肠癌)的辅助诊断和结直肠肿瘤性病变(包括腺瘤和结直肠癌)无症状高危人群的筛查,使得结直肠肿瘤性病变(包括腺瘤和结直肠癌)的诊断更加方便易行,为临床医生快速准确对结直肠肿瘤性病变(包括腺瘤和结直肠癌)无症状高危人群进行筛查诊断,为临床治疗效果评价奠定基础,并为发现具有潜在治疗价值的新型小分子药物靶标提供帮助。
附图说明
图1为本发明一实施例中tRFs高通量测序分析5对腺瘤,5对结直肠癌及其配对的癌旁组织中异常表达的tRFs的结果图;
图2为显示结直肠肿瘤性病变(包括腺瘤和结直肠癌)病例组织中tRF-Tyr-GTA-081和tRF-Ala-AGC-060的表达;
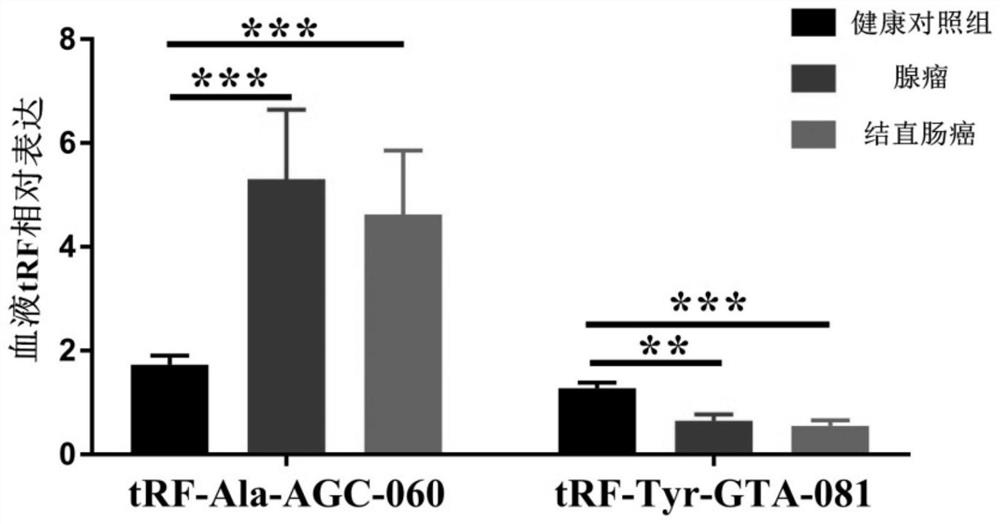
图3为显示结直肠肿瘤性病变(包括腺瘤和结直肠癌)病人及健康志愿者的全血中tRF-Tyr-GTA-081和tRF-Ala-AGC-060的表达;
图4为tRF-Tyr-GTA-081和tRF-Ala-AGC-060联合在结直肠肿瘤性病变以及腺瘤和结直肠癌中的ROC曲线分析;
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
以下通过具体的实施例对本发明作进一步详细说明,但并不限制本发明的范围。
本发明提供的结直肠肿瘤性病变(包括腺瘤和结直肠癌)tRFs标志物tRF-Tyr-GTA-081和tRF-Ala-AGC-060通过以下具体实施例验证其可以作为结直肠肿瘤性病变(包括腺瘤和结直肠癌)的诊断和预后标记物。
实施例1
本实施例通过高通量测序法筛选5对腺瘤,5对结直肠癌及其配对的癌旁组织中差异表达的tRFs。其中,所有腺瘤、结直肠癌及配对的癌旁组织以及病人的全血均收集于上海中医药大学附属龙华医院胃肠外科及内镜室,经病理检查证实。患者知情并同意样本用于该研究,并且本研究经龙华医院伦理科学委员会批准并实施。
由图1可知,其中1个tRFs(tRF-Ala-AGC-060)的表达水平在腺瘤和结直肠癌组织中显著上调,11个tRFs在腺瘤和结直肠癌组织中显著下调,包含tRF-Tyr-GTA-081。qPCR法检测tRF-Tyr-GTA-081和tRF-Ala-AGC-060在腺瘤和结直肠癌组织中的差异表达,并以健康志愿者血液、腺瘤和结直肠癌病人的血液来验证tRF-Tyr-GTA-081和tRF-Ala-AGC-060的表达。
具体的实验步骤如下:
一、组织RNA的提取
1、组织匀浆
每50-100mg组织样品,加入1ml的TRIZOL试剂,用电动匀浆器进行匀浆。
2、两相分离
每1ml的TRIZOL试剂匀浆的样品中加入0.2ml的氯仿,剧烈振荡管体15秒后,室温孵育10分钟。4℃下12,000rpm离心15分钟。离心后混合液体将分为下层的红色酚氯仿相,中间层以及上层的无色的水相。RNA全部被分配于水相中。
3、RNA沉淀
将水相转移到新离心管中,并加入等体积的异丙醇混合,沉淀其中的RNA,混匀后室温孵育10分钟后,于4℃ 12,000rpm离心10分钟。
4、RNA清洗
移去上清液,加入1ml的75%乙醇,清洗RNA沉淀。振荡后,4℃ 7,500rpm离心5分钟。
5、重新溶解RNA沉淀
去除乙醇溶液,空气中干燥RNA沉淀5-10分钟。加入无RNA酶的水,然后55到60℃孵育10分钟。获得的RNA溶液保存于-70℃。
6、使用
二、全血RNA的提取
1.从-80℃冰箱取出全血样本,取300μl全血,加入800μl TRIzol LS;
2.上下摇动EP管使样品充分混匀,静置5分钟,使核蛋白复合物完全解离。
3.加入200μl氯仿,盖好管盖,充分混匀,静置10min。
4. 4℃,12,000g离心15min。取上层含有RNA的上清液转移到新的EP管中。
5.加入500μl异丙醇(TRIZOL:异丙醇=3:2),静置10min。4℃,12000×g离心10min,弃上清。
6.加入1ml 75%乙醇(75%乙醇:TRIZOL=4:3),涡旋,4℃7500g离心5min,弃上清,晾干5~10min。
7.加入20μl DEPC水,在55~60℃的水浴10–15min。
8.使用
三、RNA前处理与cDNA合成。
1.RNA前处理
将5μg RNA与3μL的Deacylation Reaction Buffer和1μL的RNase Inhibitor涡旋混合,37℃孵育40分钟。然后再将1μL的Adaptor,10μL Ligation Reaction和3μL LigationEnzyme Mix混合,25℃孵育1小时。将处理后的RNA用于后续的cDNA合成。
2.cDNA合成试剂配制
热循环仪50℃,孵育1小时。
四、qPCR验证tRF-Ala-AGC-060和tRF-Tyr-GTA-081的表达水平。
以逆转录所得的cDNA为模板,按照如下qPCR反应体系配制反应液:
所有的指标均按以下程序进行:预变性:95℃,10min;95℃,10秒;60℃,60秒,总共40个PCR循环。
由图2可知,tRF-Ala-AGC-060在结直肠肿瘤性病变(包括腺瘤和结直肠癌)组织中的表达水平显著高于癌旁组织。tRF-Tyr-GTA-081在结直肠肿瘤性病变(包括腺瘤和结直肠癌)组织中的表达水平显著低于癌旁组织。
由图3可知,tRF-Ala-AGC-060在结直肠肿瘤性病变(包括腺瘤和结直肠癌)病人全血中的表达水平显著高于健康志愿者。tRF-Tyr-GTA-081在结直肠肿瘤性病变(包括腺瘤和结直肠癌)病人全血中的表达水平显著低于健康志愿者。
实施例2:分析tRF对结直肠肿瘤性病变(包括腺瘤和结直肠癌)的诊断价值。
根据实施例1中qPCR的结果,利用MedCalc软件绘制ROC曲线来评估诊断的灵敏性,进而评估这2种tRFs对结直肠肿瘤性病变(包括腺瘤和结直肠癌)发病的判断能力,其结果见图4。单独使用tRF-Ala-AGC-060为指标区分结直肠肿瘤性病变和健康对照组时,其AUC值为0.626,敏感性为29.85%。单独使用tRF-Tyr-GTA-081区分结直肠肿瘤性病变和健康对照组时,其AUC值为0.762,敏感性为52.24%。基于单个tRF的特异性较差,我们把两种tRF联合作为tRF Combination,利用tRF Combination区分结直肠肿瘤性病变和健康对照组时,其AUC值为0.801,敏感性为73.13%,因此,tRF-Ala-AGC-060和tRF-Tyr-GTA-081联合使用能够很好地将健康志愿者和结直肠肿瘤性病变患者区分,而且诊断结直肠肿瘤性病变的敏感性均高于单独使用其中任何一种tRF。此外,我们还分别分析了tRF联合诊断在腺瘤和CRC中的诊断价值。在腺瘤中,tRF Combination区分腺瘤组和健康对照组,其AUC值为0.777,敏感性为67.57%。而在CRC中,tRF Combination区分CRC组和健康对照组,其AUC值为0.847,敏感性为73.33%;而CRC的传统经典指标CA199区分CRC组和健康对照组,其AUC值为0.656,最佳临界点的敏感性为60.00%。与结果可知,tRF Combination诊断CRC的效能和敏感性显著优于传统指标CA199。
实施例3:结直肠肿瘤性病变辅助诊断试剂盒的制作。
结直肠肿瘤性病变辅助诊断试剂盒的制作和操作流程是基于tRF芯片检测和QPCR定量检测技术。该结直肠肿瘤性病变辅助诊断试剂盒应用于检测血液中的tRF-Ala-AGC-060和tRF-Tyr-GTA-081;该试剂盒包含检测tRF-Ala-AGC-060和tRF-Tyr-GTA-081的检测试剂;所述检测试剂包括QPCR实验中使用的RNA反转录引物和DNA扩增引物,所述RNA反转录引物为Oligo(dt)引物;用于检测tRF-Ala-AGC-060和tRF-Tyr-GTA-081的DNA扩增引物的核苷酸序列。tRF-Tyr-GTA-081的扩增引物为Forward:5'GAGTTCTACAGTCCGACGATCT3’;Reverse:5’CTCTTCCGATCTAGATTTA CAGTC 3’,亦即,如SEQ ID NO.1和SEQ ID NO.2所示。用于检测tRF-Ala-AGC-060的扩增引物为Forward:5'GTCCGACGATCTCCCCAGTA3’;Reverse:5’TGTGCTCTTCCGATCTTGGT 3’,亦即,如SEQ ID NO.3和SEQ ID NO.4所示。进一步地,所述试剂盒还包含检测内参基因SnRNA U6的检测试剂,所述内参基因SnRNA U6的检测试剂包括QPCR实验中使用的RNA反转录引物和DNA扩增引物,所述RNA反转录引物的核苷酸序列,用于检测SnRNA U6的DNA扩增引物的核苷酸序列为Forward:5’GCTTCGGCAGCACATATACTAAAAT 3’;Reverse:5’CGCTTCACGAATTTG CGTGTCAT 3’,亦即,如SEQ ID NO.5和SEQ ID NO.6所示。更进一步地,所述试剂盒还包含常用的反转录反应试剂和PCR扩增试剂,如反转录酶、dNTPs,MgCl2,双蒸水,Taq酶等,这些常用试剂都是本领域技术人员熟知的,另外还可以含有标准品和对照样本。
该试剂盒的检测方法包括:(1)提取样本总RNA;(2)将提取的RNA预变性并逆转录成cDNA;(3)在荧光实时定量PCR仪上将tRF和参照基因进行扩增检测;(4)通过融解曲线分析目的条带,ΔΔCT法进行相对定量等步骤;每一个步骤的具体操作参见实施例1。
该试剂盒的价值在于只需要全血而不需要其它组织样品,通过最精简和特异的引物检测tRF-Ala-AGC-060和tRF-Tyr-GTA-081的表达辅助判断结直肠肿瘤性病变,不仅稳定,检测方便,而且定量精确,大大提高疾病诊断的敏感性,因此将此试剂盒投入实践,可以帮助指导临床准确做出诊断。
以上所述仅为本发明的较佳实施例而已,但不仅限于上述实例,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
序列表
<110> 上海中医药大学附属龙华医院
<120> 结直肠肿瘤性病变血液tRF标志物及其应用
<130> CNF2020139
<141> 2020-06-18
<160> 6
<170> SIPOSequenceListing 1.0
<210> 1
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
gagttctaca gtccgacgat ct 22
<210> 2
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
ctcttccgat ctagatttac agtc 24
<210> 3
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
gtccgacgat ctccccagta 20
<210> 4
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
tgtgctcttc cgatcttggt 20
<210> 5
<211> 25
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
gcttcggcag cacatatact aaaat 25
<210> 6
<211> 23
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
cgcttcacga atttgcgtgt cat 23
- 结直肠肿瘤性病变血液tRF标志物及其应用
- 血浆外泌体tRFs标志物及其在乳腺癌诊断中的应用
