一种硫代酰胺类化合物在调节昼夜节律中的应用
文献发布时间:2023-06-19 19:27:02
技术领域
本发明涉及一种硫代酰胺类化合物的应用,特别涉及在调节昼夜节律中的应用。
背景技术
地球自转引起了近24小时昼夜节律性的光照、温度、湿度以及可获得食物的周期性变化,因此地球上的生物必须相应地调整其生理行为才能与环境相适应,在此过程中,绝大多数生物都形成了近24小时的行为和生理生化水平的生物节律,如人体睡眠、觉醒、进食、排泄、激素分泌、体温、血压等各种生理以及代谢活动为了适应这种外界环境周期性的变化而具有一定的节律性。
研究发现,哺乳动物昼夜节律系统主要是集中在中枢神经系统内的某一特定脑区,昼夜节律过程主要发生于下丘脑前区的视交叉上核(suprachiasmatic nucleus,SCN)及其邻近结构。SCN是哺乳动物最重要的昼夜节律中枢,它参与控制睡眠与觉醒周期等多种节律性活动。SCN活动节律的自我发生和维持能力依赖于少数几种基因所形成的自发转录反馈环路,这些基因主要包括Bmal1、Clock、Per、Cry、CKIε,上述任何一个时钟基因的突变或缺失将会导致机体的自由运转周期延长或缩短。SCN自身节律受外界环境和集体内源性的双重影响,外界环境所致体内核心生物钟和外周生物钟系统的节律性紊乱是人体出现生物节律紊乱以及其他并发症状的关键原因。
根据从事夜班、轮班工作以及进行长途跨时区飞行等工作的昼夜节律紊乱的人员的需求,目前国内外主要通过结合作业任务需求调整睡眠作息规律、控制劳动作业强度和时间、减少“倒班”以改善和校正复杂工作环境下人员的昼夜节律紊乱,作用较为有限或被动,缺乏积极有效的措施,尤其是缺乏作用明显、副作用小且应用方便的有效靶向药物。
近年来,各国开展了一系列常规睡眠管控药物的研究。咖啡因、莫达非尼、阿莫非尼可作为促觉醒药改善嗜睡症状,促进警觉性提升;褪黑素、褪黑素受体激动药以及催眠镇静药可用来促进睡眠;咖啡因、褪黑素、虫草素以及地塞米松等类激素类药物也可用于时差调整。但上述药物均存在药效低、耐受性高等问题,且有一定的不良反应,不适合长期服用,不能满足调节昼夜节律、提高特殊环境人员作业能力以及医学保障的需求。因此,开发高效、低毒的改善昼夜节律紊乱的药物具有重要的意义。
作为主要通透Ca
发明内容:
本发明的目的在于提供一种硫代酰胺类化合物的应用,所述化合物为如下式(I)所示的氮-[2-(4-氯苯基)乙基]-7,8-二羟基-1,3,4,5-四氢-2氢-2-苯并氮卓-2-硫代酰胺化合物,式(I)所示化合物或其药用盐可以用于调节昼夜节律,所述化合物具体为如下结构。
本发明式(I)化合物的药用盐,包括无机酸盐和有机酸盐,如盐酸盐、磷酸盐、硫酸盐、醋酸盐、马来酸盐、甲磺酸盐、富马酸盐、枸橼酸盐、苯磺酸盐、甲基苯磺酸盐或酒石酸盐。
式(I)化合物或其药用盐的使用剂量。虽然剂量依治疗对象、给药方式、症状及其它因素而改变,但对准备调节昼夜节律的成人口服或非口服给药时通常为每剂量约0.1mg/kg-1000mg/kg体重,优选剂量约0.1mg/kg-800mg/kg体重,更优选剂量0.5mg/kg-500mg/kg体重,并且可以每日一次或几次给药。
本发明还公开了一种用于调节昼夜节律的药物组合物,该药物组合物包含如式(I)所示的氮-[2-(4-氯苯基)乙基]-7,8-二羟基-1,3,4,5-四氢-2氢-2-苯并氮卓-2-硫代酰胺化合物或其药用盐及药学上可接受的辅料。
本发明的式(I)化合物、其药用盐能可以安全地口服或非口服给药,或者与药学上可接受的辅料如载体、赋形剂及其他添加剂形成的药物组合物如片剂、缓释制剂、糖衣剂、胶囊剂、注射剂、溶液剂等,安全地口服或非口服给药。为制备口服药物组合物制剂,可采用乳糖或淀粉做载体,明胶,羧甲基纤维素钠,甲基纤维素聚乙烯吡咯烷酮等是合适的结合剂或成颗剂。作为崩解剂可选用淀粉或微晶纤维素,常以滑石粉,胶体硅胶,硬脂酸甘油酯,硬脂酸钙或镁等作为合适的抗黏合剂和润滑剂。例如,可通过压制湿颗粒来制备片剂。活性成分与载体以及选择性的与一份崩解添加剂组成混合物,该混合物与黏合剂的含水溶液,醇性或含水醇性溶液在合适的设备中进行颗粒化,干燥颗粒随后加入其他的崩解剂,润滑剂和抗黏剂将此混合物压片。
本发明的式(I)化合物不易溶于水,为增加溶解性可将杂环类衍生物游离后制成药学上可接受的无机酸和有机酸盐,优选马来酸、甲磺酸、富马酸等盐以有利于以注射剂形式非肠道给药。制备注射剂时,将活性成分式(I)化合物或其药用盐溶于蒸馏水或各种有机溶剂中,也可加入助溶剂如山梨糖醇单月桂酸酯、单硬脂酸酯或单油酸酯等,注射剂还可含有各种常用的添加剂、防腐剂等。在灌装安瓶前,需将注射剂过滤,灌装后进行灭菌。
在不同剂型中,式(I)化合物或其药用盐含量可以根据需要进行调整,在片剂或胶囊剂等口服剂型中可以为重量浓度10%-30%。本发明的化合物可以调节昼夜节律的作用通过实验得到验证。
本发明的式(I)化合物的应用通过实验得到验证。经体外实验证实本发明的式(I)化合物可促进U2OS细胞的生物节律发生相位后移。经小鼠体内实验证实式(I)化合物对于光照后移8小时后昼夜节律的同步化具有显著的促进作用,能显著减少昼夜节律相位移动的同步化时间,并能调控下丘脑生物钟蛋白Per2、Bmal1及相关磷酸化蛋白P-Per2、P-CaMKII的表达,其对调节昼夜节律,改善昼夜节律紊乱具有重要作用。综上所述,本发明的式(I)化合物或其药用盐显示出明显的改善昼夜节律紊乱的作用,同时具有高效、低毒的特点,因此可以用于调节昼夜节律,调节因时差、轮班工作、连续多昼夜工作导致的昼夜节律紊乱以及昼夜节律相关的睡眠障碍。
本发明还公开了含有式(I)化合物或其药用盐的药物组合物在制备调节昼夜节律药物中的应用,其中调节昼夜节律包括调整因时差、轮班工作、连续多昼夜工作导致的昼夜节律紊乱以及昼夜节律相关的睡眠障碍。
附图说明:
图1为细胞实验Lumicycle实验结果图,评价药物对U2OS细胞系相位移动的影响。
图2为在原昼夜节律时间ZT15(Zeitgeber Time,基于时差周期的时间单位,ZT0是灯亮,活动开始的时间,ZT12是熄灯时间)两次给药后,评价药物对光照时间延后8小时后的小鼠昼夜节律相位适应的影响。
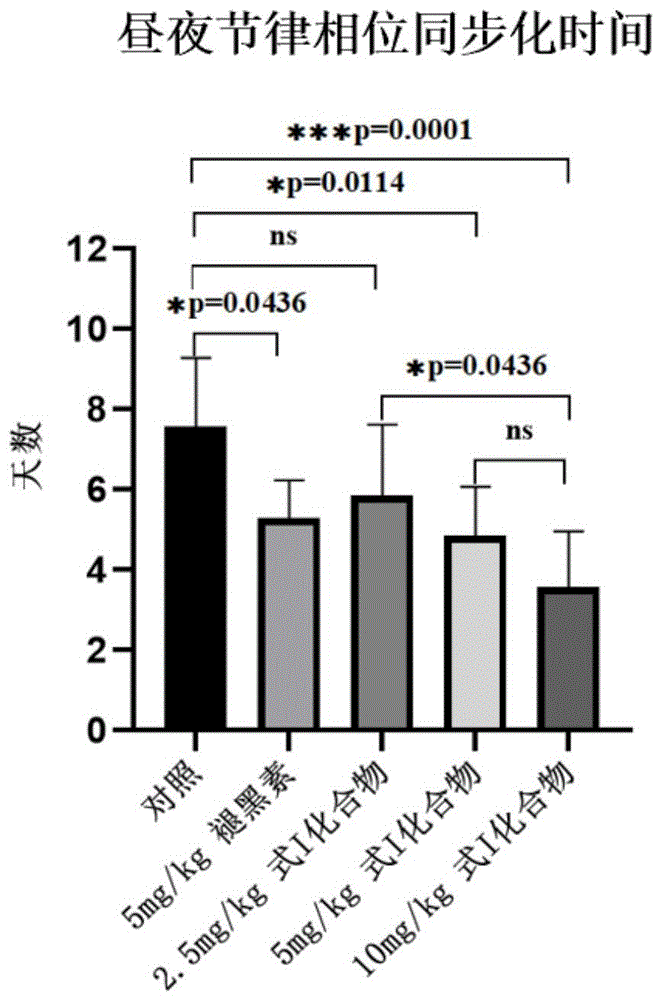
图3为在原昼夜节律时间ZT15两次给药后,评价药物对光照时间后移8小时后的小鼠昼夜节律相位同步化的影响。
图4为在昼夜节律时间ZT12给药12h、24h后,评价药物对小鼠下丘脑生物钟蛋白水平的表达情况。
具体实施方式:
为了更充分地解释本发明的实施,提供制剂制备实施例一到四。本发明提供的实施例仅是用于解释本发明,而不是限制本发明的范围。
实施例一包含本发明的化合物(I)的片剂制备
将活性成分,淀粉和纤维素过筛,并充分混合,将聚乙烯吡咯烷酮溶液与上述的粉混合,过筛,制得湿颗粒于50-60℃干燥,将羧甲基淀粉钠盐,硬脂酸镁和滑石粉预先过筛,然后加入到上述的颗粒中压片。其中式(I)化合物由Selleck公司提供,其余试剂均为市购,以下实施例同。
实施例二包含本发明的化合物(I)的缓释片剂制备
将式(I)化合物、乳糖和磷酸氢钙过筛,并充分混合,将尤特奇RS-PO与上述的粉混合,采用湿法制粒工艺进行压片。
实施例三包含本发明的化合物(I)的胶囊剂制备
每囊含100mg活性成分的胶囊的制备如下:
将式(I)化合物与上述所有成分都过筛,并充分混合,采用干法制粒法制粒,颗粒于50-60℃干燥,测颗粒含量,计算装量,装入胶囊中。
实施例四包含本发明的化合物(I)的注射剂制备
使PH值为7.0-7.5过滤滤液浓度为3/ml,按每安瓶2ml分装,冷冻干燥后即得注射液。
实施例五Lumicycle实验,评价药物对U2OS细胞系相位移动的影响
1.实验材料
实验细胞:Per2-Luc U2OS细胞、Bmal1-Luc U2OS细胞
实验仪器:CO2培养箱、显微镜、Lumicycle仪器(Actimetrics)。
实验试剂:DMEM培养基(GIBCO)、澳洲血清(GIBCO)、PBS、DMEM粉末、无菌水、HEPES、青链霉素、硫酸碳酸氢钠、庆大霉素、DMSO等。
实验药物:式(I)硫代酰胺类化合物购自Selleck。
2.实验方法
配制2×DMEM培养基:将一袋DMEM粉末加入470ml无菌水、10ml 1M HEPES、10ml青链霉素、5ml 7.5%碳酸氢钠溶液和500mg硫酸庆大霉素,充分搅拌后将PH值调整到7.2-7.4之间,0.22μm滤器过滤。
配制XM培养基:25ml 2×DMEM培养基加入25ml无菌水、1ml 100mM Luciferin和1ml B27。
Lumicycle监测生物节律:将Per2-Luc U2OS细胞或Bmal1-Luc U2OS细胞以7.5×10
数据分析:实时监测数据利用Lumicycle Analysis软件,分析相位变化,与对照组对比分析。
3.实验结果
Per2-Luc U2OS细胞给予5、10μM式(I)化合物后相位移动示意图及其相移统计结果如图1A所示,与对照组相比,给5μM式(I)化合物后相位后移0.96±0.16h(P=0.0032,有统计学差异),给10μM式(I)化合物后相位后移3.41±0.32h(P<0.0001,有统计学差异)。Bmal1-Luc U2OS细胞给予5、10μM(I)化合物后相位移动示意图及其相移统计结果如图1B所示,给5μM式(I)化合物后相位后移1.31±0.35h(P=0.0067,有统计学差异),给10μM式(I)化合物后相位后移3.76±0.68h(P<0.0001,有统计学差异)。
实施例六光照8小时后移,评价药物对小鼠昼夜节律相位同步化的影响
1.实验材料
实验动物:C57BL/6J雄性小鼠(斯贝福生物技术有限公司),体重(20±2)g。
实验仪器:CLOCKLAB节律生物学系统(武汉普百科科技公司,型号:ACT-556B)
实验药物:式(I)硫代酰胺类化合物购自Selleck、褪黑素购自MedChemExpress。
2.实验方法
小鼠自主活动筛选:购得的雄性C57BL/6J小鼠单笼饲养在配备有跑轮的笼中,每个笼子具有约200lux的光强度。通过使用记录轮转数的数字系统连续记录每只动物的运行轮活动,并每隔6分钟储存一次,以便进一步分析。小鼠生活在正常12:12小时循环的光照环境中约14天(CT8开灯,指早8点开灯;CT20是关灯,指晚8点关灯,下面描述以此类推,CT是一个标准的时间单位);在第14天进行昼夜节律相位后移调整,将光照延后8小时(即开关灯时间后移8小时,CT16开灯,CT4关灯),利用运用Clocklab节律生物学系统,观察动物适应新的光照周期的情况,筛选昼夜活动相对均一的小鼠进行后续实验,节律调整过快或活动物无规律的小鼠则被剔除。经过筛选的35只小鼠进行随机分组,对照组、5mg/kg褪黑素组、2.5mg/kg式(I)化合物组、5mg/kg式(I)化合物组、10mg/kg式(I)化合物组,每组各7只。在下一次调整光照之前给药,给药时间为开灯前1小时。给药后,调整光照时间后移8小时。CT15给药,CT16调整光照时间为CT0开灯,CT12关灯。给药24小时后进行第二次给药,共给药两次,给药方式为腹腔注射。给药后继续运用Clocklab节律生物学系统记录观察小鼠的运动十天。
3.实验结果
对照组、5mg/kg褪黑素组、2.5mg/kg式(I)化合物组、5mg/kg式(I)化合物组、10mg/kg式(I)化合物组相位调整如图2A所示,图2B为随给药天数增加相位后移的时间。图3为对5个组同步到新节律所需要的时间进行统计分析所得结果,与对照组小鼠适应灯光后移8h所用的天数为7.57±1.72天相比,5mg/kg褪黑素组需要5.29±0.95天(P=0.0436,有统计学差异),2.5mg/kg式(I)化合物组需要5.86±1.77天(P=0.1998,没有统计学差异),5mg/kg式(I)化合物组需要4.86±1.21天(P=0.0114,有统计学差异),10mg/kg式(I)化合物组需要3.57±1.40天(P=0.0001,有统计学差异);2.5mg/kg式(I)化合物组与10mg/kg式(I)化合物组相比,P=0.0436,有统计学差异;其余各组之间均无统计学差异。
4.结论
在开关灯时间后移8h后,原有昼夜节律打破紊乱,观察2.5、5和10mg/kg不同剂量式(I)化合物作用,5、10mg/kg式(I)化合物可以使小鼠加快适应灯光的调整,而2.5mg/kg式(I)化合物作用下使其加快适应的效果不明显,如图2A、图2B、图3所示。在5mg/kg和10mg/kg式(I)化合物作用下,可以明显看出,10mg/kg的作用比5mg/kg作用更为明显。因此,小鼠随式(I)化合物剂量增加而适应灯光改变的速度越快,具有剂量依赖性。同时可以看出,2.5mg/kg式(I)化合物对于加快小鼠适应灯光的作用弱于5mg/kg褪黑素,但5mg/kg和10mg/kg式(I)化合物对于加快小鼠适应灯光的作用似乎强于5mg/kg褪黑素。
实施例七在昼夜节律时间ZT12给药12h后,评价药物对小鼠下丘脑生物钟蛋白水平的表达情况
1.实验材料
实验动物:C57/B6J雄性小鼠(斯贝福生物技术有限公司),体重(20±2)g
实验仪器:组织研磨机(上海净信科技)、酶标仪、电泳仪(美国伯乐)、AmershamImager 680(GE)。
实验试剂:RIPA裂解液(碧云天)、蛋白酶抑制剂混合液(索莱宝)、磷酸酶抑制剂(碧云天)、BCA蛋白浓度测定试剂盒(碧云天)、5×蛋白上样缓冲液(碧云天)、脱脂奶粉(BD)、1.5M Tris-HCl缓冲液(索莱宝)、1.0M Tris-HCl缓冲液(索莱宝)、10%SDS(索莱宝)、AP(Thermo Scientific)、Tris(Biotopped)、甘氨酸(Biotopped)、ACTB抗体(SangonBiotech)、Bmal1抗体(Proteintech)、P-Bmal1抗体(CST)、Per2抗体(RabMAb)、P-Per2抗体(Immunoway)、P-CaMKII抗体(mAb)、ECL发光液(米鼠)。
实验药物:式(I)化合物购自Selleck。
2.实验方法
下丘脑蛋白提取:在小鼠正常昼夜节律的ZT12腹腔注射5mg/kg的药物(对照溶剂、褪黑素、式(I)化合物),于12小时后取小鼠下丘脑,放入液氮快速冷冻,随后加入100μl蛋白裂解液(RIPA:磷酸酶抑制剂:蛋白酶抑制剂=970:29:10),利用组织研磨机研磨,条件为60Hz,20s。研磨结束后所有样本在4℃的离心机中离心,转速12000r/min,10min,吸取上清液体至干净ep管中。使用BCA蛋白浓度测定试剂盒结合酶标仪进行蛋白浓度测定,定蛋白浓度,将蛋白统一浓度为10μg/μl,加入5×蛋白上样缓冲液,混匀后100℃煮10分钟,之后冰水冷却后。
Western Blot实验:上样体积为10μl即上样量为100μg,电泳条件为100V、80分钟,转膜条件为200mA、90分钟。转膜结束后使用含5%脱脂牛奶的TBST封闭PVDF膜,室温慢摇1h。封闭结束后将PVDF膜转移到一抗中在4℃下与一抗慢摇过夜。第二天TBST洗PVDF膜3次,每次10min。随后将PVDF膜转移至HRP缀合的二抗,室温摇床1h。二抗室温摇床结束后,TBST洗PVDF膜三次,每次10min。按1:1比例配制ECL发光液,均匀滴加于PVDF膜上,在AMI680系统上成像,ACTB作为内参蛋白。
3.实验结果
图4A为在昼夜节律时间ZT12,腹腔注射5mg/kg的药物(对照溶剂、褪黑素、式I化合物),12小时后取下丘脑提取蛋白验证药物对Bmal1、Per2、P-Bmal1、P-Per2、P-CaMKII蛋白表达的影响示意图。图4B-F所示分别为相比于溶剂对照组,5mg/kg褪黑素组、5mg/kg式I化合物给药12h后Per2、P-Per2、Bmal1、P-Bmal1以及P-CaMKII蛋白表达变化,如图4B-F所示,相比于溶剂对照组,式(I)化合物在给药12小时后显著性降低下丘脑Bmal1、Per2、P-Per2、P-CaMKII蛋白的表达。
4.结论
在昼夜节律时间ZT12给药12小时后,式(I)化合物在蛋白水平显著性降低下丘脑Bmal1、Per2、P-Per2、P-CaMKII蛋白的表达。
- 一种水中电催化苯并硫代酰胺类化合物合成苯并噻唑的方法
- 一种水相中微波辐射苯并硫代酰胺类化合物合成苯并噻唑的方法
- 炔酰胺介导的硫代酰胺制备方法及其在硫代多肽合成中的应用
- 炔酰胺介导的硫代酰胺制备方法及其在硫代多肽合成中的应用
