一种血液病原体核酸提取试剂盒及其使用方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于分子诊断DNA提取领域,具体涉及一种能够快速提取血液病原体DNA和人DNA的试剂盒及使用方法。
背景技术
现有对血液中核酸(DNA)提取的方法,主要包括酚抽提法、碱裂解法、CTAB抽提法、煮沸法、离心柱提取法、玻璃珠吸附法及微纳米磁珠提取法。目前可用于血液病毒提取的主要有吸附柱法和磁珠法。离心柱核酸提取法由于采用核酸特异吸附和反复洗涤杂质,最后得到的核酸纯度较传统方法具有明显优势,而磁珠法核酸提取技术由于自动化程度高、样本通量大、核酸浓度和纯度好,尤其是安全性高,已成为业内主流方法。国内核酸提取主流厂家拥有全自动核酸提取系统采用磁珠法原理,无需离心且操作自动化,可减少人员接触,并使用深孔板耗材,可避免交叉污染。
而随着临床分子诊断的发展,在某些传染病筛查领域,病毒核酸提取纯化经过PCR扩增鉴定后,检测的结果可以作为临床参考的依据。但由于外源以及内源性核酸酶的存在及其酶活性相当稳定等原因,使得在外周血中提取和纯化高质量的病毒核酸相对较困难。由于分子生物学技术的不断发展,分子生物学技术检测病原体感染已成为疾病诊断中不可或缺的重要工具。在临床病原体检测中,分子生物学技术的应用可以提高检测结果的准确性,对疾病的快速检测起到极为重要的作用。
随着核酸检测的广泛应用,核酸提取技术也在飞速发展,但目前市面上现有的病原体核酸提取试剂盒中,试剂盒中具有以下弊端:1、样本预处理操作繁琐:需对全血样本进行预处理;2、灵敏度低等原因容易造成漏检;3、核酸提取不完全造成定量偏差,不能很好地反映样本的真实浓度。
发明内容
本发明提供了一种血液中核酸提取试剂盒及其使用方法,以提高对核酸的提取效率。
本发明提供了一种血液中核酸提取试剂盒,所述血液中核酸提取试剂盒包括预裂解液、多种提取溶液,至少一种提取溶液中含有体积比为0.5%~3%的辛基葡萄糖新戊二醇。优选地,辛基葡萄糖新戊二醇的体积比为0.8%~2.5%;更优选地,辛基葡萄糖新戊二醇的体积比为1%~2%。例如,在本发明中,辛基葡萄糖新戊二醇体积比为0.5%、0.7%、0.9%、1%、1.2%、1.4%、1.6%、1.8%、2.0%、2.2%、2.4%、2.6%、2.8%、3.0%的提取溶液均能够对血液中的核酸进行高效提取。
进一步地,所述预裂解液包括5~15mmol/L SDS、0.2mmol~1mmol/L氯化钙。
进一步地,所述提取溶液包括第一提取溶液、第二提取溶液,所述第二提取溶液含有体积比为0.5%~3%的辛基葡萄糖新戊二醇、0.2~0.7mg/mL磁珠。
更进一步地,所述第一提取溶液包括1~5mol/L盐酸胍、10~200mmol/L TrisHCl、1~5mol/L硫氰酸胍、1~50mmol/L EDTA、0.01~0.5mmol/L的二硫苏糖醇。
更进一步地,所述第二提取溶液包括0.5mol/L~1mol/LNaCl、体积比为15%-30%的异丙醇、体积比为0.5%~3%的辛基葡萄糖新戊二醇以及0.2~0.7mg/mL磁珠。
进一步地,所述血液中核酸提取试剂盒还包括洗涤液、洗脱液。
更进一步地,所述血液中核酸提取试剂盒还包括第一洗涤液、第二洗涤液、洗脱液。
更进一步地,所述第一洗涤液包括体积比为10%~20%的异丙醇、体积比为0.1%~5%的NP 40、0.5~2mol/L的硫氰酸胍、1~50mmol/LEDTA、0.01~0.5mmol/L的二硫苏糖醇;第二洗涤液包括10~200mmol/LTris HCl、无水乙醇,洗脱液包括10~200mmol/L的Tris~HCl、1~50mmol/L的EDTA。
进一步地,所述血液中核酸提取试剂盒还包括蛋白酶K。
本发明另一方面还公开一种应用上述任意一项所述血液中核酸提取试剂盒的使用方法,在使用过程中,1体积的样本使用0.5~1.5体积含辛基葡萄糖新戊二醇的提取溶液。
进一步地,所述血液中核酸提取试剂盒包括预裂解液、第一提取溶液、第二提取溶液、第一洗涤液、第二洗涤液、洗脱液,所述使用方法包括步骤如下:
S1.取1体积的样本,加入0.15~0.4体积的裂解液,加入0.05~0.15体积蛋白酶K,震荡;
S2.加入2~5体积的第一提取液溶液,震荡,离心,并在30~60℃静置;
S3.加入0.5~1.5体积第二提取溶液,震荡、离心,静置;其中,第二提取溶液含有体积比为0.5%~3%的辛基葡萄糖新戊二醇及磁珠;
S4.进行磁性分离,除去废液;
S5.加入2-6体积的第一洗涤液,震荡,进行磁性分离,除去废液;
S6.加入2-6体积的第二洗涤液,震荡,进行磁性分离,除去废液;
S7.重复S6;
S8.离心,并进行磁性分离,除去废液;静置;
S9.加入0.2-0.8体积的洗脱液,震荡混匀,洗脱磁珠,静置;再次行磁性分离,完成提取过程。
本发明与现有技术相比,通过调整提取溶液的组分,在提取溶液中添加辛基葡萄糖新戊二醇(OGNG),提高了提取效率,提取出的核酸含量和纯度更高,在PCR反应中表现出更高的检测灵敏度。
附图说明
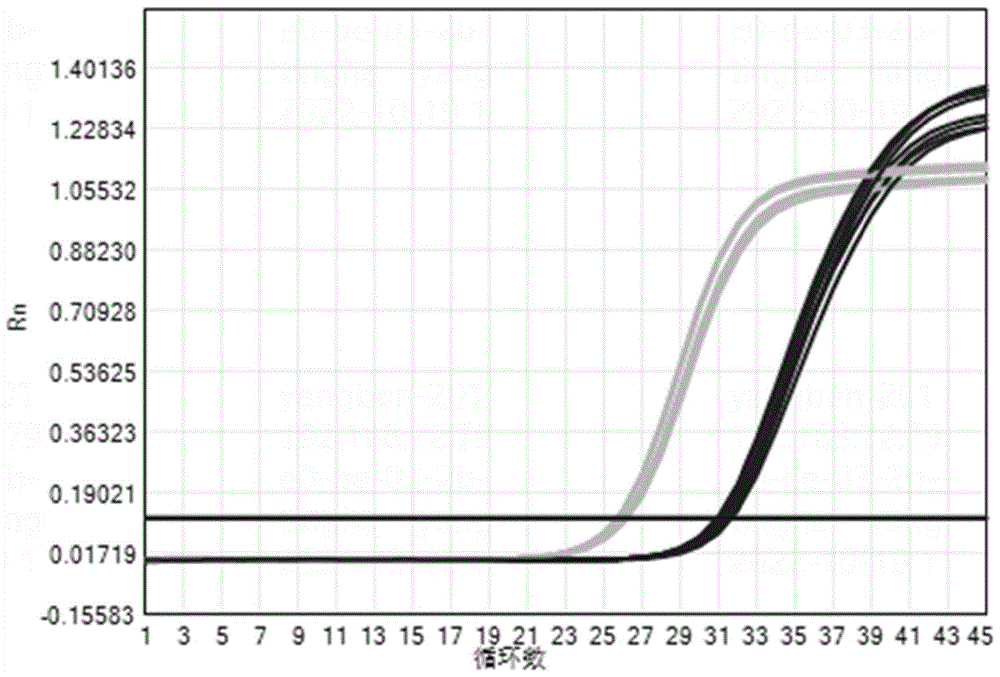
图1为本发明实施例1提取全血EB病毒样品检测结果;
图2为本发明对比例1提取全血EB病毒样品检测结果;
图3为本发明对比例2提取全血EB病毒样品检测结果。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。
本发明实施例为提高对血液中核酸的提取效率,开发了基于磁珠法的血液中核酸提取或纯化试剂盒,该提取试剂基于磁珠法原理,具备较高的提取效率,无需预处理就能够在全血中得到较高质量的核酸;同时,该提取试剂,还可以适配半自动提取仪器,采用预分装的生产工艺,缩短整体提取时间,提高效率。
本发明实施例提供方案如下:
核酸提取试剂盒包括预裂解液、多种提取溶液,至少一种提取溶液中含有体积比为0.5%~3%的辛基葡萄糖新戊二醇。
其中,核酸提取试剂盒可用于提取病毒DNA,也可以提取人DNA,本发明实施例中具体以EBV病毒为例。此外,本发明实施例提取溶液中添加辛基葡萄糖新戊二醇(OGNG),提高了提取效率,提取出的核酸含量和纯度更高,在PCR反应中表现出更高的检测灵敏度。
进一步地,所述预裂解液包括:5~15mmol/L SDS、0.2mmol~1mmol/L氯化钙。
进一步地,所述提取溶液包括第一提取溶液、第二提取溶液,所述第二提取溶液含有体积比为0.5%~3%的辛基葡萄糖新戊二醇、0.2~0.7mg/mL磁珠。
更进一步地,所述第一提取溶液包括1~5mol/L盐酸胍、10~200mmol/L TrisHCl、1~5mol/L硫氰酸胍、1~50mmol/L EDTA、0.01~0.5mmol/L的二硫苏糖醇。
更进一步地,所述第二提取溶液包括0.5mol/L~1mol/LNaCl,体积比为15%-30%的异丙醇、体积比为0.5%~3%的辛基葡萄糖新戊二醇以及0.2~0.7mg/mL磁珠。
进一步地,所述血液中核酸提取试剂盒还包括第一洗涤液、第二洗涤液、洗脱液。
更进一步地,所述第一洗涤液包括:体积比为10%~20%的异丙醇、体积比为0.1%~5%的NP 40、0.5~2mol/L的硫氰酸胍、1~50mmol/L EDTA、0.01~0.5mmol/L的二硫苏糖醇;第二洗涤液包括:10~200mmol/LTris HCl、无水乙醇,洗脱液包括:10~200mmol/L的Tris~HCl、1~50mmol/L的EDTA。
其中,应当注意的是,上述第一洗涤液、第二洗涤液和洗脱液成分为本发明实施例较优方案,但对于本领域技术人员来说,也可以采用已知的其他洗涤液和洗脱液进行替换。无水乙醇的用量具体可根据本行业人员经验设置。
进一步地,所述血液中核酸提取试剂盒还包括蛋白酶K。
本发明述血液中核酸提取试剂盒的使用方法,包括步骤如下:
S1.取1体积的样本,加入0.15~0.4体积的裂解液,加入0.05~0.15体积蛋白酶K,震荡;
其中,本发明实施例直接将样本进行裂解处理,无需预处理操作,进一步简化了提取流程;
S2.加入2~5体积的第一提取液溶液,震荡,离心,并在30~60℃静置;
S3.加入0.5~1.5体积第二提取溶液,震荡1min,瞬时离心,室温静置5min;
S4.进行磁性分离,除去废液;
S5.加入2-6体积的第一洗涤液,震荡30s,进行磁性分离2min,除去废液;
S6.加入2-6体积的第二洗涤液,震荡30s,进行磁性分离2min,除去废液;
S7.重复S6;
S8.离心,并进行磁性分离,除去废液;静置5min;
S9.加入0.2-0.8体积的洗脱液,震荡混匀,洗脱磁珠,静置10min;再次行磁性分离3min,完成提取过程。
为具体说明本发明实施例的方案及效果,现提供实施例1及对比例1、对比例2进行说明,实施例1及对比例1、对比例2的试剂盒各组分如下:
一、将本发明实施例1及对比例1-2采用下述操作步骤为:
S1随机抽取的EBV全血样本10例,震荡混匀后取200μL样本加入到1.5mL离心管中,加入45μL预裂解液PL,加入20μL蛋白酶K,震荡10s;
S2加入700μL第一提取溶液,震荡1min,瞬时离心,60℃静置12min。
S3加200μL第二提取溶液,震荡1min,瞬时离心,室温静置5min;
S4将离心管置于磁性分离器上,2min后缓慢吸弃废液(*注意不要碰到吸附于管壁内侧的磁珠);
S5加入800μL第一洗涤液,震荡30s,将离心管置于磁性分离器上,2min后缓慢吸弃废液(*注意不要碰到吸附于管壁内侧的磁珠);
S6加入800μL第二洗涤液,震荡30s,将离心管置于磁性分离器上,2min后缓慢吸弃废液(*注意不要碰到吸附于管壁内侧的磁珠);
S7重复上述步骤一次;
S8瞬时离心,将离心管置于磁性分离器上,小心吸弃管底液体,室温静置5min(*注:乙醇残留会对后续实验造成不良影响,需保证乙醇充分挥发;同时不要干燥太长时间,以免磁珠挂壁难以洗脱);
S9加入100μL洗脱液,震荡混匀30s,将离心管壁上磁珠洗脱到管底,室温静置10min(也可以选择56℃静置10min,可提高部分复杂样本的核酸洗脱效率);将离心管再次置于磁性分离器上磁吸3min,然后将洗脱下来的核酸转移到新的1.5mL离心管中,完成核酸提取。
二、对本发明实施例1及对比例1-2所获取核酸进行检测如下:
取10μL提取后的核酸,用EB病毒核酸检测试剂盒(PCR-荧光探针法)进行检测。
三、测试结果
1.洗脱液中DNA的含量和纯度比对:
对本发明实施1、对比例1~2中的提取试剂对全血样本进行提取,提取完成后,使用微量紫外分光光度计测定洗脱液中DNA的含量和纯度,具体如表1所示
2.核酸检测结果比对:
对本发明实施1、对比例1~2提取全血EB病毒样本(400copies/mL),进行核酸检测结果如下(具体见图1~图3所示,图中深色线为EBV~DNA基因和浅色线为内标检测);
全血EBV样本400copies/mL灵敏度测试
可看出,本发明实施例1通过采用辛基葡萄糖新戊二醇,可提取低至400copies/mL的EBV样本且可以准确检出,自动化仪器提取96例样品的时间为35分钟。与对比例1~2相比,本发明实施例1在提取溶液中添加OGNG,更有效地提取EBV病毒,扩增曲线Ct值合适,检出率和Ct值比对均好,充分体现了其灵敏度高、操作简单的特点,特别适合血液病原体的检测与筛查,快速准确获得检测结果(本发明实施例1在循环39次时,Rn值便与内标相近,而对比例1、对比例2均需要达到45次循环,才能有较高的Rn值,且本发明实施例1在循环45次时的Rn值远高于对比例2在45次循环时的Rn值)。
3.对血清、血浆和全血EBV样本的测试
用实施例1的试剂盒测试血清、全血、血浆中EBV样本,结果如下所示
可看出,本发明实施例1的试剂盒适用于血浆、血清、全血样本等,具有适用范围广的优点,配合具体的使用方法,可对低浓度的EBV病毒进行有效提取及检出,灵敏度高,检出效率好。
综上所述,本发明实施例具有如下优点:
1.本发明实施例的试剂盒从简化操作步骤出发,无需进行预处理,可以进行手工提取、半自动核酸提取仪器;
2.本发明实施例试剂盒可适用于全血、血浆、血清等样本的核酸提取;
3.本发明实施例还采用能够适用于上述各种样本类型的预分装好的核酸提取试剂,可搭配核酸提取设备,经实际测试,可通过半自动仪器提取方案,在35分钟之内提取48或96例样本与传统方案(对比例1、对比例2)相比,极大程度提高了核酸提取效率和报告发送时间,提高检测通量,进一步降低了成本且简单高效;
4.核酸提取得率高,所得核酸纯度较好,从而提高检测灵敏度,降低漏检和核酸提取不完全造成定量偏差,从而很好地反映样本的真实浓度。
最后应当说明的是,以上实施例仅用以说明本发明的技术方案而非对其限制,尽管参照上述实施例对本发明进行了详细的说明,所属领域的普通技术人员应当理解,技术人员阅读本申请说明书后依然可以对本发明的具体实施方式进行修改或者等同替换,但这些修改或变更均未脱离本发明申请待批权利要求保护范围之内。
