检测隐球菌的样本分析仪、方法以及计算机可读存储介质
文献发布时间:2023-06-19 11:52:33
技术领域
本申请涉及体外诊断领域,特别是涉及一种检测样本中的隐球菌的样本分析仪、方法以及计算机可读存储介质。
背景技术
隐球菌是一种常见的能引起人体侵袭性感染的真菌。隐球菌属(Cryptococcus)包括17种和18个变种,对人致病的最主要是新生隐球菌(Cryptococcus neoformans)。新生隐球菌广泛分布于自然界,也可存在于人体体表、口腔和肠道中。
隐球菌一般为外源性感染。经呼吸道侵入人体,由肺经血道播散时可侵犯所有脏器组织,最常见的部位是中枢神经系统。新生隐球菌病好发于细胞免疫功能低下者,如AIDS、恶性肿瘤、糖尿病、器官移植及大剂量使用糖皮质激素的患者。近20年来,隐球菌的发病率越来越高,在国外已成为AIDS病最常见的并发症之一,是AIDS死亡的首要原因。在免疫抑制患者中,隐球菌感染的发病率约为5%~10%,在AIDS患者中,隐球菌的感染率可高达30%。据统计,全球每年约有100万人感染隐球菌,死亡率可高达63%。在国内已将隐球菌病与病毒性肝炎等同列为乙类传染性疾病,是人类面临的一种严重的真菌病。
目前隐球菌的检测方法有墨汁负染法、培养鉴定法、抗原检测法、抗体检测法、核酸检测法等。
脑脊液墨汁负染法是目前临床上最常用的隐球菌检测手段。致病性隐球菌菌体外有宽厚荚膜,折光性强,用墨汁负染色时,荚膜包裹着菌体使其不被墨汁着色,因此可以见到圆形透亮菌体外包裹着一较厚的空白带,而脑脊液中的正常细胞、其他病原菌及非致病性隐球菌被墨汁染成黑色,在显微镜下不能被观察到。
培养鉴定法是将标本接种在沙氏培养基上,致病性隐球菌在25℃和37℃孵育均可生长,而非致病性隐球菌在37℃时不生长。培养2~5天后观察菌落形态特点,取菌落进行生化鉴定。新生隐球菌酚氧化酶试验阳性,脲酶试验阳性,能同化葡萄糖、半乳糖、蔗糖、肌醇和棉子糖,但不能发酵糖和醇类。
抗原检测法即用乳胶凝集试验、ELISA、多克隆抗体和单克隆抗体法等免疫学方法检测脑脊液或血浆中隐球菌荚膜多糖特异性抗原的方法,其中以乳胶凝集试验(latexagglutination test,LAT)最常用。LAT是一种间接凝集试验,使用聚苯乙烯胶乳颗粒作为载体,将可溶性抗体与聚苯乙烯胶乳颗粒结合,制备成致敏胶乳颗粒,然后与待测标本中的抗原发生,多个胶乳颗粒发生交联,出现凝集。
抗体检测法使用放射免疫法和试管凝集试验以检测血清中的隐球菌抗体。
核酸检测法使用聚合酶链反应(Polymerase Chain Reaction,PCR)检测样本中致病性隐球菌的特异性核酸序列,一般为隐球菌荚膜相关蛋白基因(CAP10)。
墨汁负染法和培养鉴定法的检测灵敏度较低,且培养鉴定法的培养时间较长。抗原、抗体检测法和核酸检测法虽然灵敏度较高,但其假阳性率较高,检测成本较高,且这类检测并非常规检测项目,是否进行这类检测需要根据临床医生的经验来判断,因此主观因素也是制约这类检测项目开展的原因之一。
因此,需要开发更为方便且准确的检测隐球菌的方法。
发明内容
本申请的目的在于提供一种便捷、快速,且准确的检测隐球菌的样本分析仪及方法。
为此,本申请第一方面提供一种样本分析仪,所述样本分析仪包括:
采样装置,具有带吸移管嘴的吸移管并且具有驱动装置,该驱动装置用于驱动所述吸移管通过所述吸移管嘴定量吸取待测样本;
样本制备装置,具有至少一个反应池和试剂供应部,其中,所述至少一个反应池用于接收采样装置所吸取的待测样本,所述试剂供应部将溶血试剂和荧光试剂提供给所述至少一个反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的溶血试剂和荧光试剂在所述反应池中混合,以制备成待测试样;
光学检测装置,包括光源、流动室、至少一个散射光检测器和荧光检测器,所述待测试样的粒子可逐个通过所述流动室,所述光源所发射的光照射所述流动室中的粒子以产生光学信息,所述至少一个散射光检测器用于收集至少一种散射光强度信息,所述荧光检测器用于收集荧光强度信息,其中所述光学信息包括所述至少一种散射光强度信息和所述荧光强度信息;以及
控制装置,其与所述光学检测装置电连接并包括处理器和存储有计算机程序的存储介质,其中,所述控制配置为当所述计算机程序被所述处理器执行时,执行以下步骤:从所述光学检测装置获取所述光学信息中的至少两种光强度信息,并且根据所述至少两种光强度信息区分出所述待测样本中的隐球菌粒子群。
本申请第二方面提供另一种样本分析仪,所述样本分析仪包括:
采样装置,具有带吸移管嘴的吸移管并且具有驱动装置,该驱动装置用于驱动所述吸移管通过所述吸移管嘴定量吸取待测样本;
样本制备装置,具有至少一个反应池和试剂供应部,其中,所述至少一个反应池用于接收采样装置所吸取的待测样本,所述试剂供应部配置为用于将溶血试剂提供给所述至少一个反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的溶血试剂在所述至少一个反应池中混合,以制备成待测试样;
光学检测装置,包括光源、流动室、第一散射光检测器和第二散射光检测器,所述待测试样的粒子可逐个通过所述流动室,所述光源所发射的光照射所述流动室中的粒子以产生光学信息,所述第一散射光检测器用于收集前向散射光强度信息,所述第二散射光检测器用于收集侧向散射光强度信息,其中所述光学信息包括所述前向散射光强度信息和所述侧向散射强度信息;以及
控制装置,其与所述光学检测装置电连接并包括处理器和存储有计算机程序的存储介质,其中,所述控制配置为当所述计算机程序被所述处理器执行时,执行以下步骤:从所述光学检测装置获取所述光学信息,并且根据所述光学信息区分出所述待测样本中的隐球菌粒子群。
本申请第三方面提供一种检测样本中的隐球菌的方法,所述方法包括以下步骤:
处理待测样本以得到待测试样,所述处理待测样本包括使待测样本与溶血试剂混合;
使所述待测试样中的粒子逐个通过光学检测器,获得所述待测试样中的各个粒子的光学信息;
根据所述光学信息区分出所述待测样本中的隐球菌粒子群。
本申请第四方面提供另一种检测样本中的隐球菌的方法,所述方法包括以下步骤:
处理待测样本的第一部分样本以得到第一待测试样,所述处理待测样本的第一部分样本包括使所述第一部分样本与第一溶血试剂和第一荧光染料混合;
使所述第一待测试样中的粒子逐个通过光学检测器,获得所述第一待测试样中的各个粒子的第一光学信息;
根据所述第一光学信息区分出所述第一待测试样中的隐球菌粒子群并计数,以获得第一隐球菌粒子计数值;
处理待测样本的第二部分样本以得到第二待测试样,所述处理待测样本的第二部分样本包括使所述第二部分样本与不同于所述第一溶血试剂的第二溶血试剂混合;
使所述第二待测试样中的粒子逐个通过所述光学检测器,获得所述第二待测试样中的各个粒子的第二光学信息;
根据所述第二光学信息区分出所述第二待测试样中的隐球菌粒子群并计数,以获得第二隐球菌粒子计数值;
根据所述第一隐球菌粒子计数值和所述第二隐球菌粒子计数值,判断所述待测样本中是否存在隐球菌感染。
本申请第五方面提供一种计算机可读存储介质,所述计算机可读存储介质上存储有计算机程序,其特征在于,该计算机程序被处理器执行时实现上述根据本申请第三和第四方面所述的方法的各个步骤。
本发明利用致病性隐球菌具有厚荚膜的特性,利用诸如全自动血液分析仪一类仪器,可快速准确地对样本是否存在隐球菌感染进行检测。
附图说明
附图中,相同的附图标记指代相同或相似的部件。
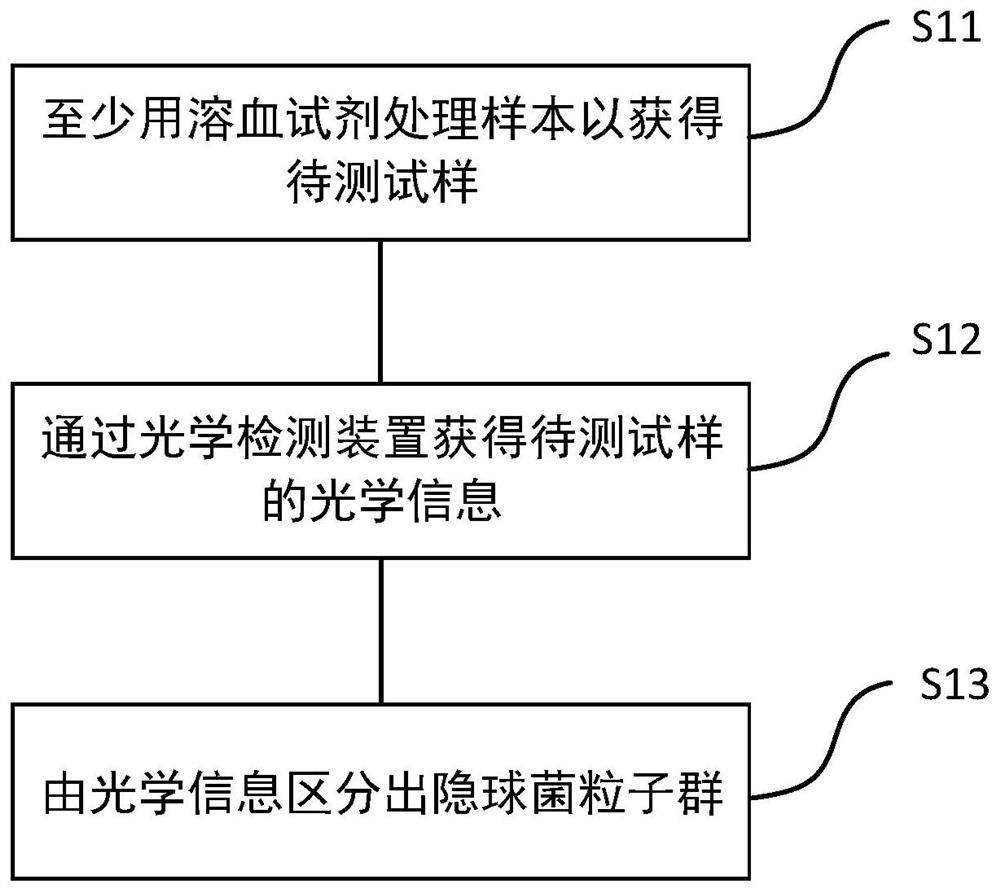
图1为根据本发明的检测隐球菌的方法流程示意图;
图2为根据本发明的一种实施方式检测隐球菌的方法流程示意图;
图3为根据本发明的第一种实施方式检测隐球菌的原理示意图;
图4为根据本发明的第一种实施方式检测隐球菌的方法流程示意图;
图5为根据第一种实施方式检测脑脊液样本中隐球菌的方法流程示意图;
图6为根据图5所示检测方法得到的隐球菌阴性和阳性的脑脊液样本的光学散点图;
图7为根据第一种实施方式检测血液样本中隐球菌的方法流程示意图;
图8为根据本发明的第二种实施方式的检测隐球菌的原理示意图;
图9为根据本发明的第二种实施方式检测隐球菌的方法流程示意图;
图10为根据图9所示检测方法得到的隐球菌阴性和阳性的脑脊液样本的光学检测散点图;
图11为根据第二种实施方式检测血液样本中隐球菌的方法流程示意图;
图12为根据本发明的另一种检测隐球菌的方法流程示意图;
图13为根据本发明的样本检测仪的结构示意图;和
图14为根据本发明的光学检测装置的结构示意图。
具体实施方式
下面将结合本发明具体实施例及附图,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明的一部分实施方式,而不是全部的实施方式。基于本发明中的实施方式,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施方式,都属于本发明保护的范围。
在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
本文中提及的‘隐球菌’,除非另外指明,是指隐球菌属(Cryptococcus)中最常见的致病性新生隐球菌(Cryptococcus neoformans)。
本文中提及的‘样本’,除非另外指明,是指体液样本或血液样本,体液样本诸如为脑脊液、胸水、腹水、心肌液、滑液、腹膜透析液或腹膜清洗得到的液体等。
本文中提及的‘溶血剂’,除非另外指明,是指能够使红细胞裂解,同时使白细胞保持基本细胞形态的试剂。
本文中提及的‘荧光染料’,除非另外指明,是指能够特异性与核酸物质(如DNA、RNA)结合并在激发下发出特定波长荧光的染料。用于本发明的核酸特异性染料没有特别限制。商品化的核酸荧光染料及一些专利申请中已经公开的核酸特异性荧光染料均可用于本发明。其中商品化的核酸荧光染料,可列举的有Thermofisher公司的SYTO系列核酸染料。此外,中国专利申请CN201010022414.6中公开的荧光染料、CN200910109215.6中公开的花青素类染料、CN200810216864.1中公开的荧光染料等,均可用于本发明。以上专利文献的全部内容通过引用并入本申请。
本文中提及的样本检测原理,指的是血液细胞分析仪吸取体液或血液样本后,样本首先经溶血剂以及可选地经荧光染料处理,红细胞被溶血剂破坏溶解,其他粒子、例如白细胞不能被溶解,荧光染料可在溶血剂的帮助下进入其他粒子、例如白细胞的细胞核,并与细胞核中的核酸物质结合。接着,经处理的样本中的粒子逐个通过激光检测孔,激光束穿过粒子时,粒子本身的特性(如体积、染色程度、细胞内容物大小及含量、细胞核密度等)可阻挡或改变激光束的方向,产生与其特征相应的各种角度的散射光,这些散射光经信号检测器接收后可以获得粒子结构和组成的相关信息。其中,前向散射光(Forward scatter,FS)反应粒子的数量和体积,侧向散射光(Side scatter,SS)反应粒子内部结构(如粒子内颗粒或细胞核)的复杂程度,荧光信号(Fluorescence,FL)反应粒子中核酸物质的含量。利用这些参数可以对样本中的粒子进行分类和计数。
本发明人发现溶血剂作用于致病性隐球菌的厚荚膜可以产生不同于样本中其他粒子的光学特性,从而能够利用常规血液分析仪的溶血通道检测样本中的致病性隐球菌。且本发明的检测方法不对溶血通道的正常检测产生影响,因而还可同时对样本中常规利用溶血通道可以检测的指标进行检测。
由此,本申请提出一种检测样本中的隐球菌的方法。参见图1,其中示出了本方法的流程示意图。所述方法包括以下步骤:
S11步骤,处理待测样本以得到待测试样,所述处理待测样本包括至少用溶血试剂处理所述样本;
S12步骤,使所述待测试样中的粒子逐个通过光学检测器,获得所述待测试样中的各个粒子的光学信息;以及
S13步骤,根据所述光学信息区分出所述待测样本中的隐球菌粒子群。
本发明的溶血试剂中可含有常规用于检测血细胞的那些溶血剂。例如,可用于本发明的溶血剂可以选自表面活性剂(如季铵盐类阳离子表面活性剂,非离子型表面活性剂,例如烷醇聚氧乙烯醚类表面活性剂等)、烷基糖苷、三萜皂苷、甾族皂苷等。所述溶血试剂中还可含有缓冲剂(如磷酸及其盐、柠檬酸及其盐、乙酸及其盐等)、防腐剂(如叠氮钠、ProClin系列等)、金属螯合剂(如EDTA的钠盐)、渗透压调节剂(如氯化钠等)等组分。
隐球菌的菌体尺寸范围较宽,约为5~20μm,反映在前向散射光强度呈由小到大延伸的趋势,其中部分与白细胞的前向散射光强度重合。而另一方面,隐球菌菌体内部结构的复杂程度比白细胞低,因此隐球菌的侧向散射光强度略低于白细胞。
因此,在一实施例中,在用溶血剂处理待测样本之后,可根据所述光学信息中的前向散射光强度信息和侧向散射光强度信息,区分出所述待测样本中的隐球菌粒子群。
进一步可对所述待测试样中的隐球菌粒子群进行计数,并可选地,当所述隐球菌粒子群的计数值超过预定值时,提示所述待测样本中存在隐球菌感染。
根据一种实施方式,可进一步用荧光染料试剂处理所述待测样本。
在该实施方式中,荧光染料试剂中可含有能够对核酸染色的荧光染料。本发明对于荧光染料的种类没有特别限制,可根据需要采用任何如上定义的荧光染料。
荧光染料试剂中同样可以包含诸如缓冲剂、表面活性剂、防腐剂、金属螯合剂、渗透压调节剂等组分,在此不再赘述。
在具体实施方式中,溶血试剂和荧光染料试剂可以是两种单独的试剂,先后或同时与样本混合以制备待测试样;或者溶血试剂和荧光染料试剂也可以合并为同时包含溶血剂和荧光染料的一种试剂。
参见图2,其中示出了本实施方式的流程示意图。如图2所示,在该实施方式中,首先在S110步骤中,待测样本与溶血试剂以及荧光染料试剂(或者是含有溶血剂和荧光染料的试剂)混合,反应后得到待测试样。在S120步骤中,使待测试样中的粒子逐个通过光学检测装置,获得试样中各粒子的光学信息。以及在S130步骤中基于检测到的荧光强度信息和至少一种散射光强度信息、例如前向散射光强度信息和/或侧向散射光强度信息可以将待测试样中的隐球菌粒子与其他粒子区分开。
在S130步骤中,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出所述待测样本中的隐球菌粒子群。
可以理解地,在在S130步骤中,也可以根据所述光学信息中的前向散射光强度信息和侧向散射光强度信息,区分出所述待测样本中的隐球菌粒子群。
进一步地,可对所述待测试样中的隐球菌粒子群进行计数,并可选地,当所述隐球菌粒子群的计数值超过预定值时,提示所述待测样本中存在隐球菌感染。
根据一种具体情况,所述待测样本为体液样本,尤其为脑脊液样本。在该情况下,可以将待测体液样本用溶血试剂处理,通过光学检测后,根据前向和侧向散射光强度信息区分出样本中的隐球菌粒子群。或者,也可以将待测体液样本用溶血试剂和荧光染料试剂处理,通过光学检测后,根据至少一种散射光强度信息(前向散射光强度信息和/或侧向散射光强度信息)和荧光强度信息来区分出样本中的隐球菌粒子群。
对于待测样本为体液样本的情况,还可根据具体需要,由所述光学信息中的侧向散射光强度信息和荧光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,进一步区分出白细胞粒子群、有核细胞粒子群、单个核细胞粒子群、多个核细胞粒子群中的至少一种粒子群。更进一步地,还可对白细胞粒子群、有核细胞粒子群、单个核细胞粒子群、多个核细胞粒子群中的至少一种粒子群进行计数。
根据另一种具体情况,所述待测样本可为血液样本。同样地,在该情况下,可用溶血试剂对血液样本进行处理得到待测试样,然后对待测试样进行光学检测以获得包括前向散射光强度信息和侧向散射光强度信息的光学信息,再通过所获得的光学信息来区分隐球菌粒子群。此外,也可同时通过所获得的光学信息、即根据前向散射光强度信息和侧向散射光强度信息区分出试样中包括淋巴细胞、单核细胞、中性粒细胞和嗜酸性粒细胞的白细胞亚群。并可进一步对隐球菌粒子群和所述区分出的白细胞亚群进行计数,并可选地,当所述隐球菌粒子群的计数值超过预定值时,提示所述待测样本中存在隐球菌感染。
根据另一种实施方式,当所述待测样本为血液样本时,可用溶血试剂和荧光染料试剂(或者用包含溶血剂和荧光染料的试剂)对血液样本进行处理得到待测试样。在该实施方式中,对待测试样进行光学检测,以获得包括荧光强度信息和至少一种散射光强度信息的光学信息。在一些实施例中,一方面通过所获得的光学信息(如,利用一种或两种散射光强度信息和荧光强度信息)来区分隐球菌粒子群;另一方面,可同时根据所述光学信息中的侧向散射光强度信息和荧光强度信息,优选地根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息区分出包括淋巴细胞、单核细胞、中性粒细胞和嗜酸性粒细胞的白细胞亚群和/或区分出幼稚粒细胞群,并可进一步选择对区分出的白细胞亚群和/或幼稚粒细胞群进行计数。在另一些实施例中,一方面通过所获得的光学信息来区分隐球菌粒子群;另一方面,可根据所述光学信息中的前向散射光强度信息和荧光强度信息,优选地根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出所述待测样本中的有核红细胞粒子群和嗜碱性粒细胞亚群中的至少一种粒子群。并可进一步选择对区分出的有核红细胞粒子群和嗜碱性粒细胞亚群中至少一种粒子群进行计数。
进一步地,所述根据所述光学信息区分出所述待测样本中的隐球菌粒子群,包括:
根据所述光学信息生成二维或三维散点图;
根据所述二维或三维散点图获得隐球菌粒子特征区域;以及
将所述隐球菌粒子特征区域中的粒子识别为隐球菌粒子。
基于致病性的新生隐球菌的菌体外有宽厚荚膜的特点,本发明人进一步发现具有不同pH值的红细胞溶血剂可对隐球菌的荚膜产生不同的作用。在中性条件下,如pH 6.5~7.5,溶血剂基本不会对隐球菌的荚膜造成破坏,即隐球菌菌体外的宽厚荚膜能够在一定程度上阻止中性溶血剂的“打孔作用”,进而在一定程度上阻止荧光染料进入隐球菌菌体。而在该pH条件下,溶血剂可使红细胞的细胞膜破裂,白细胞的细胞膜也会受到一定破坏,造成“打孔作用”,荧光染料通过白细胞的细胞膜上的孔径进入细胞,与白细胞中的核酸物质结合。而在酸性条件下,如pH 2~4,溶血剂也会对隐球菌的荚膜造成一定破坏,产生类似白细胞细胞膜的“打孔作用”,使得荧光染料能够进入隐球菌菌体。
因此根据更具体的实施方式,所述溶血试剂可具有约2.0~4.0的pH值,优选具有约3.0的pH值;或所述溶血试剂可具有约6.5~7.5的pH值,优选具有约7.0的pH值。以下分别说明在不同pH值下的具体实施方式。
根据第一种实施方式,用溶血试剂并进一步用荧光染料试剂处理样本,得到待测试样。在该实施方式中,溶血试剂可具有约6.5~7.5的pH值,优选具有约7.0的pH值。待测试样中,在溶血剂的作用下红细胞破碎;白细胞的细胞膜被打孔,荧光染色剂通过细胞膜上的孔进入白细胞内部,使其中的核物质被染色;而隐球菌的荚膜仍保持基本上完好,菌体内核物质基本上不能被染色,如图3所示。
如图4所示,在该实施方式中,首先在S111步骤中,样本与溶血试剂以及荧光染色试剂混合、反应后得到待测试样。同样的,在对样本进行处理时,可以先后加入溶血试剂和荧光染料试剂,也可同时加入。溶血试剂和荧光染料试剂可以分别单独存在于不同的试剂中,也可以存在于同一试剂中。此外,还可对样本进行其他必要处理,例如在一些实施方式中,样本可进行稀释处理。
在S112步骤中,使待测试样中的粒子逐个通过经光学检测装置,获得试样中各粒子的光学信息。
在该实施方式中,由于隐球菌菌体内的核物质基本上不能被荧光染料染色,因此表现出极低的荧光强度信号,而白细胞等有核细胞被染色,而呈现一定荧光强度。另一方面,隐球菌菌体内部结构的复杂程度比白细胞低,因此隐球菌的侧向散射光强度略低于白细胞。再一方面,隐球菌的菌体尺寸范围较宽,约为5~20m,反映在前向散射光强度呈由小到大延伸的趋势,其中部分与白细胞的前向散射光强度重合,隐球菌粒子的最大前向散射光强度大于白细胞粒子的最大前向散射光强度。因此,在S113步骤中可基于检测到的荧光强度和前向散射光强度,尤其是根据荧光强度、前向散射光强度和侧向散射光强度将隐球菌粒子与试样中的其他粒子区分开。
接着在步骤S114中对区分出的隐球菌粒子群进行计数,并在步骤S115中将计数值与预定值进行比较,可以获知被测样本是否存在隐球菌感染。
在该实施方式中,还可进一步获得样本中其他粒子的信息。
例如,参见图5,其中示出了使用中性溶血剂的情况下对于体液样本、尤其是脑脊液样本的检测步骤。S1111步骤和S1122步骤参见图4所示的S111步骤和S112步骤的描述。在获得试样中各粒子的光学信息后,一方面,在S1113步骤中,可根据光学信息(具体地,可以是前向散射光强度信息和荧光强度信息,或者可以是前向散射光强度信息、侧向散射光强度信息和荧光强度信息)区分出隐球菌粒子群;并可进一步在S1114步骤中对隐球菌粒子群进行计数;进而,在S1115步骤中将计数结果与预定值进行比较,当计数值超过预定值时可以判定该脑脊液样本中存在隐球菌感染。另一方面,在S1116步骤中,可进一步根据需要,根据测得的光学信息中的侧向散射光强度信息和荧光强度信息,尤其是前向散射光强度信息、侧向散射光强度信息和荧光强度信息区分出白细胞粒子群、有核细胞粒子群、单个核细胞(mono-nucleated cells)粒子群、多个核细胞(poly-nucleated cells)粒子群中的至少一种粒子群;还可进一步在S1117步骤中对至少一种粒子群进行计数。
进一步参见图6,其中显示了使用深圳迈瑞生物医疗电子有限公司的BC-6800血细胞分析仪及其DIFF通道配套的68-LD溶血试剂和相应的荧光染料对两种脑脊液样本检测后的由光学信息形成的散点图,该配套的68-LD溶血试剂具有约7.0的pH值。其中,在隐球菌为阳性的脑脊液样本的散点图中,三维散点图和荧光-前向散射光强度的二维散点图中可以将隐球菌与其他粒子区分开(圈出的范围为对应隐球菌的光学信息),而在隐球菌为阴性的脑脊液样本的散点图中相应的位置处没有检测到隐球菌粒子的光学信息。
参见图7,其中示出了使用中性溶血剂的情况下对于血液样本的具体检测步骤。图7中的步骤S1121、S1122与前述图4中的步骤S111、S112基本相同,在图7所示的实例中,用含有溶血剂和荧光染料的试剂在常规血液仪(例如深圳迈瑞生物医疗电子有限公司的BC-6800血细胞分析仪DIFF通道配套试剂)对血液样本进行处理并检测。S1123、S1124、S1125步骤分别与图4所示实例中S113步骤以及S114、S115步骤相同。在S1126步骤中,执行常规的DIFF通道中对白细胞的检测步骤,即,可根据所获得的光学信息区分出白细胞粒子群,并进一步对白细胞亚群进行区分。具体地,根据所测得光学信息中的侧向散射光强度信息和荧光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,可区分出包括淋巴细胞、单核细胞、中性粒细胞和嗜酸性粒细胞的白细胞亚群和/或区分出幼稚粒细胞群。进一步地,在S1127步骤中,可对区分出的上述白细胞亚群和/或幼稚粒细胞群进行计数。
根据第二种实施方式,用溶血试剂处理样本,得到待测试样。在该实施方式中,溶血试剂可具有约2.0~4.0的pH值,优选具有约3.0的pH值。待测试样中,在酸性溶血剂的作用下红细胞破碎;白细胞的细胞膜被打孔,同时隐球菌的荚膜也受到一定程度的破坏,从而在其细胞膜上形成类似白细胞的细胞膜的打孔现象。如果进一步用荧光染色试剂对样本进行染色,则染料会通过细胞膜上的孔进入白细胞内部,并且也进入隐球菌菌体内部,使白细胞和隐球菌的核物质均被染色,如图8所示。
在该实施方式中,参见图9,S121步骤中样本中的红细胞在酸性溶血剂的作用下破碎,而白细胞和隐球菌均受到溶血剂作用以及由于各自的体积和复杂程度的差异,呈现出明显的散射光强度上的差异性,从而能够将隐球菌与白细胞等其他粒子区分开。如果进一步对样本进行荧光染色试剂染色,则白细胞和隐球菌的核酸物质均能够被染色。S122步骤中,使试样中的粒子逐一通过光学检测装置获得待测试样中各粒子的光学信息。在步骤S123中,根据光学信息区分出隐球菌粒子群。其中,在未经荧光染色试剂处理的情况下,可根据前向散射光强度信息和侧向散射光强度信息区分出隐球菌粒子群。在使用了荧光染色试剂进行处理时,可根据前向散射光强度信息和侧向散射光强度信息,尤其是根据前向散射光强度信息、侧向散射光强度信息和荧光强度信息将隐球菌粒子与白细胞等其他粒子区分开。S124和S125步骤中,通过对区分出的隐球菌粒子群进行计数,并与预定值进行比较,可以获知被测样本是否存在隐球菌感染。
在该实施方式中,样本可以不用荧光染料处理,而仅用溶血试剂处理。同样的,如果需要用溶血试剂和荧光染料试剂共同进行处理,则二者可先后加入,也可同时加入。且所述样本还可进一步进行其他处理。
进一步参见图10,其中示出了使用深圳迈瑞生物医疗电子有限公司的BC-6800血细胞分析仪及其WNB通道配套的68-LN溶血试剂和相应的荧光染料对两种不同的脑脊液样本检测后的散点图,该配套的68-LN溶血试剂具有约3.0的pH值。在隐球菌为阳性的脑脊液样本的散点图中,三维散点图和前向散射光强度-侧向散射光强度二维散点图中可以将隐球菌与其他粒子区分开(圈出的范围为对应隐球菌的光学信息)。在隐球菌为阴性的脑脊液样本的三维散点图中以及前向散射光强度-侧向散射光强度的二维散点图中相应的位置处没有检测到隐球菌粒子的光学信息。
参见图11,其中示出了该实施方式中以血液为样本的一种具体实施方式。该实施方式利用诸如常规血液分析仪(如深圳迈瑞生物医疗电子有限公司BC-6800系列血细胞分析仪及其WNB通道配套试剂)在WNB通道进行检测。在S1221步骤中,在酸性条件下,用溶血试剂和荧光染料试剂处理血液样本以获得待测试样,并进一步在S1222步骤中使试样通过光学检测装置,以获取试样中各粒子的光学信息,即散射光强度信息和荧光强度信息。
接着在S1223~S1225步骤中,根据所述光学信息中的前向散射光强度信息和侧向散射光强度信息,尤其是根据前向散射光强度信息、侧向散射光强度信息和荧光强度信息区分出隐球菌粒子群,并可进一步对隐球菌粒子群进行计数,然后将隐球菌粒子群的计数值与预定值进行比较,以判断样本中是否存在隐球菌感染。
进一步地,也可以同时在S1226~S1227步骤中,根据所述光学信息中的前向散射光强度信息和荧光强度信息,尤其是根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息区分出有核红细胞粒子群和/或嗜碱性粒细胞亚群,并且进一步对有核红细胞粒子群和/或嗜碱性粒细胞亚群进行计数。
本发明还提供了另一种检测样本中的隐球菌的方法,其中,使用对隐球菌的荚膜产生不同作用的溶血剂分别处理待测样本的两个部分样本,获得待测样本中隐球菌的第一计数和第二计数,根据第一计数和第二计数来确定待测样本中是否存在隐球菌感染。
具体地,参见图12的方法流程图,在步骤S1310中,待测样本(体液样本或血液样本)被分为第一部分样本和第二部分样本。接着分别使用不同的溶血试剂对第一部分样本和第二部分样本进行处理。
在S1311~S1314步骤中,使用第一溶血试剂和第一荧光染料试剂处理第一部分样本以获得第一待测试样,并经光学检测装置检测获得第一待测试样的第一光学信息。然后根据第一光学信息区分出第一待测试样中的隐球菌粒子群,并对第一待测试样中的隐球菌粒子群进行计数,得到第一计数值。
在一些实施例中,第一光学信息包括前向散射光强度信息和荧光散射光强度信息,优选包括前向散射光强度信息、侧向散射光强度信息和荧光强度信息。
在一些实施例中,第一溶血试剂具有约6.5~7.5的pH值,优选具有约7.0的pH值。
同时或先后地,在S1321~S1324步骤中,使用不同于第一溶血剂的第二溶血试剂处理第二部分样本以获得第二待测试样,并经光学检测装置检测获得第二待测试样的第二光学信息。根据第二光学信息区分出第二待测试样的隐球菌粒子群,并对第二待测试样中的隐球菌粒子群进行计数,得到第二计数值。
在一些实施例中,第二光学信息包括前向散射光强度信息和侧向散射光强度信息。
在一些实施例中,步骤S1321包括:使第二部分样本与不同于第一溶血试剂的第二溶血试剂和不同于第一荧光试剂的第二荧光试剂混合。其中,第二光学信息包括前向散射光强度信息、侧向散射光强度信息和荧光强度信息。
在一些实施例中,第二溶血试剂具有约2.0~4.0的pH值,优选具有约3.0的pH值。
在步骤1330中,根据第一计数值和第二计数值,判断待测样本中是否存在隐球菌感染。例如,当第一计数值超过第一预设值,第二计数值超过第二预设值,且第一计数值与第二计数值的差值在预设范围内时,判断待测样本中存在隐球菌感染。
在一种具体的实施例中,例如通过样本分析仪的两个检测通道(例如深圳迈瑞生物医疗电子有限公司BC-6800系列血细胞分析仪的DIFF通道及其配套试剂和WNB通道及其配套试剂)同时分别对待测样本的第一部分样本和第二部分样本进行检测以得到第一隐球菌计数值和第二隐球菌计数值。
相应地,本申请进一步提供一种可检测隐球菌的样本分析仪。
参见图13,所述样本分析仪包括:第一机壳100、第二机壳200、采样装置10、样本制备装置30、光学检测装置50、控制装置70及输出部90。在实际应用中,输出部90可以为用户界面。光学检测装置50及数据处理装置70设置在第二机壳200的内部,例如可以分别设置在第二机壳200两侧。样本制备装置30例如设置在第一机壳100的内部,输出部90例如设置在第一机壳100的外表面并且用于显示样本分析仪的检测结果,例如显示隐球菌的检测结果给用户。
采样装置10具有带吸移管嘴的吸移管并且具有驱动装置,该驱动装置用于驱动所述吸移管通过所述吸移管嘴定量吸取待测样本。采样装置可将采集的血液样本输送至样本制备装置30。根据不同的实施方式,采样装置可采集多份血液样本,提供给样本制备装置的不同腔室进行不同的处理,并随后进行不同的检测。采样装置可用于吸取体液样本或血液样本。
样本制备装置30具有至少一个反应池和试剂供应部,其中,所述至少一个反应池用于接收采样装置所吸取的待测样本,所述试剂供应部将溶血试剂和荧光试剂提供给所述至少一个反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的溶血试剂和荧光试剂在所述反应池中混合,以制备成待测试样。
光学检测装置50包括光源、流动室、至少一个散射光检测器和荧光检测器,所述待测试样的粒子可在所述流动室内流动,所述光源所发射的光照射所述流动室中的粒子以产生光学信息,所述至少一个散射光检测器用于收集至少一种散射光强度信息,所述荧光检测器用于收集荧光强度信息,其中所述光学信息包括所述至少一种散射光强度信息和所述荧光强度信息。
如图14所示,其中示出了光学检测装置50的一个具体实例。该光学检测装置具有依次布置在一条直线上的光源101、光束整形组件102、流动室103和前向散射光检测器104。在流动室103的一侧,与所述直线成45°角布置有二向色镜106。通过流动室103中的粒子发出的侧向光,一部分透过二向色镜106,被与二向色镜106成45°角布置在二向色镜106后面的荧光检测器105捕获;另一部分侧向光被二向色镜106反射,被与二向色镜106成45°角布置在二向色镜106前面的侧向散射光检测器107捕获。
控制装置70与所述光学检测装置电连接并包括处理器和存储有计算机程序的存储介质,其中,所述控制装置配置为当所述计算机程序被所述处理器执行时,执行以下步骤:从所述光学检测装置获取所述光学信息中的至少两种光强度信息,并且根据所述至少两种光强度信息区分出所述待测样本中的隐球菌粒子群。
输出部90配置为输出对应所述样本中隐球菌的检测结果,以及可选地其他粒子的检测结果。
其中,样本、溶血试剂和荧光染色试剂如前所述,在此不再赘述。
在一些实施例中,所述至少一个散射光检测器包括用于收集前向散射光强度信息的前向散射光检测器,可选地包括用于收集侧向散射光强度信息的侧向散射光检测器。其中,所述控制装置70配置为当所述计算机程序被所述处理器执行时,执行以下步骤:
根据所述光学信息中的前向散射光强度信息和荧光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出所述待测样本中的隐球菌粒子群。
在一些实施例中,对于待测样本为脑脊液样本的情况,所述控制装置70配置为当所述计算机程序被所述处理器执行时,进一步执行以下步骤:
根据所述待测样本的光学信息中的侧向散射光强度信息和荧光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出白细胞粒子群、有核细胞粒子群、单个核细胞粒子群、多个核细胞粒子群中的至少一种粒子群,以及可选地对所述至少一种粒子群进行计数。
在一些实施例中,对于待测样本为血液样本的情况,所述控制装置配置为当所述计算机程序被所述处理器执行时,进一步执行以下步骤:
根据所述光学信息中的侧向散射光强度信息和荧光强度信息或根据所述光学信息中的前向散射光强度信息和侧向散射光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出包括淋巴细胞、单核细胞、中性粒细胞和嗜酸性粒细胞的白细胞亚群和/或区分出所述待测样本中的幼稚粒细胞群,以及可选地对区分出的白细胞亚群和/或幼稚粒细胞群进行计数,或者
根据所述光学信息中的前向散射光强度信息和荧光强度信息,优选根据所述光学信息中的前向散射光强度信息、侧向散射光强度信息和荧光强度信息,区分出所述待测样本中的有核红细胞粒子群和嗜碱性粒细胞亚群中的至少一种粒子群,以及可选地对所述至少一种粒子群进行计数。
进一步地,所述控制装置可配置为在根据所述至少两种光强度信息区分出所述待测样本中的隐球菌粒子群时,执行以下步骤:
根据所述至少两种光强度信息生成二维或三维散点图;
根据所述二维或三维散点图获得隐球菌粒子特征区域;和
将所述隐球菌粒子特征区域中的粒子识别为隐球菌粒子。
所述控制装置配置为当所述计算机程序被所述处理器执行时,还可进一步执行以下步骤:
对所述待测样本中的隐球菌粒子群进行计数;和
可选地,当所述隐球菌粒子群的计数值超过预定值时,提示所述待测样本中存在隐球菌感染。
本申请还提供了另一种样本分析仪,所述样本分析仪与图13所示的分析仪具有基本相同的结构,同样包括前述的第一机壳、第二机壳、采样装置、样本制备装置、光学检测装置、控制装置及输出部。
不同之处在于,该样本分析仪的样本制备装置具有至少一个反应池和试剂供应部,其中,所述至少一个反应池用于接收采样装置所吸取的待测样本,所述试剂供应部可将溶血试剂提供给所述至少一个反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的溶血试剂在所述反应池中混合,以制备成待测试样。
或者,可替代地,所述样本制备装置的试剂供应部可将溶血试剂和荧光染料试剂提供给所述至少一个反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的溶血试剂以及荧光染料试剂在所述反应池中混合,以制备成待测试样。
在一些实施例中,光学检测装置包括光源、流动室、第一散射光检测器和第二散射光检测器,并且优选地还包括荧光检测器。所述待测试样的粒子可在所述流动室内流动,所述光源所发射的光照射所述流动室中的粒子以产生光学信息,所述第一散射光检测器用于收集前向散射光强度信息,所述第二散射光检测器用于收集侧向散射光强度信息,其中所述光学信息包括所述前向散射光强度信息和所述侧向散射强度信息,并且优选地,当包括荧光检测器时,该荧光检测器用于收集荧光强度信息,且所述光学信息包括前向散射光强度信息、侧向散射强度信息和荧光强度信息。
同样地,控制装置与所述光学检测装置电连接并包括处理器和存储有计算机程序的存储介质,其中,所述控制配置为当所述计算机程序被所述处理器执行时,执行以下步骤:从所述光学检测装置获取所述光学信息,并且根据所述光学信息区分出所述待测样本中的隐球菌粒子群。
在一些实施例中,样本制备装置包括第一反应池和第二反应池,该样本制备装置的试剂供应部一方面将第一溶血试剂和第一荧光染料提供给第一反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的第一溶血试剂和第一荧光染料在所述第一反应池中混合,以制备成第一待测试样,另一方面试剂供应部还将第二溶血试剂提供给第二反应池,从而由所述采样装置所吸取的待测样本与由所述试剂供应部提供的第二溶血试剂在第二反应池中混合,以制备成第二待测试样。也就是说,所述控制装置配置为当所述计算机程序被所述处理器执行时,执行以下步骤:
控制所述样本制备装置制备第一待测试样,其方式为使所述待测样本的第一部分样本与第一溶血试剂和第一荧光试剂混合以得到所述第一待测试样;
控制所述光学检测装置对所述第一待测试样进行检测,以获取所述第一待测试样中的各个粒子的第一光学信息;
根据所述第一光学信息中的至少两种光强度信息区分出所述第一待测试样中的隐球菌粒子群并计数,以获得第一隐球菌粒子计数值;
控制所述样本制备装置制备第二待测试样,其方式为使所述待测样本的第二部分样本与不同于第一溶血试剂的第二溶血试剂混合以得到所述第二待测试样;
控制所述光学检测装置对所述第二待测试样进行检测,以获取所述第二待测试样中的各个粒子的第二光学信息;
根据所述第二光学信息中的至少两种光强度信息区分出所述第二待测试样中的隐球菌粒子群并计数,以获得第二隐球菌粒子计数值;
根据所述第一隐球菌粒子计数值和所述第二隐球菌粒子计数值,判断所述待测样本中是否存在隐球菌感染。
在一些实施例中,第一光学信息包括前向散射光强度信息和荧光强度信息,优选包括前向散射光强度信息、侧向散射光强度信息和荧光强度信息。
在一些实施例中,第二光学信息包括前向散射光强度信息和侧向散射光强度信息。
在一些实施例中,所述控制装置配置在控制所述样本制备装置制备所述第二待测试样时,执行以下步骤:
控制所述样本制备装置制备第二待测试样,其方式为使所述待测样本的第二部分样本与不同于第一溶血试剂的第二溶血试剂和不同于第一荧光试剂的第二荧光试剂混合以得到所述第二待测试样;
其中,所述第二光学信息包括前向散射光强度信息、侧向散射光强度信息和荧光强度信息。
在一些实施例中,所述控制装置配置为在判断所述待测样本中是否存在隐球菌感染时执行以下步骤:
当所述第一隐球菌粒子计数值和所述第二隐球菌粒子计数值的差值在预设范围之内时,判断所述待测样本中存在隐球菌感染。
本申请还提供一种计算机可读存储介质,所述计算机可读存储介质上存储有计算机程序,其特征在于,该计算机程序被处理器执行时实现前述方法的各个步骤。
上述计算机可读存储介质可以是易失性存储器或非易失性存储器,也可包括易失性和非易失性存储器两者。其中,非易失性存储器可以是只读存储器、可编程只读存储器、可擦除可编程只读存储器、电可擦除可编程只读存储器、磁性随机存取存储器、快闪存储器、磁表面存储器、光盘、或只读光盘;磁表面存储器可以是磁盘存储器或磁带存储器。易失性存储器可以是随机存取存储器,其用作外部高速缓存。通过示例性但不是限制性说明,许多形式的RAM可用,例如静态随机存取存储器、同步静态随机存取存储器、动态随机存取存储器、同步动态随机存取存储器、双倍数据速率同步动态随机存取存储器、增强型同步动态随机存取存储器、同步连接动态随机存取存储器、直接内存总线随机存取存储器。本发明实施方式描述的存储器旨在包括这些和任意其它适合类型的存储器。
以上提及的特征,只要在本发明的范围内是有意义的,均可以任意相互组合。针对所述方法的各个方面所说明的优点和特征以相应的方式适用于相应的样本分析仪和相应的计算机可读存储介质,反之亦然。
以上所述仅为本发明的优选实施方式,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书及附图内容所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
- 检测隐球菌的样本分析仪、方法以及计算机可读存储介质
- 样本分析仪、样本分析方法及计算机可读存储介质
