全景旋转内窥双光子显微成像系统
文献发布时间:2023-06-19 13:46:35
技术领域
本发明涉及显微成像技术领域,特别涉及一种全景旋转内窥双光子显微成像系统。
背景技术
目前,介观神经环路研究日益成为健康和疾病中大脑功能研究的关键点。在过去十几年中,支持介观神经环路研究的新方法和新技术取得迅速发展,比如光学钙成像和光遗传学技术,迅速成为神经环路科学研究的中流砥柱。光学钙成像能够以高采样密度记录大量遗传或解剖学定义的神经元细胞,并且可以随着时间推移在纵向跟踪单个神经元。这种强大的光学成像能力已在小鼠动物模型中取得巨大的成功,并促进脑神经科学家深入理解大脑基本功能而提出新的独特见解。然而,为了研究更复杂的或者与临床疾病相关的人类行为和认知过程中神经元活动和神经网络是如何发挥作用的,仍然迫切需要将这些新技术应用到与人类相关的大型动物模型物种上,即,大脑结构和功能以及复杂的认知和行为能力与人类高度相似的非人类灵长类动物物种上。
只有活的、在体的大脑才具备认知、学习、记忆等独特的高等智能功能,而死去、离体的大脑则不具备。因此,在活体大脑中以单个神经细胞精度观测和操控神经细胞活动信号的技术,构成了现代脑科学仪器技术的前沿主体。在诸多使用荧光标记物的高分辨光学显微成像技术之中,双光子成像技术具有天然的层析成像能力、亚微米级别的空间分辨率和毫秒级别的实时性,而且穿透深度可以达到近1mm,是当前动物在体神经活动信号研究的最佳方法之一。
最近,在非人类灵长类动物上,基于GCaMP系列荧光蛋白的双光子钙成像克服了一些技术上挑战。然而,绝大多数技术挑战的克服主要是基于台式双光子工作范式进行的,这种成像方式不可避免地还存在一些技术上的不足,包括:(1)透明玻璃窗口存在感染风险,随着时间推移,光学清晰度下降,成像周期缩短,需要日常维护;(2)为了维持长时间在一个稳定的视野内最终神经元活动信息,需要繁琐的显微镜校准;(3)无法对深度大于500μm的脑皮层、甚至大脑深度的脑回沟皮层或皮层下结构进行成像;(4)无法用单一激光扫描光束真正实现多个大脑区域的同时测量;(5)需要头部固定约束,从而限制了动物可执行的认知行为。
为了克服上述台式双光子成像方式在自由行为动物模型研究中存在的局限性,将双光子成像系统进行微型化和集成化,构建成为易拆装的头戴式光学成像系统是破解上述难题的关键。首先,头戴式微型光学成像探头非常适合自由行为活动动物神经活动研究,特别是大型的非人灵长类动物模型;其次,通过特殊的机械设计,可以在重复过程准确地对准同一个成像区域进行观察;最后,简易的安装、拆卸和日常维护,非常适合对同一区域长时间重复观察。典型的代表性研究成果是:2017年,北京大学程和平院士团队研制的微型化双光子显微镜FHIRM-TPM,目前的FHIRM-TPM2.0可以在视场420μm×420μm范围内,对自由活动小鼠实现了分辨率达亚微米级的神经元实时动态成像。然而,该方法仍然利用透明窗口对神经元活动进行观察,因此,其观察范围仍然无法超越脑皮层以下500μm的深度限制,无法实现对大脑深层神经元成像,目前,该技术方案仅成功应用于小鼠动物模型上,还未成功应用于非人灵长类动物模型的研究中。
另一个典型头戴式光学成像的代表是,Inscopix,Inc.开发的重量不足2g、成像视场可达900μm×700μm的nVista微型单光子显微镜,该方案是将一个Grin lens植入大脑深层,根据植入Grin lens长度的不同,可以允许神经科学家可视化小鼠大脑几乎所有区域的神经元的活动信息,包括其他大规模记录技术无法触及的大脑深层结构。目前,nVista不仅在小鼠脑科学研究中取得了成功,也在非人灵长类动物上展示了应用的可行性。它克服了采用透明玻璃窗口的双光子微型成像技术中成像深度的限制,实现对深层脑组织的神经元活动成像,迈出了微型钙成像技术在非人灵长类动物中应用的重要一步,使得已经在啮齿类动物模型中建立研究范式可以相对简单和顺畅地转换到狨猴的小脑和无脑回皮层的研究中。但是,由于单光子荧光激发在物理原理层面不可抗拒的限制,nVista仅局限于解析尺寸较大神经元结构(如细胞体)的动态信号,完全无法实现双光子成像技术具有的在精细解剖结构(如树突棘)尺度上解析静态和动态信号的能力。
所以现在有必要对现有的FHIRM-TPM、nVista等方案进行改进,以提供一种更可靠的方案。
发明内容
本发明所要解决的技术问题在于针对上述现有技术中的不足,提供一种全景旋转内窥双光子显微成像系统。
为解决上述技术问题,本发明采用的技术方案是:一种全景旋转内窥双光子显微成像系统,包括:近红外飞秒脉冲激光器、主机、成像探头组件和轴向扫描装置,所述成像探头组件包括旋转输出单元以及旋转驱动单元;
所述旋转输出单元植入到动物的脑组织中,用于将飞秒脉冲激光导入脑组织,并收集脑组织被激发而产生的荧光;所述轴向扫描装置用于驱动所述旋转输出单元沿Z轴运动,以实现轴向扫描;所述旋转驱动单元用于驱动所述旋转输出单元绕Z轴旋转,以实现360度环形扫描;
所述近红外飞秒脉冲激光器发出的飞秒脉冲激光经过所述主机后耦合到所述成像探头组件中,并由所述旋转输出单元射出,照射到动物的脑组织上;脑组织被激发产生的荧光信号再经所述旋转输出单元收集,并传入所述主机。
优选的是,所述主机包括色散补偿模块、扩束透镜组、二向色片、光纤耦合透镜和光电倍增管探测器;
所述近红外飞秒脉冲激光器发出的飞秒脉冲激光经过所述色散补偿模块产生负或正GDD后,通过扩束透镜组将飞秒脉冲激光扩展到设定的光束直径,再透射所述二向色片,然后通过所述光纤耦合透镜耦合到所述成像探头组件中,最后由所述旋转输出单元射出,照射到动物的脑组织上;脑组织被激发产生的荧光信号由所述旋转输出单元收集,然后进入所述光纤耦合透镜,最后被所述二向色片反射到达所述光电倍增管探测器;所述旋转驱动单元驱动所述旋转输出单元绕Z轴旋转,以实现360度环形扫描,所述轴向扫描装置用于驱动所述旋转输出单元沿Z轴运动进行轴向扫描,以对轴向不同深度的脑组织进行扫描。
优选的是,所述成像探头组件还包括输入光纤、外壳以及设置在所述外壳内的第一梯度折射率透镜和衍射光学元件;
所述旋转输出单元包括设置在所述外壳内的双直角棱镜对以及与所述双直角棱镜对连接的第二梯度折射率透镜,所述旋转驱动单元包括设置在所述外壳内的微型旋转电机以及与所述微型旋转电机的输出轴驱动连接的旋转轴,所述双直角棱镜对连接在所述旋转轴上;
光纤耦合透镜射出的飞秒脉冲激光耦合到所述输入光纤后,再依次经过所述第一梯度折射率透镜形成准直为平行光、衍射光学元件进行轴向像差校正后,被所述双直角棱镜对反射,然后经过所述第二梯度折射率透镜后形成聚焦光斑射出,所述微型旋转电机通过所述旋转轴带动所述双直角棱镜对和第二梯度折射率透镜一起旋转,使得射出的聚焦光斑实现环形扫描。
优选的是,所述双直角棱镜和第二梯度折射率透镜替换为一个离轴抛物面反射镜,即所述旋转输出单元为一个离轴抛物面反射镜,所述离轴抛物面反射镜连接在所述旋转轴上;
光纤耦合透镜射出的飞秒脉冲激光耦合到所述输入光纤后,再依次经过所述第一梯度折射率透镜形成准直平行光、衍射光学元件进行轴向像差校正后,被所述离轴抛物面反射镜聚焦和反射,形成聚焦光斑射出,所述微型旋转电机通过所述旋转轴带动所述离轴抛物面反射镜旋转,使得射出的聚焦光斑实现环形扫描。
优选的是,所述成像探头组件还包括输入光纤、外壳以及设置在所述外壳内的第一梯度折射率透镜和衍射光学元件;
所述旋转驱动单元包括设置在所述输入光纤上的旋转光纤连接器以及用于驱动所述旋转光纤连接器的输出端旋转的旋转机构;
所述旋转输出单元包括设置在所述外壳内的双直角棱镜对以及与所述双直角棱镜对连接的第二梯度折射率透镜,所述外壳与所述旋转光纤连接器的输出端驱动连接;
所述旋转光纤连接器包括与所述输入光纤连接的光纤固定件、与所述传输光纤连接的光纤旋转件以及分别设置在所述光纤固定件和光纤旋转件上的两个第三梯度折射率透镜,所述旋转机构带动所述光纤旋转件以及所述外壳整体进行旋转;
光纤耦合透镜射出的飞秒脉冲激光耦合到所述输入光纤后,再经过所述光纤固定件上的第三梯度折射率透镜准直,然后经所述光纤旋转件上的第三梯度折射率透镜耦合到所述传输光纤中;再依次经过所述第一梯度折射率透镜形成准直为平行光、衍射光学元件进行轴向像差校正后,被所述双直角棱镜对反射,然后经过所述第二梯度折射率透镜后形成聚焦光斑射出;
所述旋转机构带动所述光纤旋转件、光纤旋转件上的第三梯度折射率透镜、传输光纤以及所述外壳整体进行旋转,使得射出的聚焦光斑实现环形扫描。
优选的是,所述双直角棱镜和第二梯度折射率透镜替换为一个离轴抛物面反射镜,即所述旋转输出单元为一个离轴抛物面反射镜;
所述光纤耦合透镜射出的飞秒脉冲激光耦合到所述输入光纤后,再经过所述光纤固定件上的第三梯度折射率透镜准直,然后经所述光纤旋转件上的第三梯度折射率透镜耦合到所述传输光纤中;再依次经过所述第一梯度折射率透镜形成准直平行光、衍射光学元件进行轴向像差校正后,被所述离轴抛物面反射镜聚焦和反射,形成聚焦光斑射出;
所述旋转机构带动所述光纤旋转件、光纤旋转件上的第三梯度折射率透镜、传输光纤以及所述外壳整体进行旋转,使得射出的聚焦光斑实现环形扫描。
优选的是,所述外壳上具有透光部,例如增透处理的玻璃或透明塑料等材质,使得环形扫描的聚焦光斑能够透过所述外壳射出。
优选的是,该全景旋转内窥双光子显微成像系统还包括探头支架,所述轴向扫描装置和成像探头组件的固定部分设置在所述探头支架上;
优选的是,所述轴向扫描装置为一维位移台。
优选的是,该全景旋转内窥双光子显微成像系统还包括图形工作站,所述图形工作站接收所述光电倍增管探测器探测得到的荧光信号,并进行图像重构,获得360度扫描图像。
本发明的有益效果是:
本发明将高速旋转扫描与微型内窥双光子成像系统结合,提出了一种能特别适用于灵长类较大型动物的全景内窥双光子显微成像系统,通过将成像探头组件的旋转输出单元置入到脑组织,藉由360度环形柱面扫描能实现所观察脑区内360度全景成像,藉由轴向扫描进行不同深度的探测,能实现从深脑区到脑皮层管道所覆盖连续多个脑功能区的神经活动观测;相比小鼠,对于灵长类动物较大尺寸的脑而言,本发明提出的全景内窥双光子显微成像系统具有很高的效率和优异的效果,脑部尺寸越大,旋转输出单元前进扫描前端扫描死区相对越小,从而使得旋转输出单元前进路径上的几乎全部侧向区域都可以被观测到;
本发明采用双光子成像原理,可以实现单神经元解析精度的静态和动态信号观测;
本发明通过旋转驱动单元实现高速旋转扫描,结合快速的轴向扫描装置,能够实现从脑皮层到深层脑区的连续多个不同深度部位的脑区成像;
本发明得到成像探头组件具有高NA的聚集能力,能保证秒脉冲激光有效的聚集和激发荧光;
本发明能够实现对从脑皮层到深脑核团的单神经元解析的神经元活动信号检测,成像探头组件的数值孔径NA约为0.5,根据成像探头组件的外壳直径D和外壳之外的工作距离WD,成像探头组件可以实现π(D+2WD)×L的成像视场(例如,在一种实施例中,D=2mm,WD=0.5mm,L=10mm,成像视场为:9.42mm×10mm)的观测,L是沿Z轴的轴向的扫描长度,其成像视场能远远大于目前的FHIRM-TPM2.0(420μm×420μm)和nVista(900μm×700μm)的技术方案;
本发明通过成像探头组件的设计,使得其中的旋转输出单元可实现微型化,例如在一些实施例中,旋转输出单元的尺寸可做到2~3mm,从而能非常方便地安装在非人灵长类动物的脑部,便于进行自由行为或部分自由行为下的动物脑神经元活动的长时间观察。
附图说明
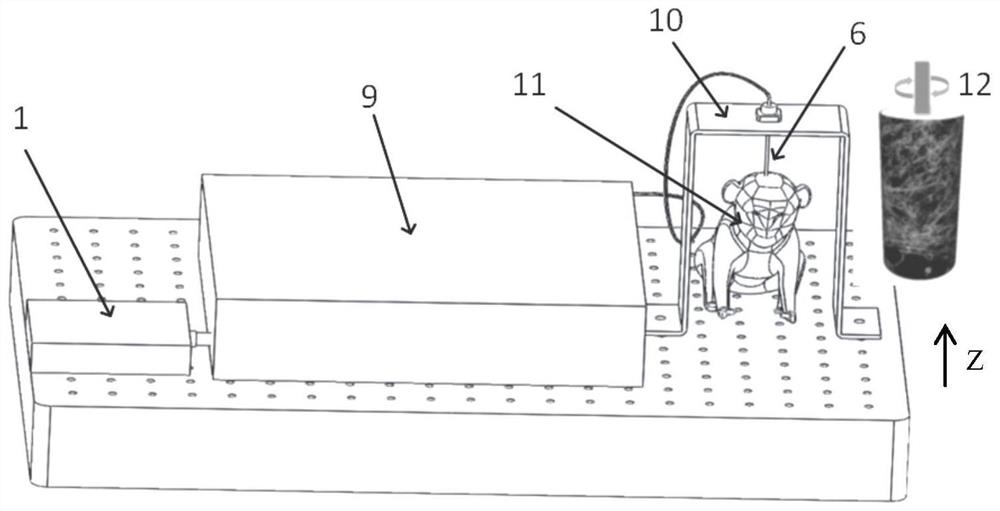
图1为本发明的实施例1中的全景旋转内窥双光子显微成像系统的整体结构示意图;
图2为本发明的实施例1中的全景旋转内窥双光子显微成像系统的光路结构示意图;
图3为本发明的一种实施例中的轴向扫描装置与成像探头组件配合的结构示意图;
图4为本发明的实施例2中的成像探头组件的结构示意图;
图5为本发明的实施例3中的成像探头组件的结构示意图;
图6为本发明的实施例4中的成像探头组件的结构示意图;
图7为本发明的一种实施例中的旋转机构的结构示意图;
图8为本发明的实施例5中的成像探头组件的结构示意图。
附图标记说明:
1—近红外飞秒脉冲激光器;2—色散补偿模块;3—扩束透镜组;4—二向色片;5—光纤耦合透镜;6—成像探头组件;7—光电倍增管探测器;8—轴向扫描装置;9—主机;10—探头支架;11—非人灵长类动物;12—360度全景扫描神经元图像;6.0.1—旋转驱动单元;6.0.2—旋转输出单元;6.1—输入光纤;6.1.0—传输光纤;6.2—第一梯度折射率透镜;6.3—衍射光学元件;6.4a—双直角棱镜对;6.4b—离轴抛物面反射镜;6.5—第二梯度折射率透镜;6.6.1—旋转轴;6.6.2—微型旋转电机;6.7—外壳;6.8—聚焦光斑;6.9—旋转光纤连接器;6.9.1—光纤固定件;6.9.2—第三梯度折射率透镜;6.9.3—光纤旋转件;6.10—无刷高速旋转电机;6.11—皮带。
具体实施方式
下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它元件或其组合的存在或添加。
实施例1
参照图1,本实施例的一种全景旋转内窥双光子显微成像系统,包括:近红外飞秒脉冲激光器1、主机9、成像探头组件6和轴向扫描装置8,成像探头组件6包括旋转输出单元6.0.2以及旋转驱动单元6.0.1;
旋转输出单元6.0.2植入到非人灵长类动物11的脑组织中,用于将飞秒脉冲激光导入脑组织,并收集脑组织被激发而产生的荧光;轴向扫描装置8用于驱动旋转输出单元6.0.2沿Z轴运动,以实现轴向扫描;旋转驱动单元6.0.1用于驱动旋转输出单元6.0.2绕Z轴进行高速旋转,以实现360度环形扫描;
近红外飞秒脉冲激光器1发出的飞秒脉冲激光经过主机9后耦合到成像探头组件6中,并由旋转输出单元6.0.2射出,照射到动物的脑组织上;飞秒脉冲激光激发脑组织中的神经细胞产生荧光信号,产生的荧光信号再经旋转输出单元6.0.2收集,并传入主机9;最终可得到360度全景扫描柱面神经元图12。
参照图2,其中,主机9包括色散补偿模块2、扩束透镜组3、二向色片4、光纤耦合透镜5和光电倍增管探测器7;
近红外飞秒脉冲激光器1发出的飞秒脉冲激光经过色散补偿模块2产生负或正GDD(群延迟色散)以补偿后端光纤中产生的正或负GDD,然后通过扩束透镜组3将飞秒脉冲激光扩展到设定的光束直径,再透射二向色片4,然后通过光纤耦合透镜5耦合到成像探头组件6中,最后由旋转输出单元6.0.2射出,照射到动物的脑组织上;脑组织被激发产生的荧光信号由旋转输出单元6.0.2收集,然后进入光纤耦合透镜5,最后被二向色片4反射到达光电倍增管探测器7;旋转驱动单元6.0.1驱动旋转输出单元6.0.2绕Z轴旋转,以实现360度环形扫描,轴向扫描装置8用于驱动旋转输出单元6.0.2沿Z轴运动进行轴向扫描,以对轴向不同深度的脑组织进行扫描。
参照图3,在一种优选的实施例中,轴向扫描装置8为一维位移台,带动成像探头组件6整体或是成像探头组件6中的植入到了脑组织内部的旋转输出单元6.0.2进行轴向移动,从而配合旋转输出单元6.0.2的旋转,能实现从深脑核团到脑皮层的360度全景连续多个脑区的神经元信号静态或动态成像。图3中,成像探头组件6中的旋转驱动单元6.0.1设置在一维位移台上,旋转输出单元6.0.2驱动连接在旋转驱动单元6.0.1的输出端上;从而通过一维位移台能带动旋转驱动单元6.0.1、旋转输出单元6.0.2整体进行Z轴方向的移动,再通过旋转驱动单元6.0.1能带动旋转输出单元6.0.2绕Z轴进行转动。
在一种优选的实施例中,该全景旋转内窥双光子显微成像系统还包括探头支架10,轴向扫描装置8和成像探头组件6的固定部分设置在探头支架10上,再参照图1。
在一种优选的实施例中,该全景旋转内窥双光子显微成像系统还包括图形工作站,图形工作站接收光电倍增管探测器7探测得到的荧光信号,并进行图像重构,获得360度扫描图像。图形工作站可为计算机。进一步优选的实施例中,还包括运动控制系统和/或数据采集系统,运动控制系统用于对旋转驱动单元6.0.1和轴向扫描装置8进行控制,数据采集系统采集光电倍增管探测器7的信号,再上传至图形工作站。
实施例2
参照图4,作为实施例1的基础上的进一步改进,本实施例中,成像探头组件6还包括输入光纤6.1、外壳6.7以及设置在外壳6.7内的第一梯度折射率透镜6.2和衍射光学元件6.3;
旋转输出单元6.0.2包括设置在外壳6.7内的双直角棱镜对6.4a以及与双直角棱镜对6.4a连接的第二梯度折射率透镜6.5,旋转驱动单元6.0.1包括设置在外壳6.7内的微型旋转电机6.6.2以及与微型旋转电机6.6.2的输出轴驱动连接的旋转轴6.6.1,双直角棱镜对6.4a连接在旋转轴6.6.1上;
光纤耦合透镜5射出的飞秒脉冲激光耦合到输入光纤6.1后,再依次经过第一梯度折射率透镜6.2形成准直为平行光、衍射光学元件6.3进行轴向像差校正后,被双直角棱镜对6.4a反射,然后经过第二梯度折射率透镜6.5后形成具有高NA(约0.5)的聚焦光斑6.8射出,微型旋转电机6.6.2通过旋转轴6.6.1带动双直角棱镜对6.4a和第二梯度折射率透镜6.5一起高速旋转,使得射出的聚焦光斑6.8实现环形扫描。
在一种实施例中,外壳6.7通过一柔性轴或刚性轴与一维位移台的输出端连接,一维位移台通过该柔性轴或刚性轴驱动成像探头组件6整体进行轴向移动;使用时外壳6.7整体植入到动物脑组织内。
实施例3
参照图5,作为实施例1的基础上的另一种实现方式,本实施例中,双直角棱镜和第二梯度折射率透镜6.5替换为一个离轴抛物面反射镜6.4b,即旋转输出单元6.0.2为一个离轴抛物面反射镜6.4b,离轴抛物面反射镜6.4b连接在旋转轴6.6.1上;
光纤耦合透镜5射出的飞秒脉冲激光耦合到输入光纤6.1后,再依次经过第一梯度折射率透镜6.2形成准直平行光、衍射光学元件6.3进行轴向像差校正后,被离轴抛物面反射镜6.4b聚焦和反射,形成具有高NA的聚焦光斑6.8射出,微型旋转电机6.6.2通过旋转轴6.6.1带动离轴抛物面反射镜6.4b高速旋转,使得射出的聚焦光斑6.8实现环形扫描。
实施例4
参照图6,作为实施例1的基础上的进一步改进,本实施例中,成像探头组件6还包括输入光纤6.1、外壳6.7以及设置在外壳6.7内的第一梯度折射率透镜6.2和衍射光学元件6.3;
旋转驱动单元6.0.1包括设置在输入光纤6.1上的旋转光纤连接器6.9以及用于驱动旋转光纤连接器6.9的输出端旋转的旋转机构;
旋转输出单元6.0.2包括设置在外壳6.7内的双直角棱镜对6.4a以及与双直角棱镜对6.4a连接的第二梯度折射率透镜6.5,外壳6.7与旋转光纤连接器6.9的输出端驱动连接;
旋转光纤连接器6.9包括与输入光纤6.1连接的光纤固定件6.9.1、与传输光纤6.1.0连接的光纤旋转件6.9.3以及分别设置在光纤固定件6.9.1和光纤旋转件6.9.3上的两个第三梯度折射率透镜6.9.2,两个梯度折射率透镜之间是空气或者是折射率匹配液,旋转机构带动光纤旋转件6.9.3以及外壳6.7整体进行旋转;
光纤耦合透镜5射出的飞秒脉冲激光耦合到输入光纤6.1后,再经过光纤固定件6.9.1上的第三梯度折射率透镜6.9.2准直,然后经光纤旋转件6.9.3上的第三梯度折射率透镜6.9.2耦合到传输光纤6.1.0中;再依次经过第一梯度折射率透镜6.2形成准直为平行光、衍射光学元件6.3进行轴向像差校正后,被双直角棱镜对6.4a反射,然后经过第二梯度折射率透镜6.5后形成具有高NA的聚焦光斑6.8射出;
旋转机构带动光纤旋转件6.9.3、光纤旋转件6.9.3上的第三梯度折射率透镜6.9.2、传输光纤6.1.0以及外壳6.7整体进行旋转,使得射出的聚焦光斑6.8实现环形扫描;使用时外壳6.7整体植入到动物脑组织内。
在一种实施例中,参照图7,旋转机构包括无刷高速旋转电机6.10和皮带6.11,无刷高速旋转电机6.10通过皮带6.11带动光纤旋转件6.9.3进行旋转;光纤旋转件6.9.3通过转轴或其他驱动连接件带动后端的外壳6.7及外壳6.7内的元件进行旋转;传输光纤6.1.0同步跟随进行转动,例如转轴内部中空,传输光纤6.1.0设置在转轴内部。
在一种实施例中,旋转光纤连接器6.9通过一柔性轴或刚性轴与一维位移台的输出端连接,通过一维位移台驱动成像探头组件6整体进行轴向移动。
实施例5
参照图8,作为实施例4的基础上的另一种实现方式,双直角棱镜和第二梯度折射率透镜6.5替换为一个离轴抛物面反射镜6.4b,即旋转输出单元6.0.2为一个离轴抛物面反射镜6.4b;
光纤耦合透镜5射出的飞秒脉冲激光耦合到输入光纤6.1后,再经过光纤固定件6.9.1上的第三梯度折射率透镜6.9.2准直,然后经光纤旋转件6.9.3上的第三梯度折射率透镜6.9.2耦合到传输光纤6.1.0中;再依次经过第一梯度折射率透镜6.2形成准直平行光、衍射光学元件6.3进行轴向像差校正后,被离轴抛物面反射镜6.4b聚焦和反射,形成具有高NA的聚焦光斑6.8射出;
旋转机构带动光纤旋转件6.9.3、光纤旋转件6.9.3上的第三梯度折射率透镜6.9.2、传输光纤6.1.0以及外壳6.7整体进行旋转,使得射出的聚焦光斑6.8实现环形扫描。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
