吡非尼酮在制备治疗多房棘球蚴病药物中的应用及联合用药组合物
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及抗纤维化药物吡非尼酮(PFD)的新用途,尤其涉及吡非尼酮(PFD) 在制备治疗多房棘球蚴病药物中的应用及联合用药组合物。
背景技术
棘球蚴病(Echinococcosis)又称包虫病,一种呈世界性分布的人兽共患病。目前主要分为由细粒棘球蚴绦虫(E.granulosus,E.g)感染引起的细粒棘球蚴病,俗称囊型包虫病(Cystic echinoccosis,CE)和由多房棘球蚴绦虫(E.mulilocularis,E.m)引起的泡球蚴病,俗称泡型包虫病(Alevolar echinoccosis,AE)两种类型。。两型包虫病的感染途径为吞食了细粒棘球蚴和泡状多房棘球蚴虫卵的粪口传播途径,人类作为中间宿主,囊型包虫病主要通过狗传播;泡型包虫病主要通过狼、狐、野鼠等传播。肝脏是包虫病感染的主要脏器,大约占据70%,肺占20%,其他脏器占据10%。囊性包虫病多为占位性病变,压迫周围的组织和器官,有明显的界线和包膜;泡型包虫病具有类癌样生长、浸润性强且恶性程度高的特性,故称“虫癌”,多以浸润或出芽的方式增殖,可经淋巴道和血管转移至腹腔、脑和肺脏等部位,无明显的界限和包膜。临床治疗多以切除病变组织为主要治疗方案,对于早期干预、术后预防和无法进行手术治疗的患者可使用口服阿苯达唑片剂或者脂质体进行长期干预治疗。
阿苯达唑,是世界卫生组织唯一指定棘球蚴病的治疗药物,但在临床使用过程中出现许多不良反应,且阿苯达唑的治疗作用主要依赖抑虫发挥作用,导致阿苯达唑对棘球蚴病的治疗发挥作用受限。
吡非尼酮(PFD),是一种新的具有广谱抗纤维化作用的吡啶酮类化合物,在临床主要用于治疗特发性肺纤维化,认为该药的确切机制尚不清楚,可能与干扰转化生长因子-β(TGF-β)和肿瘤坏死因子-α(TNF-α)的产生相关。TGF-β是一种小分子蛋白参与纤维化的形成,TNF-α是一种参与炎症反应的小分子蛋白,也有报道证实该药对于肝纤维化的抑制作用。然而,对于抗纤维化吡非尼酮(PFD)治疗多房棘球蚴病的应用尚未见报道。
发明内容
本发明的目的是提供吡非尼酮在制备治疗多房棘球蚴病药物中的应用及联合用药组合物。
第一方面,本发明保护吡非尼酮(CAS编号53179-13-8)在制备治疗多房棘球蚴病药物中的应用。
第二方面,本发明保护吡非尼酮在制备增强式Ⅰ所示咔唑氨基醇类化合物杀伤棘球蚴活性药物中的应用;
式Ⅰ中,X
上述的应用中,式Ⅰ所示咔唑氨基醇类化合物具体可为式Ⅰ-A所示化合物或式Ⅰ-B所示化合物;
第三方面,本发明保护一种联合用药组合物,包括吡非尼酮和式Ⅰ所示咔唑氨基醇类化合物;
式Ⅰ中,X
上述的联合用药组合物中,式Ⅰ所示咔唑氨基醇类化合物具体可为式Ⅰ-A所示化合物或式Ⅰ-B所示化合物;
优选地,联合用药时,所述吡非尼酮和所述式Ⅰ所示化合物的给药剂量比为 5:1~20:1。
在本发明中,所述联合用药组合物含有有效剂量的吡非尼酮和式Ⅰ所示化合物。所述有效剂量具体可为治疗的患者的单位剂量(如单位体重剂量)。在本发明中,药物治疗的对象为人或家畜类。人的给药剂量具体可如下:吡非尼酮的给药剂量为 300~1800mg/kg,式Ⅰ所示化合物的给药剂量为50~150mg/kg。作为实例,对8周龄的BALB/c小鼠灌胃吡非尼酮和式Ⅰ所示化合物,吡非尼酮和式Ⅰ所示化合物的有效剂量分别为600mg/kg和80mg/kg。
上述的联合用药组合物中,所述联合用药组合物可为单一的复方制剂;或,
所述联合用药组合物可为吡非尼酮制剂和式Ⅰ所示咔唑氨基醇类化合物制剂两种单独制剂的组合;两种单独的制剂可同时施用或者依次施用。
第四方面,本发明保护所述的联合用药组合物在制备治疗多房棘球蚴病药物中的应用。
在本发明中,所述药物的剂型可为药剂学上可接受的任意一种剂型,包括片剂、胶囊剂、颗粒剂、散剂、混悬剂、糖浆剂、口服液和注射剂中的一种或几种。所述药物的给药途径包括静脉注射、腹腔注射、肌肉注射、皮下注射和舌下给药,优选口服给药。
本发明具有如下有益效果:
本发明首次公开了抗纤维化药物吡非尼酮(PFD)作为治疗多房棘球蚴病药物的应用。本发明还首次公开了抗纤维化药物吡非尼酮(PFD)联合具有杀虫效果的咔唑氨基醇类化合物H1402协同治疗多房棘球蚴病药物的应用,通过药效学实验数据可知,抗纤维化药物吡非尼酮(PFD)联合具有杀虫效果的咔唑氨基醇类化合物H1402 协同治疗多房棘球蚴病的治疗效果优于或相当于临床常用的阿苯达唑(ABZ)治疗多房棘球蚴病的治疗效果,说明抗纤维化药物吡非尼酮(PFD)联合具有杀虫效果的咔唑氨基醇类化合物H1402和DLP1932协同治疗多房棘球蚴病具有治疗效果,即说明吡非尼酮(PFD)对多房棘球蚴病能够作为新型的抗包虫病药物,从而为多房棘球蚴病的治疗提供新途径。
附图说明
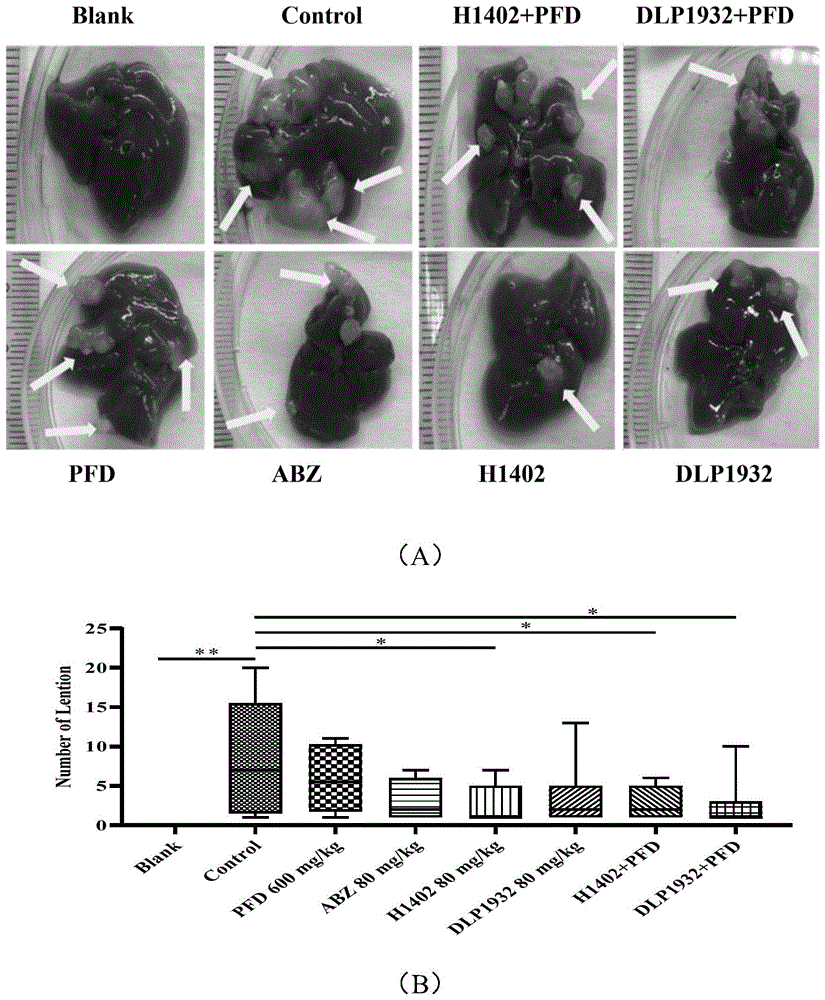
图1为本发明实施例1中药物干预对多房棘球绦虫原头蚴感染小鼠肝脏病灶面积和数量的影响,图1(A)为小鼠肝脏标本的照片,图1(B)为感染病灶数量统计结果(*P<0.05,**P<0.01,)。
图2为本发明实施例1中药物干预后多房棘球绦虫原头蚴感染小鼠肝脏病理变化(HE,40×)(*P<0.05,****P<0.0001)。
图3为本发明实施例1中药物干预后多房棘球绦虫原头蚴感染小鼠肝组织α-SMA表达(40×)(**P<0.01,***P<0.001,****P<0.0001)。
图4为本发明实施例1中药物干预后多房棘球绦虫原头蚴感染小鼠肝脏在mRNA 水平α-SMA表达(*P<0.05,**P<0.01,***P<0.001)。
图5本发明实施例1中药物干预后多房棘球绦虫原头蚴感染小鼠肝脏α-SMA在蛋白水平的表达情况,其中,1:空白组;2:感染模型组;3:PFD组;4:ABZ组;5: H1402组;6:DLP1932组;7:PFD+H1402组;8:PFD+DLP1932组。
具体实施方式
为了更好的理解本发明,下面以H1402和DLP1932为例,结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法;所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实验材料:
吡非尼酮原药,CAS:53179-13-8,购于上海阿拉丁生化科技股份有限公司,产品名称:吡非尼酮,货号:P129335。
式Ⅰ-A所示化合物(H1402)按照专利CN201510586459.9中公开的方法合成,具体步骤如下:
3,6-二氯咔唑(470mg,2mmol)溶于20mLDMF中,于冰浴条件下缓慢加入氢氧化钾(135mg,2.4mmol),加毕后搅拌0.5-1小时,直至氢氧化钾固体完全溶解。然后在该体系中缓慢滴加环氧氯丙烷(2.4mmol),反应4-5小时。反应结束后,加入 30mL水,用乙酸乙酯萃取(30mL×3),饱和氯化钠溶液(30mL×3)洗涤,有机层用无水硫酸钠干燥,过滤,滤液减压回收溶剂,粗产物经柱层析纯化得中间体3,6- 二氯-9-环氧丙基咔唑,白色固体,收率50%。
中间体3,6-二氯-9-环氧丙基咔唑(2mmol)溶于20mL乙醇,加入丙胺(2.4mmol) 和BiCl
式Ⅰ-B所示化合物(DLP1932)按照专利CN201510586459.9中公开的方法合成,具体步骤如下:
操作过程参见上述式Ⅰ-A所示化合物的合成方法,用咔唑代替3,6-二氯咔唑,得中间体9-环氧丙基咔唑,白色固体,收率70%。中间体9-环氧丙基咔唑(2mmol) 溶于20mL乙醇,加入正庚胺(2.4mmol)和BiCl
SPF级别的BALB/c小鼠,雌性,约8周龄,体重为18±2g,购自于河南斯克贝斯生物科技股份有限公司,饲养于新疆医科大学第一附属医院实验动物中心。
多房棘球绦虫原头蚴采自新疆医科大学第一附属医院动物室保种传代的长爪沙鼠,腹腔接种3月后分离原头蚴,用于动物模型建立。
实验方法:
动物模型建立:
(1)多房棘球绦虫原头蚴(Em-PSC)采集:新鲜采集Em-PSC于生理盐水,依据小鼠感染注射剂量200μl/只,含500个Em-PSC制备虫体悬液2500个/ml置于4℃备用。
(2)麻醉与固定:接种前,小鼠行断食断水,腹部剃毛处理;诱导麻醉后,使用医用胶带,固定四肢于接种台,放置洞巾后准备开腹。
(3)接种:碘伏消毒小鼠上腹部,于胸骨突下缘0.5cm处,经腹中线将腹腔打开约1.5cm,使用生理盐水湿润的棉签,暴露肝门静脉,经头皮针注射将虫体悬液接种于小鼠肝门静脉,按压止血约3min,使用可吸收性外科缝线将腹部全层间断缝合约3针,碘伏消毒缝合处。
(4)复苏:将缝合后的小鼠于约25℃的电热毯上复苏,约5min小鼠苏醒转至正常饲养环境。
HE染色:
(1)烤片:将切片于65℃烘烤箱中预热约2h。
(2)脱蜡水化:环保脱蜡液Ⅰ/Ⅱ浸泡约20min;梯度酒精(无水乙醇Ⅰ/Ⅱ、95%乙醇Ⅰ/Ⅱ、80%乙醇和75%乙醇)各浸泡约2min,ddH2O浸泡洗涤3次,5min/次。
(3)染色:苏木素染液浸泡约2min,ddH2O浸泡洗涤,盐酸乙醇浸泡分化约3s,伊红染液浸泡约50s,ddH2O浸泡洗涤。
(4)脱水封片:梯度酒精(75%乙醇、80%乙醇、95%乙醇Ⅰ/Ⅱ和无水乙醇Ⅰ/ Ⅱ)各浸泡约10s,环保脱蜡液Ⅰ/Ⅱ浸泡约2min,通风橱中样本处滴加中性树脂覆盖盖玻片。
(5)镜检:显微镜下观察炎症反应情况,病理变化是根据HE染色细胞的炎症反应和病灶的面积分为4个级:0分,没有任何因感染造成的病变;1分,视野里面的病灶及细胞和炎症带小于25%;2分视野里面的病灶及细胞和炎症带25-50%之间; 3分,视野里面的病灶及细胞和炎症带50-75%;4分,视野里面的病灶及细胞和炎症带大于75%。
免疫组化染色:
(1)烤片:与H&E染色相同。
(2)脱蜡水化:与H&E染色相同。
(3)抗原修复:加入适量柠檬酸修复液,微波炉解冻,15min,冷却至室温。
(4)一抗孵育:1×PBS浸泡洗涤3次,5min/次;滴加3%H2O2(约100μl),室温,15min;1×PBS浸泡洗涤3次,5min/次;滴加10%山羊血清(约100μl),室温,1-2h;滴加一抗(约100μl),4℃过夜。
(5)二抗孵育:室温复温30min,1×PBS浸泡洗涤3次,5min/次;滴加二抗(约 100μl),室温,1-2h;1×PBS浸泡洗涤3次,5min/次;DAB显色后,ddH2O终止反应;苏木素染液浸泡约1min,ddH2O浸泡洗涤,盐酸乙醇浸泡分化约2s。
(6)脱水封片:与H&E染色相同。
qRT-PCR:
(1)将1ml Trizol RNA裂解液加入冻存肝组织的离心管中,每管放入2个钢珠(5mm),球磨仪260frequency 1/s,3min,多次研磨充分破碎组织。
(2)转移液体至1.5ml离心管中,分别加入200μl氯仿,剧烈震荡30s,静止3min, 4℃,12000rcf,15min离心。
(3)转移上层水相至1.5ml离心管中,加入等量异丙醇,上下轻轻颠倒充分混匀,室温静置10min,4℃,12000rcf,15min离心。
(4)弃上清,加1ml 75%乙醇(RNase Free dH2O配置)后,将沉淀涡旋于溶液中,4℃,7500rcf,5min离心。
(5)重复上一步。
(6)弃上清室温干燥约10min,至管内无液体波动,加入约100μl RNase Free dH2O溶解沉淀,测定RNA浓度。
(7)将上述测定浓度的RNA反转录为cDNA,置于-20℃保存,操作如下:
去除基因组DNA,反应体系如下:
Total RNA 1μg
5×gDNA Eraser Buffer 2μl
gDNA Eraser 1μl
RNase Free dH2O up to 10μl
室温放置放置5min。
反转录反应,反应体系如下:
上述反应液10μl
PrimerScript RT Enzyme Mix I 1μl
RT Primer Mix 1μl
5×PrimerScript Buffer 2 4μl
RNase Free dH2O 4μl
Total volume 20μl
充分混匀并离心,PCR仪反应37℃,30min,85℃,15s,4℃∞,将产物每管加入80μlRNase Free dH2O存于-20℃。
(8)组成体系:SYBR Green 10μl
Forward PCR Reverse primer(2μM)1μl
Rervese PCR Reverse primer(2μM)1μl
cDNA template 2μl
yellow die 0.2μl
RNase Free dH2O 3μl
Total volume 20μl
(9)反应条件:混匀后,瞬时离心,放置PCR仪94℃预热3min,1个循环; 94℃、30s,68-50℃、30s,68℃、45s,9个循环,每个循环降2℃;68℃、5min,1 个循环;4℃、Forever。PCR的引物使用由上海生工合成。α-SMA引物序列为:
正向序列:GTCCCAGACATCAGGGAGTAA
反向序列:TCGGATACTTCAGCGTCAGGA
Westen blotting:
(1)准备1.5mm的玻璃板,十孔的梳子用ddH2O清洗干净后备用;将长玻璃与短玻璃对齐后直立于夹子中央,底部紧贴胶条,调整好后用夹子夹紧。
(2)12%聚丙烯酰胺分离胶的配制:
30%制胶液,2ml;10%SDS,50μl;1.5MTris-Hcl,1.25ml;PAGE,5μl;1%PAGE, 50μl;ddH2O,1.65ml
(3)用1ml的加样枪轻轻混匀后吸取溶液加入两玻璃板的间隙中,至距顶部2cm 处停止灌胶,然后缓缓加入75%的酒精压线,待分离胶凝固后,倒掉酒精并用滤纸小心将水分吸干。
(4)5%聚丙烯酰胺浓缩胶的配制:
30%制胶液,0.83ml;10%SDS,50μl;1MTris-Hcl,625μl;PAGE,7.5μl;1%PAGE,75μl;ddH2O,3.42ml
(5)用1ml的加样枪轻轻混匀后吸取溶液加入两玻璃板的间隙中,直至顶部确定无气泡后,将事先准备好的梳子平齐插入凝胶中,室温放置直至凝固。
(6)装配电泳槽,加入1×电泳缓冲液,观察内槽不漏液后小心的拔出梳子;每孔12μl含20μg蛋白的样品加至加样孔中。
(7)接通电源,设置电泳进程,将浓缩胶部分设置为80V,30min,分离胶部分设置为100V,80min。至溴酚蓝至边缘约后1cm后停止电泳,取出凝胶。
(8)电转移:转膜夹打开,于黑色负极板依次放上海绵,滤纸,凝胶,NC膜,滤纸,海绵,每层须除尽气泡后加紧转膜夹并放入装有转膜液的转移槽中,注意正负极装置,其中NC膜需提前经甲醇溶液浸泡2min。
(9)将转膜槽导入冰盒,设置转膜进程为100V,100min;转膜结束后取出NC 膜。
(10)封闭:将PVDF膜正面朝上放入小盒中,用5%脱脂奶粉室温摇床封闭2h。
(11)封闭结束后倒去脱脂奶粉,1×PBST洗涤3次,每次5min。加入一抗,4℃摇床孵育过夜。于次日,用1×PBST在室温摇床洗涤3次,每次5min。加入二抗室温孵育2h后,用1×PBST在室温摇床上洗3次,每次5min。最后ECL显影,应用凝胶成像仪观察结果并拍照保存。
实施例1、吡非尼酮、吡非尼酮和咔唑氨基醇类化合物联合用药组合物的药效学实验
(一)检测抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠后肝脏组织胶原沉积情况
建立多房棘球蚴肝门静脉感染小鼠模型,将48只小鼠行实验分组设置,并设假手术组为空白对照(n=6);将其中42只多房棘球绦虫原头蚴感染小鼠随机分为6组,每组6只,分别设单独给药干预组(n=6)PFD(600mg/kg)、ABZ、H1402和DLP1932 组(80mg/kg);设联合给药组(n=6)H1402+PFD(80+600mg/kg)和DLP1932+PFD (80+600mg/kg);设感染模型组(n=6)。感染60天后连续灌胃给药30天,为观察药物作用效果,停药30天后解剖小鼠,获取小鼠肝脏标本,观察同药物干预组小鼠肝脏病灶大小和数量变化情况,通过HE染色观察不同药物干预组炎性反应情况。
由图1可知,停药30天后解剖小鼠,观察小鼠肝脏大体观察结果,病灶数量变化情况,肝脏病灶数量H1402组,H1402+PFD和DLP1932+PFD组低于感染模型组 (P<0.05)。以上结果表明:药物干预后对小鼠肝脏感染病灶的数量影响较大,H1402 组,DLP1932组及联合PFD组均效果明显。
由图2可知,药物干预后小鼠肝脏组织HE染色显示,病灶周围炎性带面积PFD 组较感染模型组无差异,其他给药组炎症反应减弱均低于感染模型组,H1402及 DLP1932联合PFD低于感染模型组(P<0.05)。PFD干预组,病灶面积较大炎性反应带明显变窄;ABZ干预组,炎性反应与感染模型组无较大差别;H1402和DLP1932 干预组,炎性细胞浸润带无明显差异,但弱于ABZ干预组;H1402+PDF和 DLP1932+PFD干预组,炎性细胞浸润明显较弱。结果显示:PFD干预后可减弱病灶周围的炎性细胞浸润,与H1402和DLP1932联用后对减弱病灶周围的炎性细胞浸润有加强效果。
(二)检测抗抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠后肝脏组织α-SMA情况
依据上述实验操作获取小鼠肝脏标本,通过免疫组化染色观察不同药物干预组小鼠肝脏组织α-SMA表达情况情况,通过qRT-PCR观察α-SMA在小鼠肝脏组织mRNA 水平表达情况,通过Westen blotting观察α-SMA在小鼠肝脏组织蛋白水平表达情况。
由图3可知,药物干预后小鼠肝脏组织免疫组化染色显示,H1402组、DLP1932 组、H1402+PFD和H1402+PFD组α-SMA表达较感染模型组α-SMA表达均降低(P <0.05);PFD干预组,α-SMA表达在病灶周围;H1402和DLP1932药物干预组以及联合给药组病灶周围α-SMA表达减弱,纤维化改善明显。结果显示:与H1402和 DLP1932干预后α-SMA表达减弱联用也有这样的效果。
由图4可知,药物干预后小鼠肝脏组织α-SMA在mRNA水平表达结果显示,PFD 组、H1402组、DLP1932组、PFD+H1402组和PFD+DLP1932组较感染模型组α-SMA 表达下降(P<0.05);所有药物干预组较ABZ组都呈现降低态势。结果显示:与H1402 和DLP1932干预后α-SMA在mRNA水平表达较ABZ干预组减弱联用也有这样的效果。
(三)检测抗抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠后肝脏组织α-SMA情况
依据上述实验操作获取小鼠肝脏标本,通过Westen blotting观察α-SMA在小鼠肝脏组织蛋白水平表达情况。
由图5可知,通过Western blotting实验,抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠肝脏组织α-SMA在蛋白水平表达结果显示,PFD干预后显著降低纤维化指标在蛋白水平的表达,与杀伤棘球蚴的药物联用也有这样的作用。
综上所述,本发明首次公开了一种抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠干预效果,用于治疗多房棘球蚴病的应用。本发明还首次公开了本发明首次还公开了抗纤维化药物吡非尼酮(PFD)干预多房棘球蚴病小鼠肝脏的纤维化和病灶发育,用于多房棘球蚴病的治疗的应用。通过HE染色、免疫组化、qRT-PCR和Western blotting检测实验数据可知,抗纤维化药物吡非尼酮(PFD)联合杀伤棘球蚴的药物作用优于杀伤棘球蚴的药物单独的效果,说明抗纤维化药物吡非尼酮(PFD)用于治疗多房棘球蚴病,即说明抗纤维化药物吡非尼酮(PFD)能够作为新型的多房棘球蚴病治疗药物,从而为棘球蚴病的治疗提供新途径。
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本申请欲包括任何变更、用途或对本发明的改进,包括脱离了本申请中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
- 一种索拉菲尼与青蒿素类化合物的组合药物及其在制备抗癌药物中的应用
- 一种中药组合物在用于制备治疗牙痛的药物中的应用
- 一种中药组合物在制备治疗口舌生疮,痈肿疔疮的药物中的应用
- 以缓释片剂形式制备含有吡非尼酮的药物组合物的方法及其在人慢性肾功能衰竭、乳房包膜挛缩和肝纤维化的复原中的应用
- 吡非尼酮在制备治疗狼疮肾炎肾纤维化的药物中的应用
