一株牛病毒性腹泻病毒BVDV-SDJN01及其应用
文献发布时间:2023-06-19 18:37:28
技术领域
本发明涉及一株牛病毒性腹泻病毒BVDV-SDJN01及其应用,属于牛病毒性腹泻病毒疫苗试剂领域。
背景技术
牛病毒性腹泻是由牛病毒性腹泻病毒(bovine viral diarrhea virus,BVDV)引起的以犊牛腹泻、生长迟缓和继发感染其他疾病等为主要特征的一种急性、热性、接触性传染病。 BVDV可以感染多种宿主,在世界范围内广泛存在。根据BVDV 5′UTR、Npro 等基因序列的差异,可将BVDV分为2 种基因型,即BVDV1 和BVDV2型,BVDV1又分别进一步分为21个基因亚型(1a-1u),BVDV2又分为4个基因亚型(2a-2d)1a和1c亚型是我国近年流行的主要亚型,17省份已检出1c亚型,包括东部5省份。从生物学角度每个基因型可分为致细胞病变(CP)和不致细胞病变型(NCP)。BVDV 感染后机体可表现出典型的临床症状, 主要表现为发烧、腹泻、持续性感染、免疫抑制性疾病、呼吸系统疾病、生殖障碍和粘膜病等。BVDV 持续性感染牛后,可使牛终身带毒并排毒,形成了重要传染源,增加了BVD 诊断与防治的难度。目前,国际上用于BVD 的防控措施主要有两个,一是鉴别和扑杀持续性感染动物,其次是疫苗免疫。有研究显示,接种BVDV 疫苗后可以有效降低对生殖造成的不良影响,比如怀孕母牛的流产、降低持续性感染牛的产生等。因此筛选合适的疫苗是当下的研究重点。
发明内容
针对现阶段牛病毒性腹泻的治疗存在的问题,本发明对实验室分离的牛病毒性腹泻病毒BVDV-SDJN01进行了鉴定,该毒株为BVDV1c亚型,是临床上常见的基因亚型,以该病毒为抗原制备出BVDV1c灭活疫苗,免疫原性较好,可刺激机体产生较高水平的中和抗体,该病毒株为我国牛病毒性腹泻病的有效防治提供一种有效的疫苗候选株。
本发明的技术方案如下:
一株牛病毒性腹泻病毒,所述的病毒为牛腹泻病毒BVDV-SDJN01,于2022年6月30日送至中国典型培养物保藏中心保藏,保藏号为:CCTCC NO: V202255。
上述牛病毒性腹泻病毒在制备治疗牛病毒性腹泻疫苗上的应用。
优选地,上述应用,包括以下步骤:
(1)取纯化病毒接种于牛肾细胞将病毒扩大培养,收集病毒液,经甲醛灭活得到灭活的病毒液;
(2)将灭活病毒液与氢氧化铝佐剂混合,制备灭活铝胶疫苗。
进一步地,将步骤(2)替换为:以灭活病毒液为水相,以白油、司盘80、硬脂酸铝为油相,制备油乳剂灭活疫苗为油乳剂疫苗或铝胶疫苗。
本发明的另一目的,保护一种牛病毒性腹泻病毒病灭活疫苗,采用上述牛病毒性腹泻病毒制备而成。
进一步地,所述的灭活疫苗中病毒含量≥10
保藏信息
保藏时间:2022-06-30
保藏单位:中国典型培养物保藏中心
保藏编号:CCTCC NO:V202255。
保藏单位地址:湖北省武汉市武昌区八一路299号
分类命名:牛病毒性腹泻病毒-1(
本发明的有益效果
牛病毒性腹泻病毒BVDV-SDJN01株具有良好的免疫原性,应用其制备的灭活油乳剂疫苗安全可靠,免疫后能够产生较强免疫力,能够有效的预防牛病毒性腹泻病毒的流行和传播,降低本病造成的经济损失,有着广阔的应用前景。
附图说明
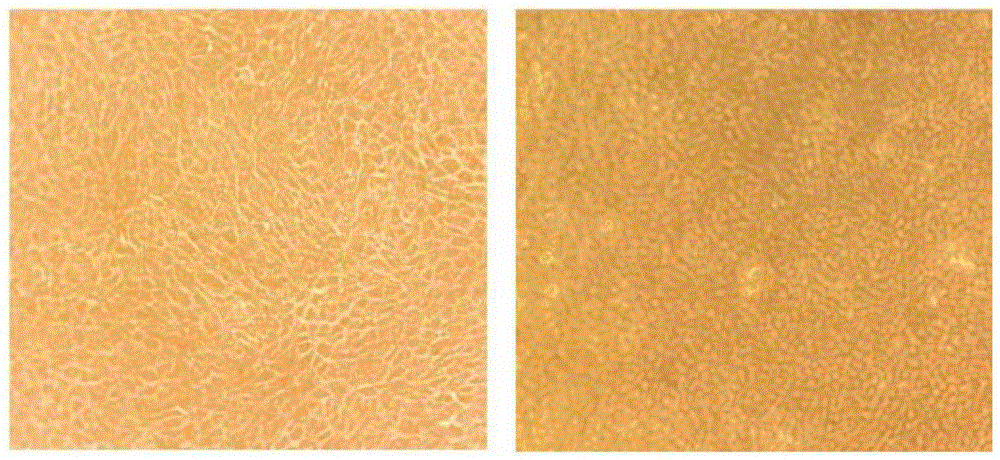
图1为BVDV-SDJN01株接种MDBK细胞96h后的细胞病变(左图为接种BVDV-SDJN01株96h后,与对照相比细胞无明显病变,右图为对照);
图2为BVDV-SDJN01株 RT-PCR鉴;其中M: DL2000 DNA Maker;1-3: BVDV-SDJN01株;
图3为BVDV-SDJN01全基因组核苷酸序列的系统进化分析。
具体实施方式
实施例1
细胞培养用培养基,即含10%胎牛血清的DMEM培养基;其配制:取500ml液体DMEM培养基,按照10%的体积加入胎牛血清,充分混匀后备用。
1.1 BVDV的分离纯化及传代方法
从山东省某大型牛场送检的犊牛腹泻粪便中,收集BVDV检测结果为阳性的样本,加入PBS,12000r/min离心2min,取上清,0.22μm滤膜过滤。将过滤后上清按照1 ml/10cm
1.2 BVDV-SDJN01株序列测定
1.2.1引物设计:根据BVDV参考毒株(GenBank登录号MT079816.1)序列,将该病毒基因组分为9个片段进行扩增,引物序列如下:
引物名称 序列(5’-3’)
BVDV-1F GGAAAACACTCGTGTAC,如SEQ ID NO.2所示;
BVDV-1R TTGTACCAGTTGCACCAACC,如SEQ ID NO.3所示;
BVDV-2F CAAGTGAAAAGACCAACTAC,如SEQ ID NO.4所示;
BVDV-2R CCAAGGATACAGTCGTGG,如SEQ ID NO.5所示;
BVDV-3F GACACAACTGTAGTACAGA,如SEQ ID NO.6所示;
BVDV-3R ACCAGTTAAGCTCTACAAGTG,如SEQ ID NO.7所示;
BVDV-4F ATGTATTACATGCACAGG,如SEQ ID NO.8所示;
BVDV-4R TATTGGTAGACAGACTCTGC,如SEQ ID NO.9所示;
BVDV-5F CAGTGATAGAGGAGATAG,如SEQ ID NO.10所示;
BVDV-5R TCTGTGATCATTGGGACATG,如SEQ ID NO.11所示;
BVDV-6F ATGGGACTGTCCTCTGCTG,如SEQ ID NO.12所示;
BVDV-6RGCCACATGGACACCTTGTC,如SEQ ID NO.13所示;
BVDV-7F CAAGCAGATAAACAGAGG,如SEQ ID NO.14所示;
BVDV-7R ATCCTTGTTTGATCTGTAG,如SEQ ID NO.15所示;
BVDV-8F GAAAGACAAGTATCACTTGG,如SEQ ID NO.16所示;
BVDV-8R CTGGATTTCTCCGATAAGC,如SEQ ID NO.17所示;
BVDV-9F GGACTTATTCAATGAACC,如SEQ ID NO.18所示;
BVDV-9R GGGGCTGTTAGAGGTTTC,如SEQ ID NO.19所示;
1.2.2 病毒RNA的提取及RT-PCR扩增
a)取冻融后的病毒培养液0.2 ml,加入0.5 ml裂解液,涡旋震荡10 sec,12000r/min 离心2 min;
b)加入0.6 ml洗液,12000r/min 离心1 min,弃滤液;
c)重复1次步骤b;
d)12000r/min离心2 min;
e)加入适量洗脱液,室温静置1min,12000r/min离心1 min,洗脱液即为提取的RNA样品;
f)使用引物列表中的引物,按照一步法RT-PCR试剂盒说明书进行扩增;扩增产物序列如SEQ ID NO.1所示。
g) BVDV-SDJN01株全基因序列系统进化分析,从GenBank获取26株BVDV分离株全基因序列,并与BVDV-SDJN01株全基因序列进行全基因进化分析,结果见图3,BVDV-SDJN01株与GXNN1、GSTZ、Bega-like等分离株同源性最高,聚为一簇,为1c基因型。
实施例2
BVDV-SDJN01株在制备的牛病毒性腹泻病毒灭活疫苗中的应用:取毒种保藏编号为CCTCC NO:V202255的BVDV-SDJN01株,接种于MDBK细胞扩增病毒,收集病毒液,经甲醛灭活后,与氢氧化铝佐剂混合配置成灭活铝胶疫苗。操作步骤如下:
2.1毒种选择
制苗毒种为BVDV-SDJN01,其藏编号为CCTCC NO:V202255,免疫原性良好,最低免疫剂量应≥2.0×10
2.2生产用毒种的制备
2.2.1一级生产种子繁殖
取毒种保藏编号为CCTCC NO:V202255的BVDV-SDJN01株,按照1mL/75cm2的比例接种MDBK细胞,病毒感作1.5h后更换病毒培养用培养基并置于37℃ 5%CO2培养箱中培养,96h后收取培养液,并将培养液中病毒含量调整至10
2.2.2 二级生产种子的繁殖
取一级生产种子按照5%的接种量接种于MDBK细胞,于37℃ 5%CO2培养箱中培养,96h后收取培养液。经纯粹检验合格后,作为二级种子。
2.3 制苗病毒液的制备
将二级种子按照5%的接种量接种于MDBK细胞,于37℃ 5%CO2培养箱中培养,96h后收取培养液并进行纯粹检验和病毒滴度测定。纯粹检验和病毒滴度测定均按照《中华人民共和国兽药典》附录进行。每批制苗用病毒液均纯粹,无其他病毒生长,且调整毒价至2×10
2.4 病毒液的灭活
用甲醛对病毒液进行灭活:向病毒液中加入甲醛溶液分别至终浓度 (v/v)为0.3%,将其置于37℃灭活24 h,期间每隔4 h~6h振摇一次。灭活病毒液经检验无菌生长为合格,以该灭活病毒液作为制苗用抗原。
2.5 免疫佐剂的筛选
2.5.1油苗的制备
取病毒液96份(所述份为重量份,下同)加入4份吐温混匀作为水相,取白油93份加入6份司盘80、硬脂酸铝1份混合,121℃灭菌30 min后作为油相。按水相与油相1:2(体积比)进行乳化制备油乳剂灭活疫苗。成品疫苗中含病毒量10
2.5.2 铝胶疫苗的制备
取20 g铝胶加入100 mL灭菌蒸馏水中,搅拌至完全溶解,121℃高压灭菌1 h配制成20%的铝胶,按体积比1:2加入灭活病毒液中,混匀后,2~8℃静置2d~3d,抽弃上清约浓缩成全量的三分之二,分装保存。成品疫苗中含病毒量10
2.5.3安全检验
1月龄犊牛分别注射油苗、铝胶疫苗和PBS 2mL,每组3头,间隔3周免疫第二次,注射后连续观察2周,结果免疫后绝大部分犊牛的精神、体温、食欲均正常,但油苗组注射部位到试验结束仍稍有肿胀,疫苗吸收不良,铝胶苗组无肿胀和坏死,无其他不良反应。
2.5.4 效力检验
免疫1个月后,分别按照10
油苗组:1头犊牛攻毒后出现厌食,精神沉郁,体温升高(39.5℃),于攻毒后第2天出现腹泻症状,另外2头体温变化不大,精神食欲正常,该组疫苗的保护率为80%。
铝胶苗组:3头犊牛体温、精神食欲均无异常。该组疫苗的保护率为100%。
对照组:3头犊牛体温均升高(>40.5℃),食欲明显减退,精神沉郁,被毛粗乱,出现腹泻症状。
综上所述,油苗和铝胶苗均能为犊牛提供保护,但铝胶苗的保护效果要强于油苗。
- 用于鉴定牛支原体、牛病毒性腹泻病毒和牛传染性鼻气管炎病毒的引物组及其应用
- 用于检测牛轮状病毒、牛细小病毒和牛病毒性腹泻病毒的多重纳米PCR引物组及其应用
