一种副溶血性弧菌和大肠杆菌O157:H7标准质粒、构建方法及其应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于食源性致病菌检测领域,具体涉及一种副溶血性弧菌和大肠杆菌O157:H7标准质粒、构建方法及应用。
背景技术
副溶血性弧菌(Vibrio parahaemolyticus)是一种引起沿海地区食源性疾病的主要病原菌,广泛分布在海洋环境中,经常从各种生海鲜中分离出来,食用被副溶血性弧菌污染的食物会引发腹泻、头痛、呕吐、恶心、腹部绞痛和低热等症,严重时会出现败血症甚至危及生命安全。大肠杆菌O157:H7(Escherichia coli O157:H7)是肠出血性大肠杆菌的代表菌株。感染大肠杆菌O157:H7可导致广泛的临床表现,包括无症状感染、轻度腹泻或严重疾病,如出血性结肠炎和溶血尿毒症综合征等。
目前针对副溶血性弧菌和大肠杆菌O157:H7较为普遍且易行的检测方法为基于核酸的分子生物学方法,如普通PCR、荧光PCR、环介导等温扩增等。此类方法的精准度和特异性主要依赖于检测靶点的选择。目前副溶血性弧菌常用检测靶基因集中于gyrB、toxR、trh、tdh、tlh及groEL基因等有限的几种,前期试验表明,这些基因的检测准确率均达不到100%,存在一定的误检率和漏检率。大肠杆菌O157:H7常用检测靶点主要包含rfbE、fliC、stx1、stx2以及其他毒力基因,而fliC、rfbE、stx1、stx2的特异性较差,在大肠杆菌O157:H7中的覆盖率分别为81.80%、90.90%、36.40%、54.50%,在非O157:H7菌株中也有检出。针对以上问题,亟须发掘新的特异性新靶点进行补充。本发明前期针对副溶血性弧菌和大肠杆菌O157:H7,通过生物信息学技术分别筛选到了高特异性靶基因,并且在供试菌株中表现出100%的特异性。在实际应用中仅仅依赖一种靶基因鉴定致病菌是困难的,多个靶基因联合使用可以弥补单基因检测的不足,更加准确和有效鉴定致病菌。
目前,核酸检测过程中,检测结果的可靠性、准确性、可对比性离不开阳性标准物质。质粒标准样品是一类含有检测靶基因特异性片段的重组质粒分子,具有可大量培养、稳定性好、定量简单、易于生产和制备和纯度高等优点,可作为核酸定性检测中的阳性对照。目前质粒标准样品的研究相对缺乏,且常用检测靶基因难以满足现现实需求,本发明分别将副溶血性弧菌和大肠杆菌O157:H7核酸检测中主要的靶基因与自筛靶基因串联制备成多靶基因标准质粒,覆盖率广、特异性强,可结合多种分子生物学检测方法进行副溶血性弧菌和大肠杆菌O157:H7的定性检测,为致病菌检测的质量控制提供了有力保障,具有重要的应用前景。
发明内容
本发明提供了副溶血性弧菌和大肠杆菌O157:H7标准质粒,并公开了副溶血性弧菌和大肠杆菌O157:H7标准质粒构建方法及其应用,为质粒标准品的制备和应用提供重要参考,为食源性致病菌快速核酸检测提供技术支持。
为实现上述目的,本发明提供了如下方案:
第一方面,本发明提供了一种标准质粒样品,选自(1)或(2):
(1)副溶血性弧菌标准质粒样品:
采用副溶血性弧菌tlh、trh、toxR、gyrB、groEL基因及自筛靶基因VPA1585的特异性扩增片段串联并克隆至pUC19质粒形成副溶血性弧菌标准质粒样品,所述副溶血性弧菌标准质粒样品的插入片段核苷酸序列如SEQ ID No.1~6所示;
(2)大肠杆菌O157:H7的标准质粒样品:
采用大肠杆菌O157:H7的rfbE、fliC、stx1、stx2以及自筛靶基因ECS2840的特异性扩增片段串联并克隆至pUC19质粒形成;所述大肠杆菌O157:H7的标准质粒样品的插入片段核苷酸序列如SEQ ID No.7~11所示。
在一些具体的实施方案中,在260nm和280nm处的光密度比值在1.8-2.0之间,浓度经picogreen试剂盒定量至100ng/μL。
第二方面,本发明还保护一种标准质粒样品的制备方法,其包括:
步骤1,PCR扩增获得副溶血性弧菌tlh、trh、toxR、gyrB、VPA1585及groEL基因特异性扩增片段,或,PCR扩增获得大肠杆菌O157:H7的rfbE、fliC、stx1、stx2及ECS2840基因特异性扩增片段;
步骤2,使用重叠延伸PCR将特异性扩增片段串联;
步骤3,克隆至pUC19载体中,经大肠杆菌DH5α扩大培养,提取并提纯质粒;
步骤4,测定浓度和质量并分装,即所述副溶血性弧菌或大肠杆菌O157:H7的标准质粒。
在一些具体的实施方案中,所述方法还包括对标准质粒的核酸定性验证,通过特异性引物进行PCR扩增和测序分析,来确认所制备的标准质粒包括准确的目的序列。
第三方面,本发明还保护前文所述的标准质粒样品,在下述的应用:
(1)当标准质粒样品为副溶血性弧菌标准质粒样品时,所述应用选自如下(A1)-(A4):
(A1)检测副溶血性弧菌;
(A2)制备用于检测副溶血性弧菌的产品;
(A3)确认待测样品是否含有副溶血性弧菌;
(A4)制备确认待测样品是否含有副溶血性弧菌的产品;
(2)当标准质粒样品为大肠杆菌O157:H7标准质粒样品时,所述应用选自如下(B1)-(B4):
(B1)检测大肠杆菌O157:H7;
(B2)制备用于大肠杆菌O157:H7的产品;
(B3)确认待测样品是否含有大肠杆菌O157:H7检测;
(B4)制备确认待测样品是否含有大肠杆菌O157:H7的产品。
在一些具体的实施方案中,在进行副溶血性弧菌和大肠杆菌O157:H7检测时,所述标准质粒作为参考品或对照品。
有益效果
本发明具有以下有益效果:
(1)本发明提供一种标准质粒样品的构建方法,使用重叠延伸PCR实现多个特异性扩增片段串联并克隆至质粒载体,简单高效。
(2)本发明用于检测副溶血性弧菌的参考品针对副溶血性弧菌tlh、trh、toxR、gyrB、VPA1585及groEL基因的检测,提供统一参考品。
(3)本发明用于检测大肠杆菌O157:H7的参考品针对大肠杆菌O157:H7rfbE、fliC、stx1、stx2及ECS2840基因的检测,提供统一参考品。
(4)相对于传统基因组参考样品,多基因联用、序列来源清晰、定量简单、易于生产制备和纯度高,可用于定性检测以及不同实验室之间能力评价的参考品。
(5)本发明制备的副溶血性弧菌和大肠杆菌O157:H7标准质粒相对于已有标准质粒,加入高特异性靶基因,更加准确和有效鉴定致病菌。
(6)本发明还提供了一种副溶血性弧菌和大肠杆菌O157:H7标准质粒在核酸检测中的应用,为标准质粒的实际应用提供重要参考。
附图说明
图1为副溶血性弧菌标准质粒VP-pUC和大肠杆菌O157:H7标准质粒EC-pUC的图谱;
图2为副溶血性弧菌靶基因特异性扩增片段琼脂糖凝胶电泳图;M:DNA2000Marker;1-3:tlh基因,大小为450bp;4-6:trh基因,大小为205bp;7-9:toxR基因,大小为367bp;10-12:VPA1585基因,大小为161bp;13-15:gyrB基因,大小为285bp;16-18:groEL基因,大小为511bp。
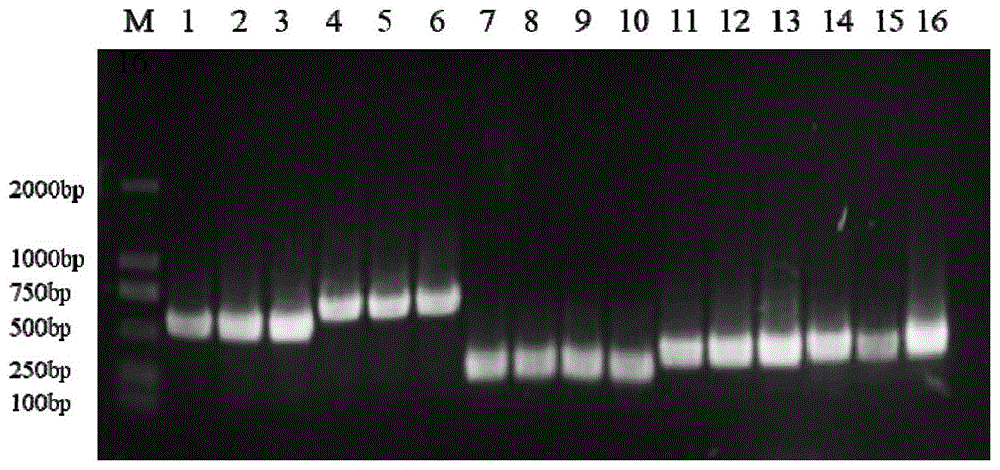
图3为大肠杆菌O157:H7靶基因特异性扩增片段琼脂糖凝胶电泳图;M:DNA2000Marker;1-3:rfbE基因,大小为500bp;4-6:fliC基因,大小为625bp;7-10:stx1基因,大小为244bp;11-13:stx2基因,大小为324bp;14-16:ECS2840基因,大小为334bp。
图4为荧光定量PCR检测方法检测10倍梯度稀释的副溶血性弧菌标准质粒的结果;A.tlh基因;B.trh基因;C.toxR基因;D.VPA1585基因;E.gyrB基因;F.groEL基因。
图5为荧光定量PCR检测方法检测10倍梯度稀释的大肠杆菌O157:H7标准质粒的结果;A.rfbE基因;B.fliC基因;C.stx1基因;D.stx2基因;E.ECS2840基因。
具体实施方式
现详细说明本发明的多种示例性实施方案。以下实施案例仅用于更加清楚地说明本发明的技术方案,而不能以此来限制本发明的保护范围。
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例对本发明进行详细说明,下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的实验材料,如无特殊说明,均为常规生化试剂供应商购买得到。
实施例1副溶血性弧菌和大肠杆菌O157:H7标准质粒的构建方法,包括以下步骤:
1.获得副溶血性弧菌和大肠杆菌O157:H7检测靶基因特异性扩增片段重组片段;
以副溶血性弧菌实验室分离株基因组为模板,根据菌株tlh、trh、toxR、gyrB、VPA1585和groEL基因序列设计特异性引物,并在引物序列首位添加合适的同源序列,通过重叠延伸PCR将特异性扩增片段连接,获得tlh-trh-ToxR-VPA1585-gyrB-groEL重组片段,各基因序列如序列表SEQ ID No.1~6所示。
以大肠杆菌O157:H7实验室分离株基因组为模板,根据菌株基因序列设计特异性引物,并在引物序列首位添加合适的同源序列,扩增含有相邻片段同源序列的靶基因,并通过重叠延伸PCR将特异性扩增片段连接,获得rfbE-fliC-stx1-stx2-ECS2840重组片段,各基因序列如序列表SEQ ID No.7~11所示。
重叠延伸PCR采用50μL PCR反应体系,体系组成为:2×Phanta Master Mix 25.0μL,10μM上下游引物各2μL,上游片段1μL,下游片段1μL,无菌ddH
2.标准质粒的构建
按照一步克隆试剂盒说明书配置反应体系,将获得的重组片段与线性化pUC19载体进行连接,构建重组质粒。并转化至大肠杆菌DH5α感受态中,涂布于含氨苄青霉素的固体LB培养基中筛选阳性克隆子,提取纯化阳性克隆子以大量获得标准质粒。
3.重组质粒的验证;
使用不含接头的引物对质粒标准品中的插入片段进行验证,保证其被正确扩增,经测序分析,重组质粒中插入片段的序列准确度为100%。将测序结果在NCBI中进行BLAST对比(https://blast.ncbi.nlm.nih.gov/Blast.cgi),序列同源性可达99%以上,符合预期,获得正确的标准质粒。
4.质粒标准品的质量检测与分装;
使用Nano Drop 2000超微量分光光度计对质粒进行纯度测定,结果表明,质粒的A260/A280的比值在1.8-2.0之间,A260/A230的比值大于2.0。该质粒纯度良好,无杂质污染。使用PicogreendsDNA Quantitation Reagent双链DNA(dsDNA)定量试剂对经过质量评估的质粒标准品进行浓度测定,并调节浓度至100ng/μL左右,在生物安全柜中用移液枪分装至1.5mL无菌离心管,每管50μL,共100管,获得副溶血性弧菌和大肠杆菌O157:H7标准质粒。
实施例2副溶血性弧菌和大肠杆菌O157:H7标准质粒的应用
1.对标准质粒进行10倍梯度稀释
对经过定量为100ng/μL的标准质粒进行10倍梯度稀释,制备10ng/μL、10ng/μL、100pg/μL、10pg/μL、1pg/μL、100fg/μL、10fg/μL、1fg/μL和100ag/μL的稀释样品。
2.荧光定量PCR反应条件
荧光定量PCR反应所使用的引物序列和扩增子大小见表1-2。PCR采用20μL反应体系,2×Taq Pro Universal SYBR qPCR Master Mix(南京诺唯赞生物科技有限公司)
10μL,10μM上下游引物各0.5μL,质粒及稀释样品1μL,最后用ddH
3.标准质粒在荧光定量PCR中的应用
每个反应重复三次,根据相应的动力学曲线绘制标准曲线,考察副溶血性弧菌质粒标品在荧光定量PCR中的应用能力。
副溶血性弧菌质粒标品在10ng/μL-100ag/μL浓度范围内,tlh、trh、ToxR、VPA1585和GroEL基因扩增曲线良好,目的基因可被检出,在10ng/μL-1fg/μL度范围内gyrB基因扩增曲线良好,目的基因可被检出。应用能力良好,可作为副溶血性弧菌核酸检测参考样品。
大肠杆菌O157:H7质粒模版浓度在10ng/μL-100ag/μL浓度范围内,质粒标品靶基因均可被有效检测,可作为大肠杆菌O157:H7检测阳性质控,为获得准确、可靠、具有可比性的检测结果提供保障。
表1副溶血性弧菌荧光定量PCR引物序列
表2大肠杆菌O157:H7荧光定量PCR引物序列
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换和改进,均应包含在本发明的保护范围之内。
- 一种捕获探针、大肠杆菌O157:H7的双通道检测方法及其应用
- 一种检测大肠杆菌O157:H7的特异性靶点、引物、检测方法及应用
