使用声学液滴喷射从样品中提取目标部分的系统和方法
文献发布时间:2023-06-19 09:33:52
发明背景
(1)技术领域:
本发明总体上涉及使用声学液滴喷射从流体组合物中提取目标分析物的系统和方法。本发明可用于许多领域,包括化学和生物学。
(2)相关技术的描述
从混合物中提取分子是许多技术领域中所采用的方法中的必不可少的步骤,这些领域包括合成有机化学、材料科学、药物研究与开发以及分子生物学。尽管现在在许多情况下都需要,但是就生物分子(例如核酸和蛋白质)的提取而言特别具有挑战性,因为它们通常包含在复杂的主体(host)环境(例如细胞、组织和血液)中。然而,在许多方法和产品中,高效并且有效地提取DNA、RNA和蛋白质是必需的。诊断试剂盒(kits,工具包)、识别和相关性测试、病原体检测、组织分型和基因研究只是几个实例。
DNA的纯化可涉及从生物环境中分离和移出染色体和/或线粒体DNA,或其可在分离重组DNA构建体(即,含有重组序列的DNA,例如质粒)的情况下进行。DNA的聚合酶链反应(PCR)扩增、诊断测试程序以及敏感的分析主体都需要高度的纯度。DNA样品中的污染物可抑制诊断或分析程序中的一个或多个关键步骤。例如,某些污染物可抑制聚合酶链反应或抑制限制性酶的作用。
任何DNA纯化方法都需要(1)有效破坏含有目标DNA的生物主体环境,例如细胞或组织;(2)使用蛋白酶和/或变性剂使蛋白质和核蛋白复合物变性;(3)使内源性核酸酶失活;和(4)从样品中移出目标DNA。分离的目标DNA应不含最初存在的任何化合物或物质,例如蛋白质、脂质、RNA、其他核酸等,并且在大多数情况下,纯化过程必须避免由机械剪切或污染物的存在而导致的DNA片段化(断裂)。RNA的分离甚至更加复杂,因为RNA固有地不稳定,必须使用强变性剂来抑制内源性RNA酶,RNA酶是热稳定的并且在热变性后会重新折叠,并且难以使缺乏辅因子的RNA酶则失活。
在核酸纯化中,通常使用清洁剂破坏细胞膜的脂质双层来进行细胞或组织的破坏。清洁剂会破坏细胞膜中的脂质-脂质和脂质-蛋白质相互作用,从而能够使膜组分溶解。对于除细胞膜之外还含有细胞壁的生物体,可需要另外的处理;例如,必须用溶菌酶处理以消化革兰氏阳性细菌的肽聚糖细胞壁,并且需要用溶细胞酶(裂解酶)或消解酶(酶解酶)处理以破坏酵母的多糖细胞壁。
蛋白质和核蛋白的变性涉及通过破坏二级结构来改变蛋白质构象,并且使用蛋白质变性剂(例如离子清洁剂、离液剂(促溶剂)、还原剂、热和/或蛋白酶)来进行。在哺乳动物细胞中,DNA被组蛋白压在大分子核蛋白结构(即染色质)中,并且变性能够使得染色体DNA从核蛋白复合物中释放。螯合剂(例如乙二胺四乙酸(EDTA))典型地用于使核酸酶失活,蛋白酶K也是如此。某些商业系统需要逐步处理,即细胞裂解、变性和核酸酶失活,而其他系统提供了单一解决方案,其含有用于进行所有三个上述步骤的组件。
最终,必须从经处理的生物样品中分离目标DNA,该样品可能会含有蛋白质、蛋白质片段、脂质、碳水化合物、盐和细胞碎片。从历史上看,DNA通过液-液提取纯化。将水性细胞水解产物与苯酚-氯仿混合物(任选地含有一些异戊醇以抑制RNA酶活性)一起振摇。该混合物分成两层,其中疏水的氯仿-苯酚下部相含有蛋白质、脂质、碳水化合物和细胞碎片,而核酸保留在上部水相中。收集上部相的DNA水溶液,从上清液中沉淀DNA,并且清洗DNA沉淀物并且用缓冲液溶解。然而,该技术麻烦且耗时,并且,如已广泛指出的,氯仿具有剧毒并且苯酚也是易燃的、腐蚀性的和有毒的。
使用基于离心的柱的固相核酸纯化方法已大部分地替代了液-液提取。在这种情况下,将细胞裂解物与缓冲溶液和离液剂或短链醇混合。将裂解物转移至柱并且离心以驱动液体通过固体相,该固体相已经过表面处理以保留带负电荷的核酸。蛋白质和其他污染物通过柱洗涤,而核酸与柱结合。在洗涤步骤后,用水或缓冲液(例如,pH为约8.4的稀释的TRIS-EDTA缓冲液)洗脱核酸。还公开了混合床固相提取;参见授予Smith等的美国专利No.6,376,194。尽管比采用苯酚-氯仿技术的常规液-液提取更容易和安全,但是基于柱的DNA提取仍需要手工干预,并且不容易自动化。
在传统固相分离的一种变体中,已经开发了基于磁珠的核酸纯化方法。在此方法中,在离液剂的存在下,具有经涂覆的或经过其他处理的表面的磁珠会结合核酸。珠与生物样品结合,并且样品中的核酸结合至珠表面。使用磁铁将具有与表面结合的核酸的珠拉至微板孔、离心管或其他容器中的稳定位置。一旦珠以磁力方式被固定,就移出含有杂质的上清液,用干净的洗涤缓冲液洗涤珠,并且用低体积的稀洗脱缓冲液将核酸从磁珠中置换出来。通过消除离心,该技术通常比其他固相纯化方法更适合自动化并且有更高的通量。但是,清理每个样品的成本是显著的。Tan等(2009)J.Biomed.Biotech.,Article ID 574398中描述了用于分离和纯化DNA、RNA和蛋白质的各种类型的提取技术。如其中所解释的,一直需要分离和纯化生物分子的改进的方法。Tan等注意到,为了减少工作时间、降低人工成本、提高工人安全性并且理想地提高结果的可重复性和质量,提取程序的自动化是期望的。Tan等进一步注意到,市售的自动化系统在一定程度上受到限制,因为它们倾向于为大型、昂贵和复杂的,其旨在用在中型到大型实验室中,而适用于小型和中型样品通量的最新的自动化方法仍然需要耗时的提取过程,每个样品的处理时间约为20至40分钟的级别。对于自动化程序的每个提取步骤和对于必要时转移液体这两者,合适的液体处理都至关重要;如Tan等所解释的,最佳地,自动操作工作站应是完全自动化的,由此消除预处理步骤的需要。Tan等另外指出小型化的不断改进是必须的,并且将弥补现有提取系统的弱点。
声学液滴喷射(ADE)是一种已公开用于不混溶流体的喷射的方法;参见授予Ellson等的美国专利No.6,548,308和6,642,061。前述专利描述了使用ADE将来自不混溶液体的液滴喷射到基底表面上,其中液滴通常具有对应于一种液体的第一区域和对应于另一种液体的第二区域。然而,尚未在从样品中提取目标部分的过程中实施ADE,并且众所周知,如上文的Tan等所解释,提取技术的开发可为复杂且有问题的。
理想的提取系统和方法至少将实现以下目标:
提供高纯度的分离的目标分子;
能够用于提取多种目标分子中的任何一种;
产生准确、一致且可重复的结果;
完全自动化;
能够在标准实验室条件下使用而无需高温或惰性气氛;
使每个样品的处理时间最小化并且使得高通量样品处理成为可能;
允许有效并且高效地处理非常小的样品尺寸,约纳升或更小的级别;准确性和可靠性;
消除对有毒、挥发性溶剂的需求;
依靠可在后续提取步骤中再循环和再利用的试剂;和
使得能够将提取的目标部分快速引入到分析设备(例如质谱仪)中。
发明内容
本发明针对本领域中的上述需求,并且提供了一种使用声学液滴喷射(ADE)技术提取目标分析物的方法和系统。目标分析物在流体组合物中,例如溶解在溶剂或溶剂混合物中,并且可在多组分组合物中包含单一分析物或分析物的混合物。流体组合物可包含生物样品,例如活组织、细胞、血液等,其在提取之前可已经或可不以某种方式被处理。本发明采用ADE技术,并且在一个优选的实施方案中,采用液-液分配,利用了例如对于样品中的各种类型的组分具有不同亲和性的液体,和/或所关注的组分在其中具有不同的溶解度的液体。本发明的方法和系统在高通量的情况下可容易地实施,并且可用于从样品中提取各种目标分子,包括低体积的由复杂生物混合物组成的生物样品。
本提取方法包括从初始流体组合物中部分或完全移出目标分析物,并且还包括其中最终流体组合物以比初始流体组合物中更低的浓度含有非目标组分的分离方法(过程)。
在本发明的第一实施方案中,提供了一种用于产生含有处于选定的浓度的目标分析物的流体液滴的方法。该方法包括:(a)在流体储藏器中提供含有目标分析物并且包括上部区域和下部区域的流体组合物,其中分析物在上部区域中处于第一浓度,并且在下部区域中处于第二浓度,并且进一步地其中第二浓度不同于第一浓度;(b)以有效地将流体液滴从流体组合物喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能,其中喷射的液滴包含处于选定的浓度的目标分析物,并且进一步地其中选定的浓度(i)基本上等于第一浓度或第二浓度,和(ii)在整个液滴是基本上均匀的。流体储藏器中的流体组合物通常包括含有目标分析物的样品,例如生物样品。生物样品可包括溶解或悬浮在流体中的样品,或者本身可为流体的生物样品。
在前述实施方案的一个方面中,流体组合物的上部区域包括第一液体的上层,而流体组合物的下部区域包括第二液体的下层。取决于目标分析物、第一液体和第二液体,分析物可优先分配到第一液体或第二液体中。即,选择第一液体和第二液体,使得第一液体对目标分析物具有第一亲和性并且第二液体对目标分析物具有第二亲和性,并且第一亲和性和第二亲和性不同。例如,对于亲水的(例如离子的)目标分析物、亲水的上部液体和疏水的下部液体,目标分析物将倾向于分配到上部的亲水的液体中。作为另一个实例,当目标分析物在下部液体中的溶解度大于在上部液体中的溶解度时,目标分析物将倾向于分配到下部液体中。第一液体和第二液体的挥发性、密度、粘度和/或其他物理或化学特性可不同。
在一个相关方面中,目标分析物在下部液体中的溶解度与其在上部液体中的溶解度相差至少约50%。
在另一个相关方面中,目标分析物在下部液体中的溶解度与其在上部液体中的溶解度相差至少约85%。
在前述实施方案的另一个方面中,目标分析物是离子目标分析物,即在所选择的pH(例如在约6至约8范围内的pH)下被离子化的分析物。离子目标分析物可为分别与阳离子或阴离子抗衡离子缔合(相关)的带负电荷的部分或带正电荷的部分。
在另一个方面中,目标分析物包括生物分子。该生物分子可为核酸、肽或蛋白质、脂质部分等。在一个相关方面中,生物分子包括DNA。肽、蛋白质等的分子量可在约100道尔顿至约200,000道尔顿的范围内。然而,可设想更大的目标分析物,只要本发明可与大核酸片段、未片段化的单链或双链DNA、整个基因组或多于一个的整个基因组以及完整细胞结合使用。
在又一个方面中,流体组合物包括离子液体,即,在用于提取的条件下为液体形式的盐。
在一个相关方面中,该方法在带电荷的生物分子例如核酸(例如,DNA)从流体组合物中声学喷射中采用离子液体。
在另一个相关方面中,离子液体用作第一液体,并且水性液体用作第二液体,其中将水性液体缓冲至改变了离子分析物对离子液体和水性液体的相对亲和性的pH。
在前述实施方案的另一个方面中,该方法进一步包括,在步骤(a)之前:使样品与第一液体和第二液体的可混溶混合物的组合处于使所述两种液体基本上不混溶的条件下,使得将流体组合物分配为上部区域和下部区域。
在实施方案的另一个方面中,液滴接收器包括分析仪器。在一个相关方面中,分析仪器是质谱仪。
在实施方案的另一个方面中,该方法的步骤(b)被重复多次以将多个流体液滴喷射到液滴接收器中。
在实施方案的另一个方面中,液滴接收器包括液滴接收储藏器。在一个相关方面中,该方法的步骤(b)被重复多次,直到目标分析物的至少20重量%从流体储藏器转移至液滴接收储藏器。
在实施方案的另一个方面中,流体储藏器是多个储藏器中的一个,每个储藏器容纳含有目标分析物的流体组合物,其中任何两个流体组合物可相同或不同,和/或任何两个目标分析物可相同或不同。多个储藏器可以阵列布置和/或容纳在包括集成的多个储藏器单元的基底内。在一个相关方面中,流体液滴从一个流体储藏器的阵列中被以声学方式喷射到相应的液滴接收储藏器的阵列中。
在实施方案的另一个方面中,流体储藏器中的流体组合物的体积不超过约125μL。
在实施方案的另一个方面中,喷射的流体液滴的体积不超过约60nL。
在实施方案的另一个方面中,流体液滴的体积不不超过约30nL。
在该实施方案的一个相关方面中,关于(针对)多个流体储藏器相继地进行声学液滴喷射,其中储藏器到储藏器的过渡迅速,例如至多约0.5秒,或至多约0.1秒,或至多约0.001秒。
在实施方案的另一个方面中,流体储藏器的内部表面涂覆有表面涂料组合物。在一个相关方面中,选择表面涂料以排斥或吸引上部流体层,由此改变上部流体层的弯液面的形状和中央区域的厚度。
在实施方案的另一个方面中,该方法进一步包括检测上部流体层和下部流体层之间的液-液边界的存在。在一个相关方面中,流体液滴从上部流体层重复地被喷射直到没有检测到液-液边界,这意味着基本上所有的上层都已经从流体组合物中移出并且声学喷射过程可停止。
在本发明的另一个实施方案中,提供了一种从样品中提取离子目标分析物的方法,其中该方法包括在有利于将离子分析物分配到离子液体中的条件下将样品与离子液体和非离子液体混合,然后从混合物中以声学方式移出非离子液体。
在本发明的另一个实施方案中,提供了一种从样品中提取离子目标分析物的方法,其中该方法包括在有利于将离子分析物分配到离子液体中以提供离子分析物在离子液体中的溶液的条件下将样品与离子液体和非离子液体混合,从混合物中移出非离子液体,以及将离子分析物溶液的液滴以声学方式喷射到液滴接收器中。
在另一个实施方案中,本发明提供了一种提取方法,其包括:(a)在流体储藏器中提供含有目标分析物并且包含第一液体的上层和第二液体的下层的初始流体组合物,其中分析物在上层中处于第一浓度并且在下层中处于第二浓度,其中第二浓度高于第一浓度;(b)以有效地喷射流体的上层的流体液滴的方式向流体储藏器重复地施加聚焦的声能,由此移出上层的至少一部分,同时允许下层保留在流体储藏器中。
在本发明的又一个实施方案中,提供了一种从生物样品中提取离子分析物的方法,其包括:(a)将包含离子分析物和水性介质的生物样品的液滴以声学方式喷射到容纳在液滴接收储藏器中的离子液体中;(b)倒置液滴接收储藏器,由此形成上部水层和包含离子分析物的下部离子液体层;(c)移出上部水层以提供在离子液体中包含离子分析物的离子分析物溶液。生物样品可为经处理的生物样品,例如含有裂解细胞的样品。
在实施方案的一个方面中,水性介质包括将生物样品维持在第一pH的缓冲体系,其中选择第一pH使得生物样品中的离子分析物的至少60重量%在与离子液体混合时分配到离子液体中。
在实施方案的另一个方面中,该方法进一步包括在步骤(c)之后的步骤(d):将离子分析物溶液与具有第二pH的提取缓冲液混合,所述第二pH被选择为使得离子液体中的离子分析物的至少60重量%分配到提取缓冲液中。
在另一个实施方案中,本发明提供了一种从水性生物样品中以声学方式提取DNA的方法,其中该方法包括:
(a)在有效提供包含上部水层和下部离子液体层的流体组合物的条件下,将水性生物样品与离子液体在流体储藏器中混合;
(b)处理流体组合物使得生物样品中的DNA分配到下部离子液体层中;
(c)移出上部水层使得离子液体中的DNA溶液保留在流体容器中;
(d)将DNA溶液与提取缓冲液混合,所述提取缓冲液的pH被选择为使得离子液体中的DNA的至少60重量%分配到提取缓冲液中;和
(e)将含DNA的提取缓冲液的液滴相继地以声学方式喷射到液滴接收器中。
在另一个实施方案中,本发明提供了一种从水性生物样品中提取脂质类组分的方法,其包括:将水性生物样品与有机溶剂在流体储藏器中混合,由此提供经分配的流体组合物,其具有包含脂质溶液的上部有机层和下部水层;和将脂质溶液的液滴相继地以声学方式喷射到液滴接收器中。
在本发明的又一个实施方案中,提供了一种用于从样品中提取离子目标分析物的声学提取系统,其包括:(a)流体储藏器,其容纳包含离子目标分析物和离子液体的流体组合物;和(b)与流体储藏器成声学耦合(偶联)关系的声学液滴喷射器,用于以有效地将流体液滴从流体组合物喷射到液滴接收器中的方式产生声辐射,所述喷射器包括声辐射产生器和用于将声辐射聚焦在储藏器内的焦点处的聚焦装置。
在该实施方案的一个方面中,该系统进一步包括液滴接收器,例如,诸如质谱仪等的分析仪器,或液滴接收储藏器。
在该实施方案的另一个方面中,该系统包括多个流体储藏器,每个流体储藏器容纳包含离子目标分析物和离子液体的流体组合物,其中任何两个流体组合物可相同或不同,和/或任何两个目标分析物可相同或不同。多个储藏器可以阵列布置和/或容纳在包括集成的多个储藏器单元的基底内。在该实施方案的一个相关方面中,该系统进一步包括用于将喷射器相对于每个流体储藏器以声学耦合关系相继安置的装置。
在实施方案的一个相关方面中,目标分析物包括生物分子。
在另一个实施方案中,提供了一种用于从反应混合物中合成和声学提取反应产物的方法。该方法包括:
(a)在流体储藏器中提供含有第一反应物、第二反应物和流体介质的反应混合物,其中所述反应混合物的体积典型地在约1nL至约3mL的范围内;
(b)使反应混合物经历引起第一反应物和第二反应物之间的化学反应以产生反应产物的反应条件,其中流体介质包含反应产物在其中具有第一溶解度的第一液体;
(c)将与第一液体基本上不混溶的第二液体混合到反应混合物中,并且其中反应产物在第二液体中的第二溶解度与所述第一溶解度相差至少50%,由此提供流体组合物,其具有含有不同浓度的反应产物的上层和下层;和
(d)以有效地将含有反应产物的流体液滴喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能。
在前述实施方案的一个相关方面中,反应混合物进一步包括反应催化剂。在另一个相关方面中,该方法使得反应产物和催化剂分配到不同的液体中,由此基本上分离反应产物和催化剂。
在前述实施方案的另一个相关方面中,反应混合物进一步包括表面活性剂。在另一个相关方面中,该方法使得反应产物和表面活性剂分配到不同的液体中,由此基本上分离反应产物和表面活性剂。
在又一个实施方案中,本发明提供了一种合成和声学转移反应产物的方法,该方法包括:
(a)在流体储藏器中提供包含第一反应物、第二反应物和流体介质的反应混合物,所述反应混合物的体积典型地在约1nL至约3mL的范围内;
(b)使反应混合物经历引起第一反应物与第二反应物之间的化学反应以产生反应产物的反应条件;
(c)以有效地将含有反应产物的流体液滴喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能。
在另一个实施方案中,本发明另外提供了一种确定分析物在两种溶剂的混合物中的分配系数D的方法,其中该方法包括:
(a)在流体储藏器中合并已知量X的分析物与第一体积V
由此形成具有第一溶剂的上层和第二溶剂的下层的两相流体组合物,其中分析物在第一溶剂中具有浓度C
(b)以声学方式喷射上层的液滴;
(c)确定在喷射的液滴中的C
(d)根据关系C
(e)通过确定C
在另一个实施方案中,本发明提供了一种确定分析物在两种溶剂的混合物中的分配系数D的声学方法,其中分析物的量可为已知的或未知的,并且该方法包括:
(a)在流体储藏器中合并分析物、第一体积V
(b)以声学方式喷射上层的液滴;
(c)确定在(b)中的喷射的液滴中的C
(d)从经分配的流体组合物中移出上层;
(e)以声学方式喷射下层的液滴;
(f)确定在(e)中的喷射的液滴中的C
(g)通过确定C
在本发明的又一个实施方案中,提供了一种用于从样品中提取目标分析物的声学系统,其中该系统包括:
(a)容纳流体组合物的流体储藏器,其中所述流体组合物是包含第一反应物、第二反应物和流体介质的反应混合物,所述反应混合物的体积在约1nL至约3mL的范围内;和
(b)与流体储藏器为声学耦合关系的声学液滴喷射器,用于以有效地将流体液滴从流体组合物喷射到液滴接收器中的方式产生声辐射,所述喷射器包括声辐射产生器和用于将声辐射聚焦在储藏器内的焦点处的聚焦装置。
在另一个实施方案中,本发明提供了从水性样品中移出金属离子的方法,其中该方法包括:
向包含目标分析物和金属离子的水性样品添加金属提取组合物,所述金属提取组合物包含包括(a)带正电荷的冠醚、带正电荷的穴状配体(cryptands,穴醚)或其组合和(b)带负电荷的抗衡离子的离子液体;
温热初始双相溶液直至两相变得可混溶,由此将金属离子与金属提取组合物混合在单相溶液中;和
冷却该单相溶液以产生第二双相溶液,所述第二双相溶液包括上部水层和金属提取组合物和金属离子的下层。
在一个相关的实施方案中,本发明提供了一种用于前述(或其他)方法的金属提取组合物,其包含带正电荷的冠醚、带正电荷的穴状配体或其组合和带负电荷的抗衡离子的离子液体。
在另一个实施方案中,本发明提供了一种液-液分离方法,其包括:
(a)在流体储藏器中提供流体组合物,其含有目标分析物和非分析物组分并且包括上层和下层,其中(i)目标分析物在上层中处于第一分析物浓度并且在下层中处于第二分析物浓度,以及(ii)非分析物组分在上层中处于第一组分浓度并且在下层中处于第二组分浓度;和
(b)以有效地将流体液滴从流体组合物喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能。
在又一个实施方案中,提供了一种液-液分离方法,其包括:
(a)提供在第一流体中包含目标分析物和非分析物组分的样品;
(b)将样品与第二流体合并以提供流体组合物;
(c)使流体组合物经历混合条件;
(d)使流体组合物沉降成包含上层和下层的分离的流体组合物,其中目标分析物在上层中具有上部分析物浓度并且在下层中具有下部分析物浓度,以及非分析物组分在上层中具有上部浓度并且在下层中具有下部组分浓度,其中(i)下部分析物浓度和上部分析物浓度不同,(ii)下部组分浓度和上部组分浓度不同,或(i)和(ii)两者。
附图说明
图1示意性地示出本发明的一个代表性方法,其中将脂质组分从生物样品中提取到上部有机层中,随后声学喷射脂质层。
图2和图3示意性地示出本发明的另一个代表性方法,其中将DNA从水性缓冲液中提取到离子液体中,之后以声学方式移出缓冲液(图2),然后使用提取缓冲液处理离子液体中的DNA以进行进一步分析(图3)。
图4示意性地示出本发明的一种方法,其中在两步提取过程中使用离子液体从生物样品中移出DNA。
具体实施方式
1.定义和术语:
除非另有定义,否则本文中使用的所有技术和科学术语都具有本发明所属领域的普通技术人员通常理解的含义。以下定义了对于本发明的说明书特别重要的特定术语。
在本说明书和所附的权利要求书中,单数形式的“一(a)”、“一个(an)”和“该(the)”包括复数对象,除非上下文另外明确指出。因此,例如,“一个流体”不仅指单一流体,而且还指可合并会或可合并的两种或更多种不同流体的组合,“溶剂”或“液体”,例如“离子液体”是指单一溶剂或液体,以及两种或多种溶剂和两种或多种液体,其中两种或多种溶剂或两种或多种液体可为分离的或合并的。
术语“辐射”以其通常的含义使用,并且是指通过介质行进的波形干扰形式的能量的发射和传播,使得能量从介质的一个粒子传递到另一个粒子而不会引起介质本身的任何永久位移。与当前基于声学的提取方法和系统结合使用的辐射是声辐射。
术语“声辐射”和“声能”在本文中可互换使用,并且是指声波形式的能量的发射和传播。与其他波形一样,可使用聚焦装置聚焦声辐射,如下所述。
术语“聚焦装置”和“声聚焦装置”是指用于使声波在焦点处会聚的装置,其通过与起到像透镜一样的作用的与声能源分开的设备来进行,或通过声能源的空间布置以通过相长和相消干涉在焦点处实现声能的会聚来进行。聚焦装置可像具有弯曲表面的固体构件一样简单,或者可包括例如在菲涅耳(Fresnel)透镜中发现的复杂结构,该复杂结构采用衍射来引导声辐射。合适的聚焦装置还包括本领域已知的并且例如在授予Nakayasu等的美国专利5,798,779和Amemiya等(1997)Proceedings of the 1997IS&T NIP13InternationalConference on Digital Printing Technologies,pp.698-702中描述的相控阵(phasedarray)方法。
本文中使用的术语“声学耦合”和“以声学方式耦合”是指一种状态,其中物体被放置成与另一物体直接或间接接触以允许声辐射在物体之间传递而基本上不损失声能。当两个物品间接地以声学方式耦合时,需要“声学耦合介质”以提供可通过其传输声辐射的中间物。因此,喷射器可以声学方式耦合至流体,例如,通过将喷射器浸没在流体中或通过在喷射器和流体之间插入声学耦合介质以使由喷射器产生的声辐射传递通过声学耦合介质并且传递到流体中。
如本文所使用,术语“流体储藏器”和“储藏器”是指用于容纳或含有流体的容器、腔室或表面区域。因此,储藏器中的流体必须具有自由表面,即允许液滴从其喷射的表面。在其最简单的形式之一中,储藏器可为固体表面上的一个位置,该位置具有足够的润湿性质以仅由于流体和表面之间的接触而将流体保持在局部的区域内,其中所述局部的区域用作储存器。
如本文所使用,术语“流体”是指至少部分为液体的物质。流体可含有最少地、部分地或完全地溶解、分散或悬浮的固体。流体的实例包括但不限于水性液体(包括水本身和盐水);水溶液;非水性液体例如有机溶剂等;非水溶液;胶体;悬浮液;乳液和凝胶。流体可为生物样品流体,其中所关注的分析物只是许多组分中的一种组分。
如本文所使用,术语“部分”是指物质的任何特定组成,例如分子片段,完整分子(包括单体分子、低聚物分子或聚合物),或其他材料或完整分子的混合物(例如,不同长度和/或序列的DNA的混合物)。
如本文所使用,术语“附近”是指从聚焦的声辐射的焦点到要从其喷射液滴的流体的表面的距离,并且表示该距离应使得聚焦的声辐射被引导到流体中引起液滴从流体表面喷射,因此本领域普通技术人员将能够使用直接而常规的实验为任何给定的流体选择适当的距离。然而,通常,声辐射的焦点和流体表面之间的合适距离为在流体中的声辐射(即,用于喷射液滴的声辐射)的波长的约1倍至约15倍的范围内,更典型地在该波长的约1至约10倍的范围内,优选在该波长的约1至约5倍的范围内。
术语“基本上”,如例如在短语“基本上相同的储藏器”中的“基本上”,是指在声学性质上没有实质性偏离的储藏器。例如,“基本上相同的储藏器”的声衰减彼此相差不超过10%,优选不超过5%,更优选不超过1%,并且最优选至多0.1%。术语“基本上”的其他用途涉及类似的定义。
流体样品中的“目标分析物”(有时在本文中简称为“分析物”)可为作为所关注的分析物的任何部分。分析物可为具有共同特征的原子、离子、盐、分子、一类分子(例如脂质或盐),其中该分子和分子类包括有机化合物、无机化合物和有机金属化合物。分析物可为在环境工作(例如,与水质评估有关)、制药领域、化学工业、能源领域以及许多其他领域中相关的分析物。分析物的代表性实例包括但不限于药物、代谢物、抑制剂、配体、受体、催化剂、合成聚合物、金属、金属离子、染料、农药(杀虫剂,例如DDT、芸香甙(eldrin)、四氯二苯并二噁英[TCDD]等)、致癌物(例如多环芳烃[PCAH])、变构效应剂、抗原和病毒(例如HIV、HPV、甲型肝炎、乙型肝炎、丙型肝炎、丁型肝炎、戊型肝炎、己型肝炎或庚型肝炎)、巨细胞病毒、爱泼斯坦-巴尔病毒、黄热病等)。目标分析物也可为多步反应中的反应产物或中间体。另外,目标分析物可为所关注的部分,其中本发明的提取方法涉及将分析物的某些级份从第一流体转移到第二流体中。目标分析物也可为要从流体中移出的组分,例如污染物。
通常,分析物是“生物分子”,在本文中也称为“生物学分子”,其中这些术语是指在细胞和组织中常见的任何分子实体,并且可为天然存在的、重组产生的、生物衍生的、全部或部分化学合成的或化学或生物修饰的。该术语包括,例如,核酸;氨基酸;肽,包括寡肽、多肽、蛋白质及其与非肽部分的结合物,例如核蛋白和糖蛋白;糖,包括单糖、二糖和多糖;脂质部分;以及前述物质中的任意两个或更多个的共价或非共价结合物,例如核蛋白、糖蛋白、脂蛋白、肽聚糖、粘多糖等。生物分子的代表性实例包括酶、受体、糖胺聚糖、神经递质、激素、细胞因子、细胞反应调节剂(例如生长因子和趋化因子)、抗体、疫苗、半抗原、毒素、干扰素、核酶、反义剂、质粒、DNA和RNA。
“核酸”本身可为核苷或核苷酸,但也可包括不仅含有常规嘌呤和嘧啶碱基(即,腺嘌呤(A)、胸腺嘧啶(T)、胞嘧啶(C)、鸟嘌呤(G)和尿嘧啶(U))而且还含有其保护形式(例如,其中碱基被保护基例如乙酰基、二氟乙酰基、三氟乙酰基、异丁酰基或苯甲酰基保护)以及嘌呤和嘧啶类似物的核苷和核苷酸。合适的类似物是本领域技术人员已知的,并且在相关的文本和文献中进行了描述。常见的类似物包括但不限于:1-甲基腺嘌呤,2-甲基腺嘌呤,N
核酸还包括寡核苷酸,其中出于本发明的目的,术语“寡核苷酸”是以下的通称:聚脱氧核糖核苷酸(含有2-脱氧-D-核糖),聚核糖核苷酸(含有D-核糖),为嘌呤或嘧啶碱基的N-糖苷的任何其他类型的聚核苷酸,以及含有非核苷酸主链的其他聚合物。因此,本文中的寡核苷酸分析物可包括寡核苷酸修饰体,例如,用类似物取代一个或多个天然存在的核苷酸,核苷酸间修饰体,例如具有不带电荷的连接单元(例如,甲基膦酸酯、磷酸三酯、氨基磷酸酯、氨基甲酸酯等)、具有带负电荷的连接单元(例如,硫代磷酸酯、二硫代磷酸酯等)和具有带正电荷的连接单元(例如,氨基烷基氨基磷酸酯和氨基烷基磷酸三酯)的那些,含有侧部分例如蛋白质(包括核酸酶、毒素、抗体、信号肽、聚-L-赖氨酸等)的那些,具有嵌入剂(例如,吖啶、补骨脂素等)的那些,含有螯合剂(例如,金属、放射性金属、硼、氧化性金属)的那些。术语“聚核苷酸”和“寡核苷酸”之间没有长度上的预期区别,并且这些术语可互换使用。这些术语仅指分子的一级结构。如本文所使用,核苷酸和聚核苷酸的符号根据IUPAC-IUB生化命名委员会推荐(Biochemistry 9:4022,1970)。
“肽”分析物(或“肽类”分析物)涵盖包括一个或多个氨基酸的任何结构,并且因此包括肽、二肽、寡肽、多肽和蛋白质。形成肽分析物的全部或一部分的氨基酸可为二十种常规的天然存在的氨基酸中的任何一种,即丙氨酸(A)、半胱氨酸(C)、天冬氨酸(D)、谷氨酸(E)、苯丙氨酸(F)、甘氨酸(G)、组氨酸(H)、异亮氨酸(I)、赖氨酸(K)、亮氨酸(L)、蛋氨酸(M)、天冬酰胺(N)、脯氨酸(P)、谷氨酰胺(Q)、精氨酸(R)、丝氨酸(S)、苏氨酸(T)、缬氨酸(V)、色氨酸(W)和酪氨酸(Y),以及非常规氨基酸,例如常规氨基酸的异构体和修饰体,例如,D-氨基酸、非蛋白质氨基酸、翻译后被修饰的氨基酸、酶修饰的氨基酸、β-氨基酸、设计为模拟氨基酸的构建体或结构体(例如,α,α-二取代的氨基酸、N-烷基氨基酸、乳酸、β-丙氨酸、萘基丙氨酸、3-吡啶基丙氨酸、4-羟基脯氨酸、O-磷酸丝氨酸、N-乙酰基丝氨酸、N-甲酰基甲硫氨酸、3-甲基组氨酸、5-羟基赖氨酸和正亮氨酸,以及其他非常规氨基酸,例如在授予Rosenberg等的美国专利No.5,679,782中所描述的。肽分析物可还含有非肽主链连接单元,其中天然存在的酰胺-CONH-连接单元在肽主链内的一个或多个位点处被非常规连接单元(例如N-取代的酰胺、酯、硫代酰胺、逆(retro)肽(-NHCO-)、逆硫代酰胺(-NHCS-)、磺酰胺基(-SO
“糖”或“糖类分析物”包括但不限于单糖、二糖、寡糖、多糖、粘多糖或肽聚糖(肽多糖)、假肽聚糖等,其中单糖(包括二糖、寡糖、多糖等中的单糖单元)包括己糖、戊糖和丁糖,并且可为D-或L-形式,并且进一步地其中单糖单元之间的糖苷连接单元可为α-糖苷连接单元或b-糖苷连接单元。糖类分析物的说明性实例包括:单糖果糖、葡萄糖、右旋糖、半乳糖、甘露糖、核糖、脱氧核糖、阿洛糖、岩藻糖、鼠李糖、赤藓糖、苏糖和甘油醛;二糖蔗糖、乳糖、麦芽糖、乳果糖、海藻糖、纤维二糖;多糖直链淀粉、支链淀粉、糖原、纤维素、几丁质、胼胝质、海带多糖、金藻昆布多糖、木聚糖和半乳甘露聚糖;和粘多糖(也称为糖胺聚糖)硫酸软骨素、硫酸皮肤素、硫酸角质素、肝素、硫酸乙酰肝素和透明质酸。
“脂质”或“脂质类分析物”是指疏水性或两亲性分子,并且包括脂肪酸、磷脂、甘油脂、甘油磷脂、鞘脂、糖脂和聚酮的宽泛类别。脂质类材料的代表性实例包括但不限于以下:磷脂,例如磷酸化的二酰基甘油酯,特别是选自二酰基磷脂酰胆碱、二酰基磷脂酰乙醇胺、二酰基磷脂酰丝氨酸、二酰基磷脂酰肌醇、二酰基磷脂酰甘油、二酰基磷脂酸以及其混合物的磷脂,其中每个酰基含有约10至约22个碳原子并且是饱和或不饱和的;脂肪酸,例如异戊酸,戊酸,己酸,庚酸,辛酸,壬酸,癸酸,月桂酸,肉豆蔻酸,棕榈酸,硬脂酸,花生酸,山萮酸,二十四烷酸,油酸,亚油酸酸,亚麻酸和花生四烯酸;包含前述脂肪酸的酯的低级脂肪酸酯,其中脂肪酸的羧酸基团-(CO)-OH被酯部分-(CO)-OR替代,其中R为任选地被一个或两个羟基取代的C
如本文中使用的那些术语“提取(Extraction)”和“提取(extracting)”是指涉及目标分析物从第一流体迁移到第二流体中的过程,并且因此涵盖如上一节中所解释的分离过程。该术语典型地是指组合物的一种组分(目标分析物)在两个流体相之一中相对于组合物的其他组分(例如污染物)的增强。提取可为完全的,这意味着目标分析物与样品的其他组分完全分离,因此在提取后,一个流体相含有100%的目标分析物。提取也可为部分的,在这种情况下,小于100%的目标分析物的一部分级份与组合物中的其他组分分离。相应地,使用本发明的方法进行提取可出于以下目的:提高或降低一种流体中的目标分析物的浓度;从一种流体中移出部分或全部分析物;浓缩一种流体中的分析物的量;分离分析物;纯化分析物;移出最初与目标分析物缔合的组分,例如污染物;或前述两种或更多种的组合。如本文所使用,术语“液-液提取”是指这样一种提取方法(过程),其中第一流体和第二流体独立地选自包含液体的流体;这样,液-液提取涵盖凝胶-液体提取、悬浮液-液体提取等。在此,提取过程与声学喷射方法(过程)相结合,使得从具有提高或降低浓度的目标分析物(相对于样品中或初始的、提取前的流体层或流体组合物中的目标分析物的初始浓度)或提高或降低浓度的非目标组分(相对于样品中或初始的、提取前的流体层或流体组合物中的非目标组分的初始浓度)的流体中以声学方式喷射流体液滴。
提及“含有”或“包含(包括)”分析物的样品包括已知含有分析物的样品(尽管分析物的身份(识别)可为未知的)和怀疑含有分析物的样品两者。
如本文所使用,术语“阵列”是指特征的二维布置,例如储藏器(例如,孔板中的孔)的布置或基底表面上的流体液滴或分子部分的布置(例如寡核苷酸或肽阵列)。阵列通常包括规则有序的特征,例如以直线网格、平行条纹、螺旋形等,但是也可有利地使用无序的阵列。阵列与图案的不同之处在于,图案不一定含有规则和有序的特征。另外,如本文所提供的,通过在表面上沉积喷射的液滴而形成的阵列和图案对于没有协助的人类肉眼通常是基本上不可见的。阵列典型地,但并非必须地,包括至少约4至约10,000,000个特征,通常在约4至约1,000,000个特征的范围内。
2.提取方法:
本发明在从流体组合物中提取目标分析物时利用声学液滴喷射(ADE)。在一个实施方案中,在提取过程中实施ADE以产生含有选定的浓度的目标分析物的流体液滴。在流体储藏器中提供了含有目标分析物的流体组合物,其中该流体组合物包括两个或更多个相。即,流体组合物包括上部区域或上层,以及一个或多个下部区域或下层,例如,流体组合物可包括两层、三层、四层或五层或更多层。为简单起见,将针对两相体系描述该方法,其中流体组合物包括第一流体的上层和第二流体的下层,其中第一流体和第二流体在提取所采用的条件下基本上不混溶。流体组合物中的目标分析物以第一浓度存在于第一流体中,并且以不同于第一浓度的第二浓度存在于第二流体中。通常,第一浓度和第二浓度相差至少约50%,例如至少约85%,例如至少50%、55%、60%、65%、70%、75%、80%、85%或更高。以有效地将流体液滴从流体组合物一般地(大体上)向液滴接收器喷射和喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能。选定的浓度,即喷射的流体液滴中的目标分析物的浓度,基本上等于第一浓度或第二浓度。另外,选定的浓度在整个液滴是基本上均匀的。在一个实例中,将目标分析物的一部分级份从一种流体(例如,含有生物样品的流体,例如细胞裂解物等)移动到第二流体。在另一个实例中,两种流体中的目标分析物的浓度可改变或可不改变,但是在提取过程之后,第二流体中可不存在与一种流体中的目标分析物缔合的组分。例如,提取后,一种流体可含有目标分析物和多种污染物,而第二流体含有不存在污染物或污染物的浓度显着降低的目标分析物。作为另一个实例,提取过程涉及改变一个或多个流体层中的目标分析物或其他组分的浓度。在前述实例的变型中,提取涉及两种目标分析物,其中该过程使得一个或多个流体层中的一种目标分析物的浓度提高而其他目标分析物的浓度降低。
由于本方法对于非常小的样品尺寸是有效的,因此储藏器中的全部流体组合物通常占据的体积不超过约125μL,例如,不超过约60μL,不超过约45μL,不超过约30μL等。
流体组合物可包括含有目标分析物的样品,例如生物样品。生物样品可包括溶解或悬浮在流体中的样品,或者生物样品本身可为流体的。生物样品包括,例如,组织、组织匀浆、细胞、细胞悬浮液、细胞提取物、全血、血浆、血清、唾液、痰、鼻分泌物、脑脊髓液、间质液、淋巴液、精液、阴道液或粪便。更典型的生物样品包括组织、细胞或血液。在提取之前,可或可不以某种方式处理生物样品;初步处理方法是本领域已知的,并且包括例如将抗凝剂掺入到血液样品中;将血液分离成血浆和血清;各种样品类型的交替离心和再悬浮程序;将防腐剂或含防腐剂的运输介质掺入到样品中;等等。然而,本发明在这方面不受限制,并且可容易地用未经过任何初步处理的生物样品以及非生物样品实施。
生物样品中的目标分析物包括但不限于蛋白质,肽,肽片段,脂质类化合物,以及核酸,特别是DNA。其他生物目标分析物和其他类型的目标分析物在本节的部分(1)“定义和术语”中列出。
使用两种或更多种流体提取目标分析物依赖于分析物对一种流体相对于另一种流体的不同亲和性。术语“亲和性”包括使分析物相对于另一种流体而分配到一种流体中的任何因素或因素的组合。这些因素的实例包括但不限于:分析物和流体相对于极性程度的相容性;分析物和流体之间的离子相互作用;分析物和流体之间的氢键;分析物和溶剂的相对亲水性或疏水性;以及更一般地且并非与前述因素无关地,分析物在流体中溶解的程度。
在一些实施方案中,本发明的提取过程涉及使用两种液体,其中目标分析物在所述两种液体中的溶解度是不同的,溶解度的差异对应于如上所解释的第一浓度和第二浓度的差异。溶解度的差异可为至少约50%,例如至少约85%,例如至少50%、55%、60%、65%、70%、75%、80%、85%。在一些实施方案中,溶解度的差异可小于约50%。在其他实施方案中,如上文所提及,溶解度差异是由于使用相对疏水的第一液体和相对亲水的第二液体,使得亲水部分将优先分配到亲水液体中,而疏水部分将优先分配到疏水液体中。这样的体系例如对于包含多种具有不同疏水性的组分的流体组合物是有用的,例如,含有疏水性与样品中还存在的其他组分的疏水性不同的目标分析物的样品。
在其他实施方案中,目标分析物可为极性分子或盐,在这种情况下,在提取过程中,将相对极性的溶剂(其可为质子或非质子的)与相对非极性的溶剂合并。对于经历氢键键合的目标物,质子溶剂是有用的;在这种情况下,将质子溶剂与可为或可不为非极性的非质子溶剂合并。
另外,一些分析物,包括但不限于某些离子分析物,可容易地用离子液体提取,如下文所解释。在一些情况下,使用离子液体来从另一种流体组合物中提取离子分析物。在其他情况下,使用这样的离子液体,其引起离子分析物优先分配到不是离子液体的第二流体组合物中。在一些情况下,这两个过程在多步提取方法(过程)中结合在一起,这将在以下进一步详细解释。
多种溶剂可与本发明结合使用。事实上,只要对本发明的提取过程没有不利影响,实际上可使用任何溶剂。当然,无毒溶剂是优选的。在单个提取步骤或过程中使用的液体的粘度、挥发性和其他化学和物理特性可不同。使用相对不粘的流体有助于从粘性材料中提取目标分析物。当一种溶剂是挥发性的时,可通过使用密度较低并且挥发性较低的第二溶剂来消除对蒸发的担忧;挥发性较低、密度较低的溶剂将在下部的挥发性较高的溶剂上形成上层,从而防止其蒸发。
可在本发明的方法和系统中采用的溶剂包括水性和有机溶剂、质子和非质子溶剂、离子和非离子液体、聚合物和非聚合物液体等。以组合形式,流体可形成单相、双相、三相或更高的多相流体组合物;在两种流体的组合下,所得流体组合物是单相或双相的。在一些实施方案中,本发明利用所选择的流体的可混溶的程度以及可使所选择的液体的组合或多或少地可混溶的条件。
可用于与本发明结合的溶剂的实例包括但不限于:乙酸,丙酮,乙腈,氨,苯,正丁醇,异丁醇,2-丁醇,叔丁醇,2-丁酮,乙酸丁酯,叔丁基醇,四氯化碳,氯苯,氯仿,环己烷,环己酮,环戊烷,1,2-二氯乙烷,二氯甲烷,乙醚,二乙二醇,二乙二醇二甲基醚(二甘醇二甲醚),二异丙基醚,1,2-二甲氧基乙烷(甘醇二甲醚,DME),二甲基醚,二甲基甲酰胺(DMF),二甲亚砜(DMSO),1,4-二噁烷,乙醇,乙酸乙酯,乙二醇,甲酸乙酯,甲酸,呋喃,甘油,庚烷,六甲基磷酰胺(HMPA),六甲基亚磷酸三酰胺(HMPT),正己烷,甲醇,甲基叔丁基醚(MTBE),二氯甲烷,甲基乙基酮(MEK),甲酸甲酯,N-甲基-吡咯烷酮(NMP),硝基甲烷,1-辛醇,正戊烷,石油醚(轻石油),哌啶,聚乙二醇,正丙醇,异丙醇,吡啶,四氢呋喃(THF),甲苯,三氯乙烯,三乙胺(TEA),水,氧化氘,邻二甲苯,间二甲苯,对二甲苯,以及授予Ellson等的两个美国专利No.6,548,308号和6,642,061(通过引用的方式并入本文)中描述的其他溶剂。优选的水性溶剂包括水、缓冲性化合物和/或盐的水溶液,例如磷酸盐缓冲液、Tris缓冲液、MES缓冲液、HEPES缓冲液、碳酸氢铵等。
本文中可用的溶剂体系和溶剂组合的具体实例包括但不限于:水性溶剂例如水或缓冲溶液,以及有机溶剂例如环己烷,二氯甲烷,1-辛醇,正戊烷,正丁醇或全氟化或半氟化的烷烃溶剂例如全氟庚烷、1,1,1,2,3,3-六氟丙烷、五氟戊烷等;水性溶剂例如水或缓冲溶液,以及脂质溶剂例如油;具有两个水层的二元体系,其中水性液体含有不同的溶质并且是不溶混的——参见,例如,Partitioning in Aqueous Two-Phase System:Theory,Methods,Uses,and Applications to Biotechnology,Eds.Harry Walter等(AcademicPress,1985);Hamta等(2017),"Application of polyethylene glycol based aqueoustwo-phase systems for extraction of heavy metals,"Journal of MolecularLiquids231:20-24;和Eiden等(2016),"Two-Phase System Rehydration of Antibody-Polymer Microarrays Enables Convenient Compartmentalized MultiplexImmunoassays,"Analytical Chemistry 88(23)(还参见Tavana等(2010)Adv.Mater.22(24):2628-2631和Fang等(2012)Tissue Engineering Part C:Methods 18)9):647-657);含有相同溶质但具有不同pH的两种水性液体的组合会出现这种情况,例如,两种具有相同缓冲液组成但第一和第二水性液体被缓冲至不同pH的水性液体;以及具有两个有机层的二元体系,其中有机液体是不溶混的,例如乙醇/环己烷的结合、己烷/二氯甲烷的结合、醚/氯仿的结合等;
在提取所采用的条件下,为提取过程选择的两种流体应该是不混溶的。如本领域所理解的,混溶性是指一种流体在另一种流体中溶解的程度。该溶解度可随温度、液体静压力或其他因素而变化,并且该变量可有利地结合到本方法中。即,可使流体组合物经历引发相变并且使两种流体可混溶的条件,使得目标分析物与两种流体充分混合。此后,可使流体组合物经历使两种流体回到不混溶状态的条件,使得声能可将两个流体层之一中的聚焦区作为目标,并且喷射仅由两层之一形成且主要仅包含两层之一的流体液滴。溶剂在各种条件下的混溶性可通过参考相关的文本和文献来确定,和/或可通过合并两种溶剂并且确定在一个范围的温度、压力等条件下的混溶性来凭经验确定。最通常地,本文中的两种流体的混溶性通过如下改变:温度的变化(使得升高或降低含有两种流体的流体组合物的温度而改变其互溶性)和/或以化学方式,例如通过添加盐例如氯化钠或通过改变pH。在一些情况下,本提取过程中采用的两种流体在约40℃和约90℃之间可混溶,
应当理解,目标分析物和两种流体也可在提取之前使用其他技术进行混合,例如重复倒置容纳分析物和流体的容器、搅拌、超声、搅动、调节流体温度、将一种流体的液滴喷射(例如,声学喷射)通过另一种流体(如图2中所示,下文讨论)等。
在一个实施方案中,提取方法涉及使用离子液体。如本节的部分(1)所述,离子液体包括液体形式的盐。即,与主要由电中性物质组成的普通液体相比,离子液体主要或全部由离子组成(即,“基本上为离子的”,这意味着基本上所有的离子液体都是离子的)。与本发明结合使用的优选的离子液体为纯离子的或基本上为离子的,并且在提取条件下呈液体状态。更优选的离子液体是“室温离子液体”(RTIL)。RTIL包括具有相对低的熔点并且在低于100℃的温度下(例如在约0℃至约100℃范围的温度下)呈液体形式的盐。在本文中RTIL是优选的,只要它们提供有利于可在不改变流体组合物的温度的情况下进行的提取过程的便利性。离子液体可用于提取离子分析物,例如带负电荷的分析物,例如DNA,但也可用于提取其他类型的分析物。常见的离子液体包括但不限于咪唑鎓盐、吡咯烷鎓盐、哌啶鎓盐、吡啶鎓盐、吗啉鎓盐、铵盐、鏻盐、锍盐和胍盐。合适的离子液体列在例如由Sigma-Aldrich(2012年10月)和EMD Chemicals Inc.发布的离子流体目录中,并且可作为市售产品获得。以下提供离子液体的具体实例。在以下列表中,阴离子的缩写如下:
乙酸根(CH
双[草酸根(2-)]硼酸根,bob;
双(三氟甲基磺酰基)酰亚胺,Tf
双氰胺,DCA;
甲酸根(HCO
六氟磷酸根,PF
硫酸氢根,HSO
羟基乙酸根(CH
甲烷磺酸根(甲磺酸根),CH
2-(2-甲氧基乙氧基)乙基硫酸根,CH
甲基硫酸根(CH
辛基硫酸根(C
硝酸根,NO
氨基磺酸根,H
四氰基硼酸根,B(CN)
四氟硼酸根BF
硫氰酸盐,SCN
对甲苯磺酸根,或甲苯磺酸根,Tos;
三氰基甲烷(C(CN)
三氟乙酸根(CF
三氟甲烷磺酸根(三氟甲磺酸根,CF
三(五氟乙基)三氟磷酸根,FAP。
代表性的离子液体包括但不限于以下,其中应理解为第一个所示的物质是阳离子而第二个所示的物质是阴离子(其中省略了正号和负号以符合标准化的离子液体命名法):
1-苄基-甲基咪唑鎓(Zmim)盐,例如[Zmim][Cl];
N,N-双(2-羟乙基)丁基铵(HEBA)盐,例如[HEBA][Tf
双(2-羟乙基)铵(HEA)盐,例如[HEA][TFA]和[HEA][OAc];
双(2-甲氧基乙基)铵(MEA)盐,例如MEA氨基磺酸盐;
1-丁基-2,3-二甲基咪唑鎓(Bmmim)盐,例如[Bmmim][Cl]、[Bmmim][I]、[Bmmim][PF
1-丁基-3-甲基咪唑鎓(Bmim)盐,例如[Bmim][Tf
1-丁基-3-甲基吡啶鎓(B3mpy)盐,例如[B3mpy][Cl]、[B3mpy][DCA]、[B3mpy][MeSO
1-丁基-4-甲基吡啶鎓(B4mpy)盐,例如[B4mpy][Cl]和[B4mpy][BF
1-丁基-1-甲基吡咯烷鎓(Bmpyr)盐,例如[Bmpyr][bob]、[Bmpyr][Tf
氯化N-丁基吡啶鎓(Bpy)盐,例如[Bpy][Cl]、[Bpy][PF
N,N-二甲基(2-羟乙基)铵(MMHEA)盐,例如[MMHEA][HOOAc]、[MMHEA][Tf
1,3-二甲基咪唑鎓(Mmim)盐,例如[Mmim][Cl]、[Mmim][Br]和[Mmim][MeSO
1,1-二甲基吡咯烷鎓(MMpyr)盐,例如[MMpyr][I]和[MMpyr][Tf
N-十二烷基-N,N-二甲基-3-磺丙基铵Tf
1-(2-乙氧基乙基)-1-甲基吡咯烷鎓(EOEMpyr)盐,例如[EOEMpyr][Tf
1-乙基-2,3-二甲基咪唑鎓(Emmim)盐,例如[Emmim][Br]、[Emmim][Cl]、[Emmim][MeSO
N-乙基-N,N-二甲基-2-甲氧基乙基铵Tf
N-乙基-N,N-二甲基-丙基铵Tf
1-乙基-3-甲基咪唑鎓(Emim)盐,例如[Emim][bob]、[Emim][Tf
胍(gua)盐,例如[gua][OTf]和[gua][FAP];
1-十六烷基-2,3-二甲基咪唑鎓(Cmmim)盐,例如[Cmmim][Cl];
1-十六烷基-3-甲基咪唑鎓(Cmim)盐,例如[Cmim][Cl]和[Cim][FAP];
1-己基-1-甲基吡咯烷鎓(Hmpyr)盐,例如[Hmpyr][Tf
1-己基-2,3-二甲基咪唑鎓(Hmmim)盐,例如[Hmmim][Cl]和[Hmmim][FAP];
1-己基-3-甲基咪唑鎓(Hmim)盐,例如[Hmim][Tf
N-己基吡啶鎓(HPy)盐,例如[HPy][Cl]、[HPy][Tf
1-(2-羟乙基)-3-甲基咪唑鎓(HOE-Mim)盐,例如[HOE-Mim][Tf
N-(3-羟丙基)吡啶鎓(HOP-Py)盐,例如[HOP-Py][Tf
1-(3-甲氧基丙基)-1-甲基哌啶鎓(MOPMpi)盐,例如[MOPMpi][Tf
1-甲基咪唑鎓(Mim)盐,例如[Mim][BF
甲基三辛基铵[MOc
1-辛基-3-甲基咪唑鎓(Omim)盐,例如[Omim][Cl]、[Omim][I]、[Omim][BF
1-辛基-1-甲基吡咯烷鎓(OMpyr)盐,例如[OMpyr][Cl];
1-丙基-3-甲基咪唑鎓(Pmim)盐,例如[Pmim][I];
1-(3-磺丙基)-3-丁基咪唑鎓Tf
N-(3-磺丙基)-吡啶鎓Tf
四丁基铵(NB
四甲基铵(Nm4)盐,例如[Nm4][bob]和[Nm4][FAP];
三己基(十四烷基)鏻(P(h3)t)盐,例如[P(h3)t][bob]、[P(h3)t][Tf
1,2,3-三甲基咪唑鎓(Mmmi)盐,例如[Mmmi][I];
2-氨基-1,6-二甲基咪唑并[4,5-b]-吡啶盐,例如2-氨基-1,6-二甲基咪唑并[4,5-b]-吡啶Tf
三乙基十六烷基鏻(THP)盐,例如[THP][DCN]。在本文中特别感兴趣的是[Bmim][Tf
聚合物型离子液体也可与本发明结合使用。聚合物型离子液体在本领域中是已知的,并且例如在以下中描述:Shaplov等(2011),"Polymeric Ionic Liquids:Comparisonsof Polycations and Polyanions,"Macromolecules44(24):9792-9803;Wu等(2017),"Polymerizable ionic liquids and polymeric ionic liquids:facile synthesis ofionic liquids containing ethylene oxide repeating unit via methanesulfonateand their electrochemical properties,"RSC Advances 7:5394-5401;以及Mecerreyes等(2011),"Polymeric ionic liquids:Broadening the properties and applicationsof poly electrolytes,"Progress in Polymer Science36(12):1629-1648。还适合用于本文中的是由Zhang等(2015)Molecules20:17378-17392描述的基于热响应性聚(离子液体)的纳米凝胶,该出版物中还描述了其制备。
应理解的是,离子液体的前述列表仅是说明性的,而不是旨在进行限制。可用于本文中的其他离子液体包括以下描述的那些:Plechkova等(2008)Chem.Soc.Rev.37:123-150;Branco等,"Physico-Chemical Properties of Task-Specific Ionic Liquids,"inIonic Liquids:Theory,Properties,New Approaches,Ed.A.Korkorin(Intech,2011);以及Plechkova等(2015),in Ionic Liquids Completely Uncoiled(Wiley,2015)。还可用于与本发明方法结合的其他离子液体在文献中的其他地方有所描述和/或对于本领域普通技术人员将是显而易见的。用于本文中的通常优选的离子液体能够从样品中提取显著级份的目标分析物(量级为50%或更多,例如50%至100%,50%至95%,50%至85%,50%至75%等),和/或提供一种流体组合物,其中最初与目标分析物缔合的至少一种非目标组分(例如,至少一种污染物)的浓度在流体层之一中降低(例如降低至少50%,例如50%至100%,50%至95%,50%至85%,50%至75%等)。优选的离子液体是相对无毒的,并且在实验室中易于使用,并且对流体储藏器表面具有高亲和性,从而将水性提取流体浓缩在储藏器中心。在一些情况下,可期望所选择的离子液体具有可听的声阻抗。另外,在一些情况下,呈现出基于分析物尺寸的提取偏差(extraction bias)的离子液体是优选的,而在其他情况下,优选的离子液体是不呈现出与分析物尺寸有关的提取偏差的离子液体(核酸分析物(例如DNA)通常是这种情况)。
在一些实施方案中,在本提取过程中使用的离子液体是磁性离子液体。磁性离子液体作为磁珠的液体形式起作用,并且含有所关注的目标分析物的磁性离子液体可被拉到流体储藏器的一侧,以允许容易地移出耗尽的非离子(例如水)层。磁性离子液体(MIL)在本领域中是已知的,并且已在文献中进行了描述。参见,例如,Clark等(2015)Anal.Chem.87:1552-1559。如其中所述,MIL的实例包括苄基三辛基铵溴三氯高铁(III)酸盐和1,12-二-(3-十六烷基-苯并咪唑鎓)十二烷双[((三氟甲基)磺酰基]酰亚胺溴三氯高铁(III)酸盐。
在一个实施方案中,该方法用于从生物样品中提取生物分子,其中该生物分子相对于第二液体优先分配到第一液体中,并且在完成混合和后续的分配之后使用声学喷射技术移出两相之一。例如,并且如将在下文中进一步详细描述的,可实施声学喷射技术,以从流体储藏器中快速且相继地喷射含分析物的上部流体层的液滴,其中在流体储藏器中将含分析物的流体液滴喷射到液滴储藏器中用于进一步处理和/或分析。还可实施声学喷射技术,以重复地喷射不含有分析物的上部流体层的液滴,由此从流体储藏器中移出不含分析物的上部流体,并且使分析物保留在下部流体层中。
这种方法的一个实例描绘在图1中。在图1中,在流体容器中提供生物样品。样品是在水性流体中的多组分混合物。添加第二流体,其由于至少一种组分对第二流体的亲和(preference)而从样品中移出该组分。然后可通过倾析或更优选地通过使用例如下文将描述的聚焦声学喷射系统进行的重复的声学喷射从流体容器中移出上层。在图1中示出的具体实例中,期望从生物样品中移出脂质类组分。相应地,“第一流体”是水性样品本身,例如50μL的细胞分析物(其中术语“细胞分析物”在本文中用于指可已经或未经处理到一定程度的细胞样品,细胞裂解物),如图所示,含有核酸、蛋白质、脂质和其他组分。由于脂质在非极性或低极性溶剂中的溶解度远远更高,因此所选择的“第二流体”是有机溶剂,例如10μL的乙醚。在该提取过程之后,可如上所述移出水层的顶部上的含脂质的醚层。
引人关注的是,如在图1中可看到的那样,在所选择的流体储藏器中合并具有不同性质的两种溶剂可导致弯液面倒转。即,在添加第二流体之前,第一流体具有凹的弯液面,但是在添加第二流体时,凹的弯液面在流体-流体边界处转变成凸形。在多种情况下这可为期望的。例如,在声辐射聚焦在流体容器的中心点处的情况下,下部流体可通过中心“液体孔”喷射而不接触(或最小程度地接触)上部流体层。这允许省略上层移出步骤,从而简化了整个提取过程。通过使用具有吸引或排斥特定流体类型(例如,有机溶剂、水性液体、离子液体等)的内部表面的流体储藏器,可实现以这种方式进行的弯液面的倒转。具有这样的内部表面的流体储藏器可从许多来源商购获得,例如,以具有不同类型涂层的微孔板。
将针对相对于非离子液体优先分配到离子液体中的生物分子的提取来描述本发明的提取过程的另一个实例。一种重要的这样的生物分子是DNA,其可为或可不为双链DNA(dsDNA)。这种方法的第一步在图2中示意性地示出。可最初通过裂解其中的细胞和/或组织材料来处理生物样品,然后将样品再悬浮在合适的水性缓冲液(例如Tris缓冲液)中,在本文中称为“初始缓冲液”。生物样品还可包括循环的无细胞DNA。当在微孔板(例如384-孔板)中进行时,将已知量的离子液体添加到多个孔中的每个孔中,因为各个孔用作进行提取的流体储藏器。选择离子液体以对DNA具有强的亲和性,并且选择初始缓冲液使得DNA优先分配到离子液体中,即相对于缓冲溶液。如图2所示,该方法可涉及向各个孔中添加5至30μL,例如25μL的离子液体,例如[Bmim][PF
如图2所示,两种液体的密度可不同。图2提供了代表性的和非限制性的密度数,离子液体密度通常被示为大于1.3g/mL,并且DNA水溶液的密度约为1.1g/mL。结果,倒置的流体储藏器中的两种液体将分配为代表在孔的“底部”上的上层的水性缓冲液以及作为下层的在缓冲液下方的含有DNA的离子液体。然后,可将孔板倒置,从而切换两层的相对位置,如图所示。即,在倒置之后,含有DNA的离子液体处于孔的底部,并且水性缓冲液层已经上升穿过离子液体层并在离子液体层上方。
此时,采用进一步的步骤以移出水性缓冲液层。该步骤利用第二水性缓冲溶液,在本文中称为“提取缓冲液”。与初始缓冲液相反,选择提取缓冲液使得DNA优先从离子液体分配到提取缓冲液中。初始缓冲液和提取缓冲液可含有不同的缓冲液组分,或者它们可含有相同的缓冲液组分但具有不同的pH水平。该过程在图3中示意性地示出。在这种情况下,将提取缓冲液引入到其中含有具有DNA的离子液体的流体储藏器中,然后将两种液体混合。由于微孔板中的微孔可很容易地用作流体储藏器,因此可通过多次快速倒置孔板来简单地实现混合。在混合并且留出时间使两相分离后,每个储藏器均含有作为下层的离子液体以及作为上层的提取缓冲液(其中具有DNA)。上层——即水性DNA层——可用任何合适的方式移出,但是声学喷射该层是优选的。如上所述,使用声学喷射,可将该层转移到倒置的各个容器中,或者可以将其以声学方式直接喷射到分析仪器(例如质谱仪)中。使用声学喷射将DNA水溶液转移至分析仪器可如Sinclair等(2016)Journal of Laboratory Automation 21(1):19-26和授予Ellson等(Labcyte Inc.,San Jose,CA)的美国专利No.7,405,395所描述的来进行,两者都通过引用的方式将其全部内容并入本文。如果需要的话,使用声学液滴喷射将含DNA的水性液体转移至分析仪器可用非常少的样品(大约几纳升的级别)进行。另外,可非常快速地将声音转移至分析仪器,每小时能够产生超过10,000个数据点,因此非常理想地适合于高通量处理(方法)。
在另一个实施方案中,提供了使用三种不同流体的提取方法,其中在第一步中使用第一流体和第二流体,目标分析物分配到第二流体中,但是在第二步中使用第二流体和第三流体,目标分析物分配到第三流体中。即,当替代物是第一流体时,目标分析物优先分配到第二流体中,但是相对于第二流体而言第三流体是优先的(优选的)。选择第一、第二和第三流体,以从样品中移出多种物质,例如,用于单独处理的分析物或污染物,由此在第三流体中提供目标分析物的较纯溶液。此方法的实例如下:将水性生物样品(即,第一流体,含有DNA作为目标分析物)与离子液体(即,第二流体,目标分析物将分配到其中)混合,以及使之分配为上部水层和下部离子液体层。选择离子液体,使得在该第一步中DNA将分配到该层中。然后移出上层,优选使用如本文其他地方所述的声学喷射移出,从而留下在离子液体中包含DNA(目标分析物)的流体组合物。在随后的步骤中,将含有DNA的离子液体与具有一定pH的水性提取缓冲液混合,选择所述pH使得DNA的至少60重量%(并且优选至少75重量%,例如DNA的至少85重量%、至少90重量%、至少95重量%或100重量%)现在将从离子液体移动到提取缓冲液中,该提取缓冲液在离子液体的顶部上形成上部流体层。然后可像之前一样以声学方式喷射含DNA的水层。
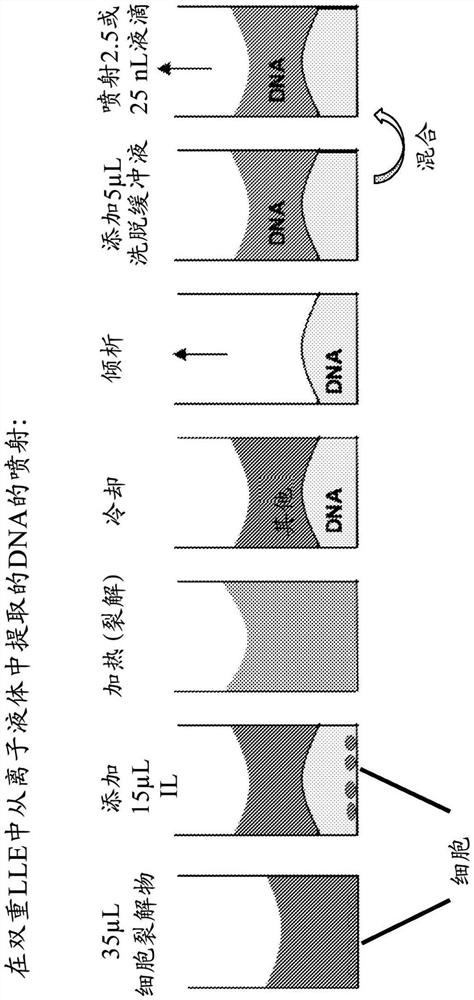
图4示意性地示出了使用35μL的含有DNA作为目标分析物的生物样品(在图中示为细胞裂解物)的前述双重提取方法。生物样品容纳在一个储藏器中,所述储藏器可为独立的单个储藏器、一组其他这样的储藏器之一的独立的储藏器(例如,容纳其他管(试管)的管架中的管)、微孔板(例如384-孔板)中的孔等。如图所示,“第一流体”可为含有DNA的水性缓冲液。将离子液体添加至流体储藏器,形成在水相下方的下层。使用合适的方法将两个流体层混合;加热是优选的,如图4所示。加热不仅会混合各层并使它们可混溶(条件是选择合适的离子液体,使得可使其在相对温和的温度下与水性液体可混溶),而且还使生物样品中的细胞裂解,释放细胞内容物。DNA仍将优先保留在离子液体中,条件是将第一流体缓冲至合适的pH,即在该pH处DNA将分配到离子液体中而不是保留在水相中。通过倾析、水喷射或任何其他合适的方法移出含有不期望的细胞组分的上部流体;同样,优选的方法涉及聚焦声学喷射。在移出水相之后,含有目标分析物的离子液体的单一相保留在流体储藏器中。然后添加提取缓冲液,并且将两相混合。在一个实施方案中,如上所解释,将提取缓冲液缓冲至一定pH,所述pH被选择为使得DNA的至少60重量%(并且优选DNA的至少75重量%等,如上)可从离子液体移动到提取缓冲液中,提取缓冲液形成上部水性碱。然后可像之前一样以声学方式喷射含DNA的水性流体层。
3.反应产物
如本文前面所解释的,目标分析物不限于包含在生物样品中或源自生物样品的分析物。目标分析物可为无机化合物、有机金属化合物或甚至是原子或离子;请参阅本节的部分(1)。然后,在又一个实施方案中,目标分析物可为多步反应中的反应产物。即,本发明另外提供了一种合成和声学提取反应产物的方法,其中该方法包括:在流体储藏器中提供第一反应物、第二反应物和包含第一液体的流体介质的反应混合物;使反应混合物经历引起第一反应物和第二反应物之间发生化学反应以产生具有第一溶解度的反应产物的条件;将与第一液体不混溶的第二液体混合到反应混合物中,并且其中反应产物在第二液体中的第二溶解度与所述第一溶解度相差至少50%,由此提供流体组合物,其具有含有不同浓度的反应产物的上层和下层;和以有效地将含有反应产物的流体液滴喷射到液滴储藏器中的方式向流体储藏器施加聚焦的声能。反应混合物可进一步包括反应催化剂、表面活性剂或另外的有用的组分。当使用反应催化剂和/或表面活性剂时,可选择两种液体,使得反应产物分配到一层中并且催化剂和/或表面活性剂分配到另一层中,从而使得能够从反应产物中移出这些其他部分。在前述方法的一种变型中,反应产物不必分配到两层之一中,但是其他组分,即催化剂和表面活性剂(其相对于反应产物而言可视为污染物),相对于另一层对一层确实具有亲和性。因此,在这种情况下的提取过程使得污染物从一层移动至另一层而目标分析物没有伴随的移动,因此两层都含有目标分析物,但是其中一层的污染物的浓度要低得多。
反应条件通常但非必须地选自:使反应在反应混合物中进行预定的反应时间;混合反应物;改变反应混合物的温度;向反应混合物添加至少一种催化剂;向反应混合物添加至少一种表面活性剂;将至少一种另外的反应物引入到反应混合物中;以及前述的两种或更多种的组合。
在本发明的一个相关方面中,提供了一种合成和声学转移反应产物的方法。该方法包括以下步骤:
(a)在流体储藏器中提供包含第一反应物、第二反应物和流体介质的反应混合物,所述反应混合物的体积典型地在约1nL至约3mL的范围内;
(b)使反应混合物经历引起第一反应物与第二反应物之间的化学反应以产生反应产物的反应条件;和
(c)以有效地将含有反应产物的流体液滴喷射到液滴接收器中的方式向流体储藏器施加聚焦的声能。
反应条件如上,即选自:使反应在反应混合物中进行预定的反应时间;混合反应物;改变反应混合物的温度;向反应混合物添加至少一种催化剂;向反应混合物添加至少一种表面活性剂;将至少一种另外的反应物引入到反应混合物中;以及前述的两种或更多种的组合。
在一个相关的实施方案中,提供了一种用于从样品中提取目标分析物的声学系统,其中该系统包括:(a)容纳流体组合物的流体储藏器,其中所述流体组合物是包含第一反应物、第二反应物和流体介质的反应混合物,所述反应混合物的体积在约1nL至约3mL的范围内;和(b)与流体储藏器为声学耦合关系的声学液滴喷射器,用于以有效地将流体液滴从流体组合物喷射到液滴接收器中的方式产生声辐射,所述喷射器包括声辐射产生器和用于将声辐射聚焦在储藏器内的焦点处的聚焦装置。在一个实施方案中,液滴接收器是倒置的流体储藏器,例如倒置的微孔板中的孔。在另一个实施方案中,液滴接收器是分析仪器,例如质谱仪,并且喷射到质谱仪中的液滴——直接或间接地——通过该仪器进行分析。
4.金属离子的提取
在另一个实施方案中,提供了一种从水性样品中移出金属离子(例如碱金属离子和碱土金属离子)的提取方法,所述水性样品含有目标分析物和至少一种碱金属离子(典型地为锂阳离子、钠阳离子或钾阳离子)和/或至少一种碱土金属离子(例如钙或镁离子)。这在质谱分析的情况下特别有用,其中含有所关注的目标分析物的水性流体被转移(例如,通过声学喷射)到质谱仪中进行分析。离子抑制,即抑制目标分析物离子化,是质谱领域中众所周知的问题,并且离子抑制的最常见的原因之一是存在显著量(10
相应地,在该实施方案中,提供了一种从生物样品和其他水性组合物中有效地提取碱金属和/或碱土金属的新方法。该方法涉及向包含目标分析物和碱金属离子和/或碱土金属离子的水性样品添加金属提取组合物,所述金属提取组合物包含离子液体和选自冠醚、穴状配体及其组合的结合金属的化合物,由此形成初始双相溶液;向双相溶液施加条件,使得两相变得可混溶(例如加热),由此将金属盐与金属提取组合物混合在单相溶液中;和重新产生双相溶液,例如通过冷却,其中在该步骤中产生的双相溶液包括上部水层以及金属提取组合物和金属离子的下层。然后可将水层喷射到质谱仪(或其他类型的液滴接收器)中以分析目标分析物。金属提取组合物包含离子液体和结合金属的化合物,其重量比在约1:100至约100:1的范围内,更典型地在约1:10至约10:1的范围内。
优选的结合金属的化合物是冠醚,例如12-冠-4、15-冠-5和18-冠-6。一种特别优选的结合金属的化合物包括这样的冠醚,该冠醚已经通过用阳离子部分官能化而转化为离子液体,典型地但不是必须地,用对应于包含在本节的部分2“提取方法”中列举的液体盐内的阳离子官能化。通过举例而非限制的方式,以这种方式进行的冠醚的修饰可通过用与带负电荷的抗衡离子缔合的含有带正电荷的氮原子的官能团替代氢原子(C-H基团内)来实现。一种这样的冠醚盐具有式(I)的结构:
(I):
其中R可选自叔氨基和氮杂环,并且X是阴离子物质例如卤离子。这样的冠醚盐的一个具体实例具有式(II)的结构
(II):
该冠醚盐可使用类似于Dharaskar等(2016),"Synthesis,characterization andapplication of l-butyl-3-methylimidazolium tetrafluoroborate for extractivedesulfurization of liquid fuel,"Arabian Journal of Chemistry 9:578-587中描述的技术由氯甲基18-冠-6和N-甲基咪唑合成。
在一个相关的实施方案中,本发明提供了一种用于前述提取(或其他)方法的金属提取组合物,其中该组合物包含离子液体和选自冠醚、穴状配体及其组合的结合金属的化合物。应当注意,这些官能化的冠醚和穴状配体在本发明的提取方法中可起到双重目的,它们是对某些类型的目标分析物具有选择亲和性的离子液体,以及用于移出碱金属离子和碱土金属离子的螯合剂。
5.确定分析物在两种溶剂中的分配系数:
在任何提取方法中,包括本文所述和要求保护的提取方法,知晓特定目标分析物在两种溶剂中的分配系数都极其有用。一种溶剂可为水,如在水性生物样品、水性缓冲液等中,并且另一种溶剂可为考虑用于提取方法的候选溶剂。相应地,在又一个实施方案中,本发明提供了一种确定分析物在两种溶剂的混合物中的分配系数D的方法,其中该方法包括以下步骤:
(a)在流体储藏器中合并已知量X的分析物与第一体积V
(b)以声学方式喷射上层的液滴;
(c)确定在喷射的液滴中的C
(d)根据关系C
(e)通过确定C
在一个相关的实施方案中,提供了一种确定在两种溶剂中的分配系数D的方法,其包括:
(a)在流体储藏器中合并分析物、第一体积V
(b)以声学方式喷射上层的液滴;
(c)确定在(b)中的喷射的液滴中的C
(d)从经分配的流体组合物中移出上层;
(e)以声学方式喷射下层的液滴;
(f)确定在(e)中的喷射的液滴中的C
(g)通过确定C
6.声学喷射和高通量处理:
声学喷射使得能够快速处理以及产生具有预定和一致尺寸的纳升尺寸的液滴;参见授予Steams等的美国专利No.6,416,164,其在先通过引用的方式并入本文。前述专利描述了如何可通过改变声功率、声频率、猝发音持续时间和/或聚焦透镜的F数(通常优选F数大于约2的透镜)来仔细控制从流体表面喷射的液滴的尺寸。因此,ADE使得“超单分散”液滴的喷射成为可能,这在本发明的上下文中意味着喷射的颗粒具有一致的直径,具有约1%的变化系数。这继而使得能够将精确且预定量的流体样品引入到系统中以进行分析。使用声学喷射的另一个优点是可从非常小的样品尺寸(5μl或更小的级别)喷射液滴。当样品的可用性受到限制并且出于必要性必须分析小的流体样品时,这是特别有利的。在处理能力方面,授予Mutz等的美国专利No.6,938,995解释了,声学喷射技术与对多个储藏器中的流体样品的声学评估结合使用,可实现每秒分析超过5个、10个或甚至25个储藏器,转换(translating)为每天超过50,000个流体样品。
由于使用声学喷射技术可能达到的精度,因此本系统可用于以声学方式喷射非常小的尺寸的流体液滴样品。然而,本发明在这方面不受限制,并且以声学方式喷射的液滴的体积可在约0.5pL至约3mL的范围内。对于许多应用,本发明的系统用于产生纳升尺寸的流体液滴以进行分析,其中“纳升尺寸”的液滴通常含有至多约30nL的流体样品,典型地不超过约10nL,优选不超过约5.0nL,更优选不超过约3.0nL,例如不超过1.0nL,不超过约50pL,不超过约25pL,并且不超过约1pL,包括约0.5pL至2.0nL的范围,约0.5pL至1.5nL,约0.5pL至1.0nL,约1.0pL至2.0nL,约1.0pL至1.5nL,约1.0pL至1.0nL等。典型的运行范围产生在约1nL至约30nL的范围内的液滴。如以下将详细描述的,使用声学喷射器从流体样品的表面进行液滴的声学喷射。在缺乏易于自动化的样品制备和上样、保存样品的需要、消除交叉污染的需要、无法直接从流体储藏器进入到分析设备中以及无法产生适当尺寸的液滴而使得HTMS受到了阻碍的情形下,声学喷射技术特别适用于高通量处理,特别是高通量质谱(HTMS)。
然后,在一个实施方案中,本发明的系统和方法利用声学喷射器作为流体样品液滴产生设备,以在液-液提取的情况下从流体组合物中喷射液滴。声学喷射器以引起从流体的表面向上喷射流体液滴的方式将声能引导到容纳含分析物的流体组合物的储藏器中。
该系统还可包括用于以声学耦合关系安置储藏器和声学喷射器的装置。典型地,使用单个喷射器,其包括声辐射产生器和用于聚焦由声辐射产生器产生的声辐射的聚焦装置。但是,也可有利地使用多个喷射器。同样,尽管可使用单个储藏器,但是该设备典型地包括多个储藏器,例如如阵列。当该系统用于从多个储藏器中的每一个中喷射含分析物的流体样品的液滴时,并入安置装置以相对于声学喷射器移动容纳储藏器的基底(例如,可将其安置在可移动平台上),反之亦然。由此容易地促进了从一系列的储藏器中的每一个中快速且相继地声学喷射流体液滴。两种类型的安置装置,即喷射器安置装置或储藏器或储藏器基底安置装置,都可由例如电动机、杠杆、滑轮、齿轮、其组合或其他机电或机械装置构造而成。
尽管任何声学液滴喷射系统都可与本系统和方法结合使用,但是优选的ADE系统是在以下美国专利、其所有的共同转让中描述的系统,并且通过引用的方式并入本文:授予Steams等的美国专利No.6,416,164;授予Ellson等的6,666,541;授予Ellson等的6,603,118;授予Ellson等的6,746,104;授予Ellson等的6,802,593;授予Ellson等的6,938,987;授予Mutz等的7,270,986;授予Ellson等的7,405,395;授予Mutz等的7,439,048。用于本文中的优选的ADE系统是可从Labcyte Inc.获得的系统,特别是
如以上专利中所述,可将声学喷射设备构造为从单个储藏器或多个储藏器中喷射流体液滴。为了提供组件的模块化和互换性,有时可优选将该设备与多个可移动储藏器(例如,架中的管等)结合使用。通常,将储藏器以图案或阵列布置以向每个储藏器提供单独的系统寻址能力(systematic addressability)。另外,尽管每个储藏器可作为离散的或独立的容器提供,但是在需要大量储藏器的情况下,优选的是,储藏器被容纳在集成的多个储藏器单元内。作为一个实例,多个储藏器单元可为固体表面,在其上通过表面润湿性质将离散的含流体的区域保持在适当位置,每个局部的含流体的区域构成储藏器。作为另一个实例,多个储藏器单元可为具有各个孔作为储藏器的孔板。许多适合于与该设备一起使用的孔板是可商购的,并且每个孔板可含有例如96、384、1536或3456个孔,并且具有全裙边(skirt)、半裙边或无裙边。孔板或微量滴定板已成为常用的实验室用品。实验室自动化与筛选协会(SLAS)与美国国家标准协会共同建立并维护了微量滴定板的标准。这样的孔板的孔通常成直线阵列的形式。
这样的可商购的孔板的可用性并不排除以含有至少约10,000个孔或多达100,000至500,000个孔或更多的其他几何构造定制的孔板的制造和使用。此外,用于建造储藏器的材料必须与容纳在其中的流体样品相容。因此,如果意图使储藏器或孔容纳有机溶剂例如乙腈,则在乙腈中溶解或溶胀的聚合物将不适合用于形成储藏器或孔板。类似地,意图容纳DMSO的储藏器或孔必须与DMSO相容。对于基于水的流体,许多材料适合用于构造储藏器,并且包括但不限于:陶瓷例如氧化硅和氧化铝,金属例如不锈钢和铂,以及聚合物例如聚酯、聚丙烯、环烯烃共聚物(例如,可以
另外,为了减少在运行期间使声辐射产生器与每个储藏器或储藏器孔对准所需的运动量和时间,优选的是每个储藏器的中心安置为距相邻储藏器中心不超过约1厘米,更优选不超过约1.5毫米,还更优选不超过约1毫米并且最佳地不超过约0.5毫米。这些尺寸倾向于将储藏器的尺寸限制至最大体积。将储藏器构造为容纳典型地不超过约1mL、优选不超过约100μL、更优选不超过约1μL并且最佳地不超过约1nL的流体。为了有利于处理多个储藏器,还优选的是,储藏器基本上在声学上不可区分。
与本系统和方法结合使用的声学喷射设备能够以至少约250Hz的速率声学喷射液滴,但是更高的喷射速率是可能的,包括500Hz、1kHz或更高,较小的液滴能够实现更高的重复(速)率。该设备还能够从多个储藏器中的每一个中快速喷射液滴,这些储藏器可以阵列布置,例如在孔板或单个管的架的情况下就是如此。即,基底安置装置或喷射器安置装置以快速相继的方式将喷射器以声学方式耦合至一系列的流体储藏器中的每一个,由此允许从不同的储藏器中快速且受控地喷射流体样品液滴。当前的市售技术以在每个储藏器处可重复且受控的声学耦合方式允许基底相对于喷射器移动,和/或允许喷射器从同一基底内的一个储藏器移动到另一个储藏器,对于高性能安置装置而言所述移动小于约0.1秒,并且对于普通安置装置而言所述移动小于约1秒。如授予Ellson等的美国专利No.6,666,541中所解释,定制设计的系统可将储藏器到储藏器的过渡时间(相当于声学喷射事件之间的时间)降低至小于0.001秒。为了提供定制设计的系统,重要的是要记住,有两种基本类型的运动:脉冲运动和连续运动。脉冲运动涉及以下离散的步骤:将基底或喷射器移动到适当位置使得喷射器以声学方式耦合至基底内的储藏器,从储藏器中的样品流体中以声学方式喷射液滴,和重新安置基底和/或喷射器使得喷射器以声学方式耦合至下一个储藏器。通过这种方法使用高性能安置装置,允许在小于0.1秒在每个储藏器处进行可重复且受控的声学耦合。另一方面,连续运动设计连续地移动基底和/或喷射器(虽然不以相同的速度),并且在移动期间提供喷射。由于脉冲宽度非常短,因此这种类型的方法能够实现超过10Hz的喷射器过渡,和甚至超过1000Hz的喷射器过渡。
因此,本发明的方法对于在高通量情况下实施所公开的提取方法是理想的。提取可如本文所述在一系列的流体储藏器(例如,微孔板中的孔)中的每一个中进行,其中储藏器到储藏器的过渡和声学液滴喷射到任何类型的液滴储藏器(例如,倒置的微孔中板或分析仪器)中是非常迅速的。
在授予Ellson等的美国专利No.6,666,541的图1中示出了可在本文中有利地使用的代表性聚焦声学喷射系统,该专利的公开内容通过引用的方式并入本文。如其中所解释的,声学液滴喷射设备包括声学喷射器,该声学喷射器包括声辐射产生器和用于在流体表面附近将产生的声辐射聚焦在流体样品内的焦点处的聚焦装置。因此,声学喷射器适于产生和聚焦声辐射,以从流体储藏器中的流体组合物中喷射流体的液滴。声辐射产生器和聚焦装置可作为由单个控制器控制的单个单元起作用,或者它们可被独立地控制。包括本领域已知的曲面或菲涅耳透镜的多种聚焦装置中的任何一种都可与本发明结合使用。这样的聚焦装置描述在授予Lovelady等的美国专利No.4,308,547和授予Quate等的美国专利No.5,041,849以及美国专利申请公开No.2002037579中。另外,有多种方式将喷射器以声学方式耦合至每个单独的储藏器,由此耦合至其中的流体。尽管可通过与储藏器中容纳的流体的直接接触来实现声学耦合,但是优选的方法是将喷射器与储藏器和储藏器流体以声学方式耦合,而不允许喷射器的任何部分(例如,聚焦装置)与任何待喷射的液体接触。
声学液滴喷射器可与每个储藏器的外部表面直接接触或间接接触。在直接接触的情况下,为了将喷射器以声学方式耦合至储藏器,优选的是直接接触是完全共形的,以确保有效的声能传递。即,喷射器和储藏器应具有适于配合接触的相应表面。因此,如果通过聚焦装置在喷射器和储藏器之间实现声学耦合,则期望储藏器具有对应于聚焦装置的表面轮廓的外部表面。在没有共形接触的情况下,声能传递的效率和准确性可受到损害。另外,由于许多聚焦装置具有弯曲的表面,因此直接接触方法可需要使用具有特别形成的反表面的储藏器。
最佳地,通过由放置在喷射器和流体储藏器的底部之间的声学耦合介质所提供的间接接触,在喷射器和每个储藏器之间实现声学耦合。声学耦合介质可为声学耦合流体,优选与声聚焦装置和储藏器的底侧两者都共形接触的在声学上为均质的材料。该系统可含有单个声学喷射器,或其可含有多个喷射器。相对于多个喷射器设计通常优选单个喷射器设计,因为使用单个喷射器更容易实现液滴放置的准确度和液滴尺寸和速率的一致性。但是,本发明不限于单个喷射器设计。
当在本方法中使用多于一个流体储藏器时,尽管不需要相同的构造,但是优选地这些储藏器是基本相同的并且在声学上基本不可区分。如本节前面所解释,储藏器可为托盘、架或其他此类结构中的单独的可移动组件,但是它们也可固定在板(例如微孔板)或其他基底内。如图所示,每个储藏器优选地是基本上轴向对称的,具有从圆形储藏器底部向上延伸的竖直壁,但是也可使用其他储藏器形状和储藏器底部形状。每个储藏器底部的材料和厚度应使得声辐射可通过其传播并且进入到容纳在每个储藏器内的流体样品中。
在运行中,流体储藏器用流体组合物填充,该流体组合物包括含有目标分析物的样品,如前所解释。目标分析物通常呈提取形式,在溶剂或溶剂混合物中,或者其可在下部流体层中,如本文前面所解释。声学喷射器安置于流体储藏器的正下方,在喷射器和储藏器之间提供声学耦合。一旦喷射器和储藏器相对于彼此正确地安置,则声辐射发生器就被激活以产生声辐射,该声辐射被聚焦装置引导至储藏器内的流体表面附近的焦点(其中流体表面可代表液-气界面或液-液界面。结果,流体液滴从流体表面朝向液滴接收器(例如基底、倒置的储藏器、倒置的微孔板中的孔、液滴输送设备或分析仪器)喷射。然后,在具有多个储藏器的系统中,例如将多孔板或管架,可相对于声学喷射器重新安置,使得另一个储藏器与喷射器对准并且可喷射下一流体组合物的液滴。
可将喷射的液滴引导到其中的分析仪器可为用于检测目标分析物、确定样品中的目标分析物的量或浓度或确定目标分析物的化学组成的任何仪器。当分析仪器是质谱仪或要求分析物为离子化形式的其他类型的设备时,离开的液滴在进入质谱仪或要求分析物为离子化形式的其他分析仪器之前通过离子化区域。在离子化区域中,所选择的离子化源(例如电喷雾离子源)将分析物转换成离子化形式。对于含有离子化形式的目标分析物的喷射的流体液滴,不需要暴露于离子化源;参见,例如,Datwani等于2017年11月22日提交的临时美国专利申请序列No.62/590,079"System and Method for the Acoustic Loading ofan Analytical Instrument Using a Continuous Flow Sampling Probe",其公开内容通过引用的方式并入本文。示例性的分析仪器包括但不限于质谱仪、光谱设备、分离系统及其组合。示例性的离子化技术包括但不限于:化学离子化,电子碰撞离子化,解吸化学离子化,电感耦合等离子体离子化,和大气压离子化,包括电喷雾离子化和大气压化学离子化以及大气压光离子化。示例性的分离方法包括但不限于液相色谱、固相提取、HPLC、毛细管电泳或任何其他液相样品净化或分离方法。示例性的质谱仪包括但不限于扇区质谱仪、飞行时间质谱仪、四极质谱过滤器质谱仪、三维四极离子阱质谱仪、线性四极离子阱质谱仪、环形离子阱质谱仪以及傅立叶变换离子回旋共振质谱仪。
另外,如前所述,本发明在此涵盖声学喷射过程的修改以优化结果。例如,如在以下专利中所解释:授予Ellson等的美国专利No.6,932,097,授予Ellson等的6,938,995,授予Ellson等的7,354,141,授予Qureshi等的7,899,645,授予Ellson等的7,900,505,授予Stearns等的8,107,319,授予Ellson等的8,453,507,和授予Steams等8,503,266,以上的声学液滴喷射器可用于表征储藏器中的流体组合物,例如,以测量流体弯液面的高度以及其他性质,例如流体的体积、粘度、密度、表面张力、组成、声阻抗、声衰减、流体中的声速等,然后可使用其中的任何一个或全部来确定用于液滴喷射的最佳参数,包括声功率、声频率、猝发音持续时间和/或聚焦透镜的F数。作为另一个实例,如授予Ellson等的美国专利No.8,544,976和8,882,226中所述,可使用声学询问方法(interrogation processes)来优化在聚焦激活的声学喷射系统中的声学喷射器和含(容纳)流体的储藏器的相对位置。另一个实例是通过分析在喷射之前从储藏器内的表面反射的声辐射的波形来优化用于喷射流体液滴的声辐射的振幅的方法;参见授予Stearns等的美国专利No.7,717,544和8,770,691。使用授予Hadimioglu等的美国专利No.6,383,115的方法可确保液滴的尺寸和一致性,并且可使用授予Mutz等的美国专利No.7,481,511和授予Ellson等的7,784,331的方法来控制储藏器性质的变化。
7.液-液体边界的动态跟踪:
在一个优选的实施方案中,在本上下文中可有利地使用优化声学喷射过程的前述方法和系统的组合。更具体地,可在每次声学喷射事件之前跟踪流体储藏器中的两个流体层之间的边界的垂直位置,以及可跟踪在储藏器中的整个流体组合物的高度。这可使用前述专利中描述的声学询问技术来完成。然后,在本发明的提取方法期间,可由流体组合物的总(中心)高度和液体边界的(中心)垂直位置的组合来计算上部流体的高度(即,在中心点处从液-液边界到弯液面的距离);即,上部流体的高度等于总流体高度减去所识别的边界的高度。进而,这有利于这样的过程:其中在完全喷射上层之后可停止声学喷射而不喷射下层。
应当理解,虽然已经结合许多具体实施方案描述了本发明,但是前述描述以及随后的实施例旨在说明而非限制本发明的范围。在这方面,没有试图比对本发明的基本理解所必须的还更详细地示出本发明的结构细节,结合附图和/或实施例进行的描述使得如何可在实践中实现本发明对于本领域技术人员而言是显而易见的。如适用法律所允许,本公开内容包括所附权利要求书中叙述的主题的所有修改和等同。而且,除非本文另外指出或与上下文明显矛盾,否则本文所描述的本发明的要素的任何组合均被本公开内容所涵盖。
本文引用的所有专利、专利出版物、文献参考和其他材料都通过引用的方式以其全文并入本文。
实验:
流体储藏器是384-孔微孔板中的孔。向流体储藏器添加,即向微孔板的加载样品的孔添加合适的生物相容性缓冲液,例如20μL Tris/EDTA缓冲液和20μL BMIM PF
- 使用声学液滴喷射从样品中提取目标部分的系统和方法
- 用于处理液滴中样品的仪器及其使用方法
