核酸二级结构非特异荧光吸附用于微流控芯片检测的方法
文献发布时间:2023-06-19 09:52:39
技术领域
本发明属于分子诊断及微流控芯片检测技术领域,尤其涉及使用微流控芯片进行分子诊断的生产制造、操作使用的过程控制,具体为一种核酸二级结构非特异荧光吸附用于微流控芯片检测的方法。
背景技术
基因芯片是基于生物分子间特异相互作用的原理,将生化分析过程集成于芯片表面,从而实现对DNA、RNA的高通量快速检测。而微流控芯片属于基因芯片的一种,是以芯片为操作平台,同时以分析化学为基础,以微机电加工技术为依托,以微管道网络为结构特征,多种功能集成的一种技术,把整个化验室的功能,包括采样、稀释、加试剂、反应、分离、检测等集成在芯片上。
目前主流的微流控芯片主要是用于对用户提取好的核酸进行检测。由于微流控芯片集成了流路自动分配、扩增等多种功能,对于用户来说,操作简便,实现“样本进,结果出”,但对于检测结果的质量控制就需要有更为严格的把控或监控手段。
现有微流控芯片检测过程中可能存在的不足有:(1)对于对称型芯片,可能出现用户放反芯片,导致结果完全混乱的情况,而用户在不知情的情况下,得到了完全错误的结果;(2)微流控芯片存在比较多的预加样孔,需要提前加入核酸等反应物质,而可能存在部分预加样孔在生产过程中因为微量喷头控制失误等原因而导致漏样的情况,而在这种情况下,用户并不能发现预加样孔少加了核酸反应物质,造成出现结果的假阴性;(3)对于待检样品,用户预先的核酸浓度过高或过低均会导致结果异常,这就需要检测前预先测定核酸浓度,这让检测更加繁琐耗时,即使这样病毒细菌等超低浓度微量样品测定难度依然是大的挑战,将核酸定量与检测整合可能是一个很好的解决方案。
发明内容
本发明的目的在于提供一种核酸二级结构非特异荧光吸附用于微流控芯片检测的方法,以把控微流控芯片在使用过程中,对可能出现的芯片正反放置错误,预加样缺失,以及核酸模板浓度过高或过低导致的检验过程失控进行判断和提示。
本发明目的通过以下技术方案来实现:
一种核酸二级结构非特异荧光吸附用于微流控芯片检测的方法,所述方法为在以核酸检测的微流控芯片的反应体系中加入荧光显色剂,通过不同反应孔产生的荧光信号值差异,对微流控芯片的检测状态进行判断,包括以下三种中的一种或多种:(1)微流控芯片的正反放置位置;(2)微流控芯片的预加样孔是否加样;(3)核酸模板浓度进行半定量。
本申请将荧光显色剂加入到微流控芯片配套的反应体系中,荧光显色剂为可以与微流控芯片上的核酸二级结构结合产生荧光信号的非特异性荧光染料,单链核酸在较低温度(10~50℃)下具有非特异二聚体的特性,与荧光显色剂结合后会产生荧光,同时微流控芯片的模板浓度的高低也会产生不同信号强度的荧光,以此原理基础上进行微流控芯片检测状态的判断,最终通过荧光信号值数据的采集和分析,可实现以下效果:(1)通过预加样反应孔的非对称性,可判断微流控芯片的正反;(2)可通过荧光信号的有无,判断预加样孔是否已加入核酸等反应物质;(3)加入模板后,可通过荧光信号的强弱,对模板浓度实现半定量。
进一步,所述荧光显色剂为可以与微流控芯片上的核酸二级结构结合产生荧光信号的非特异性荧光染料。
进一步,所述荧光显色剂为SYBR Green、EvaGreen、Peko Green、pico Green中的一种或多种。
进一步,所述微流控芯片在加入反应体系和荧光显色剂后,需要进行在20~50℃温度下进行预反应。
进一步,判断微流控芯片正反放置位置的公式为:R=理论需加样孔荧光信号值/理论未加样孔荧光信号值;当R>阈值1,则微流控芯片放置正确,为正放,当R<阈值1,则微流控芯片放置有误,为倒置;阈值1优选为0.2~5。
进一步,判断微流控芯片的预加样孔是否加样的公式为:T=未知孔的荧光信号值/理论已加样孔的荧光信号值;当T>阈值2,则未知孔可判断为已加样,当T≤阈值2,则未知孔判断为未加样;阈值2优选为0.1~0.5。
进一步,核酸模板浓度进行半定量的方式为:依据不同的微流控芯片所采用荧光显示剂先进行预实验,实验选取已知模板浓度梯度分别进行扩增,导出测试的荧光信号值,对荧光信号值与模板浓度值进行线性拟合,得到拟合公式及曲线后,再用未知模板测试的荧光信号值带入拟合公式,得到近似的模板的浓度值。
使用微流控芯片进行检测时,加入模板的量的差异会影响每个孔位的初始信号值,特别是空白孔位的荧光信号值影响比较明显,可依据空白孔位的强弱近似地判断模板加入量的多少。采用不同的微流控芯片的荧光显色剂,其模板浓度和荧光信号值的拟合曲线不相同,可能为线性拟合、指数拟合、对数拟合或多项式拟合,可依据不同的微流控芯片所采用荧光显色剂,先进行预实验,得到拟合曲线后,再用每次测试的荧光信号值带入拟合公式,得到近似的模板的浓度值。
与现有技术相比,本发明具有以下有益效果:
本发明核酸二级结构非特异荧光吸附用于微流控芯片检测的方法,在微流控芯片的反应体系中添加可以与微流控芯片上的核酸二级结构结合产生荧光信号的荧光显色剂,通过不同反应孔荧光信号值的差异,可以有效识别微流控芯片的正反,防止用户在放置芯片是放置错误;提示微流控芯片预加样孔是否加样,防止出现假阴性;同时实现核酸模板浓度的半定量。
附图说明
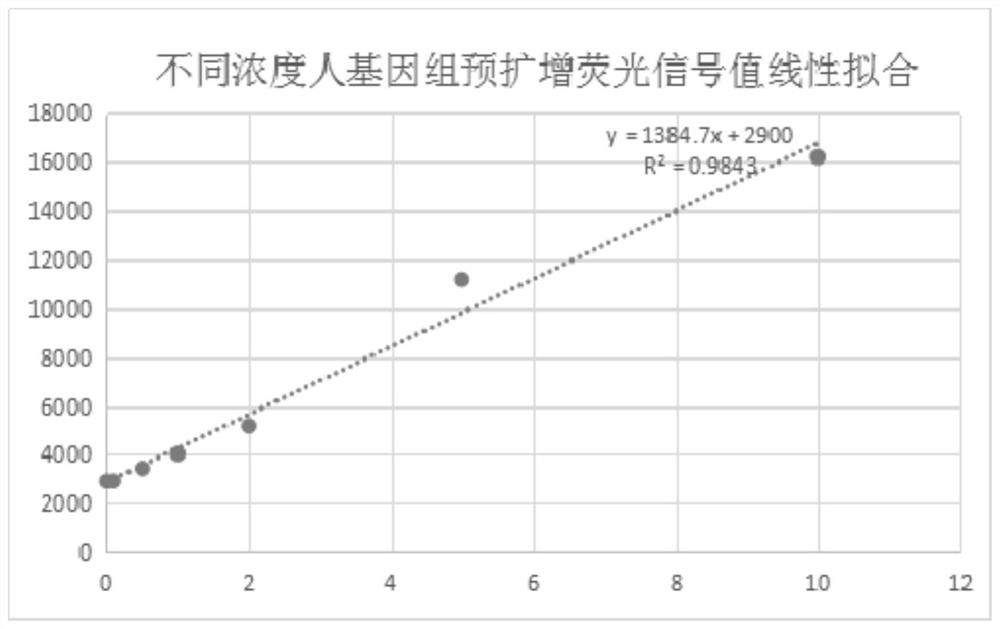
图1为不同浓度人基因组预扩增荧光信号值线性拟合结果。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例以核酸检测的恒温扩增微流控芯片为例进行核酸二级结构非特异荧光吸附微流控芯片检测状态判断方法的验证:
实施例基于呼吸道病原菌核酸检测试剂盒(恒温扩增芯片法)检测方法,流程如下:
体系分装→加核酸模板→芯片加样及离心→芯片上机仪器分析→判定结果
微流控芯片共24个孔位,其中1、4、7、10、13、16、19、22、24号孔为空,其余孔位已预加扩增引物,进行样本检测时,将一定量扩增体系(已经预加了荧光显示剂EvaGreen)与模板混合后加入到芯片通道里,经过离心将混合反应体系离心到反应孔中,再放入仪器中进行预反应(37℃反应3min)和恒温扩增反应,在扩增过程中对荧光信号值进行实时采集,扩增完成后导出荧光信号值数据进行分析。
实施例1判断微流控芯片的正反
按照呼吸道病原菌核酸检测试剂盒(恒温扩增芯片法)检测方法进行2份样本的检测,每份样本重复4次,其中2次按照正确方法放入仪器,2次倒置放入仪器。同时进行恒温扩增,扩增完成后导出荧光信号值数据,分析预扩增阶段的荧光信号值数据如下表1:
表1判断微流控芯片的正反数据
按照公式R=理论需加样孔荧光值信号/理论未加样孔荧光值信号,进行芯片正反的判断。本实施例选用2#孔位为理论需加样孔,24#孔位为理论未加样孔信号,阈值1的值设定为1,如果R>1,则微流控芯片放置正确,为正放,如R<1,则微流控芯片放置有误,为倒置。计算结果如下表2:
表2微流控芯片的正反判断结论
按照以上表2结果,判断结论与实际放置方式均相符。
实施例2判断微流控芯片是否已加入核酸等物质
按照呼吸道病原菌核酸检测试剂盒(恒温扩增芯片法)检测方法进行2份样本的检测,每份样本重复检测2次,恒温扩增完成后导出荧光信号值数据,分析预扩增阶段采集的荧光信号值数据如表3;
表3判断微流控芯片是否已加入核酸数据荧光信号值统计
按照公式T=未知孔荧光信号值/理论已加样孔荧光信号值,进行是否预加入核酸的判断。本实施例选用2#孔位为理论需加样孔,其他所有的孔均为未知孔,阈值2的值设定为0.3,如T>0.3,则未知孔可判断为已加样,如T≤0.3,则未知孔判断为未加样。计算及判定结果如表4:
表4微流控芯片是否已加入核酸T值及判定结果
根据以上案例实验结果可得,孔位1、4、7、10、13、16、19、22、24为未加样孔,其余孔位为已加样孔,符合实际理论结果。
实施例3对模板浓度的半定量
按照呼吸道病原菌核酸检测试剂盒(恒温扩增芯片法)检测方法进行不同浓度正常人基因组的检测,其浓度分别为0.1ng/μL、0.5ng/μL、1ng/μL、2ng/μL、5ng/μL、10ng/μL,以TE作为空白对照进行实验;扩增完成后,导出荧光信号值数据,对每个浓度的检测结果的预扩增阶段的荧光信号值进行统计,如下表5:
表5每个浓度的检测结果的预扩增阶段的荧光信号值
对荧光信号值和模板浓度进行线性曲线拟合,结果如图1,相关性为R
根据实验结果可得,正常人基因组的浓度分别为0.1ng/μL、0.5ng/μL、1ng/μL、2ng/μL、5ng/μL、10ng/μL,其采集的荧光信号值随着人基因组浓度的增加而增大,符合线性拟合曲线。
因此,对于未知样本,可以通过预扩增阶段的荧光信号值,带入该拟合曲线公式:y=1384.7x+2900,近似地计算出模板的浓度,实现了对模板浓度的半定量。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 核酸二级结构非特异荧光吸附用于微流控芯片检测的方法
- 一种用于实时荧光核酸扩增检测的微流控芯片及检测方法
