一种甲氨蝶呤-吲哚菁绿复合物和制备方法及其应用
文献发布时间:2023-06-19 10:03:37
技术领域
本发明涉及生物医药领域,具体涉及一种甲氨蝶呤-吲哚菁绿复合物和制备方法及其应用。
背景技术
甲氨蝶呤(MTX)是由Seeger等人在20世纪50年代首次合成且应用于临床治疗恶性病的有效药物。MTX最初被用于类风湿性关节炎和银屑病等疾病的治疗,70年代后被用于癌症化疗,尤其是白血病的化疗,另外MTX也是临床上骨肿瘤包括骨肉瘤和骨巨细胞瘤化疗的常用药物。由于甲氨蝶呤的分子结构和叶酸高度类似,其可亲和叶酸受体,对某些叶酸受体过度表达的肿瘤细胞表现出良好靶向性;目前已有研究证明,MTX对宫颈癌、乳腺癌等肿瘤具备优异的靶向和治疗效果。MTX用于癌症治疗的作用机理为MTX是叶酸代谢中一种极强竞争性拮抗剂,与二氢叶酸相比,MTX和二叶氢酸还原酶的亲和力要强一千倍,可以说几乎是不可逆结合二叶氢酸还原酶;但这种现象导致二氢叶酸无法转化为四氢叶酸(叶酸),从而使脱氧尿苷酸不能转换为脱嘧啶核苷酸,阻止DNA合成,亦干扰RNA和蛋白质的合成,属细胞周期特异性药。
吲哚菁绿(ICG)俗称靛氰绿、诊断用绿针、吲哚花青绿,具备良好的生物安全性,是目前我国心血管系统疾病以及各种肝脏疾病临床诊断中常用的一种造影剂。吲哚菁绿也可广泛应用于近红外一区(NIR-I)荧光/光声成像以及光热治疗。最新研究表明,ICG分子的荧光发射峰在近红外二区(NIR-II)有拖尾,因而具备NIR-II荧光成像功能,在生物组织成像中具有更高的时空分辨率和更深的成像深度。但目前尚无对肝癌、宫颈癌、乳腺癌和卵巢癌等叶酸受体过表达的肿瘤组织具备肿瘤靶向、近红外二区荧光成像以及化疗和光热联合治疗的多重功能的有效制剂,另外现有医药纳米制剂普遍存在化学和物理稳定性的问题,货架期交底,成本高。
发明内容
鉴于现有技术中存在的技术缺陷和技术弊端,本发明实施例提供克服上述问题或者至少部分地解决上述问题的一种甲氨蝶呤-吲哚菁绿复合物和制备方法及其应用。
作为本发明实施例的一个方面,提供了一种甲氨蝶呤-吲哚菁绿复合物,所述甲氨蝶呤-吲哚菁绿复合物包括甲氨蝶呤或甲氨蝶呤钠盐和吲哚菁绿,所述甲氨蝶呤或甲氨蝶呤钠盐与所述吲哚菁绿的质量比为10:1-1:1。
进一步地,所述甲氨蝶呤或甲氨蝶呤钠盐和吲哚菁绿的质量比为2:1。
作为本发明实施例的又一方面,提供了一种上述实施例中甲氨蝶呤-吲哚菁绿复合物的制备方法,所述制备方法包括如下步骤:
将甲氨蝶呤或甲氨蝶呤钠盐和吲哚菁绿溶解于有机溶剂A中,于20-40℃下进行搅拌混合反应12-24h,获得所述甲氨蝶呤-吲哚菁绿复合物有机溶液;
去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物;
所述有机溶剂A包括二甲基亚砜、二甲基甲酰胺、二甲基乙酰胺、甲醇、乙醇、四氢呋喃、乙腈和丙酮中的至少一种。
进一步地,所述去除有机溶液的方法包括透析法、旋蒸法、离心法中的至少一种。
作为本发明实施例的又一方面,提供了一种上述实施例所述的甲氨蝶呤-吲哚菁绿复合物的纳米粒子,所述甲氨蝶呤或甲氨蝶呤钠盐与所述吲哚菁绿的质量比为10:1-1:1,所述纳米粒子为球形,粒径为100-1000nm。
作为本发明实施例的又一方面,提供了上述实施例中甲氨蝶呤-吲哚菁绿复合物纳米粒子的制备方法,所述制备方法包括如下步骤:
(1)将甲氨蝶呤或甲氨蝶呤钠盐和吲哚菁绿溶解于有机溶剂A中,于20-40℃下进行搅拌混合反应12-24h,获得所述甲氨蝶呤-吲哚菁绿复合物有机溶液;
(2)用去离子水透析8-24h,获得所述甲氨蝶呤-吲哚菁绿复合物纳米粒子;
其中,所述有机溶剂A包括二甲基亚砜、二甲基甲酰胺、二甲基乙酰胺、甲醇、乙醇、四氢呋喃、乙腈和丙酮中的至少一种。
进一步地,所述步骤(2)中用去离子水透析采用的透析袋的截留分子量为1000~10000。
作为本发明实施例的再一方面,提供了一种甲氨蝶呤-吲哚菁绿复合物缓释制剂,包括如上述实施例所述的一种甲氨蝶呤-吲哚菁绿复合物纳米粒子,还包括表面活性剂、防冻剂;所述表面活性剂包括泊洛沙姆、DSPE-PEG、聚乙烯吡咯烷酮中的任意一种或两种;所述防冻剂包括氯化钠、右旋糖酐、葡萄糖、蔗糖中的至少一种。
作为本发明实施例的再一方面,提供了上述实施例中甲氨蝶呤-吲哚菁绿复合物缓释制剂的制备方法,所述制备方法包括如下步骤:
向甲氨蝶呤-吲哚菁绿复合物纳米粒子中加入表面活性剂、防冻剂,经真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂;
所述表面活性剂包括泊洛沙姆、DSPE-PEG、聚乙烯吡咯烷酮中的任意一种;所述防冻剂包括氯化钠、右旋糖酐、葡萄糖、蔗糖中的至少一种。
本发明实施例至少实现了如下技术效果:
本发明实施例提供的甲氨蝶呤-吲哚菁绿复合物解决了肿瘤靶向、肿瘤成像和多模态治疗的问题,对肝癌、宫颈癌、乳腺癌和卵巢癌等叶酸受体过表达的肿瘤组织具备肿瘤靶向、近红外二区荧光成像以及化疗和光热联合治疗的多重功能;其中,复合物中的甲氨蝶呤不仅保留具备抗癌活性,同时可高度亲和叶酸受体具备肿瘤靶向功能,吲哚菁绿不仅可作为一种诊断试剂具备近红外一区(NIR-I)和近红外二区(NIR-II)荧光成像功能,同时还能够作为一种光热试剂具备光热转化的功能。本发明实施例中的复合物纳米粒子可通过共组装和纳米沉淀的方法制备得到,具有缓释药物的特性,可高效靶向叶酸受体过表达的肿瘤细胞,在肿瘤诊疗领域有较广泛的应用前景。而且,该复合物中的甲氨蝶呤能够发挥化疗功能,吲哚菁绿能够发挥光热治疗功能,复合物能够在两种治疗模式发挥协同作用,增强肿瘤治疗效果。
另外,本发明的实施例提供的甲氨蝶呤-吲哚菁绿复合物及其缓释制剂,能够同时以冷冻储存的方法解决其纳米制剂的化学和物理稳定性问题,提高了制剂的货架期。
本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。本发明的目的和其他优点可通过在所写的说明书以及附图等中所记载的结构来实现和获得。
下面通过附图和实施例,对本发明的技术方案做进一步的详细描述。
附图说明
附图用来提供对本发明的进一步理解,并且构成说明书的一部分,与本发明的实施例一起用于解释本发明,并不构成对本发明的限制。在附图中:
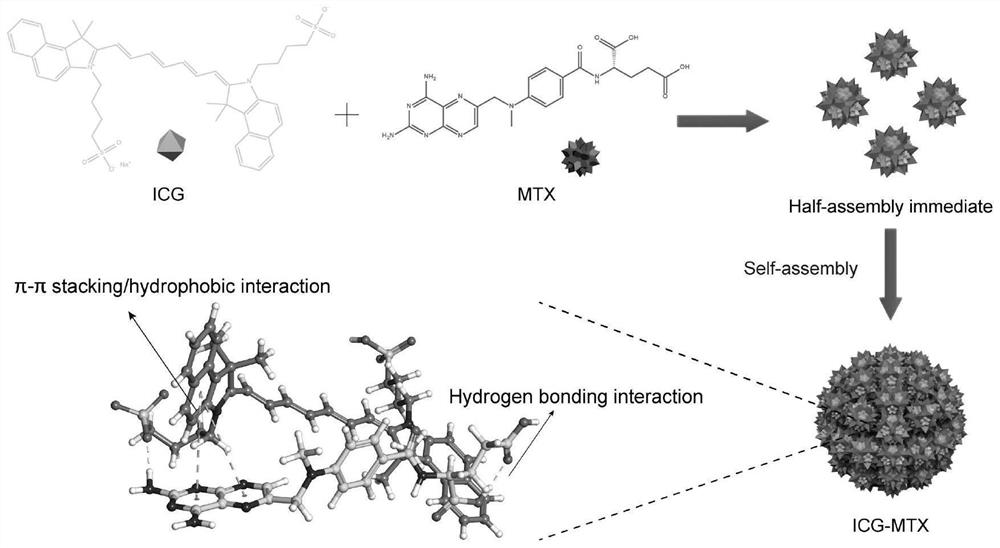
图1为本发明一实施例中甲氨蝶呤-吲哚菁绿复合物及复合物纳米粒子形成原理图。
图2为本发明一实施例中吲哚菁绿、甲氨蝶呤、甲氨蝶呤/吲哚菁绿物理混合物、甲氨蝶呤-吲哚菁绿复合物核磁氢谱图。
图3为本发明一实施例中甲氨蝶呤、吲哚菁绿、甲氨蝶呤/吲哚菁绿物理混合物、甲氨蝶呤-吲哚菁绿的差热分析图谱、紫外-可见光吸收图谱、透射红外谱图及X射线衍射图谱。
图4为本发明一实施例中不同比例甲氨蝶呤、吲哚菁绿所得甲氨蝶呤-吲哚菁绿复合物纳米粒子的(A)透射电镜图、(B)粒径分布、(C)Zeta电位、(D)分散度、(E)组装率。
图5为本发明一实施例中甲氨蝶呤、吲哚菁绿比例为2:1时所得甲氨蝶呤-吲哚菁绿复合物纳米粒子的(A)粒径分布图、(B)透射电镜图、(C)粒径稳定性、(D)冻干前后以及复分散的粒径分布图和光学图。
图6为本发明一实施例中甲氨蝶呤-吲哚菁绿复合物纳米粒子体外甲氨蝶呤累积释放图。
图7为本发明一实施例中甲氨蝶呤-吲哚菁绿复合物的细胞摄取图。
图8为本发明一实施例中甲氨蝶呤、吲哚菁绿、甲氨蝶呤-吲哚菁绿复合物纳米粒子的(A)细胞暗毒性和(B)细胞光毒性分析图。
具体实施方式
为详细说明本发明的技术内容、所实现目的及效果,以下结合实施方式并配合附图予以说明。
附图和以下说明描述了本发明的可选实施方式以教导本领域技术人员如何实施和再现本发明。为了教导本发明技术方案,已简化或省略了一些常规方面。本领域技术人员应该理解源自这些实施方式的变型或替换将落在本发明的保护范围内。本领域技术人员应该理解下述特征能够以各种方式组合以形成本发明的多个变型。由此,本发明并不局限于下述可选实施方式,而仅由权利要求和它们的等同物限定。
实施例1
本实施例提供一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法为:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL二甲基亚砜中,于20℃下进行搅拌混合反应12h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液;去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物;
本实施例甲氨蝶呤-吲哚菁绿复合物纳米粒子的制备方法为:将上述复合物有机溶剂(或复合物)用去离子水透析8h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。其中,纳米粒子中甲氨蝶呤-吲哚菁绿复合物的质量比为2:1。
本实施例甲氨蝶呤-吲哚菁绿复合物缓释制剂的制备方法为:向上述甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得所述甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例2
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为1:1。
本实施例复合物的制备方法为:将3mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL二甲基亚砜中,于20℃下进行搅拌混合反应12h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析8h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:将甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例3
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为4:1。
本实施例复合物的制备方法包括:将12mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于10mL二甲基亚砜中,于20℃下进行搅拌混合反应12h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析8h,透析采用的透析袋的截留分子量为5000,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:将甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例4
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法包括:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL二甲基亚砜中,于20℃下进行搅拌混合反应18h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析8h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例5
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法包括:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL二甲基亚砜中,于20℃下进行搅拌混合反应18h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例6
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法包括:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL二甲基亚砜中,于30℃下进行搅拌混合反应18h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例7
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法包括:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL乙醇中,于20℃下进行搅拌混合反应18h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例8
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为2:1。
本实施例复合物的制备方法包括:将6mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于1mL乙醇中,于30℃下进行搅拌混合反应18h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为3500,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和氯化钠,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例9
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为10:1。
本实施例复合物的制备方法包括:将30mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于10mL二甲基亚砜中,于40℃下进行搅拌混合反应24h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为10000,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入泊洛沙姆和蔗糖,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例10
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为8:1。
本实施例复合物的制备方法包括:将24mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于8mL二甲基亚砜中,于20℃下进行搅拌混合反应12h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为1000,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入聚乙烯吡咯烷酮和葡萄糖,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
实施例11
本实施例的一种甲氨蝶呤-吲哚菁绿复合物,甲氨蝶呤(或甲氨蝶呤钠盐)和吲哚菁绿的质量比为6:1。
本实施例复合物的制备方法包括:将18mg甲氨蝶呤(或甲氨蝶呤钠盐)和3mg吲哚菁绿溶解于8mL二甲基乙酰胺中,于20℃下进行搅拌混合反应12h,获得甲氨蝶呤-吲哚菁绿复合物有机溶液,然后用去离子水透析16h,透析采用的透析袋的截留分子量为5000,去除有机溶液得到甲氨蝶呤-吲哚菁绿复合物纳米粒子。
本实施例复合物缓释制剂的制备方法包括:向甲氨蝶呤-吲哚菁绿复合物纳米粒子溶液中加入DSPE-PEG(二硬脂酰磷脂酰乙醇胺-聚乙二醇)和右旋糖酐,真空冷冻干燥后获得甲氨蝶呤-吲哚菁绿复合物缓释制剂。
如图1、图2、图3所示,图1为甲氨蝶呤-吲哚菁绿复合物纳米粒子形成原理图,本实施例方法为通过图1所示原理反应,图2所示为吲哚菁绿、甲氨蝶呤、甲氨蝶呤-吲哚菁绿复合物的结构示意图及为吲哚菁绿、甲氨蝶呤、甲氨蝶呤/吲哚菁绿物理混合物、甲氨蝶呤-吲哚菁绿复合物核磁氢谱图。图3为分别为甲氨蝶呤、吲哚菁绿、甲氨蝶呤/吲哚菁绿物理混合物、甲氨蝶呤-吲哚菁绿复合物的(A)差热分析图谱,(B)紫外-可见光吸收图谱,(C)透射红外谱图,(D)X射线衍射图谱。由此可以确定本实施例方法得到的甲氨蝶呤-吲哚菁绿复合物并非甲氨蝶呤和吲哚菁绿简单的物理混合。
如图4所示,图4为甲氨蝶呤、吲哚菁绿比例为10:1,8:1,6:1,4:1,3:1,2:1,1:1时所得甲氨蝶呤-吲哚菁绿复合物纳米粒子的透射电镜图、粒径分布、Zeta电位、分散度、组装率。其中不同比例的甲氨蝶呤、吲哚菁绿的制备方法并不局限于上述记载的具体实施例的制备方法;图5为甲氨蝶呤、吲哚菁绿比例分别为2:1时所得甲氨蝶呤-吲哚菁绿复合物纳米粒子的粒径分布图、透射电镜图、粒径稳定性、冻干前后以及复分散的粒径分布图和光学图。可以看出表甲氨蝶呤-吲哚菁绿复合物纳米粒子为球形,粒径分布范围为100-300nm,甲氨蝶呤、吲哚菁绿比例为2:1时所得甲氨蝶呤-吲哚菁绿复合物纳米粒子的平均粒径为183.7nm,Zeta电位为-20mV。
如图6所示,图6为甲氨蝶呤-吲哚菁绿复合物纳米粒子体外甲氨蝶呤累积释放图。可以看出在pH为5.0时,甲氨蝶呤的释放都更快,起到了在肿瘤环境中快速释放药物的作用。
如图7所示,图7为甲氨蝶呤-吲哚菁绿复合物纳米粒子关于细胞摄取的激光共聚焦图和流式曲线分析。可以看出叶酸受体高表达的HeLa细胞相较于叶酸受体低表达的A549细胞而言,对甲氨蝶呤-吲哚菁绿复合物纳米粒子的摄取显著更强,并且过量叶酸与HeLa细胞的预先孵育显著降低对甲氨蝶呤-吲哚菁绿复合物纳米粒子的摄取,说明甲氨蝶呤-吲哚菁绿复合物纳米粒子可发挥自靶向作用。
如图8所示,图8为甲氨蝶呤、吲哚菁绿、甲氨蝶呤-吲哚菁绿复合物纳米粒子的细胞毒性评价图。可以看出甲氨蝶呤-吲哚菁绿复合物纳米粒子相较于甲氨蝶呤和吲哚菁绿对肿瘤细胞毒性更大,并且激光照射下,对肿瘤细胞的毒性显著增强。说明甲氨蝶呤-吲哚菁绿复合物纳米粒子提高了药效。
本领域技术人员可知,当本发明的技术参数在如下范围内变化时,可以预期得到与上述实施例相同或相近的技术效果。
上面结合附图对本发明的实施例进行了描述,但是本发明并不局限于上述的具体实施方式,上述的具体实施方式仅仅是示意性的,而不是限制性的,本领域的普通技术人员在本发明的启示下,在不脱离本发明宗旨和权利要求所保护的范围情况下,还可做出很多形式,这些均属于本发明的保护之内。
- 一种甲氨蝶呤-吲哚菁绿复合物和制备方法及其应用
- 一种吲哚菁绿-磷脂复合物及其制备方法和应用
