一种抑菌液的质量检验方法
文献发布时间:2023-06-19 10:05:17
技术领域
本发明涉及卫生消毒用品检测技术领域,具体为一种抑菌液的质量检验方法。
背景技术
消毒产品包括消毒剂、消毒器械、卫生用品和一次性使用医疗用品,消毒是指用化学、物理、生物的方法杀灭或者消除环境中的病原微生物,因此,它是一种防病的产品,用化学、物理、生物的方法消除病原微生物,卫生消毒用品应具有相应的标志标识及贮存方法,具有一定的使用时效期限以及灭杀抑制细菌生长的效果,传统的卫生用品检验一直缺少一种统一的质量检验方法,检测制度过于严苛则会造成大量的经济损失,检验制度过于简单又容易造成劣质产品扰乱市场,严重的可能会造成聚集性病毒性感染,所以如何有效地提高卫生消毒用品的监测质量,又能够避免劣质产品流向市场成为了当前急需解决的问题。
以下为文中提及的监测标准及规范性引用文件:
GB/T 191 包装储运图示标志
GB 15979 一次性使用卫生用品卫生标准
YBB 0012 固体药用高密度聚乙烯瓶
JJF 1070 定量包装商品净含量计量检验规则
《中华人民共和国药典》 2015年版
《消毒技术规范》 卫生部2002年版
《化妆品安全技术规范》 2015年版
《消毒产品生产企业卫生规范》 2009年版
《消毒产品标签说明管理规范》 卫生部卫监督发【2005】426号
《定量包装商品计量监督管理办法》 国家质量监督检疫总局(2005年)第75号令。
发明内容
本发明的目的在于提供一种能够有效地提高卫生消毒用品的监测质量,避免劣质产品流向市场的检验方法。
为实现上述目的,本发明提供如下技术方案:一种抑菌液的质量检验方法其具体操作包含以下步骤:
A、产品技术性指标检验规格;
B、产品需实施检验方法具体种类;
C、产品具体检验规则;
D、产品标志、包装;
E、运输及贮存规则。
作为优选,根据步骤A产品技术性指标检验规格包括:
a、原料要求:苦参、铁线藤、紫霄花、蛇床子、菟丝子、柴胡、蜂房、地龙、车前子、艾叶、醋酸氯己定应符合《中华人民共和国药典》(2015年版)各品名项下有关规定;
b、辅料要求:尼泊金乙酯、纯化水均应符合《中华人民共和国药典》(2015年版)各品名项下有关规定;
c、感官要求:感官要求应符合表1的规定;
d、净含量允差:应符合《定量包装商品计量监督管理办法》;
e、理化标准:理化指标应符合表2的规定;
f、微生物指标:微生物指标应符合表3的规定;
g、抑菌试验及抑菌稳定实验:抑菌试验应符合表4的规定;
h、急性眼刺激实验:应无刺激性。
作为优选,根据步骤B产品需实施检验方法具体种类包括:a、感官检验:将样品挤入透明的烧杯中,在自然光线下观察其色泽,组织形态及杂质、鼻嗅样品的气味;
b、净含量监测:按JJF 1070的规定测定;
c、PH测定方法:按《消毒技术规范》中pH值测定方法进行检验;
d、铅、砷、汞的监测:按《化妆品安全技术规范》中的方法检测;
e、醋、酸、氯已定:按《消毒技术规范》2002年版规定的方法测定;
f、微生物指标:按《一次性使用卫生用品卫生标准》4.2要求,用GB 15979附录B的方法检验;
g、抑菌试验及抑菌稳定实验:按照GB 15979-2002《一次性使用卫生用品卫生标准》规定方法(附录C4试验方法及附录C6试验方法)进行测定;
h、急性眼刺激实验:按《消毒技术规范》中的方法进行试验。
作为优选,根据步骤C产品具体检验规则包括:
a、组批:同一批投料、同一工艺、同一班次生产的同一品种的产品为一批;
b、抽样:每批产品检验用量的3倍量随机抽样;
c、出厂检验:产品出厂前,应由生产单位检验部门出厂检验,合格并签发产品质量合格证后方可出厂,出厂检验内容包括标签、感官指标、净含量允差、有效成分含量及微生物指标;
d、型式检验:型式检验包括本标准技术要求除5.7条款急性眼刺激试验外的全部项目进行检验,急性眼刺激试验在新产品申报或初次上市及国家监督管理机构要求时进行检验,有下列情况之一时应进行型式检验,产品正式投入批量生产时;生产设备进行检验或停产半年后又恢复生产时;国家质量监督机构提出型式检验要求时;有关行政主管部门提出型式检验要求时;
e、检验结果判定:检验结果全部项目符合本标准规定时,判该批产品为合格品;检验结果有一项或一项以上不符合本标准规定时,可以在原批产品中抽取双倍样品进行复检,复检结果全部符合本标准规定时,判该产品合格;如果复检结果仍有指标不符合标准要求时,则该批产品不合格,微生物指标有一项不合格的,判该批产品不合格,且不得复检。
作为优选,根据步骤D产品标志、包装包括:
a、标志:产品包装应有明显标志,内容包括:产品名称、厂名、厂址、执行标准、批号、生产日期、保存期限、产品使用说明书等内容,应符合GB/T191有关规定。
b、包装:产品内包装采用固体药用高密度聚乙烯瓶,其材质应符合YBB 0012卫生标准要求,小包装用硬纸盒包装,外包装用瓦楞纸箱,用胶带纸封口,并附有装箱单和合格证。
作为优选,根据步骤E运输及贮存规则包括:
a、运输:运输工具应清洁、干燥、无异味、无污染;运输中应注意轻装、轻缷、防雨、防潮、防晒;不得与有毒、有害、有异味或影响产品质量的物品混装运输;
b、贮存:本品应贮存在阴凉、干燥、通风的库房内,不得与有毒有害物质混放。成品堆放必须有垫板,离地10cm以上,离墙20cm以上。成品库入库必须依照先进先出的原则,依次出库,符合上述运输、贮存条件,产品包装完好无损且未启封时,产品保质期为24个月。
与现有技术相比,本发明的有益效果是:
(1)本发明设置的步骤A,产品技术性指标检验规格能够根据国家相关规定具体详细的提出自己符合规范的检验规格,能够有效提高产品检验质量、避免劣质产品流向市场。
(2)步骤B,产品需实施检验方法具体种类能够根据多种国家标准的检验方式方法具体的监测产品质量,严格把关,避免不合格产品流向市场。
(3)步骤C产品具体检验规则划定区域,对产品抽样检测,发现不合格产品后进行反复多次检验,确认是否属于特殊情况,符合标准允许流入市场,不符合标准即标注拒绝复检。
(4)步骤D产品标志、包装,标志能够明确厂家、批次能够追查溯源,且能够有效避免三无产品流入市场,生产日期、保存期限、产品使用说明书等内容能够帮助使用者正确使用产品,避免误操作影响正常使用的实际效果,包装能够有效防止在运输过程中发生破碎和泄露。
(5)步骤E运输及贮存,合理的运输能有效的减少产品的非正常损毁,合理的贮存能够有效实现产品最大保质期限,避免因为错误贮存、堆放而可能影响产品的后续使用和实际使用效果。
附图说明
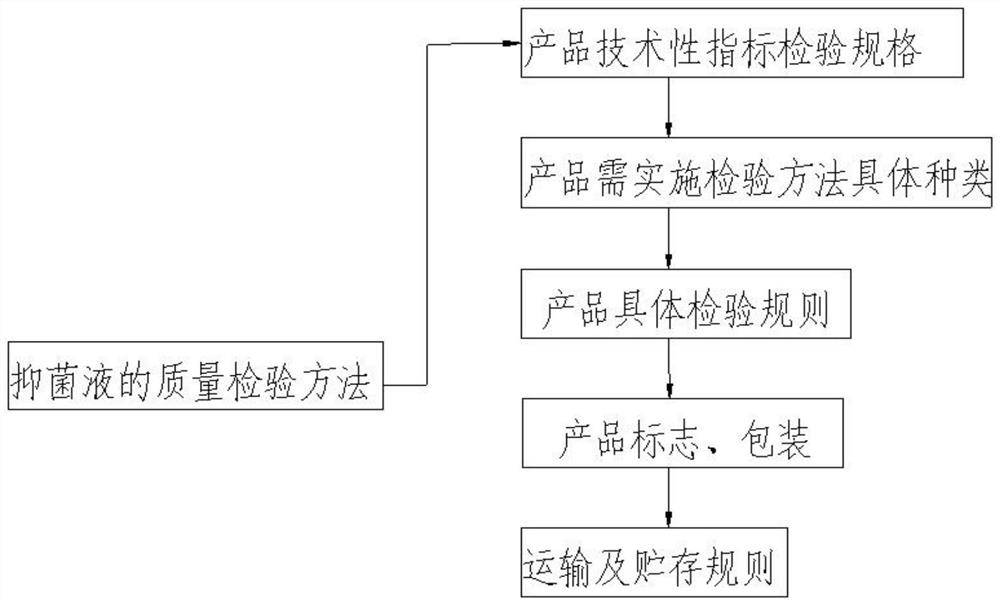
图1为本发明操作步骤示意图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
如图1所示,其具体操作包含以下步骤:
A、产品技术性指标检验规格;
B、产品需实施检验方法具体种类;
C、产品具体检验规则;
D、产品标志、包装;
E、运输及贮存规则。
根据步骤A产品技术性指标检验规格包括:
a、原料要求:苦参、铁线藤、紫霄花、蛇床子、菟丝子、柴胡、蜂房、地龙、车前子、艾叶、醋酸氯己定应符合《中华人民共和国药典》(2015年版)各品名项下有关规定;
b、辅料要求:尼泊金乙酯、纯化水均应符合《中华人民共和国药典》(2015年版)各品名项下有关规定;
c、感官要求:感官要求应符合表1的规定;
表1
d、净含量允差:应符合《定量包装商品计量监督管理办法》;
e、理化标准:理化指标应符合表2的规定;
表2
f、微生物指标:微生物指标应符合表3的规定;
表3
g、抑菌试验及抑菌稳定实验:抑菌试验应符合表4的规定;
表4
h、急性眼刺激实验:应无刺激性。
根据步骤B产品需实施检验方法具体种类包括:
a、感官检验:将样品挤入透明的烧杯中,在自然光线下观察其色泽,组织形态及杂质、鼻嗅样品的气味;
b、净含量监测:按JJF 1070的规定测定;
c、PH测定方法:按《消毒技术规范》中pH值测定方法进行检验;
d、铅、砷、汞的监测:按《化妆品安全技术规范》中的方法检测;
e、醋、酸、氯已定:按《消毒技术规范》2002年版规定的方法测定;
f、微生物指标:按《一次性使用卫生用品卫生标准》4.2要求,用GB 15979附录B的方法检验;
g、抑菌试验及抑菌稳定实验:按照GB 15979-2002《一次性使用卫生用品卫生标准》规定方法(附录C4试验方法及附录C6试验方法)进行测定;h、急性眼刺激实验:按《消毒技术规范》中的方法进行试验。
根据步骤C产品具体检验规则包括:
a、组批:同一批投料、同一工艺、同一班次生产的同一品种的产品为一批;
b、抽样:每批产品检验用量的3倍量随机抽样;
c、出厂检验:产品出厂前,应由生产单位检验部门出厂检验,合格并签发产品质量合格证后方可出厂,出厂检验内容包括标签、感官指标、净含量允差、有效成分含量及微生物指标;
d、型式检验:型式检验包括本标准技术要求除5.7条款急性眼刺激试验外的全部项目进行检验,急性眼刺激试验在新产品申报或初次上市及国家监督管理机构要求时进行检验,有下列情况之一时应进行型式检验,产品正式投入批量生产时;生产设备进行检验或停产半年后又恢复生产时;国家质量监督机构提出型式检验要求时;有关行政主管部门提出型式检验要求时;
e、检验结果判定:检验结果全部项目符合本标准规定时,判该批产品为合格品;检验结果有一项或一项以上不符合本标准规定时,可以在原批产品中抽取双倍样品进行复检,复检结果全部符合本标准规定时,判该产品合格;如果复检结果仍有指标不符合标准要求时,则该批产品不合格,微生物指标有一项不合格的,判该批产品不合格,且不得复检。
根据步骤D产品标志、包装包括:
a、标志:产品包装应有明显标志,内容包括:产品名称、厂名、厂址、执行标准、批号、生产日期、保存期限、产品使用说明书等内容,应符合GB/T 191有关规定。
b、包装:产品内包装采用固体药用高密度聚乙烯瓶,其材质应符合YBB 0012卫生标准要求,小包装用硬纸盒包装,外包装用瓦楞纸箱,用胶带纸封口,并附有装箱单和合格证。
根据步骤E运输及贮存规则包括:
a、运输:运输工具应清洁、干燥、无异味、无污染;运输中应注意轻装、轻缷、防雨、防潮、防晒;不得与有毒、有害、有异味或影响产品质量的物品混装运输;
b、贮存:本品应贮存在阴凉、干燥、通风的库房内。不得与有毒有害物质混放。成品堆放必须有垫板,离地10cm以上,离墙20cm以上。成品库入库必须依照先进先出的原则,依次出库,符合上述运输、贮存条件,产品包装完好无损且未启封时,产品保质期为24个月。
上述实施例只是本发明的较佳实施例,并不是对本发明技术方案的限制,只要是不经过创造性劳动即可在上述实施例的基础上实现的技术方案,均应视为落入本发明专利的权利保护范围内。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 一种抑菌液的质量检验方法
- 清肺抑火胶囊的制备方法及其检验方法
