TRPML1特异性小分子激活剂ML-SA5的应用
文献发布时间:2023-06-19 11:03:41
技术领域
本发明涉及医药技术领域,具体涉及TRPML1特异性小分子激活剂ML-SA5在预防和治疗溃疡性结肠炎方面的应用。
背景技术
溃疡性结肠炎(ulcerative colitis;UC)是一类病因不明的慢性非特异性胃肠道炎症性疾病,病变可累及结肠黏膜甚至整个胃肠道。临床上,患者会表现为反复的腹痛、腹泻、黏液血便,甚至出现各种全身并发症如视物模糊、关节疼痛、皮疹等。病理改变主要以肠道黏膜免疫反应异常为主,目前其发生机制可能为:在肠道菌群的参与下,环境因素作用于遗传易感者,启动肠道先天和获得性免疫应答,导致肠黏膜屏障损伤、炎性增生、溃疡不愈等病理改变,环境、感染、免疫、遗传因素与UC发病均有密切联系。
发明内容
本申请的主要目的在于提供一种TRPML1特异性小分子激活剂ML-SA5的新用途,在预防和治疗溃疡性结肠炎方面的应用,以解决相关技术中的问题。
为了实现上述目的,本发明提供如下技术方案:
TRPML1特异性小分子激活剂ML-SA5的应用,TRPML1特异性小分子激活剂ML-SA5在预防和治疗溃疡性结肠炎方面的应用。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,TRPML1特异性小分子激活剂ML-SA5在预防溃疡性结肠炎药物方面的应用。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,TRPML1特异性小分子激活剂ML-SA5在治疗溃疡性结肠炎药物方面的应用。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,所述的TRPML1特异性小分子激活剂ML-SA5的有效剂量为0.3mg/kg-1.8mg/kg。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,所述的TRPML1特异性小分子激活剂ML-SA5的有效剂量为0.3mg/kg。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,所述的TRPML1特异性小分子激活剂ML-SA5的有效剂量为0.9mg/kg。
上述TRPML1特异性小分子激活剂ML-SA5的应用,作为一种优选的实施方案,所述的TRPML1特异性小分子激活剂ML-SA5的有效剂量为1.8mg/kg。
本发明的有益效果为:本发明所述的TRPML1特异性小分子激活剂ML-SA5能够改善肠黏膜组织的损伤,为溃疡性结肠炎的预防和治疗提供了新的药物,具有良好的市场价值和临床应用前景。
附图说明
构成本申请的一部分的附图用来提供对本申请的进一步理解,使得本申请的其它特征、目的和优点变得更明显。本申请的示意性实施例附图及其说明用于解释本申请,并不构成对本申请的不当限定。在附图中:
图1为本发明TRPML1特异性小分子激活剂ML-SA5的化学结构图;
图2为DSS诱导的溃疡性结肠炎模型小鼠的制备及给药时间模式图;
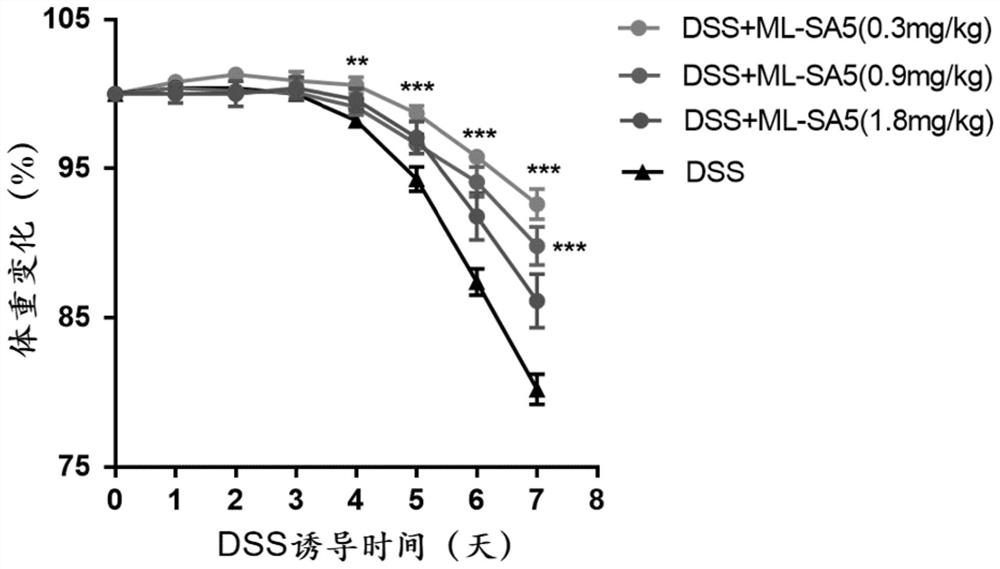
图3为ML-SA5联合给药DSS诱导的溃疡性结肠炎小鼠的体重改善结果;
图4为ML-SA5联合给药对于DSS诱导的溃疡性结肠炎小鼠导致的结肠坏死情况的改善结果;
图5为ML-SA5联合给药对于DSS诱导的溃疡性结肠炎小鼠的疾病活动指数改善结果;
图6为ML-SA5联合给药明显改善DSS诱导的溃疡性结肠炎小鼠的结肠组织的炎细胞浸润和黏膜破坏程度。
具体实施方式
为了使本技术领域的人员更好地理解本申请方案,下面将结合案例对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本申请一部分的实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本申请保护的范围。
需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本申请。
本申请发现的TRPML1特异性小分子激活剂ML-SA5的新用途,将该激活剂用于预防和治疗溃疡性结肠炎的应用。具体地将所述激活剂用于预防和治疗溃疡性结肠炎的应用时,所述激活剂能够改善肠黏膜的损伤。
所述激活剂用于预防和治疗溃疡性结肠炎的应用时,有效剂量为0.3mg/kg-1.8mg/kg,优选地,有效剂量为0.3mg/kg,更优选地,有效剂量为0.9mg/kg;进一步优选地,有效剂量为1.8mg/kg。
我们前期的研究表明溶酶体阳离子通道TRPML1是调控自噬的一个特异性靶点,通过运用TRPML1的激动剂或抑制剂改变TRPML1通道的活性可以特异性地调控自噬活动。所以,以下为本申请为了证实TRPML1的特异性小分子激活剂ML-SA5(其化学结构参见图1)对溃疡性结肠炎具有预防和治疗效果的试验。
1、试验方法
使用C57BL/6J小鼠制备DSS诱导溃疡性结肠炎模型,共分为3组,分别为正常组、DSS诱导的结肠炎模型组、DSS造模组联合低剂量ML-SA5(0.3mg/kg)组、中剂量ML-SA5(0.9mg/kg)组、高剂量ML-SA5(1.8mg/kg)组。
UC造模、ML-SA5干预的制备及给药时间模式,如图2所示:
在开始建立溃疡性结肠炎模型的前三天,所有C57BL/6J实验小鼠均自由饮用蒸馏水,同时在每天同一时间点,用腹腔注射的方式给ML-SA5干预组小鼠分别注射不同剂量等体积的ML-SA5药液,而正常组和DSS模型组腹腔注射同样体积的生理盐水作为对照。之后利用DSS造模七天,正常组继续自由饮用蒸馏水,其余四组均开始自由饮用溶有3%DSS的蒸馏水,每隔两天更换新配制的DSS溶液,并且腹腔给药方式同于前三天(正常组和DSS模型组腹腔注射生理盐水,药物干预组腹腔注射不同剂量的ML-SA5溶液)。造模给药期间,每天观察小鼠状态,称量小鼠的体重,观察小鼠粪便的性状,检测小鼠粪便的便血情况,并记录结果;于造模的第7天,测定相关指标之后,取出小鼠结肠组织,测量结肠长度并进行病理学分析结果。
2、试验结果
2.1体重变化测量方法:给与小鼠DSS后第0-7天每天测定小鼠体重,以第0天的体重作为基础体重,计算出相应天数的体重比例,并用Graphpad7.0软件作出体重变化曲线,结果如图3所示:
从图3可以看出:联合不同剂量的ML-SA5(0.3、0.9、1.8mg/kg)均明显改善DSS诱导溃疡性结肠炎导致的小鼠体重快速下降情况,0.3mg/kgML-SA5的效果最佳。
2.2结肠长度的测量方法
造模后第7天,取出小鼠结肠,并平放于0.9%的生理盐水浸透的纱布上,沿长轴轻轻拉直,用直尺测量回盲部至肛门端的长度,如图4所示。结肠长度可以反应结肠的坏死程度,坏死越严重,结肠长度越短。
从图4可以看出:所示ML-SA5干预组(0.3mg/kg)的结肠长度明显长于未干预组。统计图表对比了对照组、DSS组、联合不同剂量ML-SA5(0.3、0.9、1.8mg/kg)DSS组的结肠长度,提示ML-SA5干预可以明显改善DSS诱导溃疡性结肠炎导致的小鼠结肠坏死情况,以0.3mg/kgML-SA5的效果最佳。
2.3疾病活动指数(Disease Activity Index,DAI)的评价方法及结果
造模给药期间,每天观察小鼠体重变化情况,同时记录粪便性状和便血情况,并按照表一所述评分标准进行评分,小鼠的DAI由体重下降百分比、粪便性状和粪便隐血情况三者的总和。
表1疾病活动指数(DAI)评分标准
图5统计了对照组、DSS组、联合不同剂量ML-SA5(0.3、0.9、1.8mg/kg)DSS组第一天到第七天的疾病活动指数(DAI),从图5可以看出:ML-SA5干预可以明显改善DSS诱导溃疡性结肠炎导致的疾病活动指数。
2.4结肠组织病理学分析及评价的方法、结果
造模后第7天,取出小鼠结肠,观察结肠组织损伤情况,并根据表2所述的评分系统进行评分。
表2 DSS诱导的结肠炎病理组织评分标准
然后用0.9%的生理盐水冲洗肠腔。取相同部位远端结肠组织固定于4%多聚甲醛溶液,然后依次修块、脱水、透明、浸蜡、包埋、切片等程序制备石蜡切片,将制备好的石蜡切片放入二甲苯中进行脱蜡,30min后取出,依次转移至100%、95%、90%、80%、70%乙醇溶液中,每次5min;最后转移至蒸馏水,放置5min。之后将脱蜡后的切片进入苏木素染液中,静置3min,冲洗1min,转移至95%乙醇中,1min后,进行伊红染液染色,时间约为1min。染色完成后,将切片转移至70%、80%、90%、95%、100%的乙醇溶液中,进行脱水,然后转移至二甲苯中5min,最后可用中性胶封片密封。根据表2所述的评分方法,请病理科医生在光学显微镜下观察并进行评分。
从图6可以看出:HE染色表明ML-SA5给药组的结肠黏膜组织损伤水平明显低于未进行ML-SA5干预的造模组。
通过以上实验结果证明:ML-SA5小分子化和物可以明显改善溃疡性结肠炎模型小鼠的肠道黏膜组织损伤。本发明为溃疡性结肠炎的预防和治疗提供了新的药物,具有较好的市场价值和临床应用前景。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- TRPML1特异性小分子激活剂ML-SA5的应用
- TRPML1特异性小分子抑制剂ML-SI3的应用
