一种基于aGVHD biomarker的重度肠道aGVHD模型的方法
文献发布时间:2023-06-19 11:21:00
技术领域
本发明属于造血干细胞移植技术领域,具体为一种基于aGVHD biomarker的重度肠道aGVHD模型的方法。
背景技术
急性移植物抗宿主病(acute Graft-versus-Host Disease,aGVHD)是异基因造血干细胞移植(allogeneic Hematopoietic Stem Cell Transplantation,allo-HSCT)后致命并发症以及死亡率的主要来源。aGVHD可以影响多个器官,主要是皮肤、肝脏和胃肠道。其中,肠道aGVHD发病率高,程度较重,且重度肠道aGVHD往往难以逆转,增加了病死率。因此,重度肠道aGVHD的早期诊断与有效的治疗直接关系到疾病的预后,在aGVHD治疗中处于重要的地位。
当前,对肠道aGVHD的诊断多集中于放射学、内窥镜检查和组织学活检等方法,但最终诊断仍取决于经典的临床特征。生物标志物因其具有非侵入性,且能够特异和敏感地反映疾病状态而被应用于病人群体开始治疗之前进行早期风险分层和临床症状出现之前指导进行提前干预等。在肠道aGVHD预测和诊断方面,James Ferrara等人发现:REG3α可以作为胃肠道aGVHD诊断的生物标志物(biomarker),ROC-AUC可达0.8。Thomas Hueso等人发现:移植前血浆瓜氨酸(Citrulline)水平与胃肠道aGVHD严重程度具有相关性,其对II-IV度胃肠道aGVHD的预测AUC为0.683。Liu Yue等人发现:甘油磷脂(GPL)代谢在aGVHD的发病机理中起重要作用,其中GPL代谢的代谢物PC(13:0/0:0)与胃肠道aGVHD呈负相关,但其AUC为0.646。上述研究对胃肠道aGVHD的预测或诊断能力较低。
上述研究表明基于biomarker的肠道aGVHD诊断(预测)具有很好的临床应用价值,但是由于病人群体的差异,从西方病人群体得出的结论不能直接应用于中国的病人群体。
因而,本发明提出一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,用于对中国病人群体进行肠道aGVHD严重程度进行更为精准的划分,辅助临床决策。
发明内容
针对现有技术的不足,本发明提供了一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,以解决上述背景技术中提出的问题。
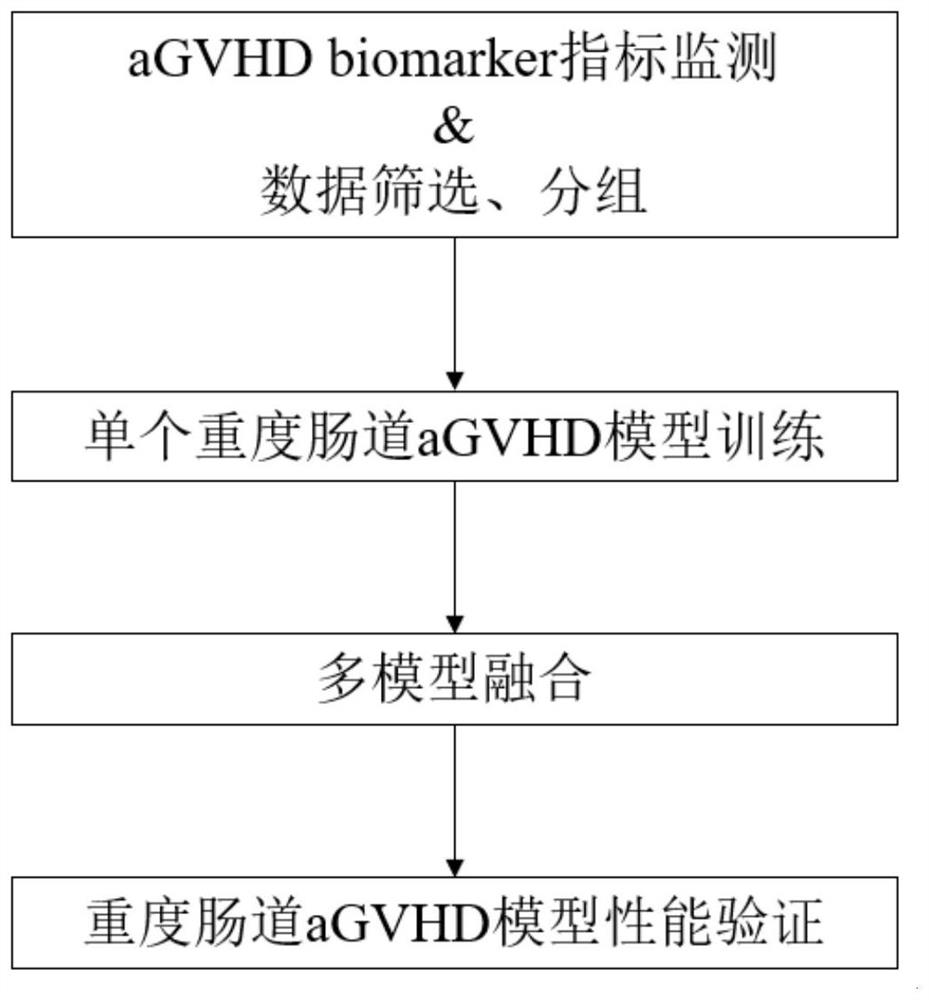
为实现上述目的,本发明提供如下技术方案:一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,包括aGVHD biomarker指标监测及数据筛选与分组、单个重度肠道aGVHD模型训练、多模型融合、重度肠道aGVHD模型性能前瞻性验证的四个步骤:
S1、aGVHD biomarker指标监测及数据筛选与分组,动态监测多中心病人群体重要时间点的aGVHD biomarker指标,并根据随访至HSCT后100天内病人是否发生肠道aGVHD进行分组,其中,发生肠道aGVHD组筛选事件发生时间点监测到的aGVHD biomarker指标,未发生肠道aGVHD组按与发生肠道aGVHD组biomarker测量时间分布相同原则筛选监测到的aGVHD biomarker指标,形成模型数据集;
S2、单个重度肠道aGVHD模型训练,对S1中提及的模型数据集按比例随机分为训练和测试集,将病人aGVHD biomarker指标与临床重度肠道aGVHD进行关联,采用机器学习领域先进的堆叠技术、逻辑回归技术,建立精准划分重度肠道aGVHD严重程度的机器学习模型;
S3、多模型融合,采用多模型融合技术,筛选多个模型效果良好的肠道aGVHD模型,对病人发生肠道aGVHD的严重程度使用评分方法进行评分,评分结果在模型数据集上ROC-AUC达到0.90以上,灵敏度、特异性达到0.80以上;
S4、重度肠道aGVHD模型性能前瞻性验证,监测参与模型训练之外的多中心病人群体的重要时间点的aGVHD biomarker指标,采用S1中提及的数据筛选及分组原则,形成模型验证集,多模型融合后的重度肠道aGVHD模型在验证集上ROC-AUC达到0.84左右,灵敏度、特异性达0.80以上,模型能够对肠道aGVHD严重程度进行更加精准划分,且稳定可靠。
进一步优化本技术方案,所述aGVHD biomarker的指标包括sST2、REG3α、IL-6、IL-8以及TNFR1。
进一步优化本技术方案,所述S1中,筛选过程中必须保证一个病人一条数据。
进一步优化本技术方案,所述S2中,单个重度肠道aGVHD模型在模型训练集和模型测试集上ROC-AUC位于0.85±0.1,灵敏度和特异性的数值达0.75以上。
进一步优化本技术方案,所述多中心病人群体的标准为重度肠道aGVHD占13%的病人群体。
与现有技术相比,本发明提供了一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,具备以下有益效果:
该基于aGVHD biomarker的重度肠道aGVHD模型的方法,通过建立机器学习模型,对病人发生肠道aGVHD严重程度进行精准划分,为临床决策提供指导;同时仅需检测血清中aGVHD biomarker指标,避免了例如内窥镜检查和肠粘膜活检等的肠道aGVHD常规诊断方法给病人带来的强烈不适感,更适应于中国病人群体。
附图说明
图1为本发明提出的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法的流程示意图;
图2为本发明提出的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法的单个重度肠道aGVHD模型在模型训练集上的ROC曲线图;
图3为本发明提出的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法的单个重度肠道aGVHD模型在模型测试集上的ROC曲线图;
图4为本发明提出的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法的多模型融合后重度肠道aGVHD模型在模型数据集上的ROC曲线图;
图5为本发明提出的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法的多模型融合后重度肠道aGVHD模型在模型验证集上的ROC曲线图。
具体实施方式
下面将结合本发明的实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例一:
请参阅图1,一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,包括aGVHDbiomarker指标监测及数据筛选与分组、单个重度肠道aGVHD模型训练、多模型融合、重度肠道aGVHD模型性能前瞻性验证的四个步骤:
S1、aGVHD biomarker指标监测及数据筛选与分组,动态监测多中心病人群体(重度肠道aGVHD占13%的病人群体)重要时间点的aGVHD biomarker指标,aGVHD biomarker的指标包括sST2、REG3α、IL-6、IL-8以及TNFR1,并根据随访至HSCT后100天内病人是否发生肠道aGVHD进行分组,其中,发生肠道aGVHD组筛选事件发生时间点监测到的aGVHD biomarker指标,未发生肠道aGVHD组按与发生肠道aGVHD组biomarker测量时间分布相同原则筛选监测到的aGVHD biomarker指标,形成模型数据集,筛选过程中必须保证一个病人一条数据;
S2、单个重度肠道aGVHD模型训练,对S1中提及的模型数据集按比例随机分为训练和测试集,将病人aGVHD biomarker指标与临床重度肠道aGVHD进行关联,采用机器学习领域先进的堆叠技术、逻辑回归技术,建立精准划分重度肠道aGVHD严重程度的机器学习模型,如图2和图3所示,单个重度肠道aGVHD模型在模型训练集和模型测试集上ROC-AUC位于0.85±0.1,灵敏度和特异性的数值达0.75以上;
S3、多模型融合,采用多模型融合技术,筛选多个模型效果良好的肠道aGVHD模型,对病人发生肠道aGVHD的严重程度使用评分方法进行评分,如图4所示,评分结果在模型数据集上ROC-AUC达到0.90以上,灵敏度、特异性达到0.80以上;
S4、重度肠道aGVHD模型性能前瞻性验证,监测参与模型训练之外的多中心病人群体的重要时间点的aGVHD biomarker指标,采用S1中提及的数据筛选及分组原则,形成模型验证集,多模型融合后的重度肠道aGVHD模型在验证集上ROC-AUC达到0.84左右,灵敏度、特异性达0.80以上,如图5所示,模型能够对肠道aGVHD严重程度进行更加精准划分,且稳定可靠。
实施例二:
采用实施例一中的一种基于aGVHD biomarker的重度肠道aGVHD模型的方法,动态监测多中心病人群体(重度肠道aGVHD约占13%)重要时间点的aGVHD biomarker指标,并根据移植后100天内是否发生肠道aGVHD分组进行数据筛选,采用一个病人一条数据,发生肠道aGVHD组病人取肠道aGVHD发生时biomarker数据,未发生肠道aGVHD组病人按照与发生组biomarker数据测量时间分布相同的原则筛选数据,形成模型数据集。
对上述模型数据集按比例随机分为训练集和测试集,将病人aGVHD biomarker指标与临床是否发生重度肠道aGVHD进行关联,采用机器学习领域的堆叠、逻辑回归技术,建立重度肠道aGVHD机器学习模型。单个重度肠道aGVHD模型赋予aGVHD biomarker不同权重,进而给定每个病人发生肠道aGVHD的严重程度p,如下式一、式二所示。注意,式一、式二分别为不同参数下的模型训练结果,N()表示归一化。
p值越大,病人发生重度肠道aGVHD的风险也越高。所选单个重度肠道aGVHD模型在训练集和测试集上的ROC-AUC均可达0.85左右,灵敏度、特异性可达0.75以上。
采用多模型融合技术,对病人重度肠道aGVHD严重程度进行评分(score),评分方法如下式三所示。多模型融合后重度肠道aGVHD模型在模型数据集上ROC-AUC可达0.90,灵敏度和特异性位于0.80以上。注意,式三中acc
动态监测参与模型训练之外的多中心病人群体(重度肠道约占4.5%)重要时间点的aGVHD biomarker指标,并按照与模型数据集相同的筛选原则形成前瞻性的模型验证集。
利用上述模型验证集对多模型融合后重度肠道aGVHD模型进行验证,ROC-AUC可达0.84,灵敏度、特异性位于0.8以上。模型稳定,可对重度肠道aGVHD进行精准划分,为临床决策提供指导。
上述两个实施例表明,本发明的有益效果是:该基于aGVHD biomarker的重度肠道aGVHD模型的方法,通过建立机器学习模型,对病人发生肠道aGVHD严重程度进行精准划分,为临床决策提供指导;同时仅需检测血清中aGVHD biomarker指标,避免了例如内窥镜检查和肠粘膜活检等的肠道aGVHD常规诊断方法给病人带来的强烈不适感,更适应于中国病人群体。很好地应用于中国病人群体在HSCT后100天内进行肠道aGVHD严重程度的精准划分,具有很好的临床参考价值。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 一种基于aGVHD biomarker的重度肠道aGVHD模型的方法
- 一种基于aGVHD biomarker的风险分层及监测方法
