pH响应性磁性纳米核壳载药体系及其构建方法和应用
文献发布时间:2023-06-19 11:27:38
技术领域
本发明属于纳米治疗技术领域,具体涉及一种pH响应性磁性纳米核壳载药体系及其构建方法和应用。
背景技术
近年来,已经有许多抗癌药物被研究和出现。尽管我们已经取得了进展,但迄今为止癌症还不能完全治愈。许多抗癌药物针对癌细胞上的特定分子,也可以进入正常细胞并产生不良作用。开发有效的药物载体或给药途径对提高药物的靶向性十分重要。目前,各种类型的纳米颗粒已被报道为潜在的药物传递或诊断药物,包括脂质体纳米颗粒、聚合物和金属纳米颗粒以及其他无机纳米颗粒。直径从几纳米到250纳米的生物相容纳米粒子被认为在癌症药物输送方面有很大的潜力。同时,由于纳米粒子的尺寸相对较大,纳米粒子可以保留实体肿瘤中肿瘤血管的血管渗漏,目前正在开发的许多纳米载体癌症治疗方法都依赖于增强的渗透性和保留(EPR)效应,在肿瘤微环境中被动积累并杀死癌细胞。
近年来纳米材料的应用活跃于生物医学及材料科学等各领域,在众多诊断治疗纳米材料中,超顺磁性四氧化三铁微球(SPION)备受抗肿瘤药物研究者的关注,极小的尺寸性质使其可充分利用增强渗透和滞留效应在病变部位处积聚,并且在外界磁场的作用下,能够实现定点递送,从而达到靶向给药的目的。众所周知,抗肿瘤药物载体对人体细胞具有一定的毒副作用,而二氧化锆(ZrO
发明内容
本发明的第一个目的是提供一种pH响应性磁性纳米核壳载药体系,通过在磁性内核表面修饰氧化锆介孔壳层,介孔壳层的孔道内装载药物,如抗癌药物道诺霉素(DNM),以纳米氧化铋作为pH响应性门控封堵孔道,该体系具有磁靶向性,且在体内酸性环境中可以释放药物。
本发明的第二个目的是提供上述pH响应性磁性纳米核壳载药体系的构建方法。
本发明的第三个目的是提供上述pH响应性磁性纳米核壳载药体系的应用。
对于上述目的,本发明通过几下技术方案予以实现:
一种pH响应性磁性纳米核壳载药体系,其是在磁性内核表面修饰介孔壳层形成核壳结构,介孔壳层的孔道内静电吸附装载抗肿瘤药物,然后以pH敏感型物质(如纳米氧化铋)静电吸附在介孔中,作为pH响应性门控封堵孔道。
本发明以纳米四氧化三铁作为磁性内核,以二氧化锆作为介孔壳层,以Bi
本发明的载药体系是一种靶向抗肿瘤药物系统,所述抗肿瘤药物为蒽环类抗生素。
进一步地,所述蒽环类抗生素为阿霉素、道诺霉素、伊达比星、米托蒽醌或表阿霉素。
另一方面,本发明的pH响应性磁性纳米载药体系的构建方法,包括如下步骤:
(1)通过化学共沉淀法制备超顺磁性四氧化三铁纳米粒子。具体包括如下操作:首先称取2.7g FeCl
(2)Fe
(3)MMZr的制备:将上一步含CTAB模板剂的Fe
(4)待加入抗肿瘤药物并成功负载药物得到MMZr@X,加入Bi
在全身给药后,直径大于200nm的较大颗粒通常由于机械过滤而被脾脏螯合,并最终被吞噬细胞系统而被除去,导致血液循环时间减少。另一方面,直径小于10nm的较小颗粒通过外渗和肾清除被迅速除去。粒子从10-100nm是静脉注射的最佳选择,并且表现出最长的血液循环时间。我们体系合成的介孔孔径是2纳米-50纳米之间。
与现有技术相比,本发明具有如下有益效果:
本发明提供的pH响应性磁性纳米核壳载药体系,具有磁靶向性,可利用外加磁场来引起磁性纳米粒子的移动,pH响应是利用肿瘤细胞相比正常细胞pH值低,当含药载体到达癌细胞组织时,其酸性的微区环境(pH=5.8)使得封盖剂“gatekeeper”降解断键,“gate”打开,从而药物释放出来杀死肿瘤细胞,通过一系列细胞实验监测材料的细胞毒性与定位情况,且随着药物浓度递增发现细胞凋亡量增多,这种新颖的pH响应的协同药物控释体系对于癌症的治疗具有潜在的应用价值。
附图说明
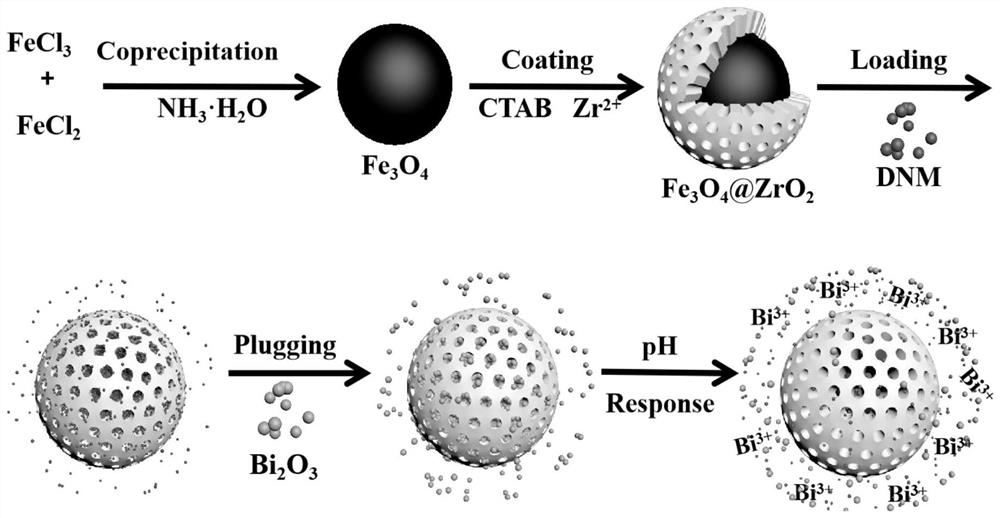
图1为MMZr@Bi
图2为在外磁场作用下载药纳米体系pH响应性控释杀死癌细胞的机制图;
图3为MMZr@Bi
图4为Fe
图5为DNM、MMZr@Bi
图6为DNM、MMZr、MMZr@Bi
图7为本发明磁性纳米载体的磁性分散效果图;
图8为未封堵(A)和封堵(B)纳米载体在不同pH条件刺激下的缓释率曲线图;
图9为血液相容性实验中不同浓度的空载体MMZr@Bi
图10为不同浓度的纳米粒子MMZr、MMZr@Bi
图11为磁靶向试验中0h和24h的培养皿中有磁场区域及对侧无磁场区域照片;
图12为本发明的磁性纳米载体系统对不同肿瘤细胞普鲁士蓝染色照片;
图13肿瘤细胞A549、MCF-7对本发明中磁性纳米载体的细胞摄取;
图14(A)为细胞迁移试验中光学显微镜下0h、24h同一位置划痕的变化照片,(B)为细胞迁移试验中发明载药纳米粒子和空白组迁移面积比较;
图15为在相同DNM、MMZr@Bi
图16为荧光显微镜在不同浓度的MMZr@Bi
图17为流式细胞仪在不同浓度的MMZr@Bi
图18流式细胞仪下检测到的不同加药浓度下的线粒体膜电位检测图;
图19为流式细胞仪在不同加药浓度下的细胞自噬图。
具体实施方式
为让本领域的技术人员更加清晰直观的了解本发明,下面将结合附图,对本发明作进一步的说明。
本发明中涉及的药物简称如下:
DNM:道诺霉素、FBS:胎牛血清、MTT:3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐、CTAB:十六烷基三甲基溴化铵。
抗肿瘤药物的pH响应性磁性纳米载药体系的构建方法,包括如下步骤:
步骤1:通过化学共沉淀法制备超顺磁性四氧化三铁纳米粒子,首先称取2.7gFeCl
步骤2:Fe
步骤3:MMZr的纳米载体制备,将步骤2含CTAB模板剂的Fe
步骤4:先取步骤3中的纳米载体5mg于试管中,加入浓度为1.0mg/mL的DNM溶液4mL。稍微振摇后,经过磁性吸附静置,吸取上清液0.2mL,作为0h的样品,然后将试管放置在恒温摇床(150rp/min,30℃)避光振摇,固载24h、48h后取0.5mL的上清液,用紫外分光光度计测出上清液浓度,计算固载量。48h回收固载后的上清液,用pH=7.40的PBS缓冲溶液清洗纳米微球,得到固载药物的磁性纳米微球。
步骤5:于上述清洗过的纳米微球当中加入5mg的纳米Bi
实施例1对MMZr@Bi
MMZr@Bi
扫描电子显微镜(TEM)和zeta电位分析仪结果如图3和图4所示,获得纳米粒子的尺寸分布和表面电荷,证明ZrO
紫外吸收光谱结果如图5所示,DNM在480nm处有吸收峰,而纯载体无吸收峰,载药纳米粒子在480nm处有紫外吸收峰,证明药物已固载上去。
红外吸收光谱结果如图6所示,DNM中C-N和N-H拉伸的特征吸收峰为1616cm
图7所示为纳米体系的磁响应效果测定结果。说明包裹了氧化锆后,载体的磁响应性能良好。而在无磁场的情况下载体短时间内不发生分离,证明磁性纳米微球的分散性较好。
实施例2带药纳米载体在不同pH条件刺激下的缓释实验
为了验证纳米载体复合物在不同pH刺激条件下药物释放情况,将载药后的未封堵和封堵的纳米粒子分别溶解在相同体积不同浓度,分别在0h,1h,2h,4h,6h,8h,12h,24h取缓释后的上清液测紫外后算出缓释率,结果见图8。可以明显看出药物随着酸性环境的增强释放的更多,这说明载药磁流体显示了pH响应性,这个特点对于癌症细胞的智能化靶向治疗是十分重要的。
实验例3细胞实验
细胞培养
细胞系A549细胞(人肺癌细胞)和MCF-7(人乳腺癌细胞)获自广东药科大学药学院,Hacat细胞(人正常皮肤细胞)获自广东药科大学生科院。以含有10%FBS、1%青霉素-链霉素的DMEM培养基作为生长环境,于37℃、5%CO
血液相容性实验
分别以去离子水和生理盐水作为阳性和阴性对照,向终浓度为3mg/mL的载体各加入2.5ml 2%红细胞悬液,测定OD值,计算出溶血率,并观察拍下溶血现象。结果如图9所示,显示加有磁流体的试管上清液淡黄色,而加入超纯水的试管发生了溶血现象,且根据溶血率得知磁流体的溶血率小于医用材料的溶血率5%,证明载体可安全用于医疗。
细胞活力测定—MTT实验
使用MTT测定法测定A549细胞在游离DNM、MMZr、MMZr@Bi
如图10所示,在癌细胞中,纯载体MMZr没有太大毒性而纳米粒子Bi
磁靶向性研究
将A549细胞接种于60mm培养皿中培养贴壁后,加入1.5μg的纳米粒子MMZr@Bi
普鲁士蓝染色
磁性纳米粒子在细胞中的摄取可以通过普鲁士蓝染色实验来验证,将A549细胞和MCF-7细胞接种于6孔板中,培养24h待细胞贴壁后空白对照组加入正常培养基,实验组加入含有浓度为2μg/mL的MMZr@Bi
流式细胞仪测试细胞摄取
于显微镜下观察培养的细胞,选取生长良好,处于对数生长期的细胞进行实验,使用0.25%的胰蛋白酶消化贴壁的细胞,消化完成后使用完全培养液重悬。计数后,将细胞接种至12孔板,每孔加入细胞量为8000-10000个。待细胞铺满80%后加入IC50值附近五个药物浓度梯度的含药完全培养液继续培养24h,用PBS洗去未被完全摄入的纳米粒子,取消化后的细胞用PBS洗三次后放入流式管,用流式细胞仪进行分析。通过流式细胞分析仪得到如图13,然后根据流式图通过flowjo软件得出荧光图,结果显示,随着载药纳米粒子药物浓度递增,流式荧光图右移,荧光强度相比空白组增强,反映药物可以被肿瘤细胞摄取且随着载药浓度递增细胞毒性越强。
细胞划痕实验-细胞迁移
将A549细胞以每孔5×10
细胞周期检测
取对数期生长的细胞,用胰酶进行消化1-2min,用移液枪吹打成细胞悬液,用血球计数板进行计数,以1.0×10
如图15所示,空白细胞组G
荧光显微镜及流式细胞仪测细胞凋亡
在对数期生长的细胞,将入胰酶消化1-2min,用移液枪轻轻的吹打细胞,制成悬浮液,用血球计数板进行计数,以1.0×10
取对数期生长的细胞,用胰酶进行消化1-2min,用移液枪吹打成细胞悬液,用血球计数板进行计数,以1.0×10
如图16所示,在不同浓度下的MMZr@Bi
为了定量评估由MMZr@Bi
线粒体膜电位检测
将肿瘤细胞(A549)分散于6孔细胞培养板的密度为2.5×10
如图18所示,经过纳米粒子处理以后的线粒体膜电位相对于未处理空白组及阳性对照组降低,且药物浓度越高,线粒体膜电位下降越明显。且细胞往右偏,JC-1由聚合物向单体方向转变,证明载药纳米粒子可以降低肿瘤细胞线粒体膜电位从而诱导细胞死亡。据此可以初步推测纳米粒子以线粒体途径引发了细胞凋亡。
自噬研究
目前,用酸标记的MDC染色细胞是另一种评估自噬活性的快速方法。从图19流式细胞仪检测结果中可以看出,MMZr@Bi
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- pH响应性磁性纳米核壳载药体系及其构建方法和应用
- 一种具有磁性和发光性能的中空核壳纳米介孔载药体系及其制备与应用
