一种苯并a蒽的工业化生产方法
文献发布时间:2023-06-19 11:30:53
技术领域
本发明属于有机合成技术领域,具体涉及一种苯并[a]蒽的工业化生产方法。
背景技术
苯并[a]蒽含有一个强活性位点,能够与N-氯代丁二酰亚胺、N-溴代丁二酰亚胺、二溴海因、溴素等反应,可以在苯并[a]蒽的7位上引入相对应的卤代物,再通过Suzuki反应、Buchwald反应、Heck反应及Ullmann反应等引入其他分子片段实现分子结构的扩张。苯并[a]蒽作为中间体合成的衍生物,被广泛用于具有共轭结构材料的合成,在场效应晶体管、有机发光二极管等领域具有广泛应用。
目前,常见的苯并[a]蒽的合成方法以1-溴萘(如图方法1)为原料(J.Med.Chem.2019,62,15,7089–7110;J.Chem.Soc.,1935,1367-1370)或萘(如图方法2)为原料(BeilsteinJ.Org.Chem.2019,15,1313–1320),通过傅克酰基化反应、强酸脱水关环,最后加氢还原得到产品苯并[a]蒽。此方法主要存在的问题是三步反应均造成大量废水。经按方法2测算,每产生1Kg苯并[a]蒽,便会产生400Kg的废水相。第一步AlCl
总体来说,上述制备方案水洗过程经常发生乳化现象,后处理操作困难,进而导致苯并[a]蒽的成本难以降低,操作复杂。
路线如下所述:
发明内容
为了解决上述问题,本发明提供了一种苯并[a]蒽的工业化生产方法,与上述方法相比,通过改变反应路线(以2-溴萘为原料,依次经过锂代、硼酯化、酸化、Suzuki反应、Weinreb反应、Witting反应、关环制得苯并[a]蒽),且各反应步骤中采用价格低廉的原料,使得反应过程及后处理简单,对环境危害小且降低生产成本,收率高,适合工业化生产。
本发明提供一种苯并[a]蒽的工业化生产方法,包括以下步骤:
S1、2-溴萘通过2,2,6,6,-四甲基哌啶锂锂代,然后通过硼酸三异丙酯进行硼酯化,之后酸化制得2-溴-3萘硼酸;
S2、将S1制得的2-溴-3萘硼酸与碘苯通过Suzuki反应制备2-溴-3苯基萘;
S3、将S2制得的2-溴-3苯基萘与正丁基锂锂代,之后通过N,N-二甲基甲酰胺发生Weinreb反应,制得2-醛基-3苯基萘;
S4、将S3制得的2-醛基-3苯基萘与氯甲醚三苯基膦盐和叔丁醇钾通过Witting反应,制得2-甲氧基乙烯基-3-苯基萘;
S5、将S4制得的2-甲氧基乙烯基-3-苯基萘通过甲基磺酸关环,制得苯并[a]蒽;
其合成路线如下所示:
优选地,所述S1具体包括以下步骤:
S11、将2,2,6,6-四甲基哌啶和四氢呋喃混合,降温至-20~0℃,加入正丁基锂,保温-20~0℃反应0.5~1h后,制得2,2,6,6-四甲基哌啶锂;
S12、将S11制得的2,2,6,6-四甲基哌啶锂体系降温至-80~-70℃,加入硼酸三异丙酯,接着加入2-溴萘,升温至-55~-45℃,保温反应3~5h,之后升温至-20~-10℃,调节pH=5~6、水洗至中性、浓缩,制得2-溴-3萘硼酸。
优选地,S1中,正丁基锂和2,2,6,6-四甲基哌啶的摩尔比为1:1~2,2-溴萘和四氢呋喃的用量比为1g:10~15mL,2-溴萘和正丁基锂的摩尔比1:2~2.5,正丁基锂和硼酸三异丙脂的摩尔比为1:1~2。
优选地,所述S2具体包括以下步骤:
将2-溴-3萘硼酸、碘苯、碳酸钾混合溶解在由甲苯、乙醇和水制成的混合溶剂中,升温至40℃~50℃,加入四三苯基膦钯,继续升温至回流,反应1~2h后,甲苯相水洗至中性,甲基环己烷溶解,析出固体,过滤,制得2-溴-3苯基萘。
优选地,S2中,2-溴-3萘硼酸与碘苯的摩尔比为1:1~1.2,2-溴-3萘硼酸与四三苯基膦钯的质量比为43~44:1,2-溴-3萘硼酸与碳酸钾的质量比为1.5:1,甲苯、乙醇和水的体积比为2:1:1。
优选地,所述S3具体包括以下步骤:
将2-溴-3苯基萘与四氢呋喃混合后,降温至-90℃~-80℃,加入正丁基锂,保温-80~-90℃反应0.5~1h,接着加入DMF,保温-80~-90℃反应1~2h,淬灭、浓缩、萃取制得2-醛基-3苯基萘。
优选地,S3中,2-溴-3苯基萘和四氢呋喃的用量比为1g:10~15mL,2-溴-3苯基萘和正丁基锂的摩尔比1:1.1~1.5,2-溴-3苯基萘和DMF的摩尔比为1:1.3~1.7。
优选地,所述S4具体包括以下步骤:
将氯甲醚三苯基磷盐与四氢呋喃混合后,降温至-10℃~0℃,加入叔丁醇钾,保温-10℃~0℃反应1~2h后,加入2-醛基-3苯基萘,保温-10℃~0℃反应1~2h后,淬灭,萃取,浓缩制得2-甲氧基乙烯基-3-苯基萘。
优选地,S4中,2-醛基-3苯基萘和四氢呋喃的用量比为1g:10~15mL,2-醛基-3苯基萘和氯甲醚三苯基磷盐的摩尔比1:1.3~1.7,2-醛基-3苯基萘和叔丁醇钾的摩尔比1:1.5~1.9。
优选地,所述S5具体包括以下步骤:
将2-甲氧基乙烯基-3-苯基萘与甲苯混合后,加入甲基磺酸,保温40℃~50℃反应1~2h后,水洗,浓缩,重结晶制得苯并[a]蒽;2-甲氧基乙烯基-3-苯基萘和甲苯的用量比为1g:10~15mL,2-甲氧基乙烯基-3-苯基萘和甲基磺酸的摩尔比1:1.5~2.5。
本发明与现有技术相比具有如下有益效果:
(1)本发明提供了一种苯并[a]蒽的工业化生产方法,采用以下步骤制备得到:2-溴萘通过2,2,6,6,-四甲基哌啶锂锂代,然后通过硼酸三异丙酯进行硼酯化,之后酸化制得2-溴-3萘硼酸;将2-溴-3萘硼酸与碘苯通过催化剂,发生Suzuki反应制备2-溴-3苯基萘;将2-溴-3苯基萘与正丁基锂锂代,然后通过DMF制得2-醛基-3苯基萘;将2-醛基-3苯基萘与氯甲醚三苯基膦盐和叔丁醇钠发生Witting反应制得2-甲氧基乙烯基-3-苯基萘;将2-甲氧基乙烯基-3-苯基萘在酸作用下关环制得目标产物苯并[a]蒽;
(2)与背景技术所述方法相比,本发明上述各步骤所采用原料简单易得,成本低,且各步骤的后处理过程简单,避免了背景技术所述方法产生大量废水的问题,对环境危害小,且收率高,便于工业化生产。
附图说明
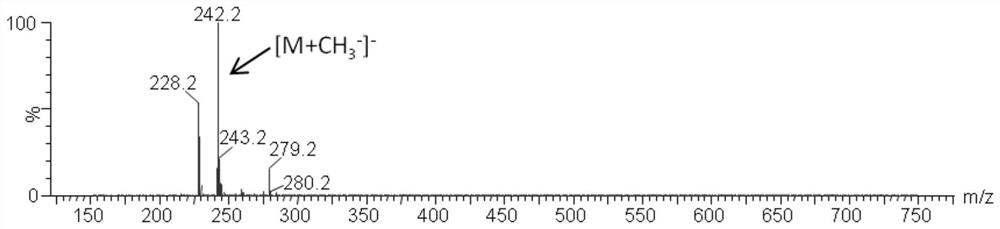
图1为实施例1制得的苯并[a]蒽的液质谱图。
具体实施方式
为了使本领域技术人员更好地理解本发明的技术方案能予以实施,下面结合具体实施例和附图对本发明作进一步说明,但所举实施例不作为对本发明的限定。下述各实施例中所述实验方法和检测方法,如无特殊说明,均为常规方法;所述试剂和材料,如无特殊说明,均可在市场上购买得到。
实施例1
一种苯并[a]蒽的工业化生产方法,具体包括以下步骤:
S1、向1L三口圆底烧瓶中依次加入四氢呋喃414mL、2,2,6,6-四甲基哌啶56.50g,搅拌下降温至-20℃-0℃,滴加正丁基锂200mL搅拌0.5h,降温至-80℃,加入硼酸三异丙脂75.23g,接着控温小于-70℃滴加2-溴萘的四氢呋喃溶液[其中含2-溴萘41.41g,四氢呋喃83mL],滴加完毕,自然升温至-55℃,保温-55~-45℃搅拌3h,升温至-20℃,加入盐酸酸化至pH=5,自然升至室温,减压浓缩至内温等于45℃,加入二氯乙烷1035mL稀释,水洗至pH=7,分相,有机相常压浓缩至体系剩余248mL,放入冰箱冷冻析晶3h,过滤,烘至恒重得淡黄色式(Ⅰ)固体27.59g,收率54.98%。LC-MS:calcd forC
其合成路线如下所示:
S2、向500mL三口圆底烧瓶中依次加入甲苯151mL、乙醇75ml、2-溴-3萘硼酸15.06g、碘苯14.69g、碳酸钾9.95g及水75ml,升温至40℃~50℃,加入四三苯基膦钯0.347g,继续升温至回流,反应1~2h,自然降温至室温,分液,甲苯相水洗至中性,浓缩剩余20ml,降温至90℃,加入甲基环己烷151ml,升温至回流,溶解清亮,自然降温至室温,过滤,烘料至恒重得白色式(Ⅱ)固体13.68g,收率80.52%。LC-MS:calcd forC
其合成路线如下所示:
S3、向250mL三口圆底烧瓶中依次加入四氢呋喃142mL、2-溴-3苯基萘14.16g,降温至-90℃~-80℃,加入正丁基锂32.5ml,-90℃~-80℃保温反应0.5h后,加入DMF 5.48g,-90℃~-80℃保温反应2h后,升温至-20℃,加入1ml水淬灭反应。自然升至室温,减压浓缩至内温等于50℃,加入甲基环己烷71ml,水洗至中性,甲基环己烷相常压浓缩至体系剩余30ml,自然降温至室温,过滤,烘料至恒重得白色式(Ⅲ)固体9.49g,收率81.74%。LC-MS:calcd forC
其合成路线如下所示:
S4、向500mL三口圆底烧瓶中依次加入四氢呋喃93mL、氯甲醚三苯基磷盐20.57g,降温至-10℃~0℃,加入叔丁醇钾6.74g(分3批次加入),-10℃~0℃保温反应2h后,滴加2-醛基-3苯基萘的四氢呋喃溶液[其中含2-醛基-3苯基萘9.29g,四氢呋喃46mL],-10℃~0℃保温反应1h后,加入1ml水淬灭反应,自然升至室温,加入甲苯93ml,甲苯相水洗至中性,常压浓缩至体系剩余20ml,自然降温至室温,过滤,烘料至恒重得白色式(Ⅳ)固体8.58g,收率82.38%。LC-MS:calcd forC
其合成路线如下所示:
S5、向250mL三口圆底烧瓶中依次加入甲苯86mL、2-甲氧基乙烯基-3-苯基萘8.58g,甲基磺酸7.69g,40℃~50℃保温反应2h后,加入水水洗至中性,甲苯相常压浓缩至剩余20ml,降温至70℃,加入乙醇86ml,升温至溶解清亮,降温至室温析晶,过滤,烘料至恒重得白色式(Ⅴ)固体6.70g,收率89.07%。如图1所示,LC-MS:calcd forC
其合成路线如下所示:
实施例2
一种苯并[a]蒽的工业化生产方法,具体包括以下步骤:
S1、向5L三口圆底烧瓶中依次加入四氢呋喃994mL、2,2,6,6-四甲基哌啶259.65g,搅拌下降温至-20℃-0℃,滴加正丁基锂750mL搅拌0.5h,降温至-80℃,加入硼酸三异丙脂338.53g,接着控温小于-70℃滴加2-溴萘的四氢呋喃溶液[其中含2-溴萘124.24g,四氢呋喃248mL],滴加完毕,自然升温至-55℃,保温-55~-45℃搅拌3h,升温至-20℃,加入盐酸酸化至pH=5,自然升至室温,减压浓缩至内温等于45℃,加入二氯乙烷2485mL稀释,水洗至pH=7,分相,有机相常压浓缩至体系剩余745mL,放入冰箱冷冻析晶3h,过滤,烘至恒重得淡黄色固体81.38g,收率54.06%。LC-MS:calcd forC
S2、向2000mL三口圆底烧瓶中依次加入甲苯755mL、乙醇375ml、2-溴-3萘硼酸75.30g、碘苯64.26g、碳酸钾49.75g及水375ml,升温至40℃~50℃,加入四三苯基膦钯1.733g,继续升温至回流,反应1~2h,自然降温至室温,分液,甲苯相水洗至中性,浓缩剩余100ml,降温至90℃,加入甲基环己烷755ml,升温至回流,溶解清亮,自然降温至室温,过滤,烘料至恒重得白色固体67.53g,收率79.49%。LC-MS:calcd forC
S3、向1000mL三口圆底烧瓶中依次加入四氢呋喃651mL、2-溴-3苯基萘65.13g,降温至-90℃~-80℃,加入正丁基锂126.5ml,-90℃~-80℃保温反应0.5h后,加入DMF21.83g,-90℃~-80℃保温反应2h后,升温至-20℃,加入5ml水淬灭反应。自然升至室温,减压浓缩至内温等于50℃,加入甲基环己烷500ml,水洗至中性,甲基环己烷相常压浓缩至体系剩余200ml,自然降温至室温,过滤,烘料至恒重得白色固体43.98g,收率82.33%。LC-MS:calcd forC
S4、向2000mL三口圆底烧瓶中依次加入四氢呋喃430mL、氯甲醚三苯基磷盐82.44g,降温至-10℃~0℃,加入叔丁醇钾26.99g(分3批次加入),-10℃~0℃保温反应2h后,滴加2-醛基-3苯基萘的四氢呋喃溶液[其中含2-醛基-3苯基萘42.97g,四氢呋喃213mL],-10℃~0℃保温反应1h后,加入1ml水淬灭反应,自然升至室温,加入甲苯430ml,甲苯相水洗至中性,常压浓缩至体系剩余85ml,自然降温至室温,过滤,烘料至恒重得白色固体40.51g,收率84.12%。LC-MS:calcd forC
S5、向250mL三口圆底烧瓶中依次加入甲苯391mL、2-甲氧基乙烯基-3-苯基萘39.05g,甲基磺酸21.62g,40℃~50℃保温反应2h后,加入水水洗至中性,甲苯相常压浓缩至剩余80ml,降温至70℃,加入乙醇391ml,升温至溶解清亮,降温至室温析晶,过滤,烘料至恒重得白色固体30.45g,收率88.92%。LC-MS:calcd forC
由上述实施例可得,本发明通过5步成功合成了苯并[a]蒽,每步反应采用的原料简单易得,价格低廉,反应后处理简单,没有产生大量废水,且收率高,适合工业化生产应用。
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内也意图包含这些改动和变型在内。
- 一种苯并a蒽的工业化生产方法
- 一种新的苯绕蒽酮的生产方法
