一种绿色荧光蛋白标记月季镰刀菌的制备方法及应用
文献发布时间:2023-06-19 11:34:14
技术领域
本发明属于植物病理学技术领域,具体涉及一种绿色荧光蛋白标记月季镰刀菌的制备方法及应用。
背景技术
月季枯萎病是由月季镰刀菌(Fusarium rosicola sp.nov.)引起的维管束系统性真菌病害,该菌可侵染月季根茎叶各个部位,病害症状前期叶片褪绿变黄,逐渐脱落,最后造成月季整株枯死。月季镰刀菌寄主范围广泛,可危害蔷薇科的月季、玫瑰、蔷薇和樱花等多种花卉。冬春日光温室及早春、秋后大棚栽培均有发生,且危害极其严重。要获得抗病品种,首先要了解月季镰刀菌的分子遗传基础和致病机制,目前国内外对于月季枯萎病的病原菌的鉴定,类群分析研究已取得了一些进展,但缺乏对月季镰刀菌致病机理的认识。
稳定表达绿色荧光蛋白标记月季镰刀菌对于研究月季镰刀菌致病相关基因、侵染过程和致病机理,对于研究月季镰刀菌侵染致病过程的组织学研究和月季镰刀菌致病相关基因、病原菌与寄主互作以及病原菌的功能基因组学研究奠定基础,同时,为月季枯萎病的控制和月季抗枯萎病抗病育种材料获得提供理论基础。然而,目前,国内外已有利用不同遗传转化方法转化绿色荧光蛋白标记(GFP)真菌的报道,但已报道的GFP标记真菌菌株方法或未涉及具体标记相关细节,或标记转化步骤繁琐,效率低下,荧光强度不稳定。目前还没有可参考的月季枯萎病病原菌月季镰刀菌GFP标记菌株及方法的报道,这已经成为月季枯萎病菌侵染致病过程与机理研究的瓶颈。因此,急需获得稳定表达绿色荧光蛋白标记月季镰刀菌及方法。
发明内容
本发明提供一种绿色荧光蛋白标记月季镰刀菌的制备方法及应用,以月季镰刀菌菌株YJ1为转化体,利用PEG介导原生质体的遗传转化方法将绿色荧光蛋白基因标记月季镰刀菌菌株YJ1,获得标记绿色荧光蛋白的月季镰刀菌菌株YJ1-GFP,可用于月季镰刀菌菌株突变体库的构建,筛选、寄主抗性定量鉴定、寄主对月季镰刀菌菌株侵染的响应机制及月季镰刀菌菌株侵染和致病机理研究。
本发明所使用的月季镰刀菌(Fusarium rosicolasp.nov.)YJ1,于2020年11月14日保藏于中国典型培养物保藏中心(CCTCC),保藏地址为中国.武汉.武汉大学,其保藏编号是CCTCC No:AF2020053
上述的月季镰刀菌(Fusarium rosicolasp.nov.)YJ1通过以下步骤筛选得到:
本实验于2020年6月在中国江苏省南京市浦口区发现了大面积的月季枯萎病,采集月季感病茎段,经过2-3天保湿培养,观察到大量的白色菌丝布满在茎段维管束内;用灭菌的接种针随机挑取白色菌丝接种到PDA培养基上,28℃培养,培养3天后,利用无菌挑针挑取菌落边缘部分接种至新的PDA平板上对菌株进行纯化,得到纯化菌株并编号为YJ1。经形态学描述和系统发育学分析,将其鉴定为新种并命名为Fusarium rosicolasp.nov.。
本发明的目的之一是提供一种绿色荧光蛋白标记月季镰刀菌的制备方法,包括以下步骤:
S1制备月季镰刀菌分生孢子液
月季镰刀菌为月季镰刀菌菌株YJ1,将月季镰刀菌YJ1在马铃薯固体培养基上培养4d后,使用无菌手术刀刮取30~40块规格为2×2mm的月季镰刀菌YJ1菌丝块,接种至CMC液体培养基中,置于暗室摇床上,250rmp、25℃摇72h,用两层滤膜过滤收集孢子于50mL离心管中,4000rpm,离心10min,弃废液,获得分生孢子液;
S2制备月季镰刀菌幼质体
用YEPD液体培养基将孢子浓度调至10
S3用幼质体制备原生质体
a、配置裂解液并800rpm离心2min,把上清液倒入步骤S2制备的幼质体中,置于暗室摇床,75rmp、30℃摇1.5h,用三层滤膜过滤到50mL离心管中,2000rpm,离心5min,弃上清液,获得原生质体;
b、加入20mL 0.7M NaCl洗涤,2000rpm,离心5min,弃上清;
c、加入20mL STC缓冲液洗涤,2000rpm,离心5min,弃上清;
d、用STC缓冲液将原生质体浓度调至10
S4将携带GFP的质粒转入月季镰刀菌的原生质体中
a、用移液枪吸取200μL原生质体到50mL离心管中,加入质粒15μL,再加入10μL肝素钠,于冰上静置30min;
b、加入1mL40%SPTC,吹打均匀后,室温静置20min;
c、加入50mLRM再生培养基,倒平板;
d、12h后50mL用RM覆盖培养基进行覆盖,其中RM覆盖培养基加终浓度为50μL0.1g/mL氨苄和50μL 70μg/mL博来霉素;
S5对标记有绿色荧光蛋白GFP的月季镰刀菌菌株进行鉴定。
待步骤S4中覆盖培养基上长出若干转化子后,从中随机挑取36个转化子,采用蔡司荧光显微镜观察转化子是否携带绿色荧光蛋白基因。
作为优选,步骤S1中所述CMC液体培养基:称取15g Carboxymethyl Cellulosesodium、1g NaNO
作为优选,步骤S2中所述YEPD液体培养基:称取0.3g Yeast extract、1g Peptone和2g Dextrose,ddH
作为优选,步骤S3中所述裂解液:称取0.05g Lysing enzyme、0.1g Driselase以及0.0005g Chetinase,用0.7M NaCl定容至10mL。
作为优选,步骤S3中所述STC缓冲液:称取145.74g Sorbitol、6.057g Tris和5.549g CaCl
作为优选,步骤S4中所述质粒为细胞核特异性表达质粒pYF11-GFP;
作为优选,步骤S4中所述40%SPTC:称取1.6g PEG4000,混合4mL STC组成。
作为优选,步骤S4中RM再生培养基:称取1g Casein enzymatic hydrolysate、342g D-Glucose、1g Yeast extract和15g Agar,ddH
作为优选,步骤S4中RM覆盖培养基:称取1g Casein enzymatic hydrolysate、342g D-Glucose、1g Yeast extract和10g Agarose,ddH
本发明的另一目的是提供如前述所述的一种绿色荧光蛋白标记月季镰刀菌的制备方法所制备的带有绿色荧光蛋白标记月季镰刀菌的应用。
与现有技术相比,本发明的有益效果是:
1、本发明提供的提供一种绿色荧光蛋白标记月季镰刀菌的制备方法,快速方便,步骤简化,耗时短,能直接在平板上挑取绿色荧光蛋白标记的月季镰刀菌菌株YJ1-GFP。
2、荧光稳定性强:在氨苄和博来霉素选择培养基上多代培养(>3代)均可获得绿色荧光强度稳定的标记月季镰刀菌菌株。
3、本发明所制得的绿色荧光蛋白标记月季镰刀菌可用于月季镰刀菌菌株突变体库的构建,筛选、寄主抗性定量鉴定、寄主对月季镰刀菌菌株侵染的响应机制及月季镰刀菌菌株侵染和致病机理研究。
附图说明
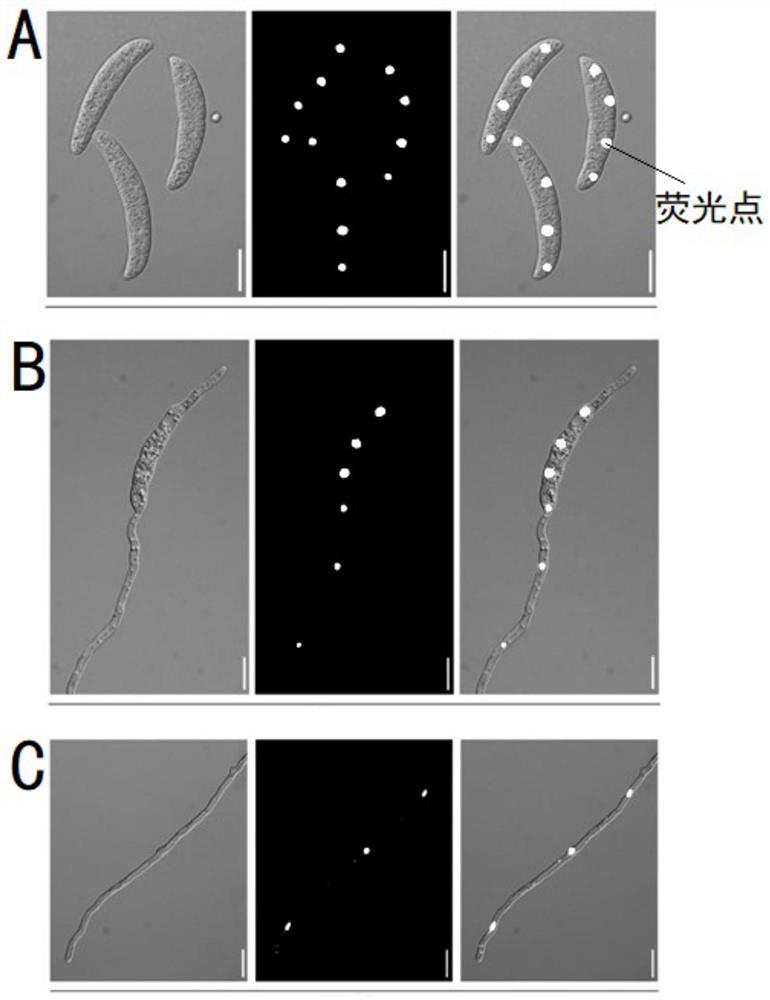
图1为绿色荧光蛋白标记月季镰刀菌菌株(YJ1-GFP)的荧光检测结果;
其中,A为带GFP标记的分生孢子状态白光、荧光和二者叠加电镜图;B为带GFP标记的孢子萌发状态白光、荧光和二者叠加电镜图;C为带GFP标记的菌丝状态白光、荧光和二者叠加电镜图,标尺为10微米。
具体实施方式
为了理解本发明,下面结合实施例对本发明作进一步说明。以下所述仅为本发明较好的实施例,仅仅用于描述本发明,不能理解为对本发明的范围的限制。应当指出的是,凡在本发明的精神和原则之内所做的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
本实验使用的Lysing enzyme、Driselase以及Chetinase均购于Sigma公司。
本发明所使用的月季镰刀菌(Fusarium rosicolasp.nov.)YJ1,于2020年11月14日保藏于中国典型培养物保藏中心(CCTCC),保藏地址为中国.武汉.武汉大学,其保藏编号是CCTCC No:AF2020053
上述的月季镰刀菌(Fusarium rosicolasp.nov.)YJ1通过以下步骤筛选得到:
本实验于2020年6月在中国江苏省南京市浦口区发现了大面积的月季枯萎病,采集月季感病茎段,经过2-3天保湿培养,观察到大量的白色菌丝布满在茎段维管束内;用灭菌的接种针随机挑取白色菌丝接种到PDA培养基上,28℃培养,培养3天后,利用无菌挑针挑取菌落边缘部分接种至新的PDA平板上对菌株进行纯化,得到纯化菌株并编号为YJ1。经形态学描述和系统发育学分析,将其鉴定为新种并命名为Fusarium rosicolasp.nov.。
本发明的目的是提供一种绿色荧光蛋白标记月季镰刀菌的制备方法,包括以下步骤:
S1制备月季镰刀菌分生孢子液
月季镰刀菌为月季镰刀菌菌株YJ1,将月季镰刀菌YJ1在马铃薯固体培养基上培养4d后,使用无菌手术刀刮取30~40块规格为2×2mm的月季镰刀菌YJ1菌丝块,接种至CMC液体培养基中,置于暗室摇床上,250rmp、25℃摇72h,用两层滤膜过滤收集孢子于50mL离心管中,4000rpm,离心10min,弃废液,获得分生孢子液;
所述CMC液体培养基:称取15g Carboxymethyl Cellulose sodium、1g NaNO
S2制备月季镰刀菌幼质体
用YEPD液体培养基将孢子浓度调至10
YEPD液体培养基:称取0.3g Yeast extract、1g Peptone和2g Dextrose,ddH
S3用幼质体制备原生质体
a、配置裂解液并800rpm离心2min,把上清液倒入步骤S2制备的幼质体中,置于暗室摇床,75rmp、30℃摇1.5h,用三层滤膜过滤到50mL离心管中,2000rpm,离心5min,弃上清液,获得原生质体;
b、加入20mL 0.7M NaCl洗涤,2000rpm,离心5min,弃上清;
c、加入20mL STC缓冲液洗涤,2000rpm,离心5min,弃上清;
d、用STC缓冲液将原生质体浓度调至10
裂解液:称取0.05g Lysing enzyme、0.1g Driselase以及0.0005g Chetinase,用0.7M NaCl定容至10mL。
STC缓冲液:称取145.74g Sorbitol、6.057g Tris和5.549g CaCl
S4将携带GFP的质粒转入月季镰刀菌的原生质体中
a、用移液枪吸取200μL原生质体到50mL离心管中,加入质粒15μL,再加入10μL肝素钠,于冰上静置30min;
b、加入1mL40%SPTC,吹打均匀后,室温静置20min;
c、加入50mLRM再生培养基,倒平板;
d、12h后50mL用RM覆盖培养基进行覆盖,其中RM覆盖培养基加终浓度为50μL0.1g/mL氨苄和50μL 70μg/mL博来霉素;
质粒为细胞核特异性表达质粒pYF11-GFP;
40%SPTC:称取1.6g PEG4000,混合4mL STC组成。
RM再生培养基:称取1g Casein enzymatic hydrolysate、342g D-Glucose、1gYeast extract和15g Agar,ddH
RM覆盖培养基:称取1g Casein enzymatic hydrolysate、342g D-Glucose、1gYeast extract和10g Agarose,ddH
S5对标记有绿色荧光蛋白GFP的月季镰刀菌菌株进行鉴定
待步骤S4中覆盖培养基上长出若干转化子后,从中随机挑取36个转化子,采用蔡司荧光显微镜观察转化子是否携带绿色荧光蛋白基因,鉴定结果如图1所示。
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专业的技术人员,在不脱离本发明技术方案范围内,当可利用上述揭示的技术内容做出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何的简单修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
- 一种绿色荧光蛋白标记月季镰刀菌的制备方法及应用
- 一种绿色荧光蛋白标记重组虹彩病毒的构建及其应用
