肝移植后巨细胞病毒的检测方法、应用及系统
文献发布时间:2023-06-19 11:42:32
技术领域
本发明涉及基因检测技术领域,具体涉及一种肝移植后巨细胞病毒的检测方法、应用及系统。
背景技术
肝移植是治疗各种终末期肝病的唯一有效办法。肝移植后的感染问题目前已成为影响患者长期存活的主要原因,发生率高达53%-80%。巨细胞病毒(CMV)是肝移植后较为常见的条件性致病病毒,而巨细胞病毒感染往往是导致并发症发生率和病死率升高的主要原因之一。接受免疫抑制剂治疗的移植患者发生巨细胞病毒感染的风险增加,在没有使用预防性抗病毒治疗的情况下,肝移植后患者巨细胞病毒的感染率为25%-85%,而其中有18%-29%的患者会发展为巨细胞病毒病。因此,尽早提高巨细胞病毒的检测发现,并应用于患者的诊断、预防和治疗过程中,可显著提高患者存活时间,并直接或间接减小其他感染的发生率。
目前临床上检测巨细胞病毒感染主要通过CMV抗体检查、pp65抗原检查及CMV DNA检查,具体检测方法包括ELISA、qPCR技术等。但CMV抗体检查、pp65抗原检查不能同时评估肝损伤的严重程度;上述检查方式也不能排除人体其他器官(如肺、肾)感染巨细胞病毒的情况;由于上述检测方法灵敏度低,从而容易导致误判断。
因此有必要提供一种新型的肝移植后巨细胞病毒的检测方法,以解决上述技术问题。
发明内容
本发明的主要目的是提供一种肝移植后巨细胞病毒的检测方法、应用及系统,以解决现有巨细胞病毒的检测方法灵敏度低的技术问题。
为实现上述目的,本发明提出的肝移植后巨细胞病毒的检测方法,包括以下步骤:
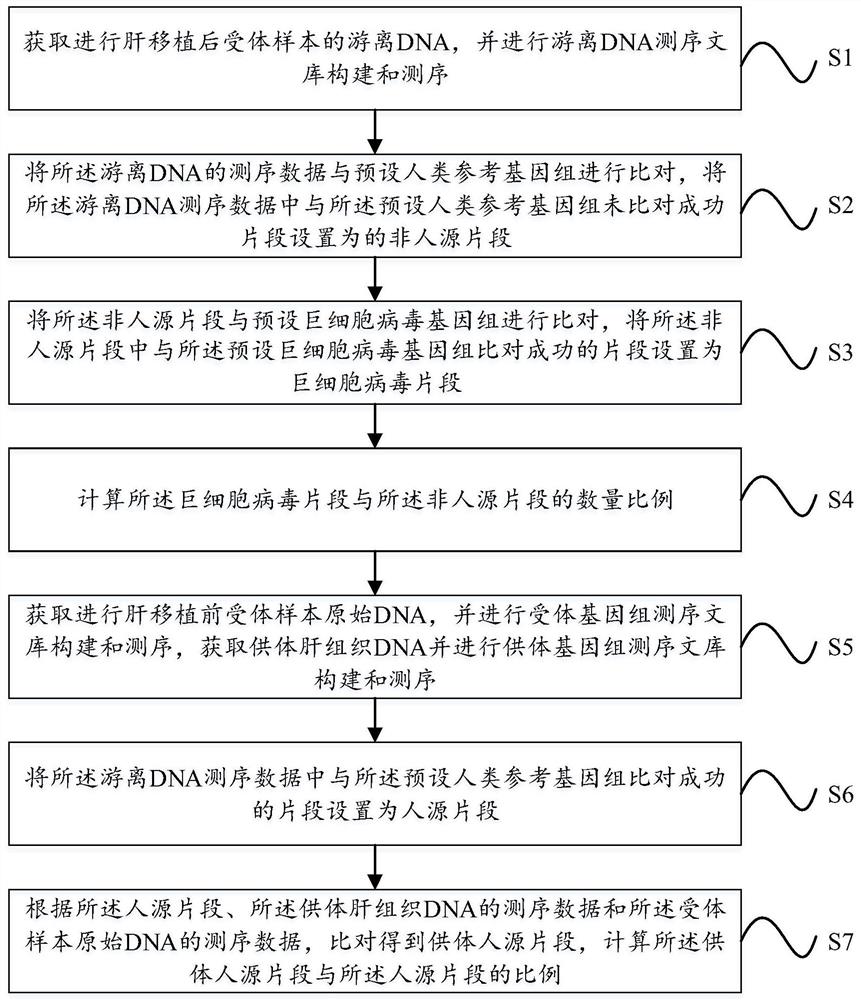
获取进行肝移植后受体样本的游离DNA,并进行游离DNA测序文库构建和测序;
将所述游离DNA的测序数据与预设人类参考基因组进行比对,将所述游离DNA测序数据中与所述预设人类参考基因组未比对成功片段设置为的非人源片段;
将所述非人源片段与预设巨细胞病毒基因组进行比对,将所述非人源片段中与所述预设巨细胞病毒基因组比对成功的片段设置为巨细胞病毒片段;
计算所述巨细胞病毒片段与所述非人源片段的数量比例。
优选地,所述检测方法还包括:
获取进行肝移植前受体样本原始DNA,并进行受体基因组测序文库构建和测序,获取供体肝组织DNA并进行供体基因组测序文库构建和测序;
将所述游离DNA测序数据中与所述预设人类参考基因组比对成功的片段设置为人源片段;
根据所述人源片段、所述供体肝组织DNA的测序数据和所述受体样本原始DNA的测序数据,比对得到供体人源片段,计算所述供体人源片段与所述人源片段的比例。
优选地,所述根据所述人源片段、所述供体肝组织DNA的测序数据和所述受体样本原始DNA的测序数据,比对得到供体人源片段,计算所述供体人源片段与所述人源片段的比例的步骤,包括:
将所述受体样本原始DNA测序数据、所述供体肝组织DNA测序数据分别与所述预设人类参考基因组进行比对,检测得到受体DNA变异位点和供体肝组织DNA变异位点;
比对所述受体样本变异位点中的纯合子和所述供体肝组织变异位点中的纯合子,将不相同的纯合子对应的位点设置为第一分析位点;
将所述人源片段与所述供体肝组织DNA测序数据对应所述第一分析位点的部分进行比对,将比对成功的所述人源片段设置为所述供体人源片段;
计算所述供体人源片段与所述人源片段比例。
优选地,所述第一分析位点为质量值大于30、测序深度大于8X的变异位点。
优选地,所述根据所述人源片段、所述供体肝组织DNA的测序数据和所述受体样本原始DNA的测序数据,比对得到供体人源片段,计算所述供体人源片段与所述人源片段的比例的步骤,包括:
将所述受体样本原始DNA进行SNP芯片检测,获得受体SNP变异信息,将所述供体肝组织DNA进行SNP芯片检测,获得供体SNP变异信息;
比对所述受体SNP变异信息中的纯合子和所述供体SNP变异信息中的纯合子,将不相同的纯合子所对应的位点设置为第二分析位点;
将所述人源片段与所述供体肝组织DNA测序数据对应所述第二分析位点的部分进行比对,生成所述供体人源片段;
计算所述供体人源片段与所述人源片段比例。
优选地,所述进行肝移植后,提取受体样本的游离DNA,并进行游离DNA测序文库构建和测序的步骤包括:
进行肝移植后,提取受体样本外周血的游离DNA,并进行游离DNA测序文库构建和测序。
本发明还提供了一种如前述的肝移植后巨细胞病毒的检测方法在制备巨细胞病毒的检测试剂盒中的应用。
本发明还提供了一种如前述的肝移植后巨细胞病毒的检测方法在评估肝细胞损伤上的应用。
本发明还提供了一种系统,包括处理器、存储器、通信器以及存储在所述存储器上的可被所述处理器执行的肝移植后巨细胞病毒的检测方法程序,其中,所述肝移植后巨细胞病毒的检测方法程序被所述处理器执行时,实现如前述的肝移植后巨细胞病毒的检测方法的步骤。
相较于现有技术中的qPCR检测及抗体检测方式,本发明提供的检测方法通过对受体游离DNA中的巨细胞病毒片段进行检测,更灵敏,可更早的在感染巨细胞病毒的患者体内检测出巨细胞病毒,尽早开展临床干预,从而可进一步提高患者存活率。
附图说明
图1为本发明肝移植后巨细胞病毒的检测方法一实施例的流程示意图;
图2为本发明肝移植后巨细胞病毒的检测方法另一实施例的流程示意图;
图3为本发明肝移植后巨细胞病毒的检测方法又一实施例的流程示意图;
图4为采用本发明提供的肝移植后巨细胞病毒的检测方法和常规qPCR检测方法的CMV感染量曲线图;
图5为采用本发明提供的肝移植后巨细胞病毒的检测方法和常规qPCR检测方法的检测结果曲线拟合图;
图6为采用本发明提供的肝移植后巨细胞病毒的检测方法的供体人源片段含量曲线图;
图7为采用本发明提供的肝移植后巨细胞病毒的检测方法的ROC曲线。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
另外,本发明各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本发明要求的保护范围之内。
除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等均可通过市场购买得到或者可通过现有方法制备得到。
请参阅图1,本发明提出一种肝移植后巨细胞病毒的检测方法,包括以下步骤:
步骤S1,获取进行肝移植后受体样本的游离DNA,并进行游离DNA测序文库构建和测序;
游离DNA(cell free DNA,cfDNA)是指存在于血液、尿液、唾液等各种体液及分泌物中的细胞外的DNA,通常在组织细胞的凋亡和坏死时释放。通过检测游离DNA,可以获得深部病灶或器官、胎儿等的遗传信息。当然广义上的游离DNA也包括病毒、细菌等病原体的DNA,通过检测游离DNA,可以获取人类体内病原体感染的情况。
受体为接收肝移植的患者。本领域技术人员可以根据实际情况,自行选择合适的提取方法提取受体样本的游离DNA。在本实施例中,采用EDTA采血管采集肝移植术后患者的外周血10ml,在2小时内进行血浆分离,以去除血细胞;取2ml血浆,采用血浆游离DNA提取试剂盒(55114,QIAamp Circulating Nucleic Acid Kit,Qiagen,Germany),提取血浆中的游离DNA。由于游离DNA本身为碎片化的DNA,在本实施例中,无须对游离DNA进行打断,直接采用常规的二代测序文库构建方法构建测序文库,选用Hiseq X平台,PE150的测序模式,测序得到至少5G的测序数据。在测序数据中包括多个read。
步骤S2,将所述游离DNA的测序数据与预设人类参考基因组进行比对,将所述游离DNA测序数据中与所述预设人类参考基因组未比对成功片段设置为的非人源片段;
参考基因组为该物种的基因组序列,是已经组装成的完整基因组序列,常作为该物种的标准参照物。预设人类参考基因组为本领域技术人员预先设置的人类基因组。将所述游离DNA测序数据与预设人类参考基因组进行比对,所述游离DNA测序数据中与预设人类参考基因组比对成功的片段,即证明该片段为来自人类基因;所述游离DNA测序数据中与预设人类参考基因组未比对成功的片段,即证明该片段为非人源片段,具体可以是巨细胞病毒,或其它病毒、细菌等病原体的DNA。
步骤S3,将所述非人源片段与预设巨细胞病毒基因组进行比对,将所述非人源片段中与所述预设巨细胞病毒基因组比对成功的片段设置为巨细胞病毒片段;
预设巨细胞病毒基因组为本领域技术人员预先设置的巨细胞病毒基因组。所述非人源片段中与预设巨细胞病毒基因组比对成功的片段,即为巨细胞病毒片段,若比对成功,则证明该受体患者已感染巨细胞病毒。
步骤S4,计算所述巨细胞病毒片段与所述非人源片段的数量比例。
具体地,计算所述巨细胞病毒片段的reads与所述非人源片段的reads数量比例,该比例可反映受体体内的巨细胞病毒的载量,即受体体内巨细胞病毒感染量。
相较于现有技术中的qPCR检测及抗体检测方式,本发明提供的检测方法通过对受体游离DNA中的巨细胞病毒片段进行检测,更灵敏,可更早的在感染巨细胞病毒的患者体内检测出巨细胞病毒,尽早开展临床干预,从而可进一步提高患者存活率。
进一步地,所述肝移植后巨细胞病毒的检测方法,还包括以下步骤:
步骤S5,获取进行肝移植前受体样本原始DNA,并进行受体基因组测序文库构建和测序,获取供体肝组织DNA并进行供体基因组测序文库构建和测序;
具体地,受体样本原始DNA为受体在接受肝移植之前的DNA。提取受体样本原始DNA的方式本发明不做限制,在本实施例中通过采集受体5ml外周血,采用常规苯酚氯仿提取法提取外周血中的DNA,该外周血中的DNA为受体样本原始DNA。本领域技术人员可以根据实际情况选择合适的基因组测序文库构建和测序方法,在本实施例中,采用取1ug受体样本原始DNA进行Covaris打断、Ampure beads回收及常规的二代测序文库构建,选用Hiseq X平台,设置PE150模式(序列两端各测150bp),测序得到各10G~20G的测序数据。
供体为提供移植肝源的捐献者。提取供体肝组织DNA的方式本发明不做限制,在本实施例中,进行肝移植前修整移植供肝时,留取黄豆大小的供肝组织一块,用研磨器匀浆后,采用常规苯酚氯仿提取法提取其中的DNA,该供肝组织中的DNA为供体肝组织DNA。本领域技术人员可以根据实际情况选择合适的基因组测序文库构建和测序方法,在本实施例中,采用与受体样本原始DNA相似方法。
步骤S6,将所述游离DNA测序数据中与所述预设人类参考基因组比对成功的片段设置为人源片段。
步骤S7,根据所述人源片段、所述供体肝组织DNA的测序数据和所述受体样本原始DNA的测序数据,比对得到供体人源片段,计算所述供体人源片段与所述人源片段的比例。
请参阅图2,在一实施例中,步骤S7具体为:
步骤S71,将所述受体样本原始DNA的测序数据、所述供体肝组织DNA的测序数据分别与所述预设人类参考基因组进行比对,检测得到受体DNA变异位点和供体肝组织DNA变异位点;
通过与预设人类参考基因组进行比对,可识别出受体和供体中变异的位点,以用于区别不同个体。
步骤S72,比对所述受体样本变异位点中的纯合子和所述供体肝组织变异位点中的纯合子,将不相同的纯合子对应的位点设置为第一分析位点;
纯合子又称纯合体,指同源染色体在同一基因座上的两个等位基因相同的基因型个体,与杂合子相对。不相同的第一纯合子位点即受体和供体中不相同的等位基因。例如:受体的一等位基因为AA,供体中与该等位基因相对应的为aa,即AA为纯合子,aa为纯合子,该AA和aa为不相同的纯合子。在步骤S62中可以设置多个第一分析位点。优选地,所述第一分析位点为质量值大于30、测序深度大于8X的变异位点。测序深度为测序得到的碱基总量(bp)与基因组大小(Genome)的比值。当然本领域技术人员也可以根据实际需要自行设置,以选择得到合适的第一分析位点。
步骤S73,将所述人源片段与所述供体肝组织DNA测序数据对应所述第一分析位点的部分进行比对,将比对成功的所述人源片段设置为所述供体人源片段;
具体地,通过变异检测软件分析所述人源片段在步骤S72中确定的第一分析位点上各个基因型的频率。其中与所述供体肝组织DNA测序数据一致的即可认为该人源片段来自于供体肝组织。
步骤S74,计算所述供体人源片段与所述人源片段比例;
通过计算来自供体肝组织DNA在所述人源片段的比例,即可反映移植后肝组织细胞损伤、死亡的情况。
请参阅图3,在另一实施例中,步骤S7具体为:
步骤S75,将所述受体样本原始DNA进行SNP芯片检测,获得受体SNP变异信息,将所述供体肝组织DNA进行SNP芯片检测,获得供体SNP变异信息;
SNP(Single Nucleotide Polymorphism)是指在基因组上单个核苷酸的变异,包括转换、颠换、缺失和插入,形成的遗传标记。在本实施例中通过1ug受体样本原始DNA进行SNP芯片检测,获得受体SNP变异信息。
步骤S76,比对所述受体SNP变异信息中的纯合子和所述供体SNP变异信息中的纯合子,将不相同的纯合子所述对应的位点设置为第二分析位点;
本领域技术人员可以自行设置第二分析位点的质量值。
步骤S77,将所述人源片段与所述供体肝组织DNA测序数据对应所述第二分析位点的部分进行比对,将比对成功的所述人源片段设置为生成所述供体人源片段;
步骤S78,计算所述供体人源片段与所述人源片段比例。
通过计算来自供体肝组织DNA在所述人源片段的比例,即可反映移植后肝组织细胞损伤、死亡的情况。
以下通过具体实施例对本发明提出的肝移植后巨细胞病毒的检测方法有效效果进行说明:
对4例接受肝移植术的患者进行巨细胞病毒检测。针对4患者同时采用本发明提供的检测方法以及常规qPCR检测。请参阅图4,为采用本发明提供的肝移植后巨细胞病毒的检测方法和常规qPCR检测方法的CMV感染量曲线图,其中A、B、C和D分别为4例接收肝移植术的患者采用本发明提供的检测方法得到的CMV感染量检测结果和qPCR的检测结果,横坐标为患者接收肝移植术的天数,纵坐标分别为巨细胞病毒片段与非人源片段的数量比例,以及qPCR定量数值。虚线为本实施例判定CMV阳性的阈值。由图4可知,在qPCR显示阳性之前,本发明提供的检测方法即可通过计算巨细胞病毒片段与非人源片段的数量比例检测出CMVDNA比例的增高,以证明相较于常规qPCR检测方法,本发明提供的检测方法灵敏性更高,可提早检出CMV感染。
请结合参阅图5,为采用本发明提供的肝移植后巨细胞病毒的检测方法和常规qPCR检测方法的曲线拟合图。图中展示了上述4例患者所有采样点的检测结果,其中横坐标为qPCR检测结果的log10变换值,纵坐标为同一样本用本发明提供方法的检测值。若患者该次qPCR检测结果为阴性的点则不标注。由图5可见,qPCR结果与本发明提供的测序分析方法结果的拟合较好,说明本方法能较好地定量患者体内的病毒载量。
请结合参阅图6,为采用本发明提供的肝移植后巨细胞病毒的检测方法的供体人源片段曲线图,横坐标为患者接受肝移植术的天数,纵坐标为供体人源片段与人源片段的百分比。由于手术过程不可避免的导致一定的肝损伤,可见肝移植后早期供体人源片段比例较高,随着时间延长逐渐降低。实验中发现,肝移植术后期患者CMV DNA比例升高时其供体人源片段比例也升高,即巨细胞病毒片段与供体人源片段呈正相关。
请结合参阅图7,为采用本发明提供的肝移植后巨细胞病毒的检测方法的ROC曲线。以常规qPCR检测方法的检测结果作为判断是否CMV阳性,对本方法检测CMV感染的性能做ROC曲线分析如下图,其曲线下面积(AUC)为0.97。
本发明还提供了一种如前述的肝移植后巨细胞病毒的检测方法在制备巨细胞病毒的检测试剂盒中的应用。
采用肝移植后巨细胞病毒的检测方法,将其中所需试剂制成巨细胞病毒的检测试剂盒。其中肝移植后巨细胞病毒的检测方法在制备巨细胞病毒的检测试剂盒中的应用可参照本发明肝移植后巨细胞病毒的检测方法的各个实施例,此处不再赘述。
本发明还提供了一种如前述的肝移植后巨细胞病毒的检测方法在评估肝细胞损伤上的应用。
其中肝移植后巨细胞病毒的检测方法在评估肝细胞损伤上的应用可参照本发明肝移植后巨细胞病毒的检测方法的各个实施例,此处不再赘述。
通过计算所述巨细胞病毒片段与所述非人源片段的数量比例可知晓被试患者是否感染巨细胞病毒,可间接评估肝细胞损伤;通过计算所述供体人源片段与所述人源片段的比例,可直接评估肝细胞损伤。
本发明还提供了一种系统,包括处理器、存储器、通信器以及存储在所述存储器上的可被所述处理器执行的肝移植后巨细胞病毒的检测方法程序,其中,所述肝移植后巨细胞病毒的检测方法程序被所述处理器执行时,实现如前述的肝移植后巨细胞病毒的检测方法的步骤。
本发明实施例中,系统可以包括处理器(例如CPU),通信总线,用户接口,网络接口,存储器。其中,通信总线用于实现这些组件之间的连接通信;用户接口可以包括显示屏(Display)、输入单元比如键盘(Keyboard);网络接口可选的可以包括标准的有线接口、无线接口(如WI-FI接口);存储器可以是高速RAM存储器,也可以是稳定的存储器(non-volatile memory),例如磁盘存储器,存储器可选的还可以是独立于前述处理器1001的存储装置。
本领域技术人员可以理解,上述硬件结构并不构成对系统的限定,可以包括更多或更少的部件,或者组合某些部件,或者不同的部件布置。
其中肝移植后巨细胞病毒的检测方法程序被执行时所实现的方法可参照本发明肝移植后巨细胞病毒的检测方法的各个实施例,此处不再赘述。
以上所述仅为本发明的优选实施例,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
- 肝移植后巨细胞病毒的检测方法、应用及系统
- 哺乳动物细胞受到人巨细胞病毒(HCMV)感染后释放的包含融合蛋白的病毒颗粒及其应用
