一种用于检测游离脂肪酸的试剂盒
文献发布时间:2023-06-19 11:52:33
技术领域
本发明涉及体外诊断领域,具体涉及一种用于检测游离脂肪酸的试剂盒。
背景技术
游离脂肪酸(NEFA)是存在于人体内的脂质,脂质大致可以分为胆固醇、中性脂肪(三酸甘油脂)、磷脂质等3种。游离脂肪酸是中性脂肪分解成的物质。主要与血清蛋白结合转运到全身组织利用,当肌肉活动所需能源--肝糖耗尽时,脂肪组织会分解中性脂肪成为游离脂肪酸来充当能源使用。所以,游离脂肪酸可说是进行持久活动所需的物质。
正常情况下,血浆中游离脂肪酸的含量极少,仅占总脂肪酸含量的5%~10%,游离脂肪酸在血浆中的半衰期2~3min,虽然游离脂肪酸只占身体脂肪很少的一部分,但却满足了能量需求的很大部分,游离脂肪酸有很强的细胞毒性,可损害细胞膜、线粒体和溶酶体膜等,引起细胞内微器损害,而且能增强细胞因子毒性。故而是监控人体脂代谢、糖代谢的重要指标。游离脂肪酸不仅能够反映人体脂肪代谢情况及血脂水平、评价血糖及辅助诊断糖尿病,还能反映人体内多种其他病理、生理情况,如胰岛素抵抗、肥胖、恶性疾病、代谢综合征和心血管疾病等。
目前临床上对人体血清游离脂肪酸的检测主要是通过游离脂肪酸检测试剂盒来检测,而市场上售卖的游离脂肪酸检测试剂盒通常使用的是酶法测定,一方面,酶法试剂盒成分比较复杂,试剂中含有多种酶,其试剂盒稳定性直接与酶活性相关,而酶的活性易受各种因素的干扰,比如pH、温度、紫外线、重金属盐、抑制剂、激活剂等,导致试剂盒缺乏稳定性,即使加入多种稳定剂,试剂的稳定剂仍然很差,保存时间短,影响临床使用。另一方面,酶法试剂盒灵敏度较低,为了加大试剂灵敏度往往会考虑加大酶的使用量,但是酶量加大会使试粘稠,剂产生沉淀,影响试剂的使用。因此研发一种稳定好、灵敏度高的游离脂肪酸测定试剂盒是游离脂肪酸测定领域亟需解决的一个问题。
发明内容
本发明所要解决的技术问题是:针对现有技术存在的不足,提供一种用于检测游离脂肪酸的试剂盒,该试剂盒灵敏度高、准确度高、稳定性好。
为解决上述技术问题,本发明的技术方案是:
一种用于检测游离脂肪酸的试剂盒,所述试剂盒包括:
试剂R1,所述试剂R1包括第一缓冲液、生物素标记的抗人NEFA抗体、FITC标记的抗人NEFA抗体、第一稳定剂、第一防腐剂、糖类化合物、第一表面活性剂;
试剂R2,所述试剂R2包括第二缓冲液、链霉亲和素修饰胶乳微球、Anti-FITC修饰胶乳微球、第二稳定剂、螯合剂、第二防腐剂、第二表面活性剂、增溶剂、促聚剂;
校准品,所述校准品包括包括第三缓冲液、NEFA-重组蛋白、第三稳定剂以及第三防腐剂。
作为一种改进的技术方案,所述生物素标记的抗人NEFA抗体的浓度为100-200μg/ml、所述FITC标记的抗人NEFA抗体的浓度为50-100μg/ml。
作为一种改进的技术方案,所述链霉亲和素(SA)修饰胶乳微球的浓度为0.07-0.5mg/L,所述Anti-FITC修饰胶乳微球的浓度为0.07-0.5mg/L。
作为一种改进的技术方案,所述第一缓冲液、第二缓冲液或第三缓冲液为磷酸盐缓冲液、TRIS缓冲液、Hepes缓冲液或Mes缓冲液;所述第一缓冲液、第二缓冲液或第三缓冲液的浓度为20-50mM。
作为一种改进的技术方案,所述第一稳定剂、第二稳定剂以及第三稳定剂分别为抗坏血栓氧化酶、牛血清白蛋白、甘油、乙二醇、山梨醇、甘氨酸、吐温20、聚氧乙烯-8-辛基苯基醚、明胶中的一种或多种;所述第一稳定剂、第二稳定剂或第三稳定剂的浓度为0.01-10%w/v。
作为一种改进的技术方案,所述第一表面活性剂或第二表面活性剂为乙基苯基聚乙二醇(NP40)、吐温40、吐温80、十二烷基硫酸钠(SDS)、山梨醇酐单硬脂酸(S-40)、山梨醇酐单硬脂酸(S-60)、聚乙二醇对异辛基苯基醚-100、十二烷基羟丙基磷酸酯甜菜碱中的一种或多种,所述第一表面活性剂和第二表面活性剂的浓度为0.1-3.5%w/v。
作为一种改进的技术方案,所述糖类化合物为乳糖、蔗糖、葡萄糖、麦芽糖、海藻糖、甘露醇的一种或多种,所述糖类化合物浓度为0.2-5%w/v;所述增溶剂为聚氧乙烯多环苯醚,其浓度为0.5-3.2%w/v;所述螯合剂为EDTA、乙二胺、草酸、山梨糖醇中的一种或多种,所述螯合剂的浓度为0.05-2.5%w/v;所述促聚剂为聚乙二醇-6000、聚乙二醇-8000、聚乙二醇-10000、聚乙二醇-20000中的一种或多种,所述促聚剂的浓度为0.5-4%w/v。
作为一种改进的技术方案,所述第一防腐剂、第二防腐剂或第三防腐剂为叠氮钠、硫柳汞、Proclin-300中的一种或多种,所述第一防腐剂、第二防腐剂或第三防腐剂的浓度为0.05-2.8%w/v。
采用了上述技术方案后,本发明的有益效果是:
(1)本发明引入了SA-生物素-抗体-抗原-抗体-FITC双重级联放大系统,由于SA结合生物素很易与蛋白质(如抗体等)以共价键结合,结合了胶乳微球的亲和素分子与结合有特异性抗体的生物素分子产生反应,其中一个抗体可以和多个生物素结合,一个生物素分子又可以和四个链霉亲和素分子结合,起到了多级放大作用,达到检测未知抗原(或抗体)分子的目的。FITC能很好的与各种抗体结合,不影响结合后的抗体与抗原结合的特异性,这样结合胶乳微球的anti-FITC能更好的与结合抗体的FITC特异的反应,检测时抗原(抗体)与SA-生物素-抗体、抗体-FITC-anti-FITC反应,反应复合物进一步增大,进一步起到多级放大系统的作用,提高试剂的灵敏度;
(2)本发明中用于检测游离脂肪酸(NEFA)的诊断试剂盒,应用免疫增强比浊法对NEFA进行检测,克服了传统的酶法检测NEFA的缺点,避免了试剂、环境等因素的影响,稳定性较好。
附图说明
图1为本发明试剂盒的标准曲线图;
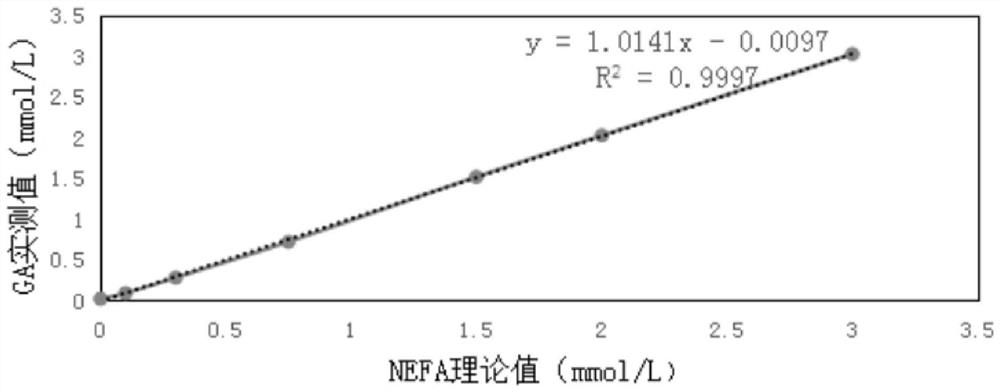
图2为本发明试剂盒的线性关系图;
图3为本发明实施例4与进口试剂测定结果的对照分析图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,结合以下实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例1
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为6.5,其配方组分如下:
第一缓冲液(磷酸盐缓冲液,50mM)、生物素偶联的人NEFA抗体(100μg/ml)、FITC标记的人NEFA抗体(50μg/ml)、第一稳定剂(0.1%w/v的山梨醇)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(1%w/v的蔗糖)以及第一表面活性剂(0.8%w/v的乙基苯基聚乙二醇);
试剂R2的pH为7.5,其配方组分如下:
第二缓冲液(磷酸盐缓冲液,50mM)、链霉亲和素修饰胶乳微球(0.1mg/ml)、Anti-FITC修饰胶乳微球(0.1mg/ml)、第二稳定剂(0.1%w/v牛血清白蛋白)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1%w/v的十二烷基硫酸钠)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(0.1%w/v的聚乙二醇-4000);
校准品的pH为7.5,其配方组分如下:
第三缓冲液(磷酸盐缓冲液,50mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例2
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为6.5,其配方组分如下:
第一缓冲液(HEPES缓冲液,20mM)、生物素偶联的人NEFA抗体(100μg/ml)、FITC标记的人NEFA抗体(50μg/ml)、第一稳定剂(0.1%w/v的山梨醇)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(2%w/v的海藻糖)以及第一表面活性剂(0.8%w/v的山梨醇酐单硬脂酸);
试剂R2的pH为7.5,其配方组分如下:
第二缓冲液(HEPES缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.1mg/ml)、Anti-FITC修饰胶乳微球(0.1mg/ml)、第二稳定剂(0.1%w/v聚氧乙烯-8-辛基苯基醚)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1%w/v的聚乙二醇对异辛基苯基醚-100)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(0.1%w/v的聚乙二醇-4000);
校准品的pH为7.5,其配方组分如下:
第三缓冲液(HEPES缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例3
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为6.5,其配方组分如下:
第一缓冲液(Mes缓冲液,20mM)、生物素偶联的人NEFA抗体(100μg/ml)、FITC标记的人NEFA抗体(50μg/ml)、第一稳定剂(0.1%w/v的山梨醇)、第一防腐剂(0.9%w/v的Proclin-300)、糖类化合物(1%w/v的麦芽糖)以及第一表面活性剂(1%w/v的吐温80);
试剂R2的pH为6.5,其配方组分如下:
第二缓冲液(Mes缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.1mg/ml)、Anti-FITC修饰胶乳微球(0.1mg/ml)、第二稳定剂(1%w/v甘油)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1%w/v的十二烷基硫酸钠)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(0.1%w/v的聚乙二醇-4000);
校准品的pH为6.5,其配方组分如下:
第三缓冲液(Mes缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例4
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为8.0,其配方组分如下:
第一缓冲液(Tris缓冲液,20mM)、生物素偶联的人NEFA抗体(100μg/ml)、FITC标记的人NEFA抗体(50μg/ml)、第一稳定剂(1.5%w/v的甘氨酸)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(1%w/v的甘露醇)以及第一表面活性剂(1.8%w/v的聚乙二醇辛基苯基醚-100);
FITC标记抗人H-FABP抗体:取抗人人NEFA抗体(鼠抗人、兔抗人、羊抗人或者牛抗人NEFA抗体)适量加入Tris缓冲液搅拌混匀,得到抗体浓度为20mg/ml的溶液;按照每1毫克抗体加入0.01毫克的量将FITC加入抗体溶液中,4℃条件下避光搅拌12h进行第一次透析,按照2500r/min离心转速离心20min(除去其中少量的沉淀物),将上清液装入透析袋中用pH8.0缓冲盐水在0~4℃的条件下进行二次透析过夜,取透析过夜后的标记物通过葡聚糖凝胶SephadexG-25或G—50柱,经过分离收集FITC标记抗人NEFA抗体。
生物素标记抗人NEFA抗体:将抗人NEFA抗体用0.1mol/L缓冲液(pH8.0)稀释到1mg/ml,向1ml抗体溶液中(即含抗体1mg)加入120μl,浓度为1mg/ml的NHSB溶液,搅拌保温2-4h,再加入9.6μL1mol/L NH
生物素标记的抗人NEFA抗体和FITC标记的抗人NEFA抗体按照1-3:1的比例混合均匀,加入相应量的稳定剂、防腐剂、糖类、表面活性剂制成试剂R1;
试剂R2的pH为8.0,其配方组分如下:
第二缓冲液(Tris缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.1mg/ml)、Anti-FITC修饰胶乳微球(0.1mg/ml)、第二稳定剂(1.5%w/v牛血清白蛋白)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1.5%w/v的吐温40)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(0.1%w/v的聚乙二醇-4000);
链霉亲和素修饰胶乳微球:反应缓冲液(Tris缓冲液)稀释SA至10mg/ml,反应缓冲液稀释胶乳微球至10mg/ml,按照每10ml胶乳微球溶液加入1mlSA溶液的量将SA加入胶乳微球溶液中,室温搅拌孵育2h,离心/超滤,除去上清液(除去未结合SA),得到SA修饰胶乳微球用Tris缓冲液作为储存液进行储存,再经过稀释得到所需要的SA修饰胶乳微球的浓度。
Anti-FITC修饰胶乳微球:反应缓冲液(Tris缓冲液)稀释Anti-FITC至10mg/ml,反应缓冲液稀释胶乳微球至1%,将FITC抗体加入胶乳微球溶液种,按照每10ml胶乳微球溶液加入1mlAnti-FITC溶液的量将Anti-FITC溶液加入胶乳微球溶液中,室温搅拌孵育2h,离心/超滤,除去未结合FITC抗体,得到Anti-FITC修饰胶乳微球,再经过稀释得到所需要的Anti-FITC修饰胶乳微球的浓度。
SA修饰胶乳微球和Anti-FITC修饰胶乳微球按照2-3:1的比例混合均匀,加入相应量的稳定剂、盐离子化合物、螯合剂、防腐剂制成试剂R2。
校准品的pH为8.0,其配方组分如下:
第三缓冲液(Tris缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例5
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为8.0,其配方组分如下:
第一缓冲液(Tris缓冲液,30mM)、生物素偶联的人NEFA抗体(120μg/ml)、FITC标记的人NEFA抗体(65μg/ml)、第一稳定剂(1.5%w/v的甘油、2%w/v乙二醇和3%w/v山梨醇)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(1%w/v的甘露醇和2%w/v的海藻糖)以及第一表面活性剂(1%w/v的吐温80、0.5%w/v的吐温20和0.5%w/v的吐温40);
试剂R2的pH为8.0,其配方组分如下:
第二缓冲液(Tris缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.2mg/ml)、Anti-FITC修饰胶乳微球(0.2mg/ml)、第二稳定剂(1.5%w/v牛血清白蛋白)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1.5%w/v的吐温40)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(0.5%w/v的聚乙二醇-4000和0.5%w/v的聚乙二醇-6000);
校准品的pH为8.0,其配方组分如下:
第三缓冲液(Tris缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例6
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为7.5,其配方组分如下:
第一缓冲液(Tris缓冲液,30mM)、生物素偶联的人NEFA抗体(150μg/ml)、FITC标记的人NEFA抗体(75μg/ml)、第一稳定剂(2%w/v的甘油、2%w/v乙二醇和3%w/v甘氨酸)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(1%w/v的甘露醇、2%w/v的海藻糖0.5%w/v的乳糖)以及第一表面活性剂(1%w/v的吐温80、0.5%w/v的吐温20和0.5%w/v的吐温40);
试剂R2的pH为7.5,其配方组分如下:
第二缓冲液(Tris缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.2mg/ml)、Anti-FITC修饰胶乳微球(0.2mg/ml)、第二稳定剂(1.5%w/v牛血清白蛋白)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1.5%w/v的吐温40)、增溶剂(聚氧乙烯多环苯醚,其浓度为1%w/v)以及促聚剂(1%w/v的聚乙二醇-6000和2%w/v的聚乙二醇-10000);
校准品的pH为7.5,其配方组分如下:
第三缓冲液(Tris缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例7
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为7.5,其配方组分如下:
第一缓冲液(Tris缓冲液,30mM)、生物素偶联的人NEFA抗体(180μg/ml)、FITC标记的人NEFA抗体(85μg/ml)、第一稳定剂(2%w/v的甘油、2%w/v乙二醇和3%w/v甘氨酸)、第一防腐剂(0.9%w/v的叠氮钠)、糖类化合物(1%w/v的甘露醇、2%w/v的海藻糖1.5%w/v的乳糖)以及第一表面活性剂(1%w/v的十二烷基硫酸钠和2%w/v的山梨醇酐单硬脂酸);
试剂R2的pH为7.5,其配方组分如下:
第二缓冲液(Tris缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.3mg/ml)、Anti-FITC修饰胶乳微球(0.3mg/ml)、第二稳定剂(2.5%w/v山梨醇、2.5%w/v甘氨酸和2%w/v明胶)、螯合剂(1mM的EDTA)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1.5%w/v的吐温40)、增溶剂(聚氧乙烯多环苯醚,其浓度为2%w/v)以及促聚剂(1%w/v的聚乙二醇-6000和2%w/v的聚乙二醇-20000);
校准品的pH为7.5,其配方组分如下:
第三缓冲液(Tris缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
实施例8
一种用于检测游离脂肪酸的试剂盒包括试剂R1和试剂R2,其中试剂R1与试剂R2的比例为2-4:1。
试剂R2的pH为7.5,其配方组分如下:
第一缓冲液(Tris缓冲液,40mM)、生物素偶联的人NEFA抗体(200μg/ml)、FITC标记的人NEFA抗体(100μg/ml)、第一稳定剂(2%w/v的山梨醇、2%w/v乙二醇和3%w/v甘氨酸)、第一防腐剂(2%w/v的叠氮钠)、糖类化合物(1%w/v的甘露醇、2%w/v的海藻糖2%w/v的麦芽糖)以及第一表面活性剂(1%w/v的吐温80、0.5%w/v的吐温20和1.5%w/v的乙基苯基聚乙二醇);
试剂R2的pH为7.5,其配方组分如下:
第二缓冲液(Tris缓冲液,20mM)、链霉亲和素修饰胶乳微球(0.5mg/ml)、Anti-FITC修饰胶乳微球(0.5mg/ml)、第二稳定剂(1.5%w/v牛血清白蛋白)、螯合剂(1.5%w/v乙二胺和0.5%w/v山梨糖醇)、第二防腐剂(0.9%w/v的叠氮钠)、第二表面活性剂(1.5%w/v的吐温40)、增溶剂(聚氧乙烯多环苯醚,其浓度为3%w/v)以及促聚剂(1%w/v的聚乙二醇-20000和2%w/v的聚乙二醇-10000);
校准品的pH为7.5,其配方组分如下:
第三缓冲液(Tris缓冲液,20mM)、NEFA-重组蛋白(浓度梯度为3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L)、第三稳定剂(0.3%w/v的牛血清白蛋白)以及第三防腐剂(0.9%w/v的叠氮钠)。
需要说明的一点是本发明实施例1-3以及5-8中生物素偶联的人NEFA抗体、FITC标记的人NEFA抗体、链霉亲和素修饰胶乳微球、Anti-FITC修饰胶乳微球的具体操作与实施例4中操作基本相同,故省略描述。
为了更好的证明本发明的试剂盒具有较好的性能,进行了以下考察。
1.试剂校准曲线
按照需要的NEFA参考校准品浓度将相应的重组NEFA纯品6mmol加入校准品稀释液2ml的缓冲液中,制备得到3mmol/l浓度的NEFA校准品在使用的时候在用缓冲液按照比例稀释浓度:3mmol/L、1.5mmol/L、0.75mmol/L、0.375mmol/L、0mmol/L。校准曲线见图1。
2.灵敏度实验
测试已知浓度为(0.3±0.1)mmol/L的样本,记录吸光度差值ΔA,换算成0.3mmol/L浓度的吸光度差值ΔA’,ΔA’=(ΔA/已知浓度)*0.3mmol/L。吸光度对比如表2所示。
表2
实验结果显示,本发明试剂在抗原将SA-生物素抗体与抗体-FITC偶联,胶乳微球进一步增大,形成基于SA-生物素-抗体-抗原-抗体-FITC的双重级联放大系统,从而大大的提高了试剂的灵敏度。说明本发明试剂盒具有较高的灵敏度,其灵敏度为0.3mmol/L。
3.线性范围实验:
用接近线性范围的高浓度样本和接近线性范围下限的低浓度NEFA样本,混合成6个稀释梯度。采用实施例2中的试剂盒检测各浓度,每个样本测试3次,求取平均值,按照判定依据R≥=0.990进行判定。测定结果见表3、图2。
表3
将测定浓度的平均值与理论浓度进行线性回归分析,计算回归方程为y=1.0077x-0.3655,相关系数为R
4.稳定性试验
检测本发明实施例2中的试剂盒及进口试剂(酶法)的稳定性,两种试剂每月选取同一样本(游离脂肪酸的含量为1.15mmol/L)测定三次,取平均值,与新鲜的本发明实施例2中试剂盒检测结果进行比对,从而确定试剂的稳定时间。检测结果如表2。
表4
实验结果显示,本发明试剂实施例4在2-8℃、密封避光的条件下,贮存15个月稳定性高于酶法试剂盒。
5.临床样本相关性检测
采用本发明实施例2中的试剂与NEFA对比试剂相比(免疫比浊法,进口国外试剂),同时测定40例临床标本血清(样本浓度覆盖标准品的检测范围),本发明的试剂盒及检测方法同实施例;NEFA对比试剂按照说明书设定相关参数,使用日立7080全自动生化分析仪对样本进行分析。以本发明检测的NEFA浓度为横坐标,进口试剂检测的NEFA浓度为纵坐标,绘制样本相关性曲线,具体检测结果见表5和图3。
表5
其中,通过表5中的数据得到NEFA的相关性方程为y=0.9872x+0.0217,相关性系数R
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种用于检测游离脂肪酸的试剂盒
- 用于临床检测血清或血浆游离脂肪酸的试剂盒及其方法
