标志物在制备结直肠癌检测试剂盒中的用途
文献发布时间:2023-06-19 12:13:22
技术领域
本发明涉及结直肠癌技术领域,具体为一种标志物在制备结直肠癌检测试剂盒中的用途。
背景技术
通过提高生物标志物的识别技术,能够推进个体化医疗的发展并提高生存率。近年来,粪便隐血试验、粪便免疫化学试验和基于粪便样本的多靶点粪便甲基化DNA检测成为筛选方法发展的重点,尽管在大多数结直肠癌中发现了一些基因甲基化,但基于体液的检测结果仍不理想,考虑到大肠癌发病机制的异质性,遗传和表观遗传学改变可能仅涵盖患者的部分病理改变,仅使用粪便样本可能会限制其他有效的生物标志物的发现,而这些生物标志物由于粪便样本采集的特点而不适用。
因此,需要一种更准确、无创、以体液(例如血液)为基础以及广泛接受的工具来提高检测的有效性和获取途径。
发明内容
本发明的目的在于提供一种标志物在制备结直肠癌检测试剂盒中的用途,能够以体液(例如血液或血清)为基础,准确、高效、无创地对结直肠癌标志物进行检测,并进一步地对结直肠癌进行检测和评估。
为实现上述目的,本发明一方面提供一种标志物在制备结直肠癌检测试剂盒中的用途,所述标志物用代谢组学特征表示,所述代谢组学特征包括如下的至少一种质荷比:m/z 562.327,m/z 558.294,m/z 534.295,m/z 146.046,m/z 148.060,m/z 128.035,m/z159.028,m/z 104.107,m/z 174.014,m/z 247.016,m/z 164.072,m/z 204.941,m/z105.111,m/z 157.012,m/z 146.983,m/z 148.980,m/z 135.003,m/z 192.024,m/z136.006,m/z 147.986。
本发明另一方面还提供一种标志物,用于结直肠癌检测,包括如下至少一种质荷比的代谢组学特征:m/z 562.327,m/z 558.294,m/z 534.295,m/z 146.046,m/z 148.060,m/z 128.035,m/z 159.028,m/z 104.107,m/z 174.014,m/z 247.016,m/z 164.072,m/z204.941,m/z 105.111,m/z 157.012,m/z 146.983,m/z 148.980,m/z 135.003,m/z192.024,m/z 136.006,m/z 147.986。
可选的,所述结直肠癌检测包括检测结直肠癌、结直肠癌癌前病变、判断结直肠癌的预后效果或者监测结直肠癌发展程度中的至少一种。
其中所述检测结直肠癌、结直肠癌癌前病变是针对于正常人的检测项目,所述判断结直肠癌的预后效果是针对于结直肠癌患者治疗后的检测项目,所述监测结直肠癌发展程度是针对于已患有结直肠癌者的检测项目。
应当理解的是,本发明所述的“检测”,在本发明的技术领域中还可称为“评估”、“诊断”、“筛查”、“早筛”等。
本发明另一方面还提供试剂盒,用于结直肠癌检测,包括至少一种上述的标志物的检测试剂。
可选的,所述试剂盒的检测样本为血液或血清。
可选的,所述试剂盒的检测样本来自健康个体、结直肠癌患者、结直肠癌癌前病变者、结直肠癌预后者的一种。
可选的,所述试剂盒还包括质控品、标准品、缓冲液、提取液中的一种或多种。
可选的,所述提取液由甲醇、乙腈和水组成。
可选的,所述甲醇、乙腈和水的体积比为(4-6):(2-4):2。
与现有技术相比,本发明的有益效果如下:
本发明技术方案采用多种代谢组学特征作为检测结直肠癌的标志物,能够检测结直肠癌、结直肠癌癌前病变、判断结直肠癌的预后效果或者监测结直肠癌发展程度,在结直肠诊断时能够更及时、更个性化,显著提高了医学工作者对结直肠发病机制的认知。较现有技术中以粪便DNA检测相比,本发明的标志物的检测样本可以取自体液,降低了患者在检测取样时的不适感,且检测准确度和灵敏度较高。
附图说明
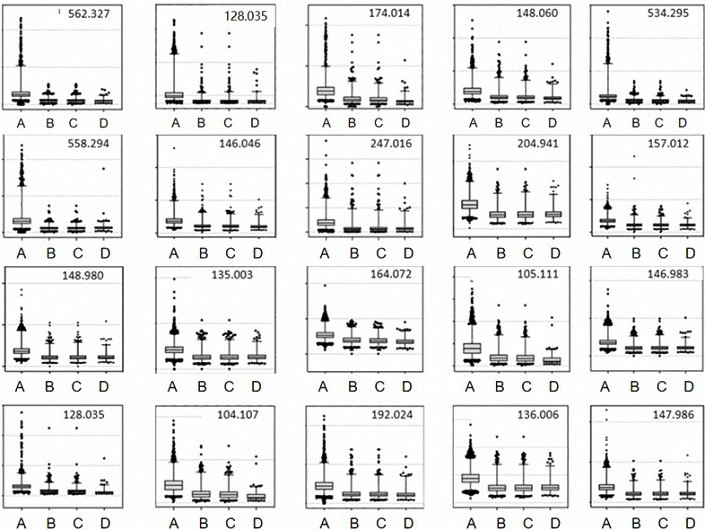
图1为本发明实施例中结直肠癌代谢组学特征不同发展阶段的归一化信号强度值;
图2为本发明中实施例中所有受试者的结直肠癌概率;
图3为本发明实施例的检测方法在晚期癌前病变检测、结直肠癌Ⅰ期和Ⅱ期(联合)检测以及结直肠癌Ⅰ、Ⅱ、Ⅲ期(联合)检测中的表现。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
结直肠癌是指发生在消化道下端的结肠或直肠癌。大多数结直肠癌始发于结肠或直肠内壁的生长,这被称为息肉。在不同类型的息肉中,腺瘤性息肉(腺瘤)可以在没有监测或特定治疗的情况下转变为癌症。因此,腺瘤被称为癌前病变(advanced precancerouslesions , APL)。当癌症在息肉中形成时,随着时间的推移它会扩散到结肠或直肠壁中,结肠和直肠壁由许多层组成,大肠癌始于最内层(粘膜),并可以通过一些或所有其他层向外生长。大肠癌的分期(扩散程度)取决于其向壁中生长的深度以及是否已扩散到结肠或直肠外部。最早的结直肠癌被称为0期(非常早期的癌症),其范围从I期到IV期。较低的数字意味着癌细胞扩散的程度低。更高的数字,例如IV期,意味着癌症扩散的程度较高。大肠癌的症状取决于癌症的大小和位置,结直肠癌的治疗取决于癌症的大小、位置和扩散程度,因此结直肠癌检测对结直肠癌的治疗具有非常大的影响。
所述的“结直肠癌检测”通常是指提供对结直肠癌的测定。例如,确定受试者目前是否患有结直肠癌(例如,具有结直肠癌临床症状的受试者、无结直肠癌但具有与结直肠癌相关的危险因素的受试者、无结直肠癌且无危险因素的受试者),又例如确定结直肠癌的严重程度等等。“结直肠癌的早期检测”通常是指在肿瘤发展的早期提供结直肠癌的测定,例如确定受试者当前是否处于大肠癌I期和II期状态。检测“癌前期晚期病变”通常是指确定受试者目前是否具有大肠息肉转化肿瘤的高风险。结直肠癌“预后”或提供结直肠癌“预后”通常是指提供结直肠癌的预测,例如受试者结直肠癌易感性的预测、疾病进展和/或疾病结局的预测,例如结直肠癌的预期发作、结直肠癌的预期持续时间、结直肠癌早期(I和II期)是否会发展到晚期(III和IV)的预期。所述结直肠癌“预后”或提供结直肠癌“预后”又例如,预测受试者对结肠直肠癌治疗的反应性,例如阳性反应、阴性反应,或者完全没有反应等等。“监测”结直肠癌通常是指监测受试者的状况,例如,通知结直肠癌的早期检测、通知结直肠癌的预后、提供有关结直肠癌治疗的效果或功效的信息等。“治疗”结直肠癌是指在患者中开处方或提供对结直肠癌的任何治疗,至少包括:在尚未被诊断为患有结直肠癌时,防止结直肠癌在可能易患结直肠癌的风险受试者中发生;通过手术抑制结直肠癌的发展;或缓解结直肠癌,即通过放射疗法或化学疗法导致肿瘤生长消退。
发明人在长期的研究工作中发现,人体血清中的代谢物与结直肠癌的诊断结果密切相关,因此可以将血清的代谢以及代谢组学特征作为结直肠癌检测时的标志物,进而对结直肠癌进行检测。
为了使代谢组学分析具有足够的动态范围,能够检测代谢浓度的潜在广泛变化,本发明实施例将高通量分析平台用于代谢组学分析,所述高通量分析平台包括质子核磁共振(1H NMR)光谱、质谱耦合的气相色谱(GC-MS)、MS耦合的液相色谱(LCMS),可以通过最少的样品预处理来分析血清样品,可靠地揭示跨越整个代谢组学系统的代谢组学途径,并具有提供深入了解大肠癌正常和病理发展所涉及的代谢过程的潜力。
本发明实施例提供一种标志物,用于结直肠癌检测,包括如下至少一种质荷比的代谢组学特征:m/z 562.327,m/z 558.294,m/z 534.295,m/z 146.046,m/z 148.060,m/z128.035,m/z 159.028,m/z 104.107,m/z 174.014,m/z 247.016,m/z 164.072,m/z204.941,m/z 105.111,m/z 157.012,m/z 146.983,m/z 148.980,m/z 135.003,m/z192.024,m/z 136.006,m/z 147.986。
在某些情况下,受试者可能会出现结直肠癌的临床症状,例如排便习惯的改变、鲜红色的直肠出血、便血、痉挛或腹部疼痛、虚弱和疲劳以及无故的体重减轻。在其他情况下,受试者可能无结直肠癌症状,但有与结直肠癌相关的危险因素,如年龄大于50岁、结直肠癌家族史;医学状况,如炎症性肠病,如克罗恩病或溃疡性结肠炎;遗传综合征,如家族性腺瘤性息肉病(FAP)或遗传性非息肉病性结肠直肠癌(Lynch综合征)。在其他情况下,受试者可能没有结直肠癌的症状,也没有与结肠直肠癌相关的危险因素。那么,此时就可以采用代谢并结合至少一种质荷比的代谢组学特征来确定受试者是否患有结直肠癌、晚期癌前病变等。
在一些实施例中,通过采用至少一种质荷比的代谢组学特征作为结直肠癌检测的标志物,进而可用于判断结直肠癌的预后。例如,所述标志物可用于预测受试者患结直肠癌的易感性或风险,通过表征标志物并与正常或癌症患者的代谢组特征进行比较来确定受测者患结直肠癌的可能性,该方法可以在结肠息肉转化为晚期癌前病变之前,方便地收集血清样本来评估结肠风险。在另一些实施例中,所述标志物还可用于预测疾病进展和/或疾病结果的进程,如预期的结直肠癌发病、预测结直肠癌将发展到哪个阶段等。所述标志物的表征还可用于预测受试者对结直肠癌治疗的反应性,如阳性反应、阴性反应、无反应。
采用至少一种质荷比的代谢组学特征作为标志物,可用于监测结直肠癌。监测受试者的状况,例如告知结直肠癌的检测情况,告知结直肠癌的预后,提供关于结直肠癌治疗的效果或效果的信息,等等。
由此,可以通过本发明实施例的标志物可以有效地检测结直肠癌。
本发明实施例还提供一种标志物在制备结直肠癌检测试剂盒中的用途,所述标志物用代谢组学特征表示,所述代谢组学特征包括如下的至少一种质荷比:m/z 562.327,m/z558.294,m/z 534.295,m/z 146.046,m/z 148.060,m/z 128.035,m/z 159.028,m/z104.107,m/z 174.014,m/z 247.016,m/z 164.072,m/z 204.941,m/z 105.111,m/z157.012,m/z 146.983,m/z 148.980,m/z 135.003,m/z 192.024,m/z 136.006,m/z147.986。
本发明还提供一种试剂盒,用于结直肠癌检测,包括:至少一种前述的标志物的检测试剂。
在本发明实施例中,所述试剂盒的检测样本可以为血液或血清。所述试剂盒的检测样本来自健康个体、结直肠癌患者、结直肠癌癌前病变者、结直肠癌预后者的一种。所述试剂盒还包括质控品、标准品、缓冲液、提取液中的一种或多种。其中所述提取液由甲醇、乙腈和水组成。优选地,所述甲醇、乙腈和水的体积比为(4-6):(2-4):2。
以下详细介绍采用本发明实施例的标志物对结直肠癌进行检测时的方法建立过程和检测过程。
样本收集:从18-85岁受试者的静脉血中分离血清样本,共9802名,其中结直肠癌患者2237名(包括一期、二期、三期)、癌前病变者756名、正常者6809名。其中经FIT(FecalImmunochemical Tests,粪便免疫化学试验)结果显示阴性的受试者作为正常对照组,病理诊断显示阳性的受试者作为癌症患者。
非靶向质谱分析:取适量血清,加入20-30倍提取液,所述提取液包括体积比为(4-6):(2-4):2的甲醇、乙腈和水。将提取的样品在低温下连续涡旋20-40分钟。将涡旋样品以12,000g,离心20-40分钟。收集适量上清液,进行质谱分析。
质谱分析采用液相系统与高分辨质谱仪联用。将10µL血清提取液注入液相系统,流动相为体积百分数为95%流动相A(甲酸的水溶液,其中甲酸的体积百分数为0.1%)和体积百分数为5%流动相B(甲酸的乙腈溶液,其中甲酸的体积百分数为0.1%)。注入样品后,通过预柱进入质谱,在正离子和负离子ESI模式下进行。Q Exactive plus质谱仪参数设置如表1和表2所示。
表1 质谱仪条件参数
表2 质谱仪条件参数
将18-85岁共名受试者的血清样品进行质谱检测。从数千种代谢指标中经单因素和多因素分析筛选出结果较好的20种代谢组学特征作为预测指标,包括m/z 562.327,m/z558.294,m/z 534.295,m/z 146.046,m/z 148.060,m/z 128.035,m/z 159.028,m/z104.107,m/z 174.014,m/z 247.016,m/z 164.072,m/z 204.941,m/z 105.111,m/z157.012,m/z 146.983,m/z 148.980,m/z 135.003,m/z 192.024,m/z 136.006,m/z147.986。
表3列出了每个特征的单变量和多变量分析,结直肠癌样本中所有20个特征均显著下降(P<0.001),且从ROCAUC评价指标结果可以看出均达到0.78以上,表明用其中一个或多个特征进行结直肠癌评估效果良好。图1显示了按结直肠癌发展的不同阶段分类的每个特征的归一化信号强度值,其中图中A为对照组,B为包含各期的结直肠癌组,C为I、II期结直肠癌组,D为癌前病变组。
表3 选定特征的单变量和多变量分析
用包含至少一种的代谢组学特征进行结直肠癌检测模型的构建。本发明实施例使用XGBoost算法构建包含本发明所述的20种代谢组学特征的结直肠癌检测算法,即结直肠癌检测模型,然后对该模型性能进行评估,即特异性、敏感性或AUC值(Area Under Curve,用于评价检测方法或预测方法的优劣性),AUC最优值对应的点即为临界值。
所述XGBoost算法是"极端梯度提升"(Extreme Gradient Boosting)的简称,所述XGBoost算法是对梯度提升算法的改进,求解损失函数极值时使用了牛顿法,将损失函数泰勒展开到二阶,另外损失函数中加入了正则化项。所述XGBoost算法是一个树集成算法,是将k(树的个数)个决策树的结果进行求和,作为最终的预测值。该算法的优点是速度快、效果好、能处理大规模数据。
在一些实施例中,将本发明实施例中的20种代谢组学特征带入XGBoost算法中,得出含有22棵决策树的结直肠癌检测模型。从0到1依次设为阈值,并计算该设置点的特异性和敏感性,AUC值最优的点即为临界值。当试验样本的结果或称分值小于临界值时表明结果为阴性即结直肠癌或癌前病变低风险,等于或大于临界值时结果为阳性即结直肠癌或癌前病变高风险。
将试验品中的20种代谢组学特征带入到各颗决策树,根据每颗决策树的指示进行分类,每颗树会有一个预测值,将每颗树的预测值求和,得到最终的预测结果。
用以上筛选出的特征建立XGBoost算法的结直肠癌评估模型,用来区分结直肠癌患者和正常对照者,以期得到更准确的评估XGBoost算法。
对结直肠癌评估模型进行验证分析,结果如表4所示。该模型可识别出2237例受试者中的2126例癌症患者,故灵敏度分别为95.0%。I-II期、I-III期的灵敏度分别为95.6%、95%。在756例晚期癌前病变患者中,识别出734例,灵敏度为97.1%(95% CI,96.6-97.4)。在6809例未患病的阴性对照组的受试者中,识别出279例,故特异性为95.9%(95% CI,95.7-96.5)。
表4 结直肠癌评估模型性能水平
将所有癌症和非癌症受试者的结直肠癌概率(检测分数)作图,如图2所示,I期,II期,III期和晚期癌前病变(APL)的结直肠癌样本可与正常样本显著分离。
如图3,其中(A)图为正常组与癌前病变组的ROC曲线图,(B)图为正常组与I期和II期结直肠组的ROC曲线图,(C)图为正常组与结直肠癌组的ROC曲线图。与正常对照相比,(A)晚期癌前病变、(B)合并的I期和II期癌症以及(C)合并的I,II和III期,其总的ROC(Receiver Operating Characteristic)AUC(Area Under Curve)区分值分别为0.9936、0.9892和0.9863,表明该检测方法效果良好。并将区分值对应的阈值设为检测方法的临界值,本申请实施例获得的临界值为0.2704,低于0.2704判断为阴性,等于或大于0.2704判断为阳性,即结直肠癌或癌前病变高风险。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 脂质标志物在制备结直肠癌检测试剂盒中的用途
- 标志物在制备结直肠癌检测试剂盒中的用途
