一种将外源性物质导入细胞的装置和方法
文献发布时间:2023-06-19 13:49:36
技术领域
本发明涉及电穿孔技术领域,涉及一种将外源性物质导入细胞的装置和方法。
背景技术
转染是真核细胞在一定条件下主动或被动导入外源性物质而获得新的表型的过程。随着基因工程技术的发展,如何高效率的将外源性物质导入细胞内成为新的研究热点。常用的转染方法包括化学手段和物理手段,化学手段包括磷酸钙沉淀法、脂质体法(Lipofectamine 2000等)、阳离子高聚物法(PEI等),化学手段对于吞噬能力弱的细胞(例如原代细胞、悬浮细胞等),和溶酶体能力强的细胞(例如巨噬细胞等),其转染效率较低,因此,对于类似这样的难转细胞,需要用到病毒感染的方法。病毒感染方法的原理是改变基因组,具有较大的风险,并且由于病毒的选择和制备周期长、操作繁琐、成本高、对插入片段的大小也有限制,一定程度上限制了病毒感染的应用。而电穿孔方法作为一种物理手段,通过外加电场在细胞膜两侧形成电势差,扰乱磷脂双分子层的排列,产生连通细胞内外的膜孔的技术,在膜孔持续的时间内,外源性物质,例如质粒,RNA,蛋白,或者多糖等,有一定几率进入细胞中。电穿孔转染可以有效地转染难转细胞,对质粒大小没有限制,而且是瞬时转染,嵌入基因组的几率很低,常常作为化学和病毒方法的补充手段,因此,电穿孔技术在基因编辑、胚胎改造、细胞机理研究、蛋白生产、细胞治疗等领域有着广泛的用途。
目前常见的电穿孔装置有Bio-Rad的Gene Pulser Xcell、Thermo Fisher的Neon系统、Lonza的Nucleofector等,其中,Gene Pulser Xcell采用比色皿式的电转杯,通过采用电转缓冲液和输出简单的方波或者指数衰减波,减少细胞的死亡率;Neon系统通过将电转杯变成电转吸头,减小了电极间的距离,使电场更加均匀,从而提高细胞的存活率;Nucleofector则在电转缓冲液中加入了促进质粒进入细胞核的试剂,即核转试剂,用以提高转染效率。然而现有的电穿孔装置均存在转染随机性强、细胞死亡率高、实验成本高等问题,如何对电穿孔装置进行改进以解决上述问题受到了越来越多的关注。
发明内容
本发明提供一种将外源性物质导入细胞的装置,用于解决常规电穿孔装置转染随机性强、细胞死亡率高、实验成本高等问题。
本发明还提供一种将外源性物质导入细胞的方法,使用上述装置对细胞进行转染,可有效解决转染随机性强的问题,提高细胞的转染成功率和细胞存活率。
本发明第一方面提供一种将外源性物质导入细胞的装置,包括反应模块和控制模块;
所述反应模块包括第一存放单元、第二存放单元和电极,所述第一存放单元包括设置有若干个贯通孔的基底,所述基底用于放置细胞,所述第二存放单元与所述贯通孔连通,用于放置所述外源性物质,所述电极分别与所述第一存放单元和第二存放单元连接;
所述控制模块与所述电极连接,用于控制所述电极产生脉冲信号。
如上述装置,所述贯通孔的孔径为50nm-8μm,高度为5μm-50μm,所述贯通孔在基底上的密度为1*10
如上述装置,所述基底包括含硅无机物或聚合物,其中,所述含硅无机物选自硅单质、氧化硅、氮化硅中的一种或多种,所述聚合物选自聚碳酸酯、聚乙烯对苯二甲酸酯、聚酰亚胺中的一种或多种。
如上述装置,所述电极包括正电极和负电极,所述正电极与所述第一存放单元连接,所述负电极与所述第二存放单元连接。
如上述装置,所述控制模块包括微控制器单元以及与所述微控制器单元连接的电压发生单元、电流检测单元和脉冲开关单元;
所述电压发生单元用于接收所述微控制器单元的信号并发出电压,所述电压发生单元与所述电流检测单元连接,所述电流检测单元与所述脉冲开关单元连接,所述电流检测单元用于检测反应模块的电流并反馈至所述微控制器单元,所述脉冲开关单元与所述电极连接,用于接收所述微控制器单元的信号并控制所述脉冲开关单元的开关。
如上述装置,所述装置包括电源模块,所述电源模块用于为所述控制模块提供电源。
如上述装置,所述装置包括触控显示模块,所述触控显示模块与所述控制模块连接,用于实现人机交互作业。
如上述装置,所述装置包括样品架,所述样品架包括围设形成的侧壁,所述侧壁设置有第一凸起和第二凸起,所述第一凸起用于承载所述第一存放单元,所述第二凸起用于承载所述第二存放单元。
本发明第二方面提供一种将外源性物质导入细胞的方法,使用上述任一所述装置进行,具体包括如下步骤:
将处于对数生长期的细胞放置于所述基底表面,将含有所述外源性物质的溶液放置于所述第二存放单元内,使部分基底浸入至含有外源性物质的溶液中,且所述细胞不与所述含有外源性物质的溶液接触,得到反应体系;
对所述反应体系进行通电,使所述外源性物质在脉冲信号下经过所述贯通孔进入所述细胞内。
如上述方法,所述脉冲信号包括第一脉冲信号、第二脉冲信号和第三脉冲信号,其中:
通过控制模块产生第一脉冲信号,其中,第一脉冲信号的第一电压U
根据所述第一电流I
通过控制模块产生第二脉冲信号,其中,第二脉冲信号以第二电压U
当第二电压U
本发明的实施,至少具有以下优势:
1、本发明提供的装置,通过设置具有贯通孔的基底,实现了外源性物质的定向导入,消除了普通电穿孔方法的随机性,提高了外源性物质的导入效率;同时,通过施加脉冲信号,能够在1-50V的低电压下完成电穿孔,提高了电穿孔的安全性,有利于提高细胞的存活率,因此,本发明提供的装置,有利于提高细胞的存活率及外源性物质的导入效率。
2、本发明提供的方法,使用上述装置进行电穿孔,有利于提高细胞的存活率及外源性物质的导入效率,此外,采用外源性物质和细胞分隔的设计,避免了额外因素对细胞的干扰,提高了系统的纯净度,简化了操作和转染流程,降低了实验成本。
3、本发明提供的方法,通过反馈和优化算法,精确控制了细胞层附近的电势差,进一步保护了细胞免受过量电流的伤害,大幅度提高了细胞的存活率,从25%提高到了90%以上。
4、本发明提供的方法可实现原位转染,无需重悬细胞,操作流程大大简化,同时使转染不能重悬的细胞,例如原代神经元细胞,成为可能。
5、本发明提供的方法无需其他辅助试剂,大大降低了实验成本,不到现有技术的1/10。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为本发明一实施例提供的装置的整体结构示意图;
图2为本发明一实施例提供的预培养装置的结构示意图;
图3为本发明一实施例提供的脉冲信号示意图;
图4a为本发明一实施例提供的人胚胎干细胞导入EGFP质粒24小时后,细胞在488nm激光下的绿色荧光照片;
图4b为图4a提供的细胞在明场下的照片;
图5a为本发明又一实施例提供的原代人源PBMC细胞导入FAM标记的siRNA片段5分钟后,细胞在488nm激光下的绿色荧光照片;
图5b为图5a提供的细胞在明场下的照片;
图6a为本发明再一实施例提供的HeLa细胞导入Alexa Fluor 488标记的H4B4单克隆抗体5分钟后,细胞在488nm激光下的绿色荧光照片;
图6b为图6a提供的细胞在明场下的照片。
附图标记说明:
1:反应模块;
1-1:第一存放单元;
1-1-1:基底;
1-1-2:贯通孔;
1-2:第二存放单元;
1-3:正电极;
1-4:负电极;
2:控制模块;
2-1:微控制器单元;
2-2:电压发生单元;
2-3:电流检测单元;
2-4:脉冲开关单元;
3:电源模块;
4:触控显示模块;
5:样品架;
5-1:第一凸起;
5-2:第二凸起;
6:细胞;
7:外源性物质;
8:预培养箱;
9:预培养箱盖子;
10:第一脉冲信号;
11:第二脉冲信号;
12:第三脉冲信号。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明的实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
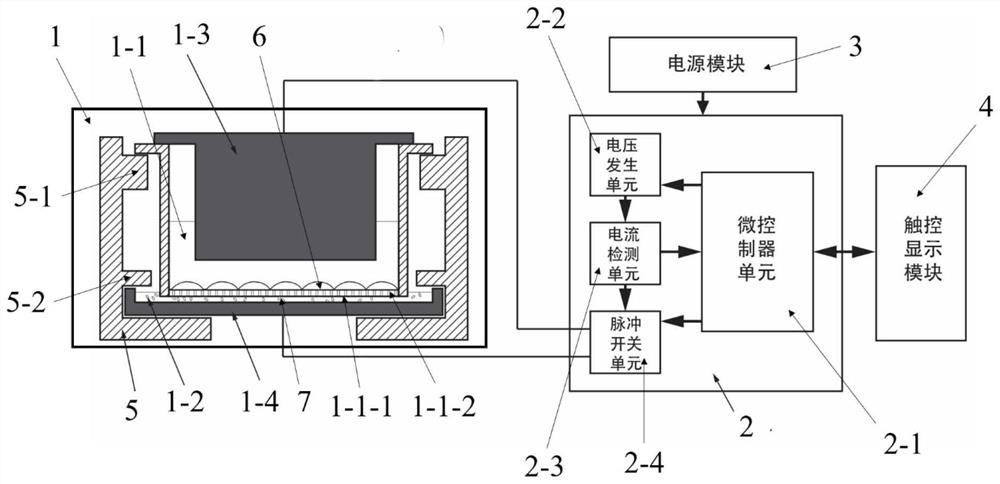
本发明第一方面提供一种将外源性物质导入细胞的装置,图1为本发明一实施例提供的装置的整体结构示意图,如图1所示,该装置包括反应模块1、控制模块2、电源模块3、触控显示模块4和样品架5,具体地:
反应模块1用于进行电穿孔实验,包括第一存放单元1-1、第二存放单元1-2、正电极1-3和负电极1-4,第一存放单元1-1位于第二存放单元1-2的上方,包括基底1-1-1和设置在基底1-1-1上的贯通孔1-1-2,基底1-1-1用于放置细胞6,第二存放单元1-2用于放置外源性物质7,且第二存放单元1-2与贯通孔1-1-2连通,能够实现物质交换,也就是说,第二存放单元1-2内存放的外源性物质7能够通过贯通孔1-1-2进入细胞6内,完成电穿孔过程。
由于基底用于放置细胞,在电穿孔过程中,为了提高细胞的存活率,基底表面需经过灭菌处理,并选择适合细胞贴壁培养的材料。
在一种可行的实施方式中,所述基底包括含硅无机物或聚合物,其中,所述含硅无机物选自硅单质、氧化硅、氮化硅中的一种或多种,所述聚合物选自聚碳酸酯、聚乙烯对苯二甲酸酯、聚酰亚胺中的一种或多种。
贯通孔1-1-2是指连通基底1-1-1上表面和下表面的通孔,本领域技术人员可以在制备得到基底的技术上,采用刻蚀工艺制备得到贯通孔,进一步地,由于深硅刻蚀或径迹刻蚀工艺可以达到很高的径深比(比如纳米级的孔径,微米级的深度)和均一度较好的贯通孔,因此,可通过深硅刻蚀或径迹刻蚀的方法得到贯通孔。
由于贯通孔的大小、密度对电穿孔结果有很大的影响,为了进一步提高导入效率,所述贯通孔的孔径为50nm-8μm,高度为5μm-50μm,所述贯通孔在基底上的密度为1*10
进一步地,贯通孔的孔径为400nm-1μm,贯通孔在基底上的密度为2*10
电极与第一存放单元1-1和第二存放单元1-2连接,其中,电极包括正电极1-3和负电极1-4,可以理解的是,正电极和负电极形成的电场方向与外源性物质的电学性质相关,由于大多数情况下外源性物质带负电,因此,正电极1-3与第一存放单元1-1连接,负电极1-4与第二存放单元1-2连接,如果外源性物质带正电,则需要颠倒电极位置,即正电极1-3与第二存放单元1-2连接,负电极1-4与第一存放单元1-1连接。
正电极和负电极的材料为本领域常规材料,例如,所述正电极和所述负电极独立地选自铝、银、镀银、导电塑料、铜、不锈钢、金、镀金、铂金、石墨中的一种或多种。
控制模块2与电极连接,用于控制电极产生脉冲信号,控制模块2包括微控制器单元2-1以及与微控制器单元2-1连接的电压发生单元2-2、电流检测单元2-3和脉冲开关单元2-4;
电压发生单元2-2用于接收微控制器单元2-1的信号并发出电压,电压发生单元2-1与电流检测单元2-3连接,电流检测单元2-3与脉冲开关单元2-4连接,电流检测单元2-3用于检测反应模块1的电流并反馈至微控制器单元2-1,脉冲开关单元2-4与电极连接,用于接收微控制器单元2-1的信号并控制脉冲信号的开关。
可以理解的是,脉冲发生方式需要经过波形产生,再放大,然后输出的过程,脉冲信号经过电压发生单元放大后,可以实现在1-50V的低电压下完成电穿孔,提高电穿孔的安全性,有利于提高细胞的存活率。
此外,因为脉冲信号之间存在停顿,本实施方式使用同一条线路(即电压发生单元-电流检测单元-脉冲开关单元)完成读取-反馈-输出的过程,此时电流检测单元检测到的电流值更接近真实情况。
电源模块3与控制模块2连接,用于为控制模块2提供电源,本领域技术人员可以根据常规手段进行设置。
触控显示模块4与控制模块2连接,用于实现人机交互作业,例如,控制模块2将通电过程反馈至触控显示模块4,并接受触控显示模块4的指令进行操作。
样品架5与反应模块1连接,用于支撑第一存放单元1-1和第二存放单元1-2,具体地,样品架5包括围设形成的侧壁,侧壁设置有第一凸起5-1和第二凸起5-2,第一凸起5-2用于承载所述第一存放单元1-1,第二凸起5-2用于承载第二存放单元5-3。
本发明提供的装置运行过程如下:将细胞放置于基底表面,将外源性物质放置于第二存放单元内,通过触控显示模块控制开始进行电穿孔,电穿孔过程中,控制模块控制电极发出脉冲信号,使外源性物质通过贯通孔进入到细胞内,本发明提供的装置,有利于提高细胞的存活率及外源性物质的导入效率。
本发明第二方面提供一种将外源性物质导入细胞的方法,使用上述任一所述装置进行,具体包括如下步骤:
将处于对数生长期的细胞放置于所述基底表面,将含有所述外源性物质的溶液放置于所述第二存放单元内,使部分基底浸入至含有外源性物质的溶液中,且所述细胞不与所述含有外源性物质的溶液接触,得到反应体系;
对所述反应体系进行通电,使所述外源性物质在脉冲信号下经过所述贯通孔进入所述细胞内。
本发明提供一种将外源性物质导入细胞的方法,用于将外源性物质导入细胞内,所使用的细胞可以本领域常用的重悬细胞,或不能重悬的细胞,例如原代神经元细胞,外源性物质例如可以是质粒等需要导入细胞内的物质,本发明在此不做特别限定,以下就导入方法进行详细阐述:
步骤1、将处于对数生长期的细胞放置于所述基底表面,将含有所述外源性物质的溶液放置于所述第二存放单元内,使部分基底浸入至含有外源性物质的溶液中,且所述细胞不与所述含有外源性物质的溶液接触,得到反应体系:
首先,培养细胞至生长对数期,细胞的培养过程可根据本领域常规技手段进行,例如使用常规培养皿或者多孔板进行细胞培养,或者可以直接将细胞放置于图1的基底表面,并放置于细胞培养箱中培养,图2为本发明一实施例提供的细胞预培养装置的结构示意图,如图2所示,包括基底1-1-1、预培养箱8和预培养箱盖子9,基底1-1-1放置于预培养箱8的内部,盖好预培养箱盖子9后进行培养;一般培养24小时后,细胞进入对数生长期,取出基底后放置在图1所示的装置中,准备电穿孔转染。
其次,将外源性物质使用无菌水配制成浓度为10μg/mL-80μg/mL的溶液,放置于第二存放单元中。
接着,将含有对数生长期细胞的基底浸入外源性物质的溶液中,且保证细胞不与含有外源性物质的溶液接触,放置过程中需注意不要有气泡,否则气泡出现的地方会阻断电流,导致部分细胞无法完成电穿孔,此外,当生成的气泡足够大时,会影响后续电流的判断,降低细胞转染效率。
最后,将正电极和负电极与反应体系连接,具体地,将正电极插入至第一存放单元中,使得上电极前端浸入细胞培养液中,将负电极放置于第二存放单元下方,需要注意的是,正电极、负电极和反应体系连接过程中不能有气泡。
步骤2、对所述反应体系进行通电,使所述外源性物质在脉冲信号下经过所述贯通孔进入所述细胞内:
随后即可打开控制模块对反应体系进行通电,由于基底表面设置有贯通孔,位于下方的外源性物质能够沿贯通孔方向定向导入至细胞内,并且为了保证细胞的存活率,本发明使用脉冲信号进行电穿孔。
为了进一步保护细胞免受过量电流的伤害,本发明通过算法优化精确控制了细胞膜表面的电势差,具体地,所述脉冲信号包括第一脉冲信号、第二脉冲信号和第三脉冲信号,其中:
通过控制模块产生第一脉冲信号,其中,第一脉冲信号的第一电压U
根据所述第一电流I
通过控制模块产生第二脉冲信号,其中,第二脉冲信号以第二电压U
当第二电压U
图3为本发明一实施例提供的脉冲信号示意图,如图3所示,控制模块首先与正电极、负电极形成回路,向反应体系输出第一脉冲信号10,通过反馈的电流值和细胞数量确定第一状态,从而确定后续电穿孔过程的合适脉冲信号,具体地,第一脉冲信号10为方波,第一脉冲信号的第一电压U
表1第一电流对照表(电流单位:mA)
表1中,小、中、大号样品是根据细胞在基底表面的培养面积决定的,基于不同的培养面积,导致不同的细胞电阻,同理,在相同培养面积下,细胞生长的密度不同也会造成电阻的差别。在具体实施过程中,样品的大小、密度根据常规技术手段对待转染的细胞进行分类,本发明对此不做限定。
接着,根据所述第一状态确定步进电压U
表2第二脉冲信号参数表(电压单位:V)
表3阈值RI表(单位:ΩA
需要说明的是,表2列举的第二电压均为4V,这是根据第一电压1-3V确定的,在实际电穿孔过程中,可以选择大于3V的电压,并不限于表2列举的4V,此外,如果第一电压选择1V,那第二电压可以选择2V,仅需大于第一电压即可。
随后,通过控制模块产生第二脉冲信号,第一脉冲信号与第二脉冲信号间隔100-500ms,第二脉冲信号11为阶梯脉冲,具体地,第二脉冲信号为方波,第二脉冲信号以第二电压U
最后,通过递增的第二脉冲信号反馈的电流值,计算细胞的电阻随电流的变化率ΔRI,找到合适的第三脉冲信号;
具体地,当第二电压U
其中,电阻随电流的变化率ΔRI的算法如下:
①首先计算第二脉冲信号中,两个相邻脉冲下样品的电阻R:
R
U
②然后计算细胞的电阻随电流的变化率ΔRI:
ΔRI=(R
③ΔRI呈先增大后减小的趋势,当ΔRI衰减到阈值RI时,生成第三脉冲信号,第三脉冲信号为方波,其大小为最后一个第二脉冲信号的电压值,第三脉冲信号的宽度为10-50ms,第三脉冲信号的间隔为10-50ms,第三脉冲信号的个数为1-20个,电穿孔转染完成。
最后,取下电极,将细胞放回原处培养,观察细胞内荧光判断外源性物质的导入/转染效率。
以下结合具体实施例进行详细阐述:
实施例1
本实施例提供一种将EGFP质粒导入人胚胎干细胞的方法,具体包括:
使用如图2所示的装置,将人胚胎干细胞培养至对数生长期,将外源性物质EGFP质粒,用无菌水配制成浓度为40μg/mL的溶液;
将处于生长对数期的细胞放置于图1所示的装置中,将100μL含有EGFP质粒的溶液放置于第二存放单元内,使放置有人胚胎干细胞的基底浸入含有EGFP质粒的溶液中,且人胚胎干细胞不与含有EGFP质粒的溶液接触。
控制触控显示单元,通过脉冲开关单元产生第一脉冲信号,其中,第一电压U
根据第一电流I
通过触控显示单元控制脉冲开关单元产生第二脉冲信号,其中,第二脉冲信号以第二电压U
当第二电压U
图4a为本发明一实施例提供的人胚胎干细胞导入EGFP质粒24小时后,细胞在488nm激光下的绿色荧光照片,图4b为图4a提供的细胞在明场下的照片,根据图4a-4b可以看出,图4a中大部分细胞具有绿色荧光,表明EGFP质粒导入至细胞中,转染效率较高(大于70%),且电穿孔后细胞状态良好。
实施例2
本实施例提供一种将FAM标记的siRNA片段导入至原代PBMC细胞中的方法,具体包括:
使用如图2所示的装置,将原代PBMC细胞培养至对数生长期,将外源性物质FAM标记的siRNA片段,用无菌水配制成浓度为100nM的溶液;
将处于生长对数期的细胞放置于图1所示的装置中,用生物胶使其临时贴附在基底上(8小时后生物胶会自动失效)。将100μL含有FAM标记的siRNA片段的溶液放置于第二存放单元内,使放置有原代PBMC细胞的基底浸入含有FAM标记的siRNA片段的溶液中,且原代PBMC细胞不与含有FAM标记的siRNA片段的溶液接触。
控制触控显示单元,通过脉冲开关单元产生第一脉冲信号,其中,第一电压U
根据第一电流I
通过触控显示单元控制脉冲开关单元产生第二脉冲信号,其中,第二脉冲信号以第二电压U
当第二电压U
图5a为本发明一实施例提供的原代人源PBMC细胞导入FAM标记的siRNA片段5分钟后,细胞在488nm激光下的绿色荧光照片,图5b为图5a提供的细胞在明场下的照片,根据图5a-5b可以看出,电穿孔后细胞状态良好,且导入效率较高(大于70%)。
实施例3
本实施例提供一种将Alexa Fluor 488标记的H4B4单克隆抗体导入HeLa细胞中的方法,具体包括:
使用如图2所示的装置,将HeLa细胞培养至对数生长期,将外源性物质AlexaFluor 488标记的H4B4单克隆抗体,用无菌水配制成浓度为80μg/mL的溶液;
将处于生长对数期的细胞放置于图1所示的装置中,将100μL含有Alexa Fluor488标记的H4B4单克隆抗体的溶液放置于第二存放单元内,使放置有HeLa细胞的基底浸入含有Alexa Fluor 488标记的H4B4单克隆抗体的溶液中,且HeLa细胞不与含有Alexa Fluor488标记的H4B4单克隆抗体的溶液接触。
控制触控显示单元,通过脉冲开关单元产生第一脉冲信号,其中,第一电压U
根据第一电流I
通过触控显示单元控制脉冲开关单元产生第二脉冲信号,其中,第二脉冲信号以第二电压U
当第二电压U
图6a为本发明一实施例提供的HeLa细胞导入Alexa Fluor 488标记的H4B4单克隆抗体5分钟后,细胞在488nm激光下的绿色荧光照片,图6b为图6a提供的细胞在明场下的照片,根据图6a-6b可以看出,电穿孔后细胞状态良好,且导入效率较高(大于70%)。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
