耐药相关基因GABRP在结直肠癌耐药中的应用
文献发布时间:2023-06-19 18:58:26
技术领域
本发明涉及耐药相关基因GABRP在结直肠癌耐药中的应用,属于生物医药领域。
背景技术
结直肠癌(CRC)是全球第三大常见癌症,也是第二致命的癌症,2020年约有190万例新发病例和超过935,000例死亡。在过去二十年中,CRC的发病率增加近10%。为此,在过去的几十年中,对化疗药物,分子靶向治疗和免疫治疗的开发快速进行,例如5-氟尿嘧啶(5-Fu),伊立替康,奥沙利铂,西妥昔单抗,贝伐珠单抗和培布利珠单抗。然而,CRC的预后仍然很差,5年生存率仅为64-67%,对于转移性或更晚期的CRC,生存率降至14-15%。临床上,癌症常用化疗药物包括奥沙利铂和5-氟尿嘧啶(5-FU),常作为转移性结直肠癌患者的一线或二线治疗药(Crit Rev Oncol Hematol 122:21-29.doi:10.1016/j.critrevonc.2017.12.010)。
奥沙利铂作为顺铂的衍生物之一,可以抑制细胞DNA和蛋白质合成,对抑制癌细胞增殖有较高的疗效,是常用的化疗药物。同时,CRC的根治性切除手术后通常采用以奥沙利铂为主的辅助化疗,例如CAPOX(奥沙利铂和卡培他滨)。这种免疫检查点抑制剂被推荐为开创性治疗,在微卫星不稳定性高(MSI-H)或缺陷错配修复(dMMR)CRC患者中显示出更好的治疗活性(Ann Transl Med 10:380.doi:10.21037/atm-22-359)。最近的研究表明,奥沙利铂可以通过与三氟利定/替吡嘧啶联合治疗CRC来改善PD-1治疗(Cancer Immunol Res7:1958-1969.doi:10.1158/2326-6066.Cir-19-0228)。然而长期奥沙利铂治疗可能积累获得性化学抵抗力,且其机制尚不清楚,这对于癌症的治疗造成极大阻碍。
自20世纪90年代至今,氟尿嘧啶一直是结直肠癌化疗的主要药物之一。作为尿嘧啶的类似物,5-FU在C5位置氟原子取代了氢原子,阻碍细胞碱基互补配对并抑制肿瘤生长。同样,获得性耐药性仍然是氟尿嘧啶治疗CRC的瓶颈(Pharmacol Ther 206:107447.doi:10.1016/j.pharmthera.2019.107447)。
耐药性是CRC治疗的主要障碍,并导致预后不良。因此,揭示潜在机制,并找到延迟或克服耐药性的策略对于改善CRC患者的预后是必要的。抗癌耐药性一直是癌症治疗中的一大难点。面对药物压力,耐药癌细胞表现出复杂的分子机制,包括表观遗传变化以维持生存。(Front Oncol.2021Oct 20;11:746789.)驱动阻力的机制很复杂,而且尚未完全建立。目前的知识表明,耐药性可能源于药物转运和靶标相关信号传导的抑制,从免疫反应和药物诱导的细胞死亡中逃脱以及药物耐受性细胞的形成和维持。也可以通过抑制剂(例如,RAF抑制剂)触发的反向信号激活或因为靶向毒性限制患者的最大耐受剂量(例如,MEK或AKT抑制剂)(Cell 2020Nov 12;183(4):850-859)。
靶向药物包括抗EGFR抗体西妥昔单抗、抗VEGFR剂贝伐珠单抗、抗c-MET抗体奥那珠单抗、抗BRAF抑制剂维莫拉非尼和抗MEK抑制剂曲美替尼等对CRC患者治疗有贡献。比如EGFR基因在CRC肿瘤上过度表达,抗EGFR单克隆抗体(西妥昔单抗、帕尼单抗和奈尼单抗)已被证明对EGFR扩增的CRC患者具有潜在益处。西妥昔单抗特异性地与EGFR结合并阻断EGFR信号通路。然而,CRC细胞可以通过激活替代途径(例如VEGFR,c-MET和HER2)来规避阻断。据报道,HER2和MET的扩增是体内外模型中对西妥昔单抗的获得性抗性的替偿机制。替代受体的扩增是EGFR阻断后癌细胞存活的适应性反应。De及其同事也发现,具有西妥昔单抗性的CRC细胞显示出相当低的EGFR表达水平,但HER2和HER3的表达水平很高。癌症基因组图谱(TCGA)数据进一步证实以上结果。新型lncRNA西妥昔单抗相关RNA转录本16(CRART16)在西妥昔单抗性Caco-2细胞中上调。CRART16通过海绵化miR-371a-5p来促进HER3的表达,从而起到ceRNA的作用。(Biochim Biophys Acta Rev Cancer.2021Dec;1876(2):188623)总之,其他分子可能通过促进替代受体的表达来促进西妥昔单抗耐药性。寻找耐药结直肠癌细胞中的替代靶点是解决化疗耐药的关键,在与奥沙利铂或者5-氟尿嘧啶(5-Fu)的联合治疗中发挥作用,降低癌细胞耐药对于结直肠癌化疗的影响。
此外,结直肠癌症患者同时也有可能伴随有糖尿病,糖尿病同时也与心血管事件风险增加有关。(N Engl J Med.2018Oct 18;379(16):1529-1539.doi:10.1056/NEJMoa1804988.)肥胖和糖尿病与患多种癌症的风险增加有关,包括肝癌、胰腺癌、子宫内膜癌、结直肠癌和绝经后乳腺癌。发展肥胖和糖尿病的途径受到多种因素的影响,包括脂肪因子、炎性细胞因子、生长激素、胰岛素抵抗和高脂血症。与肥胖和糖尿病中这些因素水平的代谢异常有关,也可能通过调节不同的信号通路显著促进癌症的发展和进展(DiabetesMetab J.2021Nov;45(6):799-812.doi:10.4093/dmj.2021.0077)。
综上,寻找结直肠癌的新靶点,尤其是在5-氟尿嘧啶(5-Fu)、奥沙利铂耐药结直肠癌中寻找到疾病治疗的靶基因,对研制抗癌细胞耐药性的辅助药物十分必要。进一步地,如果该靶点可以与糖尿病治疗药相互关联,从而改善结直肠癌患者伴随的糖尿病,起到双重治疗的效果,缓解病人在长期化疗过程中产生的抑郁情绪,将具有重要的意义。
发明内容
为解决上述至少一个问题,本发明找到了结直肠癌的新靶点GABRP(γ-氨基丁酸A型受体亚基Pi),并通过成功建立奥沙利铂和5-Fu耐药CRC细胞发现GABRP是奥沙利铂/5-Fu抗性和敏感细胞之间的差异表达基因;该发现可用于开发制备结直肠癌相关的药物,尤其是与结直肠癌癌症耐药相关的药物或者试剂或者分子标记物,能够为结直肠癌和其他产生奥沙利铂/5-FU耐药的癌症提供解决方案。此外,GABA药物目前被用于I型糖尿病治疗药的研发,临床实验表明GABA药物可以显著改善糖尿症患者的病情(ClinicalTrials.govIdentifier:NCT02002130);作为γ-氨基丁酸A型受体亚基Pi,GABRP与糖尿病治疗药GABA相互关联,将有助于改善结直肠癌患者伴随的糖尿病、缓解病人在长期化疗过程中产生的抑郁情绪。
本发明第一个目的是提供GABRP作为靶点制备结直肠癌的相关药物中的应用。
在一种实施方式中,所述相关药物为治疗结直肠癌或者耐药结直肠癌的药物;所述应用包括但不限于使用GABRP抑制剂,比如GABRP的RNA干扰载体、能够抑制GABRP表达的抑制剂、阻断GABRP与配体结合的抑制剂等。
在一种实施方式中,所述相关药物是增强结直肠癌的奥沙利铂和/或5-Fu敏感性的药物;所述应用是沉默GABRP的表达。
在一种实施方式中,所述相关药物是增强结直肠癌的奥沙利铂和/或5-Fu耐药性的药物;所述应用是增强GABRP的表达。
本发明的第二个目的是提供GABRP基因作为靶基因在制备或筛选能够治疗奥沙利铂和/或5-Fu耐药性癌症的药物和/或生物学试剂中应用。
在一种实施方式中,奥沙利铂和/或5-Fu耐药性癌症为耐药性结直肠癌。
在一种实施方式中,所述应用是以GABRP作为靶点,构建GABRP缺失或差异性表达的细胞模型,进而用于筛选药物。
本发明的第三个目的是提供结直肠癌对奥沙利铂和/或5-Fu耐药性的分子标志物/诊断标记物,所述标志物/标记物为GABRP基因。
GABRP的基因序列如下(NCBI中Gene ID:2568):NC_000005.10:170,779,586-170,817,179Homo sapiens chromosome 1,GRCh38.p14 Primary。
本发明的第四个目的是提供一种治疗结直肠癌的联合用药物,所述联合用药物中含有:(1)抑制剂,即能抑制或降低或沉默GABRP表达的物质;以及(2)抗癌药物,即结直肠癌化疗药物。
在一种实施方式中,所述结直肠癌化疗药物为奥沙利铂和/或5-Fu。
在一种实施方式中,所述联合用药物,可以提高结直肠癌的奥沙利铂和/或5-Fu敏感性、降低或减少或治疗结直肠癌的奥沙利铂和/或5-Fu耐药性。
在一种实施方式中,联合用药物可以抑制结直肠癌肿瘤细胞的增殖、迁移、侵袭或转移中的任意一种或多种。
在一种实施方式中,所述联合用药物,是用于预防和/或治疗癌症耐药和/或转移的药物。可选地,所述联合用药物,在化疗耐药性癌症的患者的后续抗癌用药中使用,即作为产生耐药性癌症的患者的后续抗癌用药。
在一种实施方式中,所述联合用药物可作用于GABRP相关蛋白及其所对应的生物活动。根据GABRP基因的KEGG通路分析及GO注释和蛋白质之间的互相作用网,GABRP与多种通路(如PI3K-Akt信号通路、GABA能突触和神经活性配体-受体相互作用)相关,且与多种蛋白(如GABARAP、GABARAPL1)具有相互作用。相关生物活动可提供一个检测或治疗结直肠癌的方向。
在本发明中,GABRP相关蛋白GABARAP、GABARAPL1,其缺失、抑制或失活,作用于结直肠癌及其耐药细胞。
在一种实施方式中,所述联合用药物中还包含GABARAP抑制剂和/或GABARAPL1抑制剂(或/和其他抑制GABARAP、GABARAPL1的物质),与GABRP抑制剂同时使用;可改善相关癌症治疗过程中出现的耐药性问题。
本发明提供了γ-氨基丁酸A型受体亚基Pi(GABRP)作为HCT-8/5-FU和SW480/LOPH两种CRC抗性细胞系的治疗靶点。本发明可以为耐药性癌症治疗辅助药的研发提供新的思路,有希望解决癌症治疗过程中出现的耐药,转移和预后差的问题,显著改善药物治疗效果,提高患者的生存率。
本发明发现GABRP在奥沙利铂/5-Fu耐药结直肠癌细胞中高度表达,可以作为介导CRC化学耐药性的诊断标志物。
本发明中,所述抑制剂和抗癌药物,可以是分开包装使用或者联合包装使用。
本发明中,所述抑制剂或抗癌药物,可以是含有相同或不同规格单位制剂。
本发明中,所述的联合用药物包括药学上可接受的载体;可选地,所述的载体为崩解剂、赋形剂、粘合剂、填充剂、润湿剂、吸附载体、缓释剂、吸收促进剂、表面活性剂或润滑剂中的任意一种或多种。
本发明中,所述的联合用药物的剂型为口服制剂、注射制剂或外用制剂中的任意一种。可选地,所述的外用制剂为喷雾剂或气雾剂;所述的口服制剂为胶囊剂、囊泡剂、颗粒剂或片剂中的任意一种;所述的注射制剂可采用皮内、皮下、肌内、局部或静脉内注射等给药方式。
本发明中,所述的联合用药物可直接或加入药学上的辅料制备成临床上可接受的制剂。可选地,所述的临床上可接受的剂型包括但不限于片剂、胶囊剂、颗粒剂、丸剂、口服液、糖浆剂、合剂、混悬剂。
本发明中,GABRP的基因序列如下(NCBI中Gene ID:2568):NC_000005.10:170,779,586-170,817,179 Homo sapiens chromosome 1,GRCh38.p14 Primary。
有益效果:
本发明首先利用生物信息学及网络药理学相关技术,分析人源CRC化疗抗药和敏感的患者样本中差异性表达的分子。本发明利用基因表达综合数据库(GEO)分析三个包括耐药性和敏感性结直肠癌患者样本的差异性表达基因,发现GABA家族的GABRP是结直肠敏感和耐药细胞之间潜在的分化基因;利用KEGG分析与GABRP相关的信号通路,发现GABRP与脑组织神经活动配体-受体相互作用、PI3K-Akt信号通路、HPV感染等通路有较大相关性,推测GABRP与神经性疾病、胰岛素分泌、HPV感染相关。
然后,本发明使用略低于IC50的药物浓度作为起始刺激细胞的浓度,循环递增药物浓度攻击CRC细胞使其逐渐耐药,经过4-6个月建立SW480-奥沙利铂(30uM)和HCT-8-5-Fu(20ug/ml)耐药细胞株。本发明分析奥沙利铂和5-Fu耐药及敏感细胞株中GABRP相对表达量的差异性,发现GABRP与结直肠癌细胞的耐药性呈正相关。
最后,从临床意义出发,TCGA数据库泛癌和结直肠癌患者均佐证GABRP高表达具有显著促癌作用。本发明发现与GABRP存在潜在互相作用的蛋白质分子包括GABARAP、GABARAPL1、GABARAPL、ANKRD66、CLIC3、CLINT1等,推测GABRP可与上述分子形成联合用药物。
GABRP高表达的肿瘤多为恶性肿瘤,且在结直肠癌治疗过程中会出现耐药问题,治疗效果不佳。本发明为研发设计GABRP靶向治疗药物提供新思路。本发明发现GABA家族的GABRP是结直肠癌及其他癌细胞潜在分化基因。通过靶向GABRP的治疗药物,可以降低结直肠癌等癌症患者的死亡率。
本发明同时发现,GABRP在奥沙利铂和5-Fu耐药性结直肠癌细胞中高表达。本发明通过提出一种包含奥沙利铂或/和5-Fu和GABRP靶向药物的联合用药物,为有效抑制GABRP高表达的其他癌症发生发展的药物提供新方案,改善抗癌类药物耐药性问题并提高肿瘤患者生存率。
附图说明
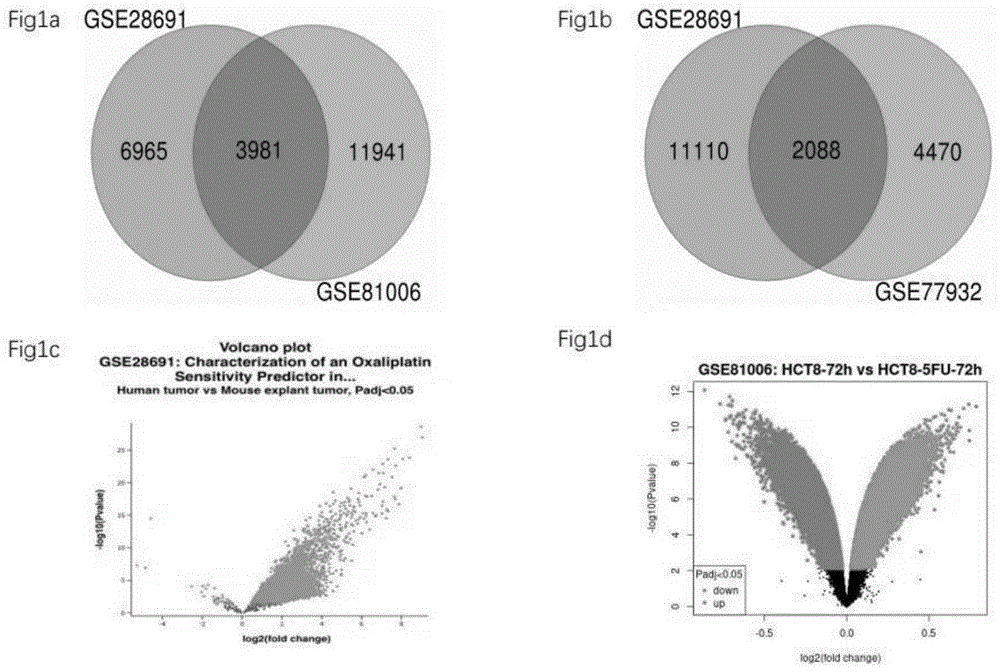
图1为在人源CRC化疗抗药和敏感的患者样本中筛选差异性表达的分子;其中,
Fig1a:来自化疗敏感性和化疗抗性结直肠患者的重叠GEO数据集的维恩图;韦恩图显示
GSE28691数据集与GSE81006数据集的交集;
Fig1b:来自化疗敏感性和化疗抗性结直肠患者的重叠GEO数据集的维恩图;韦恩图显示
GSE28691数据集与GSE77932数据集的交集;
Fig1c:奥沙利铂/5-Fu耐药与药敏患者样本之间的DEGs火山图;GSE77932数据集比较了DLD1敏感和其对应的奥沙利铂耐药细胞系;
Fig1d:奥沙利铂/5-Fu耐药与药敏患者样本之间的DEGs火山图;在72小时的时间点比较了HCT-8野生型细胞(HCT8/WT)及其5-FU抗性细胞(HCT8/5-FU)之间的甲基化状态。
图2为KEGG通路分析及GO注释;其中,
Fig2a:涉及不同生物过程(BP:biological process)的差异表达基因(DEG:differentiallyexpressed genes)数量;
Fig2b:与不同细胞组分(CC:cellular components)相关的差异基因数量;
Fig2c:涉及不同分子功能(MF:molecular function)的差异基因数量;
Fig2d:包含本发明潜在GABRP的通路。
图3为qRT-PCR和Western Blot(蛋白质印迹,WB)法检测CRC细胞与其配对的化疗耐药细胞之间的GABRP的mRNA及蛋白的表达差异;其中,
Fig3a:qRT-PCR法测量并比较SW480细胞(人直肠癌细胞)和其奥沙利铂化疗耐药细胞
SW480-LOPH中的GABRP的mRNA表达水平;
Fig3b:从转录水平比较CRC细胞HCT-8与其化疗耐药5氟尿嘧啶HCT-8-5Fu细胞中
GABRP的mRNA差异性表达。
Fig3c:为Western Blot(蛋白质印迹,WB)法从翻译水平测量并比较SW480细胞(人直肠癌细胞)和其奥沙利铂化疗耐药细胞SW480-LOPH中的GABRP蛋白的表达差异。图4为GABRP在多种结直肠癌患者中的临床相关性和重要临床意义;其中,
Fig4a:按非癌症和结直肠癌不同类型分组,数据显示GABRP在TCGA数据库中的结直肠组织中的表达;
Fig4b:按不同癌症类型分组(乳腺癌,结肠腺癌,胃癌和胰腺癌),比较GABRP在Gyorffy作者提供的细胞系中的表达情况;
Fig4c:比较GABRP在Skyrzypczak作者提供的结直肠腺癌患者组织样本中的表达与在正常结直肠组织中的表达。
图5为蛋白质之间的互相作用网络图;其中,
Fig5a:中心基因GABRP相互作用的分子网络图;
Fig5b:和中心基因GABRP最相关且距离最近的富集基因。
具体实施方案
下面将结合实施例对本发明的技术方案及进行详细的描述。
在本发明中,GABA(γ-氨基丁酸,γ-aminobutyric acid)是一种重要中枢神经系统抑制性神经递质,其与谷氨酸作用导致氨基酸神经递质系统的稳态平衡失调除在睡眠呼吸障碍(SDB)起作用外,其作为主要抑制性和兴奋性神经递质,与核内GABA-谷氨酸调节的改变与多种心血管合并症有关。此外,GABA与脯氨酸代谢会加剧微生物易位,使得微生物组功能、成分性质等发生改变进而对抑郁症产生一定影响。此外,GABA一大受体α3(Gabra3)已被证实与镇静、共济失调、健忘症、抗焦虑和睡眠活动有关,目前已有一些GABA在目前临床上被作为受体调节剂使用。Gabra3与AKT途径、氯离子通道相关,Gabra3通过活化了AKT途径,使下游分子(包括FAK,MMP等)激活,细胞运动,侵袭和转移。而其与T淋巴细胞的抗肿瘤免疫等机制存在相关性,其高表达会诱导β-连环蛋白信号传导使得癌细胞增加,影响癌细胞及其耐药细胞的生存、增殖、迁移和侵袭。
在本发明中,GABRP(γ-氨基丁酸A型受体亚基Pi)隶属于GABA家族,介导成熟中枢神经系统中的抑制性突触传递。作为富含TNBC干细胞的膜蛋白,与EGFR相互作用并显著维持其表达,从而导致干性维持和化疗抵抗。而沉默GABRP会诱导EGFR信号下调,这阻碍了细胞干性并增强了对化学疗法(包括紫杉醇,阿霉素和顺铂)的敏感性,可见,GABRP可作为解决耐药性的潜在治疗靶标。此外,GABRP是一种潜在的预后生物标志物,本发明根据KEGG通路分析及GO注释发现,GABRP在信号转导,化学突触传递和离子转运等生物学过程中富集,在质膜的组成成分、质膜、膜和投射神经元以及突触和神经活性配体-受体相互作用、PI3K-Akt信号通路中作用显著,是肿瘤微环境的可能调节剂,其作用机制与癌症耐药细胞显著相关性。
本发明中,氟尿嘧啶(5-Fu)是嘧啶类似物,属于抗代谢药的一种,现如今是治疗结直肠癌的主要药物,通过抑制胸腺嘧啶核苷酸合成酶,阻断脱氧嘧啶核苷酸转换成胸腺嘧啶核苷核,干扰DNA和RNA的合成,但其过多使用会造成细胞耐药。
本发明中,奥沙利铂(Oxaliplatin)为第3代铂类抗癌药,为二氨环己烷的铂类化合物,即以1,2-二氨环己烷基团代替顺铂的氨基。与其他铂类药作用相同,以DNA为靶作用部位,铂原子与DNA形成交叉联结,拮抗其复制和转录,与氟尿嘧啶(5-Fu)联合应用具有协同作用,过多使用会造成结直肠癌细胞耐药。但目前体外和体内研究表明,其与顺铂之间无交叉耐药性。
在整个说明书中提到的“实施方式”或“实施方案”或“在另一实施方案中”或“在某些实施方案中”或“在本申请的部分实施方式中”意指在至少一实施方案中包括与该实施方案所述的相关的具体参考要素、结构或特征。因此,在整个说明书中不同位置出现的短语“在一实施方案中”或“在实施方案中”或“在另一实施方案中”或“在某些实施方案中”或“在本申请的部分实施方式中”不必全部指同一实施方案。此外,具体要素或特征可以任何适当的方式在一个或多个实施方案中结合。
除非本申请中另外要求,在整个说明书和其后的权利要求书中,词语“包括(comprise)”及其英文变体例如“包括(comprises)”和“包括(comprising)”应解释为开放式的、含括式的意义,即“包括但不限于”。
应当理解,在本申请说明书和附加的权利要求书中用到的单数形式的冠词“一”(对应于英文“a”、“an”和“the”)包括复数的对象,除非文中另外明确地规定。
<靶点用途>
本发明可以将GABRP作为靶点制备治疗5-FU/奥沙利铂耐药性癌症的药物,包括但不限于GABRP抑制剂等。所述的抑制剂包括GABRP的RNA干扰载体、或其他能够抑制GABRP表达的或阻断GABRP与相应配体结合的抑制剂。
本发明可以将GABRP基因作为靶点,构建以GABRP缺失或差异性表达的细胞模型,用于筛选治疗5-FU/奥沙利铂耐药性癌症的药物。
<基因用途>
本发明中的GABRP基因还可作为基因治疗中的靶基因,设计并制备相关的生物学试剂,通过基因工程技术达到预防或治疗的目的。
<药物用途>
本发明提供以GABRP为靶点的药物在治疗5-FU/奥沙利铂耐药性癌症中的用途。
相应药物能够抑制GABRP的表达,从而降低肿瘤细胞及耐药性肿瘤细胞的增殖以达到治疗癌症的目的。
下面实施例用于说明而非限定本发明的确定方法。
实施例1、在人CRC化疗抗药和敏感患者的样本中筛选差异性表达因子,并对DEGs进行KEGG通路分析和GO注释
1.材料、方法
1.1方法
从基因表达综合数据库(GEO,http://www.ncbi.nlm.nih.gov/geo/)中下载了三个包括耐药性样本和敏感性样本的数据集,为GSE28691、GSE77932和GSE81006。GSE28691为将结直肠癌细胞打入老鼠体内,构建NOD/SCID(severe combined immune deficiency,SCID)小鼠给药结直肠癌临床前模型,找到介导人源CRC细胞耐药的机制,从而为CRC耐药患者或者CRC肿瘤患者提供给药方案参考。GSE77932数据集比较结直肠癌细胞DLD1敏感株和与其配对的HCT116的奥沙利铂耐药克隆的六株奥沙利铂耐药细胞源之间基因表达的差异。GSE81006在72小时的时间点比较了HCT-8野生型细胞(HCT8/WT)及其5-FU抗性细胞(HCT8/5-FU)之间的甲基化状态。调整后的p值<0.01或log2 Fold Change倍数变化(FC)>0.5的绝对值被设置为筛选结直肠敏感和耐药细胞系中DEGs的标准。然后,利用GEO2R在线工具和火山图分析DEGs,中间黑点代表没有区别的基因,右侧点代表上调基因,而左侧点代表下调基因。使用Venn图生成重叠的DEGs(http://bioinformatics.psb.ugent.be/webtools/Venn/)。京都基因和基因组百科全书(KEGG,http://www.genome.jp/)是一个知识数据库,用于识别与分子交互网络相关的DEG和信号通路,包括细胞或代谢过程,遗传或环境影响,人类疾病等。本发明使用注释、可视化和集成发现数据库(DAVID)在线工具(https://david.ncifcrf.gov/)来分析GO注释和KEGG通路富集,将来自三个数据集(GSE28691,GSE81006和GSE77932)的重叠基因导入DAVID在线工具,选择GO中的BP,CC,MF进行分析并导出结果,制作柱状图,并同样制作KEGG通路富集柱状图,得出与GABRP具有相关性的通路。依据经过本杰明矫正后的P值(<0.05)确定统计学显著性。
2.结果
为了筛选化疗耐药和化疗敏感的结直肠患者中的潜在差异性表达(DEGs),将GSE28691,GSE77932和GSE81006数据集相交。首先,GABRP在来自GSE28691和GSE81006数据集的3981个重叠基因中脱颖而出,其调整后的p值<0.01的选择条件由Venn图(图1的Fig1a)表示。其次,在跨越GSE28691和GSE77932的数据集时,GABA家族分子富集,log2 FoldChange倍数变化(FC)>0.5(图1的Fig 1b),本专利发现GABARAPL1、GABRB1、GABRA3、GABRQ重叠。参与GABA家族的GABRP是结直肠敏感和耐药细胞之间潜在的分化基因。图1的Fig 1c中,GSE77932数据集比较了DLD1敏感和其对应的奥沙利铂耐药细胞系,DLD1与SW480皆具有癌胚抗原阳性,角蛋白免疫过氧化物酶染色阳性,p53基因密码子突变引起氨基酸被替代,致癌基因c-Myc、Kras、Hras、Nras、Myb、Sis和Fos表达呈阳性等特点,可作为SW480的相似基因,预测结果与SW480相似;图1的Fig 1d中,GSE81006通过甲基化抑制基因转录,关闭基因开关。在72小时的时间点比较了HCT-8野生型细胞(HCT8/WT)及其5-FU抗性细胞(HCT8/5-FU)之间的甲基化状态。与HCT-8正常细胞相比,其耐药细胞部分基因上调,其中包含GABRP,故推测GABRP与结直肠癌细胞耐药相关。因此,本专利决定进一步在两种结直肠化疗耐药和化疗敏感性癌细胞中分析GABRP。
将3981个基因导入DAVID数据库进行GO和KEGG富集分析。图2的Fig2a结果表明,DEG主要参与基于FDR次序的生物过程,如信号转导、RNA聚合酶II启动子转录的正调控、炎症反应、对药物的反应、细胞迁移的正调控、细胞间信号传导、细胞内信号转导、轴突引导、化学突触传递、离子转运,其中,与对RNA聚合酶II启动子的转录进行正调控和信号传递相关的基因数量最多。图2的Fig2b显示,本发明的候选基因GABRP在三个生物学过程中富集:信号转导,化学突触传递和离子转运。在细胞组分方面,DEGs主要集中在细胞外泌体、质膜、细胞外区域、质膜的组成部分、细胞表面、膜、细胞质基质、细胞外空间、细胞质和投射神经元等,其中最为显著的是细胞质、细胞质基质以及细胞质膜。图2的Fig2c显示,与蛋白结合相关的基因数量最多,且与其他生物功能相比差异显著。本发明的目标基因GABRP在质膜的组成成分、质膜、膜和投射神经元中富集。KEGG通路分析富集在吞噬体、类风湿性关节炎、Th17细胞分化、松弛素信号通路、钙信号通路、人瘤病毒感染、轴突引导、PI3K-Akt信号通路、GABA能突触和神经活性配体-受体相互作用;GABRP与图中通路都具有一定相关性,且主要集中在脑组织神经活动配体-受体相互作用、PI3K-Akt信号通路、HPV感染(图2的Fig2d)。值得注意的是,本发明的柱状图所列举的最后两种通路中包含了GABRP。
实施例2:建立耐药CRC细胞系并验证GABRP在敏感和耐药CRC细胞上的表达
1材料、试剂、方法
1.1材料
细胞系来源:人SW480和HCT8 CRC细胞从中国科学院(www.cellbank.org.cn)购买并通过STR测序认证。细胞培养皿(康宁corning,美国)包括6孔板、12孔板、96孔板、6cm、10cm细胞培养盘,锡箔纸(恒康,中国),玻璃试管(国药,中国),细胞刮(奈斯nest,中国)本研究所用基因的序列:
β-actin上游引物:5′-GACCAATCCTGTCACCTC-3′(序列如SEQ ID NO:1所示);
β-actin下游引物:5′-GATCTCCGTTCCCATTAAGAG-3′(序列如SEQ ID NO:2所示);
GABRP下游引物:5′-GCCCTAACAGAGCCTCAACA-3′(序列如SEQ ID NO:3所示),GABRP下游引物:5′-TTGTCACTTCTGCCGACCTC-3′(序列如SEQ ID NO:4所示)。
蛋白marker(碧云天,中国)
1.2主要试剂
TRlzol(Invitrogen,美国),氯仿(国药,中国),异丙醇(国药,中国),乙醇(国药,中国),HiFiscript cDNA合成试剂盒(CWbio康为,中国),DEPC处理的RNAse free的水(生工,中国),TB green Premix Ex Taq II(Takara,日本),引物(生工,中国)。DMEM培养基(大连美仑,中国),1%青霉素/链霉素双抗(biosharp,中国)、磷酸盐缓冲液(1×PBS),胰蛋白酶-EDTA溶液(Biosharp,中国),10%FBS(胎牛血清)(NSERA,南非)。RPMI和DMEM培养基,1%青霉素/链霉素双抗、磷酸盐缓冲液(1×PBS),胰蛋白酶(Biosharp,中国),血清(Gibco,美国)。BCA蛋白定量试剂盒(碧云天,中国),BSA牛血清白蛋白(康为,中国)。1xlaemmli裂解液,聚丙烯凝胶电泳试剂盒(碧云天,中国)包括8%分离胶和5%浓缩胶,脱脂奶粉(碧云天,中国),PVDF膜(millipore,美国),actin内参抗体(翼飞雪,中国),EphA2抗体(cellsignaling,美国)TBST洗膜液(Biofund,中国),辣根过氧化物酶ECL显色试剂盒(碧云天,中国)。
1.3主要方法
1.3.1细胞培养
结直肠癌(CRC)细胞在杜贝克科的改良鹰培养基(DMEM)(美国西格玛)(Sigma,美国)中培养,其中含有10%FBS(胎儿牛血清)(NSERA,南非),并补充1%青霉素/链霉素抗生素(biosharp,中国)。将CRC细胞在5%CO
1.3.2建立化疗耐药细胞模型
接种对数生长期的SW480和HCT8细胞,并通过细胞活力测定法测定奥沙利铂和5-Fu的IC50值(前期初步数据)。使用略低于IC50的药物浓度作为起始刺激细胞的浓度,接下来循环递增药物浓度攻击CRC细胞使其逐渐耐药,细胞在数周的多个周期内被不同药物的增量剂量刺激。最后经过4-6个月的时间建立SW480-奥沙利铂(30uM)和HCT-8-5-Fu(20ug/ml)耐药细胞。两种CRC耐药细胞已经通过细胞活力测定,与其对应的敏感细胞相比,验证其耐药性,成功建立CRC耐药细胞模型。
1.3.3qPCR
收集SW480,HCT8及其对应的化疗耐药细胞裂解物并匀浆,通过TRIzol(英特洛,卡尔斯巴德,加利福尼亚州)收获总RNA。在每个样本中加入200μl氯仿充分震荡,静置后离心。吸取上层清液加入到异丙醇中,离心,弃上清。然后在每份样品中加入乙醇清洗,离心,弃上清,开盖晾干后加入DEPC水进行溶解。在Nano-one(中国,杭州)测定RNA样品的浓度ng/ul。然后使用HiFiscript cDNA合成试剂盒从1500ng总的RNA中逆转录cDNA20ul。根据说明书,加入TB green Premix Ex Taq II使用Thermal Cycler Bio-rad qPCR Cycler进行实时RT-PCR。经过β-actin基因表达水平归一化处理以后,进行定量分析。变性反应过程从50℃,反应2分钟开始,95℃,10分钟,再进入95℃30s,55℃30s的40个循环。熔融曲线程序为95℃15s,55℃1min。采用2
1.4Western Blot
用1xlaemmli裂解液获取细胞中的总蛋白,并用BCA蛋白质检测试剂盒检测其中蛋白质的浓度。每份蛋白质样品取6μg上样到5%浓缩胶中80V跑35分钟,然后在%SDS-PAGE分离胶中130V跑65分钟。将分离胶转移到PVDF膜上(4℃,83V,1.5小时)并用5%脱脂牛奶孵育1小时结合非特异性位点。将膜与GABRP(1:1000)和β-actin(1:2000)的一抗在4℃下孵育过夜。用TBST缓冲液洗膜3次,每次5分钟,然后与HRP偶联二抗(1:5000)在室温下孵育1小时,再洗膜4次,每次5分钟。免疫印迹化学发光底物试剂检测,并用Tannon天能公司的发光成像软件进行数据分析。
2.结果:图3的Fig3a显示,与奥沙利铂敏感细胞SW480相比,GABRP mRNA在奥沙利铂耐药细胞(即SW480-LOPH)中高表达,并且细胞中的GABRPmRNA表达量比SW480敏感CRC细胞显著增加2倍以上(***p<0.001)。有趣的是,如图3的Fig3b显示,GABRP在5-Fu耐药细胞HCT-8-5Fu中的高表达,至少是HCT-8敏感细胞株的1.5倍(*p<0.05)。β肌动蛋白作为内参基因。检测的GABRP基因均用统一内参作为参照计算的差异性。根据图3的Fig3c可知,GABRP的蛋白表达水平与转录水平一致,且与奥沙利铂敏感细胞SW480相较,奥沙利铂耐药细胞SW480-LOPH中的GABRP蛋白表达水平明显升高。由此可知,Fig3a、Fig3b、Fig3c实验结果相符,在CRC细胞耐药后,GABRP的表达量显著上调。这些结果表明,GABRP与结直肠癌细胞耐药性呈正相关。
实施例3:GABRP在结直肠癌患者中的临床相关性
1.方法
在Oncomine数据库中以TCGA数据为原始数据分析GABRP在各种癌症中的表达量。在Oncomine数据库中以Gyorffy提供的数据为原始数据比较GABRP在多种癌症(乳腺癌,结肠腺癌,胃癌和胰腺癌)中的表达量。在Oncomine数据库中以Skrzypczak提供的数据为原始数据分析GABRP在结直肠腺癌患者中与在正常结直肠组织中的表达量差异。数据分析采用ANOVA分析,并用箱线图表示最终分析结果。
2.结果
临床意义普适性的分析表明,本发明首先比较不同的癌症患者(如乳腺癌,结肠癌,胃癌和胰腺癌)组织中的GABRP的表达。很明显,与其他三种癌症类型相比,GABRP在结肠癌中显著过表达(图4的Fig4a)。当本发明聚焦到结直肠癌患者组中时,本发明发现大多数结肠癌和直肠癌患者检测到显著高表达GABRP水平(图4的Fig4b)。此外,结直肠腺癌的GABRP表达比正常结直肠组织中的GABRP表达至少上调两倍(图4的Fig4c)。在结直肠癌患者中,GABRP的高表达率或无病生存率相对低于GABRP低表达组。
恶性肿瘤与正常组织比,GABRP在恶性的肿瘤组织上显著高表达,推测结直肠癌细胞模型中建立的两种耐药CRC与药物敏感性CRC相比,恶性的耐药CRC上显著高表达GABRP。总的来说,与本发明在细胞系模型中的发现一致,临床数据支持GABRP在结直肠癌患者中的致癌作用。
实施例4、预测与基因GABRP的相互作用的蛋白
1.方法
本发明利用STRING数据库构建蛋白质-蛋白质互相作用(PPI)关系网络图。点击Search进入分析界面,选择Proteinby name,将“GABRP”分子作为蛋白质名称导入矩形框中,选择生物体物种为人,随后选择正确的GABRP分子,生成潜在蛋白质相互作用的关系网络。以中心基因GABRP为轴,其他具有潜在相互作用的蛋白通过连接线相连。每个基因都由一个单独的圆圈表示,蛋白质的二级结构呈现在圆圈内。连接线的数量代表了可能分子的相互作用的强度,且不同颜色的连接线代表不同的相互作用力,例如基因相邻,基因融合,共表达等。
2.结果
GABRP在普通PPI关系网络中为辐射中心,与10个圆圈和17条线相连(图5的Fig5a)。预测有十种蛋白质与GABRP相互作用:锚蛋白重复结构域66(ANKRD66),网格蛋白交互器1(CLINT1),亨廷顿蛋白相关蛋白1(HAP1),磷脂酶C类1(非活性)(PLCL1),GABAA型受体相关蛋白(GABARAP),GABAA型受体相关蛋白1(GABARAPL1),N-乙基马来酰亚胺敏感因子,囊泡融合ATP酶(NSF),GABA A型受体相关蛋白2(GABARAPL2),运输驱动蛋白2(TRAK2)和氯化物细胞内通道3(CLIC3)(图5的Fig5a)。该网络平均节点度为3.09,平均局部聚集系数为0.896,PPI富集P值为0.0389(具备显著差异)。其中,GABARAP、GABARAPL1两种蛋白与中心基因GABRP距离最近、连接线数目最多,说明二者与GABRP存在潜在互相作用的可能性最高。此外,本发明发现GABRP与GABARAP,GABARAPL1,ANKRD66,CLINT1和CLIII3的相互作用比上述分子更强,不仅指示更多连接线,彼此间距离也更近(图5的Fig5b)。因此,本发明富集具有高度相互作用的蛋白质,得出平均节点度为2,平均局部聚集系数为0.85的蛋白质相互作用网络(图5的Fig5b)。
- 用于检测与结直肠癌长春新碱耐药相关的miRNA表达的引物、试剂盒、方法及应用
- 与结直肠癌化疗药物耐药相关的靶点及应用
