一种肝靶向负载木犀草素纳米颗粒及构建和应用
文献发布时间:2023-06-19 19:27:02
技术领域
本发明属于纳米制剂技术领域,具体涉及一种肝靶向负载木犀草素纳米颗粒及构建和应用。
背景技术
在几乎所有年龄段和社会经济群体中,肥胖率均在急剧上升,肥胖已逐渐成为全球性的健康问题。根据最新统计数据,到2025年,全球肥胖症的男性患病率将达到18%,女性患病率将达到21%以上。肥胖症是许多代谢性疾病,如2型糖尿病、非酒精性脂肪肝、动脉粥样硬化和心血管疾病的危险因素。然而,目前的药物治疗效果有限,并存在多种副作用。因此,来自天然产物的具有更高安全性的生物活性化合物被认为是预防和治疗肥胖症的潜在替代品。
木犀草素(Lut)是一种大量存在于蔬菜、水果以及天然药草中的天然黄酮类化合物。研究表明,Lut具有改善胰岛素抵抗、降脂、抗炎、抗氧化、抗肿瘤以及免疫调节等作用。然而,Lut的水溶性较低,在人体胃肠道中迅速代谢,从而导致其生物利用度较低。肝脏是脂质和葡萄糖代谢的主要器官之一,参与脂质代谢的许多方面,是脂质合成、储存和释放的主要场所。然而,药代动力学研究表明,口服Lut后在肝组织中几乎检测不到。因此,利用肝靶向给药系统,增加肝脏中的Lut积累到有效的治疗浓度对于缓解肥胖症是非常必要的。
近年来,借助纳米颗粒较强的细胞穿透和靶向能力、高效的药代动力学、良好的生物相容性等优势,纳米颗粒已成为一种很有前途的新剂型。纳米颗粒给药系统可利用纳米载体粒径小、比表面积大、表面活性高、吸附能力强等特性,通过物理或化学作用,将活性化合物吸附或包埋在纳米给药系统上构成复合物。适当的表面修饰,可以使药物对特定器官或病灶具有靶向作用,显著提高药物的生物利用度,在保证药物效应的前提下降低给药剂量,从而减轻药物的毒副反应。由于外源性聚合物在肝脏中的积聚可能引起不良反应,因此使用生物相容的天然聚合物,如天然多糖变得很有吸引力。
近年来,基于多糖的生物功能性和识别作用,许多研究者已经开始合成和应用基于天然多糖自组装纳米颗粒的药物传递系统。近些年来已成功制备多糖纳米载体,其可有效靶向肥胖患者的脂肪组织巨噬细胞,从而达到肥胖症和相关并发症的高效靶向治疗。此外,酸敏感葡聚糖-阿霉素前药已被合成并用作治疗原位肝癌的自靶向给药系统。该多糖前药在癌肝组织中表现出超选择性积聚,在细胞内释放酸敏感性阿霉素,并且在体内具有高抗肿瘤效力。由此可见,多糖自组装形成的纳米颗粒具有广泛的应用空间和巨大的应用价值。桑叶多糖,为桑叶中主要活性成分之一,具有降血糖、降血脂、抗氧化等多种生物活性。本发明利用分离纯化得到的新型桑叶多糖作为聚合物封装材料,制备肝靶向负载木犀草素纳米颗粒。
发明内容
本发明的目的是提供一种肝靶向负载木犀草素纳米颗粒的构建及其应用,以解决上述现有技术存在的问题。
为了达到上述发明目的,本发明采用的技术方案如下:
一种肝靶向负载木犀草素纳米颗粒,以半乳糖/桑叶多糖-溶菌酶为包封载体,木犀草素为包封药物的Gal-MPL/Lut纳米颗粒,该纳米颗粒通过特异性识别唾液糖蛋白受体(ASGPR)来靶向肝细胞,增强Lut对肝组织的作用,载药率达到15±2%。
本发明的一种肝靶向负载木犀草素纳米颗粒的构建方法,包括如下步骤:
1)制备Gal-MP粉末和溶菌酶肽Lys M
Gal-MP粉末制备:
将4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
溶菌酶肽Lys M制备:
①.按照质量比1:10~50,将地衣芽孢杆菌蛋白酶(BLP)与溶菌酶(Lys)混合在Tris-HCl缓冲液中,使Lys水解;
②.将步骤①溶液用水稀释10~50倍,并使用磁力搅拌以形成溶菌酶肽(Lys M)溶液;
2)Lys M溶液处于搅拌状态下,将0.2~0.8mg/mL的木犀草素Lut乙醇溶液以1:2~1:8(v/v)的比例加入到Lys M溶液中,搅拌过夜;冷冻干燥,得到溶菌酶肽木犀草素复合物Lys M/Lut;
3)Lys M/Lut和Gal-MP以5:1~1:5的摩尔比于水中混合反应,用截留量为12KD的透析袋透析,将透析液冻干即为Gal-MPL/Lut纳米颗粒。
所述桑叶多糖是将桑叶粉末水提醇沉得到粗多糖,通过超滤柱得到30-80kDa多糖片段后,利用DEAE柱,在0.1MNaCl洗脱液下,获得桑叶多糖MP。
所述的4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
所述的pH通过HCl或NaOH调节至pH=4~6。
所述的Tris-HCl缓冲液条件是pH7.4、75mM。
所述的溶菌酶肽Lys M水解条件为:30~80℃下搅拌15-60分钟。
所述的溶菌酶肽Lys M制备的步骤②中磁力搅拌器时间为3~6小时。
本发明的肝靶向负载木犀草素纳米颗粒在抗肥胖和调节脂质代谢紊乱药物中的应用。
具体详细操作方法可以采用如下:
本发明的一种肝靶向负载木犀草素纳米颗粒的构建方法,包括如下步骤:
1)制备Gal-MP粉末和溶菌酶肽Lys M
Gal-MP粉末制备:
将4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
溶菌酶肽Lys M制备:
①.按照质量比1:10~50,将地衣芽孢杆菌蛋白酶(BLP)与溶菌酶(Lys)混合在Tris-HCl缓冲液中,使Lys水解;
②.将步骤①溶液用水稀释10~50倍,并使用磁力搅拌以形成溶菌酶肽(Lys M)溶液;
2)Lys M溶液处于搅拌状态下,将0.2~0.8mg/mL的木犀草素Lut乙醇溶液以1:2~1:8(v/v)的比例加入到Lys M溶液中,搅拌过夜;冷冻干燥,得到Lys M/Lut;
3)Lys M/Lut和Gal-MP以5:1~1:5的摩尔比于水中混合反应,用截留量为12KD的透析袋透析,将透析液冻干即为Gal-MPL/Lut纳米颗粒。
所述桑叶多糖是将桑叶粉末水提醇沉得到粗多糖,通过超滤柱得到30-80kDa多糖片段后,利用DEAE柱,在0.1MNaCl洗脱液下,获得桑叶多糖MP。
所述的4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
所述的pH通过HCl或NaOH调节至pH=4~6。
所述的Tris-HCl缓冲液条件是pH7.4、75mM。
所述的溶菌酶肽Lys M水解条件为:30~80℃下搅拌15-60分钟。
所述的溶菌酶肽Lys M制备的步骤②中磁力搅拌器时间为3~6小时。
本发明的肝靶向负载木犀草素纳米颗粒在抗肥胖和调节脂质代谢紊乱药物中的应用。
本发明制备的Gal-MPL/Lut纳米颗粒能有效将活性物质递送至肝细胞,增强肝细胞对活性物质Lut的摄取。图3的细胞摄取试验表明,纳米载体可提高Lut在肝细胞的摄取,增强纳米颗粒的肝脏靶向作用。
本发明制备的半乳糖苷靶向并负载Lut的纳米颗粒可与肝细胞表面过度表达的受体-去唾液酸糖蛋白受体(ASGPR)特异性结合,发挥其肝靶向性。
图4的油红O染色和图5的Bodipy染色结果表明,本发明制备的Gal-MPL/Lut纳米颗粒可显著抑制脂质积聚。
总之,本发明构建的Gal-MPL/Lut纳米颗粒可通过靶向作用在HepG2细胞中保留和积累,增加肝细胞中有效的Lut浓度,从而发挥抑制脂质积聚的作用,具有抗肥胖和调节脂质代谢紊乱等相关疾病的潜在应用前景。
附图说明
图1为本发明实施例1中的Gal-MLP和MLP的红外图谱。
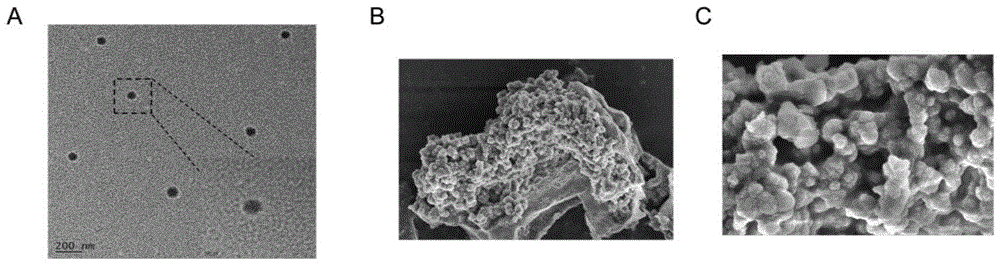
图2为本发明实施例4的纳米颗粒的透射电镜图和扫描电镜图。
(A)Gal-MPL/Lut纳米颗粒的透射电镜图(50×,200×);
(B-C)Gal-MPL/Lut纳米颗粒(500×,1000×)的扫描电镜图。
图3为本发明实施例5的Gal-MPL/Cy5和MPL/Cy5纳米颗粒的细胞摄取考察。
图4为本发明实施例6的纳米颗粒对HepG2细胞的油红O染色结果图。
图5为本发明实施例6的纳米颗粒对HepG2细胞的Bodipy染色结果图。
具体实施方式
下面结合具体实施方式,对本发明作进一步详细的描述,但本发明的实施方式并不限于此。
实施例1
Gal-MPL/Lut纳米颗粒的制备,包括如下步骤:
1)制备MP
将桑叶粉末水提醇沉得到粗多糖,通过超滤柱得到30-80kDa多糖片段后,利用DEAE柱,在0.1MNaCl洗脱液下,获得桑叶多糖MP。
2)制备Gal-MP粉末和溶菌酶肽Lys M
Gal-MP粉末制备:
将4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
溶菌酶肽Lys M制备:
①.按照质量比1:10,将地衣芽孢杆菌蛋白酶(BLP)与溶菌酶(Lys)混合在Tris-HCl缓冲液中,在30℃下搅拌15分钟,使Lys水解;
②.将步骤①溶液用水稀释10倍,并使用磁力搅拌器搅拌3小时以形成溶菌酶肽(Lys M)溶液;
3)Lys M溶液处于搅拌状态下,将0.2mg/mL的木犀草素Lut乙醇溶液以1:2(v/v)的比例加入到Lys M溶液中,搅拌过夜;冷冻干燥,得到Lys M/Lut;
4)Lys M/Lut和Gal-MP以5:1的摩尔比于水中混合反应,用截留量为12KD的透析袋透析48小时,将透析液冻干即为Gal-MPL/Lut纳米颗粒。
由图1可以看出,桑叶多糖MP的FT-IR图谱出现了O-H拉伸(3440cm
实施例2
Gal-MPL/Lut纳米颗粒的制备,包括如下步骤:
1)制备MP
将桑叶粉末水提醇沉得到粗多糖,通过超滤柱得到30-80kDa多糖片段后,利用DEAE柱,在0.1MNaCl洗脱液下,获得桑叶多糖MP。
2)制备Gal-MP粉末和溶菌酶肽Lys M
Gal-MP粉末制备:
将4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
溶菌酶肽Lys M制备:
①.按照质量比1:25,将地衣芽孢杆菌蛋白酶(BLP)与溶菌酶(Lys)混合在Tris-HCl缓冲液中,在60℃下搅拌40分钟,使Lys水解;
②.将步骤①溶液用水稀释20倍,并使用磁力搅拌器搅拌4小时以形成溶菌酶肽(Lys M)溶液;
3)Lys M溶液处于搅拌状态下,将0.4mg/mL的木犀草素Lut乙醇溶液以1:5(v/v)的比例加入到Lys M溶液中,搅拌过夜;冷冻干燥,得到Lys M/Lut;
4)Lys M/Lut和Gal-MP以2:1的摩尔比于水中混合反应,用截留量为12KD的透析袋透析48小时,将透析液冻干即为Gal-MPL/Lut纳米颗粒。
实施例3
Gal-MPL/Lut纳米颗粒的制备,包括如下步骤:
1)制备MP
将桑叶粉末水提醇沉得到粗多糖,通过超滤柱得到30-80kDa多糖片段后,利用DEAE柱,在0.1MNaCl洗脱液下,获得桑叶多糖MP。
2)制备Gal-MP粉末和溶菌酶肽Lys M
Gal-MP粉末制备:
将4-氨基苯基-β-D-吡喃半乳糖苷(Gal-NH
溶菌酶肽Lys M制备:
①.按照质量比1:50,将地衣芽孢杆菌蛋白酶(BLP)与溶菌酶(Lys)混合在Tris-HCl缓冲液中,在80℃下搅拌60分钟,使Lys水解;
②.将步骤①溶液用水稀释50倍,并使用磁力搅拌器搅拌6小时以形成溶菌酶肽(Lys M)溶液;
3)Lys M溶液处于搅拌状态下,将0.8mg/mL的木犀草素Lut乙醇溶液以1:8(v/v)的比例加入到Lys M溶液中,搅拌过夜;冷冻干燥,得到Lys M/Lut;
4)Lys M/Lut和Gal-MP以1:5的摩尔比于水中混合反应,用截留量为12KD的透析袋透析48小时,将透析液冻干即为Gal-MPL/Lut纳米颗粒。
实施例4
物理化学性质表征试验如下:
将Gal-MPL/Lut纳米颗粒配制成1mg/mL水溶液,利用动态光散射系统(Nano ZS90,Malvern),25℃下,分别检测纳米颗粒的粒径分布、ζ-电势和PDI分散指数。纳米颗粒形态特征使用透射电子显微镜(TEM,Tecnai G2 F20,FEI,USA)和扫描电子显微镜(SEM,ApreoS LoVac,ThermoFisher,USA)进行观察,获取放大倍数分别为50×、200×和500×和1000×的样本图像。
称取2mg纳米颗粒,将其溶解在甲醇中,制成1mg/mL溶液,超声提取Lut。然后在2500×g条件下离心15分钟,过滤上清液,通过高效液相色谱(HPLC)计算Gal-MPL/Lut纳米颗粒的包封率(EE,%)和载药率(LE,%)
本发明表明,该纳米粒子平均直径为65-85nm,ζ-电势为-20±5mV,分散指数PDI为0.2±0.05。由图2可以看出,TEM(图2A)和SEM(图2B-C)观察到Gal-MPL/Lut纳米颗粒为球形形状,大小均一。经HPLC检测,Gal-MPL/Lut纳米颗粒的EE(%)和LE(%)分别为85±5%和15±2%。
实施例5
细胞摄取试验如下:
为了评估本发明中实施例1获得的Gal-MPL/Lut纳米颗粒的细胞摄取效果,本发明利用亲脂性染料Cy5代替Lut加载到Lys M中作为荧光探针以进行荧光成像。将HepG2细胞接种到12孔板中,孵育24小时,之后将等量的Gal-MPL/Cy5和MPL/Cy5纳米颗粒(100mg/mL)给予细胞。孵育2小时后,PBS洗涤细胞三次以去除游离Cy5,最终利用流式细胞术测量Gal-MPL/Cy5和MPL/Cy5的细胞摄取率。
由图3可以看出,给予Gal-MPL/Cy5后,在HepG2细胞中出现了较大的Cy5荧光强度,而MPL/Cy5的荧光强度较弱,细胞摄取率由原有的25-30%提升至70-80%。这一发现表明,Gal-MPL较MPL纳米载体提高了细胞摄取,增强了纳米颗粒的肝脏靶向作用。
实施例6
脂质积聚试验如下:
以HepG2细胞为研究对象,分为四组,分别为:
将处于对数生长期的HepG2细胞用胰蛋白酶消化后,按照每孔8000个细胞的标准接种到96孔板中,并在培养箱中过夜培养。于第二日,取出96孔板,将其分为4个实验组,分别为:
空白对照组(简称Con组)
模型组(简称Mod组)
木犀草素组(简称Lut)
实施例1制备的Gal-MPL/Lut纳米颗粒组(简称Gal-MPL/Lut)
空白对照组用细胞培养液培养;
模型组和各给药组均用棕榈酸钠以诱导脂质积累模型。
脂质积聚模型建立:
将浓度为0.4mmol/L的棕榈酸钠溶于PBS缓冲溶液中,按照1:9的配比加入到含有4%无脂肪酸BSA的培养基中,并且60℃条件下水浴摇床振荡过夜。于第二天,按照1:1的比例将配置好的棕榈酸钠培养液加入到过夜培养的HepG2细胞96孔板中,并在培养箱中培养24h,以建立棕榈酸钠诱导的脂质积累模型。之后使用油红O染色试剂盒以及Bodipy(493/503)和DAPI(405/435)染料对HepG2细胞进行染色。
由图4可以看出,与Con组相比,在Mod组中观察到HepG2细胞的脂质积累有强烈的上升趋势,给予Lut和Gal-MPL/Lut纳米颗粒后,脂质积累均显著下调,且Gal-MPL/Lut纳米颗粒对脂质积聚抑制作用更为显著。
由图5可以看出,通过Bodipy染色,Gal-MPL/Lut纳米颗粒处理抑制了棕榈酸钠引起的脂质积聚,这种发现可以解释为Gal-MPL/Lut纳米颗粒在HepG2细胞中的积累和保留时间更长,从而增加肝细胞中的有效Lut浓度,增强其预防脂质积累的作用效果。
综上,本发明成功构建了肝靶向Gal-MPL给药系统,提高了肝脏有效的Lut作用浓度,为肝靶向新型给药系统的研发提供新的思路和方法。基于药理学和细胞分子生物学,阐释了Gal-MPL/Lut纳米颗粒的作用机制,为Gal-MPL/Lut纳米颗粒的应用奠定了理论基础。
本发明公开和提出的技术方案,本领域技术人员可通过借鉴本文内容,适当改变条件路线等环节实现,尽管本发明的方法和制备技术已通过较佳实施例子进行了描述,相关技术人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和技术路线进行改动或重新组合,来实现最终的制备技术。特别需要指出的是,所有相类似的替换和改动对本领域技术人员来说是显而易见的,他们都被视为包括在本发明精神、范围和内容中。
- 一种靶向线粒体的自组装蛋白质纳米颗粒的制备与应用
- 一种用作光/声敏剂的靶向纳米颗粒及其制备方法和应用
- 一种肝靶向的葡萄糖响应性纳米颗粒及其制备方法和应用
- 肝靶向的仿生细胞膜载药纳米颗粒及其制备方法和应用
