一种高稳定性的靶向接头-药物偶联物
文献发布时间:2023-06-19 19:28:50
技术领域
本发明属于药物领域,具体涉及一种高稳定性的靶向接头-药物偶联物。
背景技术
抗体-药物偶联物(Antibody-Drug Conjugate;ADC)能够选择性的向癌细胞输送药物,并杀死癌细胞,但是对正常细胞的影响较小,开创了肿瘤治疗的新纪元。ADC已有多个药物获得FDA批准上市,如CD33抗体连接卡奇霉素而成的Mylotarg,CD30抗体连接澳瑞他汀E而成的Adcetris用于霍奇金淋巴瘤和未分化大细胞淋巴瘤患者的治疗,Her2抗体和喜树碱衍生物Dxd连接而成的DS-8201用于HER2阳性的乳腺癌患者的治疗,以及靶向TROP-2抗原(也称作上皮糖蛋白1,EGP-1)的Sacituzumab govitecan用于三阴性乳腺癌。
迄今为止被FDA承认的ADC中含有的药物主要以DNA或微管蛋白为靶标。作为抗肿瘤的小分子化合物,已知作为抑制DNA拓扑异构酶I而达到抗肿瘤作用的喜树碱衍生物(如SN-38,Dxd,Dx-8951)在体内和体外均确认了对多种癌细胞有杀伤作用,显示出强抗肿瘤效果。作为抑制微管蛋白而达到抗肿瘤作用的化合物,如Eribulin,MMAE,MMAF,美登素等在体内和体外均确认了对多种癌细胞有杀伤作用,显示出强抗肿瘤效果。已知的可作用于DNA或微管蛋白的化合物结构式如下:
根据最经典的ADC药物作用机理,抗体-药物偶联物可以特异性的与细胞表面蛋白相结合,产生的结合物被细胞内吞,从而达到靶向输送药物分子至细胞内的作用。因此,细胞内药物的浓度直接跟细胞表面能够与抗体特异性识别的靶点的分布密度相关。遗憾的是分子表面能够与抗体识别的靶点密度通常较低,从而导致目标细胞内的药物浓度较低。为了解决这个问题,目前比较常用的方法是增加ADC的抗体-药物比例(Drug-antibodyratio,简称DAR),从而增加药物进入细胞内部的数量。然而,根据Hamblett等人(ClinCancer Res.2004,10,7063)的研究发现,增加ADC的DAR值通常会在药代动力学暴露中带来与预期相反的效果,ADC分子会发生严重的聚集现象,稳定性降低,导致血液中小分子毒素的增加,引起毒副作用。
第一三共株式会社自2013年以来提出了多项专利申请(CN201380053256.2、CN201910768778.X、CN201980061665.4等),公开了一系列具有特定连接子-毒素结构的抗体-药物偶联物,并具体公开了具有如下典型结构,展现出较优异效果的ADC。但是,其稳定性和治疗效果还有待进一步提高。
因此,开发出一种能够显著改善聚集现象,提高稳定性和治疗效果的能够靶向病变部位的药物偶联物具有重要意义。
发明内容
本发明的目的在于提供一种高稳定性的药物链接组装单元和靶向接头-药物偶联物。
本发明提供了一种药物链接组装单元、或其立体异构体、或其旋光异构体、或其盐、或其氘代物,所述药物链接组装单元由连接子和药物组成,连接子端能够与靶向接头连接,所述靶向接头为能够靶向结合病变部位的物质;连接子中包含式A所示的结构,式A所示的结构如式A-1所示:
其中,W
W
P
G
R
t
为无或共价键;当/>
t
k
a
a
R
b
本发明还提供了一种药物链接组装单元、或其立体异构体、或其旋光异构体、或其盐、或其氘代物,所述药物链接组装单元由连接子和药物组成,连接子端能够与靶向接头连接,所述靶向接头为能够靶向结合病变部位的物质;连接子中包含式A所示的结构,式A所示的结构如式A-1所示:
其中,W
W
P
G
R
t
为无或共价键;当/>
t
k
a
a
R
b
且当W
且当W
进一步地,式A所示的结构如式B-1所示:
其中,W
W
P
R
k
a
b
且当W
进一步地,式A所示的结构如式B-2所示:
其中,W
P
a
优选地,W
P
a
进一步地,式A所示的结构如式B-3所示:
其中,W
P
R
优选地,W
P
R
进一步地,式A所示的结构如式B-4所示:
其中,W
r
r
且当W
n’为1~40的整数,R’选自氢、甲基;
优选地,W
r
r
且当W
n’为1~30的整数,R’选自氢、甲基。
进一步地,式A所示的结构如式C-1所示:
其中,W
W
P
G
R
k
a
b
进一步地,式A所示的结构如式C-2所示:
其中,W
P
a
优选地,W
P
a
进一步地,式A所示的结构如式C-3所示:
其中,W
P
G
R
优选地,W
P
R
进一步地,式A所示的结构如式C-4所示:
其中,W
r
P
r
n’为1~40的整数,R’选自氢、甲基;
优选地,式A所示的结构如式C-5所示:
W
r
P
进一步地,式A所示的结构如式D-1所示:
其中,W
W
P
R
优选地,W
P
R
进一步地,式A所示的结构为:
/>
其中,n选自1~24的整数,R为氢或甲基,n’选自1~24的整数,R’为氢或甲基,a7选自1~24的整数,R
本发明还提供了一种药物链接组装单元、或其立体异构体、或其旋光异构体、或其盐、或其氘代物,所述药物链接组装单元由连接子和药物组成,连接子端能够与靶向接头连接,所述靶向接头为能够靶向结合病变部位的物质;连接子中包含式A所示的结构,式A所示的结构如式E-0所示:
其中,X、Y、Z分别独立选自N、N
r
r
r
r
r
K
N
R
R
进一步地,式A所示的结构如式E-1所示:
其中,X、Y、Z分别独立选自N、N
r
进一步地,:R
进一步地,式A所示的结构如式E-1-a或式E-1-a’所示:
其中,r
B
进一步地,式A所示的结构如式E-1-b所示:
其中,r
进一步地,式A所示的结构如式E-1-c所示:
其中,r
进一步地,式A所示的结构如式E-1-d所示:
其中,r
进一步地,式A所示的结构如式F-1所示:
其中,r
r
r
K
N
R
R
进一步地,式A所示的结构如式F-1-a所示:
其中,r
R
进一步地,式A所示的结构如式F-1-b所示:
其中,r
n’为1~40的整数,优选为9~16的整数,R’选自氢、甲基;
X
进一步地,式A所示的结构如式F-1-c所示:
其中,r
r
G
N
R
进一步地,式A所示的结构为:
/>
/>
n4选自1~24的整数,优选为9~16的整数,R3为氢或甲基,n’选自1~24的整数,优选为9~16的整数,R’为氢或甲基,n3选自1~24的整数,优选为3~16的整数,R
进一步地,所述连接子的结构如式G-1或式G-2所示:
其中,T是拴系基团,它能够与靶向接头连接;所述靶向接头为能够靶向结合病变部位的物质;
L
L
L
L
L
L
L
L
Z
Q的结构如式A所示。
进一步地,L
y
y
y
进一步地,所述连接子的结构如式G-3所示:
其中,T是拴系基团,它能够与靶向接头连接;所述靶向接头为能够靶向结合病变部位的物质;
L
L
L
L
Q的结构如式A所示。
进一步地,T的结构为:
进一步地,L
其中,x选自1~10的整数,优选为2~6的整数;
m选自1~25的整数,优选为2~10的整数;更优选为2~9的整数;
x
x
x
R
进一步地,L
L
其中,y、y’各自独立地选自1~10的整数,优选为1或2;
y
y
进一步地,L
其中,p选自1~24的整数,R
进一步地,L
更进一步地,上述连接子的结构选自:
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
-PEG
上述结构中右侧均为
进一步地,所述药物链接组装单元的结构如式G-4或式G-5所示:
/>
其中,T、Q、L
D
D
进一步地,D
优选地,D
更优选地,D
进一步地,所述药物链接组装单元的结构选自:
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
-PEG
本发明还提供了一种靶向接头-药物偶联物、或其立体异构体、或其旋光异构体、或其盐、或其氘代物,所述靶向接头-药物偶联物是由靶向接头和上述的药物链接组装单元连接所得,结构如式J-1所示;
/>
Ab为靶向接头;q为1~20的整数;
所述靶向接头为能够靶向结合病变部位的物质。
进一步地,所述靶向接头-药物偶联物的结构如式J-2或式J-3所示:
其中,Ab为靶向接头;q为1~20的整数;
T、L
优选地,所述靶向接头-药物偶联物的结构如式J-4所示:
Ab-(T-L
式J-4
其中,Ab为靶向接头;q为1~20的整数;
T、L
进一步地,所述靶向接头-药物偶联物的DAR值为1.00~20.00,优选为2.0~8.0,更优选为2.0~5.0。
进一步地,所述靶向接头-药物偶联物的结构选自:
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
q为1~20的整数;
-PEG
前述列举的具体靶向接头-药物偶联物根据实施例的检测结果标记了DAR值。
DAR值由于检测条件和检测人员的影响,测得的值存在误差范围。根据目前的检测手段,DAR值误差范围通常为±0.3,但是由于检测手段的变化,误差范围也可能变化。靶向接头-药物偶联物的关键核心在于结构式,只要结构式与前述列举的具体靶向接头-药物偶联物相同,则都在本发明保护范围内。
前述列举的具体靶向接头-药物偶联物在实施例采用的Ab是HER2抗体。
进一步地,所述靶向接头为抗体、抗体片段、蛋白质、小分子多肽、糖肽、模拟肽、小分子化合物或核酸寡核苷酸适配子;
优选地,所述抗体为针对细胞表面受体和肿瘤相关抗原的抗体。
本发明还提供了一种用于靶向接头-药物偶联物的连接子,或其立体异构体、或其旋光异构体、或其盐、或其氘代物,所述连接子的结构如式K-1或式K-2所示:
其中,T是拴系基团,它能够与靶向接头连接;所述靶向接头为能够靶向结合病变部位的物质;
L
L
L
L
L
L
L
L
R
R
Z
Q的结构如上文的式A所示。
进一步地,所述离去基团为羟基。
进一步地,L
y
y
y
进一步地,所述连接子的结构如式K-3所示:
T-L
式K-3
其中,T是拴系基团,它能够与靶向接头连接;所述靶向接头为能够靶向结合病变部位的物质;
L
L
L
L
R
Q的结构如上文的式A所示。
进一步地,T的结构为:
进一步地,L
其中,x选自1~10的整数,优选为2~6的整数;
m选自1~25的整数,优选为2~10的整数;更优选为2~9的整数;
x
x
x
R
进一步地,L
L
其中,y、y’各自独立地选自1~10的整数,优选为1或2;
y
y
进一步地,L
其中,p选自1~24的整数,R
进一步地,L
进一步地,所述连接子的结构为:
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
/>
-PEG
本发明还提供了一种预防和/或治疗肿瘤的药物制剂,它是以上述的靶向接头-药物偶联物、或其立体异构体、或其旋光异构体、或其盐、或其氘代物为活性成分,加上药学上可接受的辅料制成的制剂。
本发明还提供了上述的靶向接头-药物偶联物、或其立体异构体、或其旋光异构体、或其盐、或其氘代物在制备预防和/或治疗肿瘤的药物制剂中的用途。
进一步地,所述肿瘤选自肺癌、尿道癌、大肠癌、前列腺腺癌、卵巢癌、胰腺癌、乳腺癌、膀胱癌、胃癌、胃肠道间质瘤、宫颈癌、食道癌、鳞状细胞癌、腹膜癌、肝癌、结肠癌、直肠癌、结直肠癌、子宫癌、唾液腺癌、肾癌、外阴癌、甲状腺癌、阴茎癌、白血病、恶性淋巴瘤、浆细胞瘤、骨髓瘤或肉瘤。
本发明还提供了一种制备上述的靶向接头-药物偶联物、或其立体异构体、或其旋光异构体、或其盐、或其氘代物的方法,所述方法包括如下步骤:
(1)药物与连接子偶联得到药物链接组装单元;
(2)药物链接组装单元与靶向接头偶联得到靶向接头-药物偶联物;或,所述方法包括如下步骤:
(1')靶向接头与连接子偶联得到靶向接头-连接子单元;
(2')靶向接头-连接子单元与药物偶联得到靶向接头-药物偶联物。
本发明的药物链接组装单元能够与靶向接头连接,所述靶向接头为能够靶向结合病变部位的物质;所述药物链接组装单元由连接子和药物组成。
靶向接头和1~20个药物链接组装单元共价连接能够形成靶向接头-药物偶联物。当靶向接头为抗体时,该靶向接头-药物偶联物即抗体-药物偶联物(简称ADC)。
本发明中,“DAR值”表示靶向接头-药物偶联物中,一个靶向接头上偶联的药物链接组装单元的平均个数,相当于q值的平均值。DAR值可以不是整数。
关于本发明的使用术语的定义:除非另有说明,本文中基团或者术语提供的初始定义适用于整篇说明书的该基团或者术语;对于本文没有具体定义的术语,应该根据公开内容和上下文,给出本领域技术人员能够给予它们的含义。
碳氢基团中碳原子含量的最小值和最大值通过前缀表示,例如,前缀C
“芳基”指具有共轭的π电子体系的全碳单环或稠合多环(也就是共享毗邻碳原子对的环)基团,例如苯基和萘基。所述芳基环可以稠合于其它环状基团(包括饱和和不饱和环),但不能含有杂原子如氮,氧,或硫,同时连接母体的点必须在具有共轭的π电子体系的环上的碳原子上。芳基可以是取代的或未取代的。
“杂芳基”指包含一个到多个杂原子的杂芳族基团。这里所指的杂原子包括氧、硫和氮。例如呋喃基、噻吩基、吡啶基、吡唑基、吡咯基、N-烷基吡咯基、嘧啶基、吡嗪基、咪唑基、四唑基等。所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环。杂芳基可以是任选取代的或未取代的。
“氘代物”指化合物中的一个或两个以上的氢原子被氘替换后得到的化合物。
“靶向接头-药物偶联物”,是指由连接子将药物与具有靶向结合病变部位作用的靶向接头偶联,形成得到的偶联物。比如,“抗体-药物偶联物”(Antibody-Drug Conjugate;ADC),属于本发明靶向接头-药物偶联物的一种,其靶向接头为抗体或者抗体片段。
“药物链接组装单元”,是前述靶向接头-药物偶联物中的连接子与药物连接得到的产物,是制备靶向接头-药物偶联物的中间体,将其与靶向接头偶联即可得到靶向接头-药物偶联物。
“药物”或者代号为“D”、“D
“靶向接头”,是指具有靶向结合病变部位作用的物质,比如,抗体、抗体片段、蛋白质、小分子多肽、糖肽、模拟肽、小分子化合物或核酸寡核苷酸适配子。靶向接头可以与病变部位上的靶标(比如抗原)结合,使得靶向接头-药物偶联物能够靶向结合病变部位。
“抗体”是指机体由于抗原的刺激而产生的具有保护作用的蛋白质。当靶向接头为抗体或者抗体片段时,得到的靶向接头-药物偶联物为抗体-药物偶联物。本发明抗体或者抗体片段可以与病变部位的抗原结合,使得抗体-药物偶联物具有靶向结合病变部位的作用。抗体可以是任何蛋白或蛋白类分子,它可以结合或者络合或者与待治疗或生物改造的细胞群体的一部分发生反应。
本发明提供的实施例是采用Her2作为抗体来制备靶向接头-药物偶联物。
本发明中,组成抗体-药物偶联物的抗体最好保持其原有野生状态时的抗原结合能力。因此,在本发明中的抗体能够专一性的与抗原结合。涉及的抗原包括但不局限于肿瘤相关抗原(TAA),细胞表面受体蛋白和其他细胞表面分子,细胞存活调节因子,细胞增殖调节因子,与组织生长或分化相关的分子,淋巴因子,细胞因子,参与细胞循环调节的分子,参与血管生成的分子以及与血管生成相关的因子。肿瘤相关因子也可以是簇分化因子(如CD蛋白)。本发明中所述抗体结合的抗原可以是上述分类中一个或一个子集,而其他的子集则包括其他的具有特殊性质的分子/抗原。
应用于抗体-药物偶联物中的抗体包括但不局限于针对细胞表面受体和肿瘤相关抗原的抗体。这样的肿瘤相关抗原是本领域所熟知的,可以通过本领域公知的抗体制备方法和信息来制备。这些目标物能够特异性地表达在一种或多种癌症细胞表面,而在一种或者多种非癌细胞表面表达很少或不表达。通常,相对于非癌细胞表面而言,这样的肿瘤相关的多肽在癌细胞表面更加过度表达。确认这样的肿瘤相关因子,可大大提高基于抗体治疗癌症的专一靶向特性。
肿瘤相关抗原包括但不局限于,以下列出的肿瘤相关抗原。抗体靶向对应肿瘤相关的抗原包括所有的氨基酸序列变种和同种,与参考文献中确认的序列具有至少70%,80%,85%,90%或95%的同源性,或者具备与引用文献中的肿瘤相关抗原序列具有完全一致的生物性质和特性。
肿瘤相关抗原有:BMPR1B(Genbank登录号:NM-001203),E16(Genbank登录号:NM-003486),STEAP1(Genbank登录号:NM-012449),0772P(Genbank登录号:AF361486),MPF(Genbank登录号:NM-005823),Napi3b(Genbank登录号:NM-006424),Sema 5b(Genbank登录号:AB040878),PSCA hlg(Genbank登录号:AY358628),ETBR(Genbank登录号:AY275463),MSG783(Genbank登录号:NM-017763),STEAP2(Genbank登录号:AF455138),TrpM4(Genbank登录号:NM-017636),CRIPTO(Genbank登录号:NP-003203或NM-003212),CD21(Genbank登录号:M26004),CD79B(Genbank登录号:NM-000626),FcRH2(Genbank登录号:NM-030764),HER2(Genbank登录号:M11730),NCA(Genbank登录号:M18728),MDP(Genbank登录号:BC017023),IL20Rα(Genbank登录号:AF184971),Brevican(Genbank登录号:AF229053),EphB2R(Genbank登录号:NM-004442),GEDA(Genbank登录号:AY260763),BAFF-R(Genbank登录号:AF1164546),CD22(Genbank登录号:AK026467),CD79a(Genbank登录号:NP-001774.1),CXCR5(Genbank登录号:NP-001701.1),HLA-DOB(Genbank登录号:NP-002111.1),P2X5(Genbank登录号:NP-002552.2),CD72(Genbank登录号:NP-001773.1),LY64(Genbank登录号:NP-005573.1),FcRH1(Genbank登录号:NP-443170.1),IRTA2(Genbank登录号:NP-112571.1),TENB2(Genbank登录号:AF179274),CEA,B7H3,Her3,5T4,Claudin 18.2,FGFR2b,FRα,TROP2,B7H4,Nectin4,CD30,c-MET,EGFR,癌胚抗原相关细胞粘附分子5(CEACAM5),ROR1,CD20,肝细胞生长因子受体(HGFR),ROR2,IL3RA,间皮素受体,CD74,PD-L1。
本发明使用的抗体可以是前述抗原对应的抗体。
“连接子”,即linker,又叫做“接头”,是用于将具有治疗作用的化合物与靶向结合病变部位作用的靶向接头连接起来的物质。“连接子片段”是指连接子中的具有连接功能的部分结构。
按照细胞内药物释放机制,“连接子”可被分为两类:不可断裂连接子和可断裂连接子。
对于含不可断裂连接子的靶向接头-药物偶联物(如抗体-药物偶联物),其药物释放机制可以为:偶联物和抗原结合并被细胞内吞后,抗体在溶酶体中被酶解,释放出药物,连接子和抗体氨基酸残基共同组成的活性小分子。
而含可断裂连接子靶向接头-药物偶联物(如抗体-药物偶联物),则可以在目标细胞内断裂并释放出药物(如小分子药物自身)。可断裂连接子可分为两个主要的类别:化学不稳定连接子和酶不稳定连接子。化学不稳定连接子可以由于血浆和细胞质性质的不同而选择性的断裂,这样的性质包括PH值,谷胱甘肽浓度等。酶不稳定连接子,如肽连接子,能够被溶酶体内蛋白酶,如组织蛋白酶活纤溶酶有效的切断。肽连接子被认为在血浆中非常稳定。
连接子是靶向接头-药物偶联物(如抗体-药物偶联物)的核心部分,能够极大成都影响靶向接头-药物偶联物(如抗体-药物偶联物)的药代动力学、治疗指数和疗效。
本发明创造的关键正是对连接子的改进,具体在连接子中增加式A所示结构,使得连接子在具有传统连接子功能的基础上,还可以显著提升制备得到的靶向接头-药物偶联物(如抗体-药物偶联物)的安全性、稳定性、有效性、可控性,可以有效推进靶向接头-药物偶联物(如抗体-药物偶联物)药物的临床使用。
本发明实施例提供的靶向接头-药物偶联物包含靶向接头和1~20个共价连接的药物链接组装单元,其中药物链接组装单元可以通过与还原抗体中的链间二硫键产生的硫醇连接和/或每个链接组装单元与来自半胱氨酸残基的硫醇连接。
为了便于连接,药物链接组装单元通常在与靶向接头连接之前构建。不过,构建的顺序也可以改变。例如,先将具有保护基团的组装单元连接至靶向接头,在连接至靶向接头后去除保护基团并添加其他的药物单元。
本发明提供的靶向接头-药物偶联物,靶向特殊的细胞,比如肿瘤细胞,与细胞表面特异性蛋白(比如抗原)结合,结合物可以以内吞的形式进入细胞内,药物以活性形式释放到细胞内,发挥药效,或者在细胞外释放药物,药物渗入细胞内发挥药效。
本发明的有益效果:
通过在连接单元中引入式A所示结构,能够降低其与多种不同的药物单元、靶向接头连接构成的靶向接头-药物偶联物的聚体含量和裸抗百分比,维持靶向接头-药物偶联物的DAR值在适当范围内,提高靶向接头-药物偶联物的血浆稳定性、贮存稳定性,并提高疗效。
本发明提供的药物链接组装单元含有上述连接单元结构,也可发挥降低靶向接头-药物偶联物的聚体含量和裸抗百分比,维持靶向接头-药物偶联物的DAR值在恰当范围的作用。
最终制备得到的靶向接头-药物偶联物(如,抗体-药物偶联物)聚体含量和裸抗百分比低,DAR值合适,表现出优异的血浆稳定性、贮存稳定性和抗肿瘤作用,具有很好的临床应用前景。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
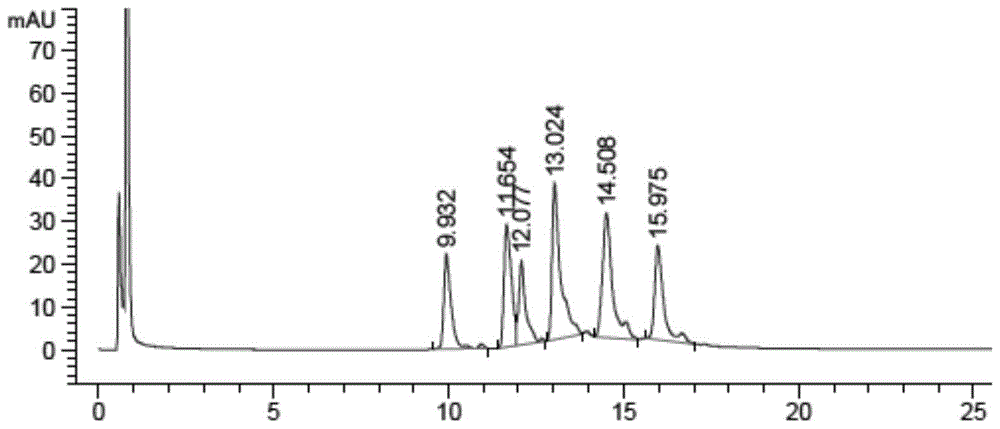
图1:SMP-93566a DAR值检测结果(RP-HPLC)。
图2:SMP-93566a聚体检测结果(SE-HPLC)。
图3:SMP-93566a裸抗检测结果(HIC)。
图4:SMP-88480a DAR值检测结果(RP-HPLC)。
图5:SMP-88480a聚体检测结果(SE-HPLC)。
图6:SMP-88480a裸抗检测结果(HIC)。
图7:单毒素ADC在人、猴、小鼠血浆中的血浆稳定性结果。
图8:双毒素ADC中Dxd在人、猴、小鼠血浆中的血浆稳定性结果。
图9:双毒素ADC中艾日布林在人、猴、小鼠血浆中的血浆稳定性结果。
图10:单毒素ADC对卵巢癌、胃癌、乳腺癌的体内肿瘤抑制效果。
图11:双毒素ADC对胃癌的体内肿瘤抑制效果。
本发明所用原料与设备均为已知产品,通过购买市售产品所得。
本发明提供的靶向接头-药物偶联物的结构,可以由本领域技术人员根据本领域常规技术知识和手段通过不同的方法策略合成得到,例如:
(1)先合成完整的连接子结构,然后进一步与靶向接头、药物偶联获得靶向接头-药物偶联物;
或,(2)以药物为起始结构,逐步偶联连接子片段,得到药物链接组装单元,然后进一步与靶向接头偶联获得靶向接头-药物偶联物;
或,(3)以靶向接头为起始结构,逐步偶联连接子片段,得到靶向接头-连接子单元,然后进一步与药物偶联获得靶向接头-药物偶联物。
本发明在以下实施例部分中提供了一种具体的制备靶向接头-药物偶联物的方法:
实施例部分
I.靶向接头-药物偶联物的制备
实施例1、中间体A的制备
步骤1:化合物A-2的制备
往500mL反应瓶中,加入A-1(20.0g,56.49mmol)和乙腈(200mL),室温搅拌。完全澄清后加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(11.0g,57.38mmol),N-羟基丁二酰亚胺(7.0g,60.82mmol),继续室温搅拌反应12小时,TLC显示反应完全。将反应体系过滤,所得固体真空干燥,得化合物A-2,重22.0g,收率86%。
步骤2:化合物A-3的制备
往500mL反应瓶中,加入L-苯丙氨酸(8.0g,48.48mmol),碳酸氢钠(8.0g,95.24mmol),水(200mL),室温搅拌。完全澄清后将化合物A-2(22.0g,48.78mmol)溶于乙二醇二甲醚(50mL)中,缓慢滴加到上述反应液中。加完后继续室温搅拌反应12小时,TLC显示反应完全。减压浓缩除去乙二醇二甲醚,剩余反应液滴加入0.5M盐酸水溶液(500mL)中,析出大量固体。过滤,所得固体真空干燥,得化合物A-3,重15.0g,收率61%。
1
步骤3:化合物A-4的制备
往500mL反应瓶中,依次加入A-3(15.0g,29.94mmol),乙腈(200mL),1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(6g,31.30mmol)和N-羟基丁二酰亚胺(4g,34.78mmol),室温搅拌反应12小时,TLC显示反应完全。将反应体系过滤,所得固体真空干燥,得化合物A-4,重13.0g,收率73%。
步骤4:化合物A-5的制备
往500mL反应瓶中,加入甘氨酸(3.0g,40.00mmol),碳酸氢钠(6.7g,79.76mmol)和水(150mL),室温搅拌。完全澄清后将化合物A-4(13.0g,21.74mmol)溶于乙二醇二甲醚(40mL)中,缓慢滴加到上述反应液中。加完后继续室温搅拌反应12小时,TLC显示反应完全,减压浓缩除去有机溶剂,剩余反应液滴加到0.5M盐酸水溶液(300mL)中,析出大量固体。过滤,所得固体真空干燥,得化合物A-5,重10.0g,收率83%。
1
步骤5:化合物A-6的制备
往25mL反应瓶中,依次加入A-5(200.0mg,0.36mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(163.0mg,0.43mmol),N,N-二异丙基乙胺(66.9mg,0.52mmol),N,N-二甲基甲酰胺(5mL),室温搅拌反应5min后加入艾立布林(263.1mg,0.36mmol)。继续室温搅拌十分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=10:1),得化合物A-6,重300.0mg,收率66%。
步骤6:化合物A的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),A-6(20.0mg,0.016mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(5.0mg,0.032mmol),室温搅拌反应30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物A,重10.0mg,收率60%。
1
实施例2、中间体B的制备
步骤1:化合物B-2的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(5mL),B-1(200.0mg,0.31mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(118.0mg,0.31mmol),N,N-二异丙基乙胺(50.0mg,0.39mmol),室温搅拌5min后加入伊喜替康(B-2,112.0mg,0.26mmol。搅拌十分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=10:1),得化合物B-3,重140.0mg,收率50%。
MS(ESI)m/z:1063[M+H]
步骤2:化合物B的制备
往25mL反应瓶中,加入N,N-二甲基甲酰胺(3mL),B-3(140.0mg,0.13mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(30.0mg,0.20mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩大部分N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物B,重70.0mg,收率64%。
MS(ESI)m/z:841[M+H]
1
实施例3、中间体C的制备
步骤1:化合物C-2的制备
往25mL反应瓶中依次加入化合物C-1(1.0g,4.90mmol),溶剂N,N-二甲基甲酰胺(15mL),室温搅拌。待反应液澄清后,依次加入碳酸钾(2.4g,17.4mmol),碘化钾(1.6g,9.64mmol),2-氯乙氧基乙醇(1.6g,12.90mmol),110℃搅拌12小时,TLC显示反应完全。将反应体系过滤,滤液减压浓缩,残余物经HPLC纯化得C-2,重1.5g,收率80%。
1
步骤2:化合物C-3的制备
冰浴下,往25mL反应瓶中依次加入二氯甲烷(10mL),C-2(1.5g,3.94mmol),丙烯酸叔丁酯(2.1g,16.40mmol),搅拌30分钟。再缓慢滴加50%的氢氧化钠水溶液(2.6g),加完后继续反应10分钟。撤去冰水浴,再在室温下反应3小时。LC-MS检测反应完全。用0.5M的稀盐酸调节pH 5~6,二氯甲烷萃取(10mL*3)。有机相用饱和食盐水洗涤,无水硫酸钠干燥,过滤,减压浓缩,得到目标产物C-,重1.7g,收率67%,直接用于下一步。
步骤3:化合物C-4的制备
往25mL反应瓶中,依次加入C-3(1.0g,1.57mmol),甲醇(10mL),钯碳(0.1g),氢气置换三次。反应体系在氢气环境下室温搅拌2小时。LC-MS显示反应完全,过滤除去钯碳,滤液减压浓缩,得化合物C-4,重800.0mg,收率93%,直接用于下一步。
1
步骤4:化合物C-5的制备
往25mL反应瓶中,依次加入C-4(800.0mg,1.46mmol),THF(10mL),水(2.5mL),室温搅拌。待反应液澄清后依次加入碳酸氢钠(184.0mg,2.19mmol),9-芴甲基-N-琥珀酰亚胺基碳酸酯(529.0mg,1.57mmol),室温搅拌2小时,LC-MS显示反应完全,减压浓缩,残余物经柱层析(二氯甲烷:甲醇=20:1)得化合物C-5,重1.0g,收率89%。
1
步骤5:化合物C-6的制备
往25mL反应瓶中,依次加入中间体C-5(1.0g,1.30mmol),二氯甲烷(5mL),三氟乙酸(5mL),室温反应2小时,LC-MS显示反应完全。减压浓缩,残余物经制备HPLC纯化得化合物C-6,重600.0mg,收率70%。
MS(ESI)m/z:657[M+H]
步骤6:化合物C-7的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),A(50.0mg,0.048mmol),C-6(65.0mg,0.10mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19.0mg,0.050mmol),N,N-二异丙基乙胺(13.0mg,0.10mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物C-7,重50.0mg,收率62%。MS(ESI)m/z:844[M/2+H]
步骤7:化合物C-8的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),C-7(30.0mg,0.018mmol),B(16.0mg,0.020mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(7.0mg,0.018mmol),N,N-二异丙基乙胺(3.0mg,0.023mmol),室温搅拌反应30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物C-8,重20.0mg,收率44%。MS(ESI)m/z:1255[M/2+H]
步骤8:化合物C的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),C-8(20.0mg,0.0080mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.45mg,0.016mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物C,重15.0mg,收率82%。
MS(ESI)m/z:1144[M/2+H]
实施例4、中间体D的制备
中间体D的合成方法参考化合物C的合成。
实施例5、中间体E的制备
步骤1:化合物E-2的制备
往25mL反应瓶中依次加入化合物D-1(1.2g,5.61mmol),溶剂N,N-二甲基甲酰胺(15mL),室温搅拌。待反应液澄清后,依次加入碳酸钾(2.6g,18.84mmol),碘化钾(1.9g,11.40mmol),溴代-七聚乙二醇-丙酸叔丁酯(6.3g,11.22mmol),90℃搅拌反应12小时,TLC显示反应完全.将反应体系过滤,滤液减压浓缩,残余物经HPLC纯化得中间体E-2,重2.0g,收率30%。MS(ESI)m/z:1175[M+H]
步骤2:化合物E-3的制备
往25mL反应瓶中加入化合物E-2(2.0g,1.70mmol),三氟乙酸(10mL),室温下搅拌0.5小时,LC-MS显示反应完全,减压浓缩除去的三氟乙酸,得中间体E-3,重1.0g,收率61%,直接用于下一步。
MS(ESI)m/z:964[M+H]
步骤3:化合物E-4的制备
往25mL反应瓶中,依次加入中间体E-3(600.0mg,0.62mmol),四氢呋喃(20mL),水(2.5mL),室温搅拌。待反应液澄清后依次加入碳酸氢钠(105.0mg,1.25mmol),9-芴甲基-N-琥珀酰亚胺基碳酸酯(252.0mg,0.75mmol)。室温搅拌1小时,LC-MS显示反应完全。减压浓缩,残余物经HPLC纯化得化合物E-4,重550.0mg,收率75%。
MS(ESI)m/z:1185[M+H]
步骤4:化合物E-5的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(4mL),A(50.0mg,0.048mmol),E-4(118.0mg,0.10mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19.0mg,0.05mmol),N,N-二异丙基乙胺(13.0mg,0.10mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经HPLC纯化得化合物E-5,重80.0mg,收率72%。MS(ESI)m/z:1108[M/2+H]
步骤5:化合物E-6的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),E-6(35.0mg,0.016mmol),B(16.0mg,0.019mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(7.0mg,0.018mmol),N,N-二异丙基乙胺(3.0mg,0.023mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经HPLC纯化得化合物E-6,重20.0mg,收率41%。
MS(ESI)m/z:1013[M/3+H]
步骤6:化合物E的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),E-6(20.0mg,0.0066mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.0mg,0.014mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经HPLC纯化得化合物E,重15.0mg,收率76%。
MS(ESI)m/z:1408[M/2+H]
实施例6、中间体Fa的制备
步骤1:化合物F-2的制备
往25mL反应瓶中依次加入化合物D-1(1.2g,5.61mmol),N,N-二甲基甲酰胺(15mL),室温搅拌。待反应液澄清后,依次加入碳酸钾(2.8g,0.29mmol),碘化钾(1.8g,10.84mmol),溴代-二聚乙二醇-丙酸叔丁酯(2.0g,6.73mmol),90℃搅拌12小时,TLC显示反应完全.将反应体系过滤,滤液减压浓缩,残余物经制备HPLC纯化得中间体F-2,重0.6g,收率25%。
MS(ESI)m/z:431[M+H]
1
步骤2:化合物F-3的制备
往25mL反应瓶中依次加入化合物F-2(600.0mg,1.40mmol),N,N-二甲基甲酰胺(15mL),室温搅拌。待反应液澄清后,依次加入碳酸钾(386.0mg,2.80mmol),碘化钾(232.0mg,1.40mmol),溴代-九聚乙二醇-丙酸叔丁酯(1.8g,2.77mmol),90℃搅拌12小时,TLC显示反应完全。将反应体系过滤,滤液减压浓缩。残余物经HPLC纯化,得中间体F-3,重870.0mg,收率62%。MS(ESI)m/z:999[M+H]
步骤3:化合物F-4的制备
往25mL反应瓶中加入化合物F-3(870.0mg,0.87mmol),三氟乙酸(3mL),室温下搅拌0.5小时,LC-MS显示反应完全。减压浓缩,得中间体F-4,重600.0mg,收率87%。直接用于下一步。
MS(ESI)m/z:787[M+H]
步骤4:化合物F-5的制备
往25mL反应瓶中,依次加入F-4(600.0mg,0.76mmol),四氢呋喃(10mL),水(2.5mL),室温搅拌。待反应液澄清后依次加入碳酸氢钠(128.0mg,1.52mmol),9-芴甲基-N-琥珀酰亚胺基碳酸酯(257.0mg,0.76mmol)。室温搅拌2小时,LC-MS显示反应完全。减压浓缩,残余物经HPLC纯化得化合物F-5,重660mg,收率86%。
MS(ESI)m/z:1009[M+H]
步骤5:化合物F-6a/F6-b的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(4mL),A(50mg,0.05mmol),F-5(101mg,0.10mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19mg,0.05mmol),N,N-二异丙基乙胺(13mg,0.10mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC,分别得化合物F-6a,重35mg,收率34%和化合物F-6b,重25mg,收率25%。
MS(ESI)m/z:1019[M/2+H]
步骤6:化合物F-7a的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),F-6a(35mg,0.017mmol),B(17mg,0.021mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(8mg,0.021mmol),N,N-二异丙基乙胺(3mg,0.023mmol),室温搅拌30分钟,TLC显示反应完全.减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物F-7a,重20.0mg,收率41%。MS(ESI)m/z:1430[M/2+H]
步骤6:化合物Fa的制备
往25mL反应瓶中,加入N,N-二甲基甲酰胺(2mL),F-7a(20.0mg,0.0070mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.0mg,0.010mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经HPLC纯化得化合物Fa,重15.0mg,收率81%。
MS(ESI)m/z:1319[M/2+H]
实施例7、中间体Fb的制备
/>
中间体Fb的合成方法参考化合物Fa的合成。
实施例8、中间体G的制备
中间体G的合成方法参考化合物A的合成。
MS(ESI)m/z:991[M+H]+.
1HNMR(400MHz,DMSO-d
实施例9、中间体H的制备
中间体H的合成方法参考化合物E的合成。
实施例10、中间体I的制备
/>
步骤1:化合物I-2的制备
往25mL反应瓶中,加入I-1(1.0g,5.15mmol),碳酸钾(1.4g,10.14mmol),N,N-二甲基甲酰胺(25mL),一次性加入PEG
MS(ESI)m/z:605[M+H]
1
步骤2:化合物I-3的制备
往25mL反应瓶中,加入I-2(1.0g,1.66mmol),碳酸钾(457.0mg,3.31mmol),N,N-二甲基甲酰胺(20mL),一次性加入溴乙酸叔丁酯(483.0mg,2.48mmol)室温搅拌1小时,LC-MS显示反应完全。反应体系过滤,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物I-3,重600.0mg,收率50%。
MS(ESI)m/z:719[M+H]
1
步骤3:化合物I-4的制备
往25mL反应瓶中,加入I-3(500.0mg,0.70mmol),钯碳(50.0mg),甲醇(10mL),氢气置换三次后,在氢气环境下室温搅拌1小时,LC-MS显示反应完全。反应体系过滤,减压浓缩除去甲醇,得化合物I-4,重360.0mg,收率88%。
MS(ESI)m/z:585[M+H]
步骤4:化合物I-5的制备
往25mL反应瓶中,加入I-4(360.0mg,0.62mmol),碳酸氢钠(103.0mg,1.23mmol),四氢呋喃(8mL),水(1mL),在0℃下缓慢加入N-甲氧基羰基马来酰亚胺(142.0mg,0.92mmol)。加入完毕后继续保持0℃反应10分钟,LC-MS显示反应完全。减压浓缩除去四氢呋喃和水,残余物经HPLC纯化得化合物I-5,重180.0mg,收率44%。
MS(ESI)m/z:665[M+H]
1
步骤5:化合物I的制备
往25mL反应瓶中,加入I-5(180.0mg,0.27mmol),三氟乙酸(3mL)。室温搅拌过夜,LC-MS显示反应完全。减压浓缩除去三氟乙酸,残余物经HPLC纯化得化合物I,重120.0mg,收率73%。
MS(ESI)m/z:609[M+H]
实施例11、中间体J的制备
步骤1:化合物J-2的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(5mL),A-1(130.0mg,0.37mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(164.0mg,0.43mmol),N,N-二异丙基乙胺(70.0mg,0.54mmol),室温搅拌反应5分钟后加入甘氨酸叔丁酯(56.0mg,0.43mmol)。继续反应25分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=20:1),得化合物J-2,重110.0mg,收率65%。
MS(ESI)m/z:468[M+H]
1
步骤2:化合物J-3的制备
往25mL反应瓶中加入化合物J-2(100.0mg,0.21mmol),三氟乙酸(2mL),室温下搅拌30分钟,LC-MS显示反应完全。减压浓缩,残余物经HPLC纯化得中间体J-3,重75.0mg,收率86%。
MS(ESI)m/z:412[M+H]
步骤3:化合物J-4的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),J-3(75.0mg,0.18mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(83.0mg,0.22mmol),N,N-二异丙基乙胺(35.0mg,0.27mmol),室温搅拌5min后加入艾立布林(138.0mg,0.19mmol)。继续搅拌10min,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备薄层色谱纯化(二氯甲烷:甲醇=10:1),得化合物J-4,重175.0mg,收率87%。
MS(ESI)m/z:1123[M+H]
步骤4:化合物J-5的制备
往25mL反应瓶中,加入N,N-二甲基甲酰胺(2mL),J-4(175.0mg,0.16mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(49.0mg,0.32mmol),室温搅拌15分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物J-5,重108.0mg,收率75%。
MS(ESI)m/z:901[M+H]
步骤5:化合物J-6的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),J-5(45.0mg,0.05mmol),C-6(66.0mg,0.10mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19.0mg,0.05mmol),N,N-二异丙基乙胺(13.0mg,0.10mmol),室温搅拌30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物J-6,重49.0mg,收率64%。MS(ESI)m/z:1539[M+H]
步骤6:化合物J-7的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(3mL),J-6(40.0mg,0.026mmol),B(26.0mg,0.031mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(12.0mg,0.031mmol),N,N-二异丙基乙胺(5.0mg,0.039mmol),室温搅拌反应30分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=12:1),得化合物J-6,重32.0mg,收率52%。
MS(ESI)m/z:1181[M/2+H]
步骤7:化合物J的制备
往25mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),J-7(32.0mg,0.014mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(3.0mg,0.020mmol),室温搅拌15分钟,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物J,重25.0mg,收率86%。
MS(ESI)m/z:1070[M/2+H]
实施例12、中间体K的制备
步骤1:化合物K-2的制备
往25mL反应瓶中,加入化合物K-1(601.0mg,1.00mmol),N,N-二甲基甲酰胺(5mL),再加入N,N-二异丙基乙胺(258.0mg,2.00mmol),然后一次性加入二(对硝基苯)碳酸酯(456.0mg,1.50mmol)室温搅拌反应过夜,TLC显示反应完全,将反应液缓慢滴加到甲基叔丁基醚(25mL)中,析出淡黄色固体。过滤所得固体真空干燥得化合物K-2,重580.0mg,收率76%。MS(ESI)m/z:767[M+H]
步骤2:化合物K-3的制备
往25mL反应瓶中,加入化合物K-2(300.0mg,0.39mmol),N,N-二甲基甲酰胺(5mL),室温搅拌。完全澄清后加入N,N-二异丙基乙胺(101.0mg,0.78mmol),1-羟基苯并三唑(27mg,0.20mmol),再一次性加入艾立布林(292.0mg,0.40mmol)室温搅拌2小时。LC-MS显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=15:1),得化合物K-3,重478.0mg,收率90%。
MS(ESI)m/z:1357[M+H]
步骤3:化合物K的制备
往25mL反应瓶中,加入N,N-二甲基甲酰胺(4mL),K-3(245mg,0.18mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(54.0mg,0.36mmol),室温搅拌20分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物K,重180.0mg,收率88%。
MS(ESI)m/z:1135[M+H]
实施例13、化合物SMP-22682的制备
步骤1:化合物SMP-22682-2的制备
往250mL反应瓶中,加入SMP-22682-1(3.0g,11.28mmol),二氯甲烷(30mL),冰水浴和氮气保护下加入草酰氯(5.7g,44.88mol),再缓慢滴加N,N-二甲基甲酰胺(0.1mL)。待滴加完毕后,室温下反应16小时,LC-MS显示原料基本反应完全。直接减压蒸馏除去溶剂以及多余的草酰氯,浓缩后加入少量甲苯,再次减压蒸馏后得到粗产品3.0g,直接用于下一步。
步骤2:化合物SMP-22682-4的制备
往250mL反应瓶中,加入SMP-22682-3(2.4g,0.01mol),三乙胺(4.0g,0.040mol),二氯甲烷(60mL。冰水浴下,缓慢滴加SMP-22682-2的二氯甲烷悬浊液(3.0g,粗品混合于20mL二氯甲烷中)。加完后继续搅拌10分钟,缓慢升温至室温,并保持室温下反应1小时。LC-MS显示有目标化合物分子量。将反应体系浓缩,粗产品经柱层析(二氯甲烷:甲醇=10:1)得化合物SMP-22682-4,重0.90g,两步收率17%。
MS(ESI)m/z:467[M+H]
1
步骤3:化合物SMP-22682-5的制备
往100mL反应瓶中,加入SMP-22682-4(0.90g,1.93mmol),再加入1M氢化铝锂的四氢呋喃溶液(20mL)。反应体系加热回流16小时,LC-MS显示大部分为目标化合物分子量。向反应液中分批加入十水硫酸钠(5.0g),过滤。滤液浓缩,所得粗产品经柱层析(乙酸乙酯:甲醇=5:1)得化合物SMP-22682-5,重0.50g,收率59%。
MS(ESI)m/z:439[M+H]
1
步骤4:化合物SMP-22682-6的制备
往100mL反应瓶中,加入乙腈(10mL),SMP-22682-5(500.0mg,1.14mmol),溴乙酸叔丁酯(178.0mg,0.91mmol),碳酸钾(126.0mg,0.91mmol)。室温搅拌1小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经柱层析(二氯甲烷:甲醇=10:1)得化合物SMP-22682-6,重240.0mg,收率48%。
MS(ESI)m/z:553[M+H]
1
步骤5:化合物SMP-22682-7的制备
/>
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),SMP-22682-6(75.0mg,0.14mmol),Mal-PEG4-acid(56.0mg,0.16mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(62.0mg,0.16mmol),N,N-二异丙基乙胺(26.0mg,0.20mmol),室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-22682-7,重65mg,收率56%。
MS(ESI)m/z:880[M+H]
步骤6:化合物SMP-22682-8的制备
往10mL反应瓶中,依次加入SMP-22682-7(65.0mg,0.074mmol),二氯甲烷(2mL),三氟乙酸(2mL)。室温搅拌16小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-22682-8,重40.0mg,收率66%。
MS(ESI)m/z:824[M+H]
步骤7:化合物SMP-22682的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-22682-8(10.0mg,0.012mmol),D(8.0mg,0.0037mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-22682,重2.2mg,收率20%。
MS(ESI)m/z:999[M/3+H]
实施例14、化合物SMP-07861的制备
/>
步骤1:化合物SMP-07861-1的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),SMP-22682-6(50.0mg,0.09mmol),马来酰亚胺己酸(23.0mg,0.11mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(41.0mg,0.11mmol),N,N-二异丙基乙胺(18.0mg,0.14mmol),室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-07861-1,重40.0mg,收率59%。
MS(ESI)m/z:746[M+H]
步骤2:化合物SMP-07861-2的制备
往10mL反应瓶中,依次加入SMP-07861-1(40.0mg,0.054mmol),二氯甲烷(2mL),三氟乙酸(2mL)。室温搅拌16小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-07861-2,重30.0mg,收率82%。
MS(ESI)m/z:690[M+H]
步骤3:化合物SMP-07861的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-07861-2(8.0mg,0.012mmol),D(8.0mg,0.0037mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-07861,重2.2mg,收率21%。
MS(ESI)m/z:954[M/3+H]
实施例15、化合物SMP-61694的制备
步骤1:化合物SMP-61694-1的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(2mL),SMP-22682-6(50.0mg,0.09mmol),Mal-PEG8-acid(57.0mg,0.11mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(41.0mg,0.11mmol),N,N-二异丙基乙胺(18.0mg,0.14mmol),室温搅拌1小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-61694-1,重20.0mg,收率21%。
MS(ESI)m/z:1056[M+H]
步骤2:化合物SMP-61694-2的制备
往10mL反应瓶中,依次加入SMP-61694-1(20.0mg,0.019mmol),二氯甲烷(1mL),三氟乙酸(1mL)。室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。浓缩,得到粗产品SMP-61694-2,重15.0mg,直接进行下一步。
MS(ESI)m/z:1000[M+H]
步骤3:化合物SMP-61694的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-61694-2(6.0mg,0.0060mmol),D(10.0mg,0.0046mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温搅拌1小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-61694,重6.8mg,收率47%。
MS(ESI)m/z:1057[M/3+H]
实施例16、化合物SMP-45539的制备
步骤1:化合物SMP-45539的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-07861-2(5.0mg,0.0073mmol),C(10.0mg,0.0044mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温搅拌20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-45539,重2.6mg,收率20%。
MS(ESI)m/z:986[M/3+H]
实施例17、化合物SMP-59034的制备
步骤1:化合物SMP-59034的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-61694-2(6.0mg,0.0060mmol),C(10.0mg,0.0044mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温搅拌1小时,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-45539,重2.8mg,收率20%。
MS(ESI)m/z:1090[M/3+H]
实施例18、化合物SMP-29438的制备
步骤1:化合物SMP-29438的制备
往10mL反应瓶中,依次加入N,N-二甲基甲酰胺(1mL),SMP-22682-8(5.0mg,0.0061mmol),C(10.0mg,0.0044mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.0053mmol),N,N-二异丙基乙胺(2.0mg,0.016mmol),室温反应20分钟,LC-MS显示大部分为目标化合物分子量。反应液浓缩,所得粗产品经制备HPLC纯化得化合物SMP-45539,重3.9mg,收率29%。
MS(ESI)m/z:1031[M/3+H]
实施例19、化合物SMP-49182的制备
/>
步骤1:化合物SMP-49182-2的制备
往250mL反应瓶中,加入SMP-49182-1(6.0g,27.03mmol),甲苯(60mL),于冰浴氮气保护下,加入草酰氯(13.7g,108.11mol),再滴加N,N-二甲基甲酰胺(0.1mL)。滴加完毕后,升温至60℃反应6小时,LC-MS显示原料基本反应完全。直接减压蒸馏除去溶剂以及多余的草酰氯,得到粗产品6.0g,直接用于下一步。
步骤2:化合物SMP-49182-4的制备
往250mL反应瓶中,加入SMP-49182-3(4.4g,23.16mmol),N,N-二异丙基乙胺(11.9g,92.66mmol),二氯甲烷(100mL)。冰水浴下,缓慢滴加SMP-49182-2的二氯甲烷悬浊液(6.0g,粗品混合于30mL二氯甲烷中)。继续搅拌10分钟后,缓慢升温至室温,并保持室温下反应1小时,LC-MS显示有目标化合物分子量。将反应体系浓缩。粗产品经柱层析(二氯甲烷:甲醇=10:1)得化合物SMP-49182-4,重1.6g,两步收率16%。
MS(ESI)m/z:379[M+H]
步骤3:化合物SMP-49182-5的制备
100mL反应瓶中,加入中间体SMP-49182-4(1.2g,3.17mmol),再加入1M氢化铝锂的四氢呋喃溶液(30mL),于油浴下回流反应16小时,LC-MS显示大部分为目标化合物分子量,将反应液降至室温后,向体系中加入十水硫酸钠(3.0g),继续搅拌30分钟,过滤,滤液减压浓缩除去溶剂得到粗产品,粗产品经柱层析(乙酸乙酯:甲醇=5:1,加入5%体积比的氨水)得化合物SMP-49182-5,重600mg,收率53.9%。
MS(ESI)m/z:351[M+H]
步骤4:化合物SMP-49182-6的制备
100mL反应瓶中,加入中间体SMP-49182-5(0.6g,1.71mmol),溴乙酸叔丁酯(0.3g,1.37mmol),碳酸钾(0.2g,1.37mmol),乙腈(10mL),于室温条件下反应1小时,LC-MS显示大部分为目标化合物分子量,反应液过滤,滤液减压浓缩,得到粗产品,粗产品经柱层析(二氯甲烷:甲醇=10:1)纯化得化合物SMP-49182-6,重0.3g,收率47.1%。
MS(ESI)m/z:465[M+H]
步骤5:化合物SMP-49182-7的制备
10mL反应瓶中,依次加入中间体SMP-49182-6(110.0mg,0.23mmol),N,N-二甲基甲酰胺(5mL),马来酰亚胺己酸(60.00mg,0.28mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(108.0mg,0.28mmol),N,N-二异丙基乙胺(46.0mg,0.35mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-49182-7,重90.0mg,收率59.5%。
MS(ESI)m/z:658[M+H]
步骤6:化合物SMP-49182-8的制备
10mL反应瓶中,依次加入SMP-49182-7(90.0mg,0.13mmol),二氯甲烷(2mL),三氟乙酸(2mL),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品加入少量乙腈溶解经制备HPLC纯化得化合物SMP-49182-8,重40.0mg,收率51.1%。MS(ESI)m/z:602[M+H]
步骤7:化合物SMP-49182的制备
10mL反应瓶中,依次加入SMP-49182-8(2.5mg,0.042mmol),中间体C(8.0mg,0.0035mmol),N,N-二甲基甲酰胺(1mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(1.6mg,0.0042mmol),N,N-二异丙基乙胺(0.7mg,0.053mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,除掉大部分溶剂后得到粗产品,粗产品经制备HPLC纯化得化合物SMP-49182,重6.4mg,收率63.7%。
MS(ESI)m/z:957[M/3+H]
实施例20、化合物SMP-40359的制备
步骤1:化合物SMP-40359-1的制备
10mL反应瓶中,依次加入中间体SMP-49182-6(120.0mg,0.26mmol),Mal-PEG4-acid(107.0mg,0.31mmol),N,N-二甲基甲酰胺(5mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(118.0mg,0.31mmol),N,N-二异丙基乙胺(50.0mg,0.38mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-40359-1,重80.0mg,收率38.9%。
MS(ESI)m/z:792[M+H]
步骤2:化合物SMP-40359-2的制备
10mL反应瓶中,依次加入SMP-40359-1(80.0mg,0.10mmol),二氯甲烷(2mL),三氟乙酸(2mL),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经加入少量乙腈溶解制备HPLC纯化得化合物SMP-40359-2,重40.0mg,收率54.4%。MS(ESI)m/z:736[M+H]
步骤7:化合物SMP-40359的制备
10mL反应瓶中,依次加入SMP-40359-2(5.8mg,0.0078mmol),中间体C(15.0mg,0.0066mmol),N,N-二甲基甲酰胺(1mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.0mg,0.0078mmol),N,N-二异丙基乙胺(1.3mg,0.0098mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-49182,重11.6mg,收率58.5%。
MS(ESI)m/z:1002[M/3+H]
实施例21、化合物SMP-93566的制备
步骤1:化合物SMP-93566-2的制备
100mL反应瓶中,依次加入中间体SMP-93566-1(1.0g,5.75mmol),溴乙酸叔丁酯(0.9g,4.60mmol),碳酸钾(0.6g,4.60mmol),N,N-二甲基甲酰胺(20mL),于室温条件下反应2小时,LC-MS显示大部分为目标化合物分子量,反应液过滤,滤液减压浓缩,得到粗产品,粗产品经柱层析(二氯甲烷:甲醇=12:1)纯化得化合物SMP-93566-2,重0.2g,收率15.1%。MS(ESI)m/z:289[M+H]
1
步骤2:化合物SMP-93566-3的制备
10mL反应瓶中,依次加入中间体SMP-93566-2(200.0mg,0.69mmol),马来酰亚胺丙酸(140.8mg,0.83mmol),N,N-二甲基甲酰胺(5mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(315.4mg,0.83mmol),N,N-二异丙基乙胺(134.2mg,1.04mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-93566-3,重220.0mg,收率72.6%。
MS(ESI)m/z:440[M+H]
步骤3:化合物SMP-93566-4的制备
25mL反应瓶中,依次加入SMP-93566-3(220.0mg,0.50mmol),二氯甲烷(5mL),三氟乙酸(5mL),于室温条件下反应2小时,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品加入少量乙腈溶解,经制备HPLC纯化得化合物SMP-93566-4,重90.0mg,收率47.0%。MS(ESI)m/z:384[M+H]
步骤4:化合物SMP-93566的制备
10mL反应瓶中,依次加入SMP-93566-4(8.8mg,0.023mmol),中间体A(20mg,0.019mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(8.7mg,0.023mmol),N,N-二异丙基乙胺(3.7mg,0.029mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-93566,重18.0mg,收率67.0%。
MS(ESI)m/z:1414[M+H]
1
实施例22、化合物SMP-88480的制备
步骤1:化合物SMP-88480的制备
10mL反应瓶中,依次加入SMP-93566-4(9.8mg,0.026mmol),中间体B(18.0mg,0.021mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(9.8mg,0.026mmol),N,N-二异丙基乙胺(4.1mg,0.032mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-88480,重12.0mg,收率47.4%。
MS(ESI)m/z:1206[M+H]
1
实施例23、化合物SMP-34048的制备
步骤1:化合物SMP-34048-2的制备
250mL反应瓶中,加入SMP-34048-1(1.0g,2.55mmol),二氯甲烷(75mL)。再加入二碳酸二叔丁酯(0.7g,3.32mmol),吡啶(6.1mL,75mmol),于室温条件下搅拌反应2小时。TLC显示反应完全,反应液依次用0.5N的盐酸水溶液(20mL*3)洗涤,再用饱和碳酸钠(20mL*3)洗涤,有机相用无水硫酸钠干燥,过滤,滤液减压浓缩得到粗产品SMP-34048-1,重1.2g,收率95.6%。
MS(ESI)m/z:493[M+H]
步骤2:化合物SMP-34048-3的制备
/>
250mL反应瓶中,加入SMP-34048-2(1.2g,2.44mmol),二氯甲烷(100mL),室温搅拌,再分批加入对硝基苯基氯甲酸酯(0.5g,2.68mmol),最后再加入4-二甲氨基吡啶(0.3g,2.44mmol),于此条件下继续搅拌反应2小时。TLC显示反应完全,反应液减压浓缩得到粗产品,粗产品经柱层析(二氯甲烷:甲醇=15:1)得到SMP-34048-3,重360.0mg,收率22.4%。
MS(ESI)m/z:658[M+H]
步骤3:化合物SMP-34048-4的制备
50mL反应瓶中,依次加入SMP-34048-3(360.0mg,0.55mmol),甲基(2-(甲基氨基)乙基)氨基甲酸叔丁酯(155.0mg,0.82mmol),N,N-二甲基甲酰胺(5mL),1-羟基苯并三唑(74.2mg,0.55mmol),N,N-二异丙基乙胺(140.6mg,1.09mmol),。于室温条件下搅拌反应30分钟。TLC显示反应完全,反应液减压浓缩得到粗产品,粗产品经柱层析(二氯甲烷:甲醇=12:1)纯化得到SMP-34048-4,重300.0mg,收率77.2%。
MS(ESI)m/z:707[M+H]
步骤4:化合物SMP-34048-5的制备
250mL反应瓶中,依次加入SMP-34048-4(300.0mg,0.42mmol),盐酸二氧六环溶液(10mL),于70℃油浴下搅拌反应1.5小时。TLC显示反应完全,反应液降至室温后,减压浓缩得到粗产品SMP-34048-5,重200.0mg,收率94.1%。
MS(ESI)m/z:507[M+H]
步骤5:化合物SMP-34048-6的制备
25mL反应瓶中,依次加入中间体B-1(225.7mg,0.35mmol),1H-苯并三唑-1-基氧三吡咯烷基六氟磷酸盐(182.0mg,0.35mmol),N,N-二甲基甲酰胺(5mL),N,N-二异丙基乙胺(59.8mg,0.46mmol),于室温条件下搅拌反应5分钟后,再加入SMP-34048-5(150.0mg,0.30mmol),反应液继续搅拌25分钟,TLC检测反应完全,反应液减压蒸馏除去N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇-10:1),制备HPLC纯化得化合物SMP-34048-6,重200.0mg,收率58.8%。
MS(ESI)m/z:1134[M+H]
步骤6:化合物SMP-34048-7的制备
25mL反应瓶中,依次加入SMP-34048-6(200.0mg,0.18mmol),N,N-二甲基甲酰胺(2mL),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(40.2mg,0.26mmol),于室温条件下反应30分钟,TLC监测反应完全,反应液减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-34048-7,重100.0mg,收率61.0%。
MS(ESI)m/z:912[M+H]
步骤7:化合物SMP-34048的制备
10mL反应瓶中,依次加入SMP-93566-4(9.2mg,0.024mmol),SMP-34048-7(18mg,0.020mmol),N,N-二甲基甲酰胺(2mL),1H-苯并三唑-1-基氧三吡咯烷基六氟磷酸盐(12.5mg,0.024mmol),N,N-二异丙基乙胺(3.9mg,0.030mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-34048,重8.0mg,收率31.3%。
MS(ESI)m/z:1277[M+H]
实施例24、化合物SMP-97962的制备
步骤1:化合物SMP-97962的制备
10mL反应瓶中,依次加入SMP-93566-4(4.6mg,0.012mmol),中间体G(10mg,0.010mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.6mg,0.012mmol),N,N-二异丙基乙胺(2.6mg,0.020mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-97962,重5.0mg,收率36.8%。
MS(ESI)m/z:679[M/2+H]
1
实施例25、化合物SMP-00171的制备
步骤1:化合物SMP-00171的制备
10mL反应瓶中,依次加入SMP-93566-4(19.4mg,0.051mmol),SMP-58054-2(50.0mg,0.042mmol),N,N-二甲基甲酰胺(4mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19.4mg,0.051mmol),N,N-二异丙基乙胺(8.2mg,0.064mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-00171,重59.0mg,收率90.6%。
MS(ESI)m/z:776[M/2+H]
实施例26、化合物SMP-24600的制备
步骤1:化合物SMP-24600-1的制备
10mL反应瓶中,依次加入SMP-93566-1(100.0mg,0.57mmol),单叔丁基琥珀酸酯(99.2mg,0.57mmol),N,N-二甲基甲酰胺(5mL),N,N-二异丙基乙胺(89.0mg,0.69mmol),于室温条件下缓慢滴加N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(197.6mg,0.52mmol,溶于1mLN,N-二甲基甲酰胺中),待滴加完毕后,继续反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-24600-1,重120.0mg,收率70.0%。
MS(ESI)m/z:331[M+H]
1
步骤2:化合物SMP-24600-2的制备
10mL反应瓶中,依次加入SMP-24600-1(120.0mg,0.36mmol),马来酰亚胺丙酸(73.7mg,0.44mmol),N,N-二甲基甲酰胺(3mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(165.8mg,0.44mmol),N,N-二异丙基乙胺(71.0mg,0.55mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-24600-2,重95.0mg,收率54.8%。
MS(ESI)m/z:482[M+H]
步骤3:化合物SMP-24600-3的制备
25mL反应瓶中,依次加入SMP-24600-2(55.0mg,0.11mmol),三氟乙酸(3mL),于室温条件下搅拌反应2小时,LC-MS显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化,得化合物SMP-24600-3,重25.0mg,收率53.5%。
MS(ESI)m/z:426[M+H]
步骤4:化合物SMP-24600的制备
10mL反应瓶中,依次加入SMP-24600-3(7.2mg,0.017mmol),中间体A(15.0mg,0.014mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(6.5mg,0.017mmol),N,N-二异丙基乙胺(2.7mg,0.021mmol),于室温条件下反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-24600,重12.0mg,收率59.0%。
MS(ESI)m/z:728[M/2+H]
实施例27、化合物SMP-36297的制备
步骤1:化合物SMP-36297-1的制备
10mL反应瓶中,依次加入SMP-22682-6(55.0mg,0.10mmol),中间体I(73.0mg,0.12mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(45.6mg,0.12mmol),N,N-二异丙基乙胺(19.4mg,0.15mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-36297-1,重50.0mg,收率43.7%。
MS(ESI)m/z:572[M/2+H]
步骤2:化合物SMP-36297-2的制备
25mL反应瓶中,依次加入中间体SMP-36297-1(50mg,0.044mmol),二氯甲烷(2mL),三氟乙酸(2mL),于室温条件下搅拌反应2小时,LC-MS显示反应完全,反应液减压浓缩,残余物经HPLC反相制备纯化得化合物SMP-36297-2,重30.0mg,收率62.7%。
MS(ESI)m/z:543.54[M/2+H]
步骤3:化合物SMP-36297的制备
10mL反应瓶中,依次加入SMP-36297-2(6.0mg,0.055mmol),中间体D(10mg,0.0045mmol),N,N-二甲基甲酰胺(1mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.1mg,0.0055mmol),N,N-二异丙基乙胺(0.9mg,0.0068mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-36297,重6.6mg,收率45.0%。
MS(ESI)m/z:1087[M/3+H]
实施例28、化合物SMP-12395的制备
步骤1:化合物SMP-12395-2的制备
100mL反应瓶中,加入中间体双甘肽(644.0mg,4.80mmol),碳酸氢钠(806.4,9.60mmol),水(2mL),四氢呋喃(20mL),室温搅拌,待溶液完全澄清后将化合物A-2(2.2g,4.80mmol)溶于乙二醇二甲醚(5mL)中,缓慢加入到上述反应液中。继续搅拌反应过夜,TLC显示反应完全,反应液减压浓缩,残余物滴入0.5M盐酸水溶液(200mL)中,析出大量固体,过滤,所得固体真空干燥,得化合物SMP-12395-2,重1.5g,收率66.7%。MS(ESI)m/z:469[M+H]
1
步骤2:化合物SMP-12395-3的制备
25mL反应瓶中加入化合物SMP-12395-2(420.0mg,0.90mmol)和溶剂四氢呋喃(5mL),室温搅拌,待溶液完全澄清后,依次加入四乙酸铅(480.0mg,1.07mmol)吡啶(107.2mg,1.34mmol),70℃搅拌反应过夜,TLC显示反应完全,反应液降至室温后过滤,滤液减压浓缩,残余物经柱层析(二氯甲烷:乙酸乙酯=2:1)纯化,得中间体SMP-12395-3,重290.0mg,收率67.0%。MS(ESI)m/z:482[M+H]
1
步骤3:化合物SMP-12395-4的制备
于100mL反应瓶中加入化合物SMP-12395-3(290.0mg,0.60mmol),溶剂四氢呋喃(25mL),羟基乙酸(50.0mg,0.66mmol),待反应液澄清后,于0℃下一次性加入对甲苯磺酸(51.0mg,0.30mmol)后室温搅拌反应1.5小时,TLC显示反应完全,过滤后减压浓缩除去多余的四氢呋喃,残余物经制备HPLC纯化得中间体SMP-12395-4,重190.0mg,收率63%。
MS(ESI)m/z:499[M+H]
步骤4:化合物SMP-12395-5的制备
于25mL反应瓶中,加入中间体SMP-12395-4(168.0mg,0.34mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(129.0mg,0.34mmol),N,N-二异丙基乙胺(55.0mg,0.43mmol),N,N-二甲基甲酰胺(8mL),室温搅拌反应5分钟后加入依喜替康甲磺酸盐(150.0mg,0.28mmol),继续搅拌25分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=8:1),得化合物SMP-12395-5,重200.0mg,收率78%。
MS(ESI)m/z:916[M+H]
步骤5:化合物SMP-12395-6的制备
于25mL反应瓶中,加入中间体SMP-12395-5(120.0mg,0.13mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(40.0mg,0.26mmol),N,N-二甲基甲酰胺(3mL),室温搅拌反应30分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得化合物SMP-12395-6,重65.0mg,收率72%。MS(ESI)m/z:694[M+H]
步骤6:化合物SMP-12395的制备
于10mL反应瓶中加入化合物SMP-93566-4(9.0mg,0.020mmol),溶剂N,N-二甲基甲酰胺(1.5mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.03mmol),室温下反应5分钟后,加入化合物SMP-12395-6(13.0mg,0.019mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物制备HPLC纯化,冻干后得白色固体SMP-12395,重5.8mg,收率29%。
MS(ESI)m/z:1059[M+H]
1
实施例29、化合物SMP-56822的制备
步骤1:化合物SMP-56822-2的制备
于100mL反应瓶中依次加入化合物SMP-56822-1(2.0g,4.4mmol),溶剂N,N-二甲基甲酰胺(30mL),于0℃下加入氢化钠(60wt%)(0.53g,13.20mmol),室温下反应10分钟后,一次性加入PEG
MS(ESI)m/z:1275[M+H]
步骤2:化合物SMP-56822-3的制备
于100mL反应瓶中依次加入化合物SMP-56822-2(4.0g,3.1mmol),溶剂四氢呋喃(32mL),于0℃下缓慢滴加1M氢化铝锂的四氢呋喃溶液(18.6mL,18.6mmol),待恢复到室温后加热至50℃搅拌反应2小时,LC-MS检测显示反应完全。0℃下分批加入十水硫酸钠(5.0g),过滤后减压浓缩除去多余的四氢呋喃,得中间体SMP-56822-3,重2.4g,收率79%。
MS(ESI)m/z:967[M+H]
步骤3:化合物SMP-56822-4的制备
于25mL反应瓶中依次加入化合物SMP-56822-3(630.0mg,0.65mmol),溶剂N,N-二甲基甲酰胺(5mL),待混合液完全澄清后依次加入碳酸钾(180.0mg,1.30mmol),溴乙酸叔丁酯(127.0mg,0.65mmol),室温搅拌反应2小时,TLC显示反应完全,过滤后减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化得中间体SMP-56822-4,重170.0mg,收率24%。
MS(ESI)m/z:1081[M+H]
步骤4:化合物SMP-56822-5的制备
于25mL反应瓶中加入化合物马来酰亚胺己酸(24.0mg,0.11mmol),溶剂N,N-二甲基甲酰胺(4mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(42.0mg,0.11mmol),N,N-二异丙基乙胺(17.0mg,0.13mmol),室温下反应5分钟后,加入化合物SMP-56822-4(102.0mg,0.094mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=20:1)纯化得中间体SMP-56822-5,重100.0mg,收率83%。
MS(ESI)m/z:1274[M+H]
步骤5:化合物SMP-56822-6的制备
于25mL反应瓶中加入化合物SMP-56822-5(100.0mg,0.08mmol),三氟乙酸(5mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-56822-6,重80.0mg,收率83%。
MS(ESI)m/z:1218[M+H]
步骤6:化合物SMP-56822的制备
于25mL反应瓶中加入化合物SMP-56822-6(30.0mg,0.025mmol),溶剂N,N-二甲基甲酰胺(4mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.032mmol),室温下反应5分钟后,加入化合物D(45.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化,冻干后得白色固体SMP-56822,重40.0mg,收率59%。
MS(ESI)m/z:1131[M/3+H]
实施例30、化合物SMP-82891的制备
步骤1:化合物SMP-82891-2的制备
于100mL反应瓶中依次加入化合物SMP-56822-1(2.0g,4.40mmol),溶剂N,N-二甲基甲酰胺(30mL),在0℃下加入氢化钠(60wt%)(0.5g,13.2mmol),室温下反应10分钟后,一次性加入PEG
MS(ESI)m/z:1804[M+H]
步骤2:化合物SMP-82891-3的制备
于100mL反应瓶中依次加入化合物SMP-82891-2(4.0g,2.2mmol),溶剂四氢呋喃(40mL),于0℃下缓慢滴加1M四氢铝锂的四氢呋喃溶液(13.2mL,13.2mmol),待回到室温后加热至50℃搅拌反应2小时,LC-MS检测显示反应完全。0℃下分批加入十水硫酸钠(5.0g),过滤后减压浓缩除去多余的四氢呋喃,残余物经柱层析(二氯甲烷:甲醇=8:1)纯化,得中间体SMP-82891-3,重2.4g,收率73%。
MS(ESI)m/z:1495[M+H]
步骤3:化合物SMP-82891-4的制备
于100mL反应瓶中依次加入化合物SMP-82891-3(2.4g,1.61mmol),溶剂N,N-二甲基甲酰胺(35mL),依次加入碳酸钾(443.0mg,3.21mmol),溴乙酸叔丁酯(314mg,1.61mmol),室温搅拌反应2小时,TLC显示反应完全,过滤后减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=12:1)纯化得中间体SMP-82891-4,重360.0mg,收率14%。MS(ESI)m/z:1609[M+H]
步骤4:化合物SMP-82891-5的制备
于25mL反应瓶中加入化合物3-(2-(2,5-二氧基-2,5二氢-1H-吡咯-1-基)乙氧基)丙酸(32.0mg,0.13mmol),溶剂N,N-二甲基甲酰胺(8mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(49.0mg,0.13mmol),N,N-二异丙基乙胺(21.0mg,0.16mmol),室温下反应5分钟后,加入化合物SMP-82891-4(170.0mg,0.11mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化得中间体SMP-82891-5,重150.0mg,收率74%。
MS(ESI)m/z:1849[M+H]
步骤5:化合物SMP-82891-6的制备
于25mL反应瓶中加入化合物SMP-82891-5(150.0mg,0.08mmol),三氟乙酸(4mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-82891-6,重130.0mg,收率90%。
MS(ESI)m/z:1793[M+H]
步骤6:化合物SMP-82891的制备
于25mL反应瓶中加入化合物SMP-82891-6(20.0mg,0.01mmol),溶剂N,N-二甲基甲酰胺(1.5mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.03mmol),N,N-二异丙基乙胺(4.0mg,0.03mmol),室温下反应5分钟后,加入化合物D(22.0mg,0.01mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化,得目标产物SMP-82891,重30.0mg,收率76%。
MS(ESI)m/z:1322[M/3+H]
实施例31、化合物SMP-51013-A的制备
步骤1:化合物SMP-51013-2的制备
于25mL反应瓶中加入化合物马来酰亚胺-二聚乙二醇-羧酸(29.0mg,0.11mmol),溶剂N,N-二甲基甲酰胺(3mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(41.0mg,0.11mmol),N,N-二异丙基乙胺(17.0mg,0.13mmol),室温下反应5分钟后,加入化合物SMP-56822-4(102.0mg,0.092mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=12:1)纯化得中间体SMP-51013-2,重100.0mg,收率84%。
MS(ESI)m/z:1320[M+H]
步骤2:化合物SMP-51013-3的制备
于25mL反应瓶中加入化合物SMP-51013-2(100。0mg,0.076mmol),溶剂三氟乙酸(4mL),室温下搅拌反应30分钟,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-51013-3,重80.0mg,收率83%。
MS(ESI)m/z:1264[M+H]
步骤3:化合物SMP-51013-A的制备
于10mL反应瓶中加入化合物SMP-51013-3(20.0mg,0.016mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物Fa(35.0mg,0.013mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-51013-A,重30.0mg,收率62%。MS(ESI)m/z:1295[M/3+H]
实施例32、化合物SMP-51013-B的制备
步骤1:化合物SMP-51013-B的制备
于10mL反应瓶中加入化合物SMP-51013-3(20.0mg,0.016mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物Fb(35.0mg,0.013mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-51013-B,重28.0mg,收率72%。MS(ESI)m/z:1295[M/3+H]
实施例33、化合物SMP-36256的制备
步骤1:化合物SMP-36256的制备
于25mL反应瓶中加入化合物SMP-56822-6(20.0mg,0.016mmol),溶剂N,N-二甲基甲酰胺(1.5mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物C(45.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-36256,重40.0mg,收率57%。
MS(ESI)m/z:1162[M/3+H]
实施例34、化合物SMP-45582的制备
步骤1:化合物SMP-45582的制备
于10mL反应瓶中加入化合物SMP-51013-3(25.0mg,0.020mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物E(60.0mg,0.021mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-45582,重48.0mg,收率59%。MS(ESI)m/z:1354[M/3+H]
实施例35、化合物SMP-01984的制备
步骤1:化合物SMP-01984-1的制备
于25mL反应瓶中加入化合物马来酰亚胺-8聚乙二醇-羧酸(57.0mg,0.11mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(41.0mg,0.11mmol),N,N-二异丙基乙胺(17.0mg,0.14mmol),室温下反应5分钟后,加入化合物SMP-56822-4(102.0mg,0.094mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化得中间体SMP-01984-1,重100.0mg,收率67%。
MS(ESI)m/z:1584[M+H]
步骤2:化合物SMP-01984-2的制备
于25mL反应瓶中加入化合物SMP-01984-1(100.0mg,0.063mmol),三氟乙酸(3mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-01984-2,重82.0mg,收率85%。
MS(ESI)m/z:1528[M+H]
步骤3:化合物SMP-01984的制备
于10mL反应瓶中加入化合物SMP-01984-2(35.0mg,0.023mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物C(60.0mg,0.026mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-01984,重48.0mg,收率55%。MS(ESI)m/z:1266[M/3+H]
实施例36、化合物SMP-30920的制备
步骤1:化合物SMP-30920-1的制备
于25mL反应瓶中加入化合物马来酰亚胺-6聚乙二醇-羧酸(48.0mg,0.11mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(41.0mg,0.11mmol),N,N-二异丙基乙胺(17.0mg,0.13mmol),室温下反应5分钟后,加入化合物SMP-56822-4(102mg,0.094mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化,得中间体SMP-30920-1,重98.0mg,收率70%。
MS(ESI)m/z:1496[M+H]
步骤2:化合物SMP-30920-2的制备
于25mL反应瓶中加入化合物SMP-30920-1(95.0mg,0.063mmol),三氟乙酸(3mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-30920-2,重80.0mg,收率88%。
MS(ESI)m/z:1440[M+H]
步骤3:化合物SMP-30920的制备
于10mL反应瓶中加入化合物SMP-30920-2(29.0mg,0.020mmol),溶剂N,N-二甲基甲酰胺(1.5mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.03mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物C(60.0mg,0.026mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-30920,重43.0mg,收率58%。
MS(ESI)m/z:1236[M/3+H]
实施例37、化合物SMP-14324的制备
步骤1:化合物SMP-14324的制备
于10mL反应瓶中加入化合物SMP-51013-3(13.0mg,0.010mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.0mg,0.029mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物C(22.0mg,0.0096mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-14324,重26.0mg,收率73%。MS(ESI)m/z:1178[M/3+H]
实施例38、化合物SMP-61393的制备
步骤1:化合物SMP-61393的制备
于10mL反应瓶中加入化合物SMP-51013-3(13.0mg,0.011mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(4.0mg,0.011mmol),N,N-二异丙基乙胺(2.0mg,0.014mmol),室温下反应5分钟后,加入化合物H(22.0mg,0.009mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-61393,重24.0mg,收率74%。MS(ESI)m/z:1207[M/3+H]
实施例39、化合物SMP-33693的制备
步骤1:化合物SMP-33693-2的制备
于50mL反应瓶中依次加入化合物SMP-33693-1(1.0g,1.75mmol),33%的溴化氢醋酸溶液(15mL),待反应液澄清后加入苯酚(494.0mg,5.25mmol),室温下反应12小时后,LC-MS检测显示完全反应,将反应液缓慢滴加到甲基叔丁基醚(20mL),有白色固体析出,过滤,收集滤饼,干燥得到目标产物SMP-33693-2,重300.0mg,收率66%。
MS(ESI)m/z:263[M+H]
步骤2:化合物SMP-33693-3的制备
于25mL反应瓶中依次加入化合物SMP-33693-2(300.0mg,1.15mmol),溶剂N,N-二甲基甲酰胺(10mL),依次加入碳酸钾(316.0mg,2.30mmol),溴乙酸叔丁酯(224.0mg,1.15mmol),室温搅拌反应4小时,TLC显示反应完全,过滤后减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=12:1)纯化得中间体SMP-33693-3,重130.0mg,收率30%。MS(ESI)m/z:377[M+H]
1
步骤3:化合物SMP-33693-4的制备
于25mL反应瓶中加入化合物马来酰亚胺己酸(87.0mg,0.41mmol),溶剂N,N-二甲基甲酰胺(5mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(156.0mg,0.41mmol),N,N-二异丙基乙胺(66.0mg,0.51mmol),室温下反应5分钟后,加入化合物SMP-33693-3(130.0mg,0.34mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=20:1)纯化得中间体SMP-33693-4,重150.0mg,收率77%。
MS(ESI)m/z:570[M+H]
1
步骤4:化合物SMP-33693-5的制备
于25mL反应瓶中加入化合物SMP-33693-4(100.0mg,0.18mmol),三氟乙酸(3mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-33693-5,重80.0mg,收率89%。
MS(ESI)m/z:514[M+H]
步骤5:化合物SMP-33693的制备
于10mL反应瓶中加入化合物SMP-33693-5(20.0mg,0.039mmol),溶剂N,N-二甲基甲酰胺(4mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(15.0mg,0.039mmol),N,N-二异丙基乙胺(6.0mg,0.047mmol),室温下反应5分钟后,加入化合物A(40.0mg,0.038mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-33693,重48.0mg,收率78%。
MS(ESI)m/z:1544[M+H]
实施例40、化合物SMP-52573的制备
步骤1:化合物SMP-52573的制备
于10mL反应瓶中加入化合物SMP-33693-5(20.0mg,0.039mmol),溶剂N,N-二甲基甲酰胺(2mL),待反应液完全澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(15.0mg,0.039mmol),N,N-二异丙基乙胺(6.0mg,0.047mmol),室温下反应5分钟后,加入化合物G(40.0mg,0.040mmol)搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得到目标产物SMP-52573,重45.0mg,收率75%。
MS(ESI)m/z:1487[M+H]
实施例41、化合物SMP-42930的制备
步骤1:化合物SMP-42930-1的制备
于25mL反应瓶中加入化合物马来酰亚胺丁酸(103.0mg,0.56mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(212.0mg,0.55mmol),N,N-二异丙基乙胺(91.0mg,0.71mmol),室温下反应5分钟后,加入化合物SMP-33693-3(176.0mg,0.47mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=20:1)纯化得中间体SMP-42930-1,重185.0mg,收率72%。
MS(ESI)m/z:542[M+H]
步骤2:化合物SMP-42930-2的制备
于25mL反应瓶中加入化合物SMP-42930-1(100.0mg,0.18mmol),三氟乙酸(4mL),室温下搅拌反应3小时,LC-MS显示反应完全,减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化得中间体SMP-42930-2,重80.0mg,收率89%。
MS(ESI)m/z:486[M+H]
步骤3:化合物SMP-42930的制备。
于10mL反应瓶中加入化合物SMP-42930-2(19.0mg,0.039mmol),溶剂N,N-二甲基甲酰胺(2mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(15.0mg,0.039mmol),N,N-二异丙基乙胺(6.0mg,0.047mmol),室温下反应5分钟后,加入化合物A(40.0mg,0.038mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-42930,重42.0mg,收率73%。
MS(ESI)m/z:1516[M+H]
实施例42、化合物SMP-80439的制备
步骤1:化合物SMP-80439的制备
于10mL反应瓶中加入化合物SMP-42930-2(20.0mg,0.041mmol),溶剂N,N-二甲基甲酰胺(3mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(15.0mg,0.039mmol),N,N-二异丙基乙胺(6.0mg,0.047mmol),室温下反应5分钟后,加入化合物G(40.0mg,0.038mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-80439,重42.0mg,收率76%。
MS(ESI)m/z:1458[M+H]
实施例43、化合物SMP-81404的制备
步骤1:化合物SMP-81404的制备
于10mL反应瓶中加入化合物SMP-01984-2(42.0mg,0.024mmol),溶剂N,N-二甲基甲酰胺(3mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入化合物J(43.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-81404,重57.0mg,收率78%。MS(ESI)m/z:1217[M/3+H]
实施例44、化合物SMP-64906的制备
步骤1:化合物SMP-64906的制备
于10mL反应瓶中加入中间体SMP-66348-2(39.0mg,0.024mmol),溶剂N,N-二甲基甲酰胺(4mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入中间体Fa(52.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-64906,重55.0mg,收率65%。
MS(ESI)m/z:1413[M/3+H]
实施例45、化合物SMP-66348的制备
步骤1:化合物SMP-66348-1的制备
于25mL反应瓶中加入中间体I(61.0mg,0.10mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(38.0mg,0.10mmol),N,N-二异丙基乙胺(15.0mg,0.12mmol),室温下反应5分钟后,加入化合物SMP-56822-4(95.0mg,0.08mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=12:1)纯化得到目标产物SMP-66348-1,重80.0mg,收率60%。
MS(ESI)m/z:1671[M+H]
步骤2:化合物SMP-66348-2的制备
于25mL反应瓶中,加入中间体SMP-66348-1(50.0mg,0.03mmol),三氟乙酸(3mL)。室温搅拌反应30分钟,LC-MS显示反应完全,过滤后减压浓缩除去三氟乙酸,残余物经制备HPLC得化合物SMP-66348-2,重35.0mg,收率72%。
MS(ESI)m/z:1615[M+H]
步骤3:化合物SMP-66348的制备
于10mL反应瓶中加入中间体SMP-66348-2(39.0mg,0.024mmol),溶剂N,N-二甲基甲酰胺(3mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温下反应5分钟后,加入中间体Fb(52.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-66348,重60.0mg,收率71%。
MS(ESI)m/z:1413[M/3+H]
实施例46、化合物SMP-34421的制备
步骤1:化合物SMP-34421-2的制备
于50mL反应瓶中,加入中间体SMP-34421-1(200.0mg,0.50mmol),N,N-二甲基甲酰胺(10mL),完全澄清后加入PEG
MS(ESI)m/z:811[M+H]
1
步骤2:化合物SMP-34421-3的制备
于25mL反应瓶中,加入中间体马来酰亚胺-二聚乙二醇-羧酸(22.0mg,0.086mmol),N,N-二甲基甲酰胺(4mL),完全澄清后加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(34.0mg,0.089mmol),N,N-二异丙基乙胺(30.0mg,0.22mmol),SMP-34421-2(60.0mg,0.074mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-34421-3,重50.0mg,收率64%。
MS(ESI)m/z:526[M/2+H]
步骤3:化合物SMP-34421-4的制备
SMP-34421-3(50.0mg,0.048mmol)置于25mL反应瓶中,加入,三氟乙酸(3mL),室温搅拌反应3小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合SMP-34421-4,重25.0mg,收率55.97%。MS(ESI)m/z:470[M/2+H]
步骤4:化合物SMP-34421-5的制备
SMP-34421-4(25.0mg,0.027mmol)溶于N,N-二甲基甲酰胺(2mL)中,完全澄清后,依次加入中间体A(28.0mg,0.027mmol),N,N-二异丙基乙胺(7.0mg,0.054mmol),完毕后,缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(10.0mg,0.027mmol)的N,N-二甲基甲酰胺(1mL)溶液,室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合SMP-34421-5,重20.0mg,收率38.2%。
MS(ESI)m/z:984[M/2+H]
步骤5:化合物SMP-34421的制备
SMP-34421-5(20.0mg,0.010mmol)溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入中间体B(9.0mg,0.010mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.0mg,0.010mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-34421,重13.0mg,收率45.8%。
MS(ESI)m/z:1395[M/2+H]
实施例47、化合物SMP-53612的制备
步骤1:化合物SMP-53612-1的制备
SMP-34421-2(70。0mg,0.086mmol)溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入6-马来酰亚胺基己酸(22.0mg,0.10mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(39.0mg,0.10mmol),N,N-二异丙基乙胺(17.0mg,0.13mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得到化合物SMP-53612-1,重50mg,收率57.7%。MS(ESI)m/z:503[M/2+H]
步骤2:化合物SMP-53612-2的制备
SMP-53612-1(50.0mg,0.05mmol)溶于三氟乙酸(3mL),室温搅拌反应3小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合SMP-53612-2,重34.0mg,收率79.6%。
MS(ESI)m/z:447[M/2+H]
步骤3:化合物SMP-53612-3的制备
SMP-53612-2(34.0mg,0.038mmol)溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入中间体A(40.0mg,0.038mmol),N,N-二异丙基乙胺(15.0mg,0.11mmol),完毕后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(15.0mg,0.039mmol)的N,N-二甲基甲酰胺(1mL)溶液,室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合SMP-53612-3,重24.0mg,收率32.8%。
MS(ESI)m/z:962[M/2+H]
步骤4:化合物SMP-53612的制备
SMP-53612-3(24.0mg,0.012mmol)溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入中间体B(10.0mg,0.012mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(5.0mg,0.012mmol),N,N-二异丙基乙胺(5.0mg,0.039mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53612,重10.0mg,收率29.2%。
MS(ESI)m/z:1373[M/2+H]
1
实施例48、化合物SMP-10215的制备
步骤1:化合物SMP-10215-1的制备
SMP-34421-2(120.0mg,0.15mmol),马来酰亚胺-四聚乙二醇-羧酸(51.0mg,0.15mmol)混溶于N,N-二甲基甲酰胺(4mL),完全澄清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(56.0mg,0.15mmol),N,N-二异丙基乙胺(57.0mg,0.45mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-10215-1,重90.0mg,收率53.4%。
MS(ESI)m/z:570[M/2+H]
步骤2:化合物SMP-10215-2的制备
SMP-10215-1(90.0mg,0.079mmol)溶于三氟乙酸(3mL),室温搅拌反应2小时,TLC显示反应完全,减压除去三氟乙酸,反应液经制备HPLC纯化得化合物SMP-10215-2,重20.0mg,收率24.6%。
MS(ESI)m/z:513[M/2+H]
步骤3:化合物SMP-10215-3的制备
SMP-10215-2(20.0mg,0.02mmol),溶于N,N-二甲基甲酰胺(1mL),完全溶清后,依次加入中间体A(20.0mg,0.02mmol),N,N-二异丙基乙胺(7.0mg,0.06mmol),完毕后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(7.0mg,0.02mmol)的N,N-二甲基甲酰胺(1mL)溶液,室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-10215-3,重19.0mg,收率48.4%。
MS(ESI)m/z:1027[M/2+H]
步骤4:化合物SMP-10215的制备
SMP-10215-3(19.0mg,0.0093mmol),中间体B(8.0mg,0.0095mmol)混溶于N,N-二甲基甲酰胺(1mL),完全澄清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.0mg,0.011mmol),N,N-二异丙基乙胺(4.0mg,0.031mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC制备得化合物SMP-10215,重12.0mg,收率43.8%。
MS(ESI)m/z:1439[M/2+H]
实施例49、化合物SMP-34710的制备
步骤1:化合物SMP-34710-1的制备
/>
SMP-10215-2(60.0mg,0.06mmol),中间体9-氨基-4,7-二氧杂壬酸叔丁酯(27.0mg,0.12mmol)混溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(44.0mg,0.12mmol),N,N-二异丙基乙胺(30.0mg,0.24mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-34710-1,重45.0mg,收率52.9%。
MS(ESI)m/z:728[M/2+H]
步骤2:化合物SMP-34710-2的制备
SMP-34710-1(45.0mg,0.03mmol),溶于三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,反应液经制备HPLC纯化得化合物SMP-34710-2,重20.0mg,收率48.2%。
MS(ESI)m/z:672[M/2+H]
步骤3:化合物SMP-34710-3的制备
SMP-34710-2(20.0mg,0.015mmol),中间体A(16.0mg,0.015mmol)混溶于N,N-二甲基甲酰胺(2mL),N完全澄清后,加入N,N-二异丙基乙胺(4.0mg,0.031mmol),完毕后,缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(5.7mg,0.015mmol)的N,N-二甲基甲酰胺(1mL)溶液,室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-34710-3,重12.0mg,收率34.0%。
MS(ESI)m/z:1187[M/2+H]
步骤4:化合物SMP-34710的制备
SMP-34170-3(12.0mg,0.005mmol),中间体B(4.2mg,0.005mmol)混溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(1.9mg,0.005mmol),N,N-二异丙基乙胺(2.0mg,0.015mmol),室温搅拌反应20分钟,TLC显示反应完全,反相制备得化合物SMP-34710,重9.0mg,收率55.7%。
MS(ESI)m/z:1598[M/2+H]
实施例50、化合物SMP-44419的制备
步骤1:化合物SMP-44419-1的制备
SMP-10215-2(60.0mg,0.06mmol),中间体15-氨基-4,7,10,13-四氧杂十五烷酸叔丁酯(38.0mg,0.12mmol)混溶于N,N-二甲基甲酰胺(2mL),完全澄清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(45.6mg,0.12mmol),N,N-二异丙基乙胺(30.9mg,0.24mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-4419-1,重48.0mg,收率50.3%。
MS(ESI)m/z:816[M/2+H]
步骤2:化合物SMP-44419-2的制备
中间体SMP-44419-1(48.0mg,0.029mmol)溶于三氟乙酸(3mL),室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-44419-2,重20.0mg,收率44.7%。
MS(ESI)m/z:760[M/2+H]
步骤3:化合物SMP-44419-3的制备
/>
于10mL反应瓶中加入中间体SMP-44419-2(20.0mg,0.013mmol),中间体A(14.0mg,0.013mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(5.0mg,0.039mmol),完全澄清后,缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(5.0mg,0.013mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-44419-3,重10.0mg,收率29.8%。
MS(ESI)m/z:1274[M/2+H]
步骤4:化合物SMP-44419的制备
于10mL反应瓶中,加入中间体SMP-44419-3(9.0mg,0.004mmol),中间体B(3.4mg,0.004mmol),N,N-二甲基甲酰胺(1mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.004mmol),N,N-二异丙基乙胺(1.6mg,0.012mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-44419,重2.0mg,收率16.8%。
MS(ESI)m/z:1124[M/3+H]
实施例51、化合物SMP-35055的制备
步骤1:化合物SMP-35055-1的制备
于10mL反应瓶中,加入中间体SMP-10215-2(60.0mg,0.06mmol),氨基-八聚乙二醇-丙酸叔丁酯(58.0mg,0.12mmol),N,N-二甲基甲酰胺(3mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(45.6mg,0.12mmol),N,N-二异丙基乙胺(30.0mg,0.24mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-35055-1,重50.0mg,收率43.1%。
MS(ESI)m/z:993[M/2+H]
步骤2:化合物SMP-35055-2的制备
SMP-35055-1(50.0mg,0.03mmol)溶于三氟乙酸(3mL),室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,反应液经制备HPLC纯化得化合物SMP-35055-2,重20.0mg,收率42.4%。
MS(ESI)m/z:937[M/2+H]
步骤3:化合物SMP-35055-3的制备
于10mL反应瓶中,加入中间体SMP-35055-2(20.0mg,0.011mmol),中间体A(11.5mg,0.011mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(4.0mg,0.032mmol),完全溶清后,缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.2mg,0.011mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-35055-3,重8.0mg,收率25.8%。
MS(ESI)m/z:968[M/3+H]
步骤4:化合物SMP-35055的制备
于10mL反应瓶中,加入中间体SMP-35055-3(8.0mg,0.003mmol),中间体B(2.5mg,0.003mmol),N,N-二甲基甲酰胺(1mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(1.1mg,0.003mmol),N,N-二异丙基乙胺(1.0mg,0.008mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-35055,重1.2mg,收率11.7%。
MS(ESI)m/z:1242[M/2+H]
实施例52、化合物SMP-94170-A的制备
步骤1:化合物SMP-94170-1的制备
中间体SMP-10215-2(250.0mg,0.24mmol)溶于N,N-二甲基甲酰胺(5mL),依次加入中间体9-氨基-4,7-二氧杂壬酸叔丁酯(57.0mg,0.24mmol),N,N-二异丙基乙胺(94.0mg,0.73mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(93.0mg,0.24mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-94170-1,重110mg,收率36.4%。
MS(ESI)m/z:621[M/2+H]
步骤2:化合物SMP-94170-2的制备
于10mL反应瓶中,加入中间体SMP-94170-1(110.0mg,0.09mmol),氨基-十二聚乙二醇-丙酸叔丁酯(59.0mg,0.09mmol),N,N-二甲基甲酰胺(3mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(34.2mg,0.09mmol),N,N-二异丙基乙胺(34.8mg,0.27mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-94170-2,重110mg,收率65.5%。
MS(ESI)m/z:948[M/2+H]
步骤3:化合物SMP-94170-3的制备
SMP-94170-2(110.0mg,0.06mmol)溶于三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-94170-3,重70mg,收率67.6%。
MS(ESI)m/z:893[M/2+H]
步骤4:化合物SMP-94170-A-1,SMP-94170-B-1的制备
SMP-94170-3(70.0mg,0.04mmol)溶于N,N-二甲基甲酰胺(3mL),依次加入A(41.0mg,0.04mmol),N,N-二异丙基乙胺(15.0mg,0.12mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(15.0mg,0.04mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-94170-A-1,重18.0mg,收率16.3%,得化合物SMP-94170-B-1,重30.0mg,收率27.2%。
MS(ESI)m/z:1407[M/2+H]
步骤5:化合物SMP-94170-A的制备
于10mL反应瓶中,依次加入中间体SMP-94170-A-1(18.0mg,0.006mmol),中间体B(5.0mg,0.006mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.3mg,0.006mmol),N,N-二异丙基乙胺(2.5mg,0.019mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-94170-A,重10.0mg,收率43.0%。
MS(ESI)m/z:1212[M/3+H]
实施例53、化合物SMP-94170-B的制备
步骤1:化合物SMP-94170-B的制备
SMP-94170-B-1(30.0mg,0.011mmol)溶于N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入中间体B(9.0mg,0.011mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.0mg,0.011mmol),N,N-二异丙基乙胺(4.3mg,0.033mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-94170-B,重15mg,收率38.7%。
MS(ESI)m/z:1212[M/3+H]
实施例54、化合物SMP-46940的制备
步骤1:化合物SMP-46940-1的制备
SMP-34421-2(300.0mg,0.37mmol)溶于N,N-二甲基甲酰胺(5mL),,完全溶清后,依次加入马来酰亚胺-八聚乙二醇-羧酸(193.0mg,0.37mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(141.0mg,0.37mmol),N,N-二异丙基乙胺(143.0mg,1.11mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-46940-1,重132.0mg,收率27.2%。
MS(ESI)m/z:657[M/2+H]
步骤2:化合物SMP-46940-2的制备
于10mL反应瓶中,依次加入中间体SMP-46940-1(132.0mg,0.10mmol),三氟乙酸(3mL),室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,反应液经制备HPLC纯化得化合物SMP-46940-2,重60.0mg,收率49.7%。
MS(ESI)m/z:601[M/2+H]
步骤3:化合物SMP-46940-3的制备
于10mL反应瓶中,加入中间体SMP-46940-3(60.0mg,0.05mmol),9-氨基-4,7-二氧杂壬酸叔丁酯(23.0mg,0.10mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(38.0mg,0.10mmol),N,N-二异丙基乙胺(39.0mg,0.30mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-46940-3,重40.0mg,收率49.1%。
MS(ESI)m/z:816[M/2+H]
步骤4:化合物SMP-46940-4的制备
于10mL反应瓶中,依次加入中间体SMP-46940-3(40.0mg,0.025mmol),三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-46940-4,重25.0mg,收率67.1%。
MS(ESI)m/z:760[M/2+H]
步骤5:化合物SMP-46940-5的制备
SMP-46940-4(25.0mg,0.016mmol)溶于N,N-二甲基甲酰胺(2mL),依次加入中间体A(17.0mg,0.016mmol),,N,N-二异丙基乙胺(6.2mg,0.048mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(6.0mg,0.016mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-46940-5,重14.0mg,收率33.4%。
MS(ESI)m/z:1275[M/2+H]
步骤5:化合物SMP-46940的制备
于10mL反应瓶中,依次加入加入中间体SMP-46940-5(14.0mg,0.005mmol),中间体B(5.0mg,0.005mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.0mg,0.005mmol),N,N-二异丙基乙胺(2.0mg,0.015mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-46940,重9.0mg,收率48.6%。
MS(ESI)m/z:1124[M/3+H]
实施例55、化合物SMP-13069的制备
步骤1:化合物SMP-13069-1的制备
于25mL反应瓶中,依次加入中间体SMP-34421-2(300.0mg,0.37mmol),马来酰亚胺-六聚乙二醇-羧酸(160.0mg,0.37mmol),N,N-二甲基甲酰胺(5mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(140.7mg,0.37mmol),N,N-二异丙基乙胺(143.2mg,1.11mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-13069-1,重153.0mg,收率33.7%。
MS(ESI)m/z:613[M/2+H]
步骤2:化合物SMP-13069-2的制备
于10mL反应瓶中,依次加入中间体SMP-13069-1(153.0mg,0.12mmol),三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,反应液经制备HPLC纯化得化合物SMP-13069-2,重80.0mg,收率57.6%。
MS(ESI)m/z:557[M/2+H]
步骤3:化合物SMP-13069-3的制备
于10mL反应瓶中,依次加入中间体SMP-13069-3(80.0mg,0.072mmol),9-氨基-4,7-二氧杂壬酸叔丁酯(33.6mg,0.144mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(54.0mg,0.144mmol),N,N-二异丙基乙胺(55.0mg,0.43mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-13069-3,重60.0mg,收率53.8%。
MS(ESI)m/z:772[M/2+H]
步骤4:化合物SMP-13069-4的制备
于10mL反应瓶中,依次加入中间体SMP-13069-3(60.0mg,0.039mmol),三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-13069-4,重35.0mg,收率62.9%。MS(ESI)m/z:716[M/2+H]
步骤5:化合物SMP-13069-5的制备
于10mL反应瓶中,依次加入中间体SMP-13069-4(35.0mg,0.024mmol),中间体A(25.0mg,0.024mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(9.3mg,0.072mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(9.0mg,0.024mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-13069-5,重18.0mg,收率29.9%。
MS(ESI)m/z:1231[M/2+H]
步骤6:化合物SMP-13069的制备
于10mL反应瓶中,依次加入中间体SMP-13069-5(18.0mg,0.007mmol),中间体B(6.0mg,0.007mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.0mg,0.007mmol),N,N-二异丙基乙胺(3.0mg,0.021mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-13069,重9.5mg,收率39.6%。
MS(ESI)m/z:1095[M/3+H]
实施例56、化合物SMP-28945的制备
步骤1:化合物SMP-28945-1的制备
于50mL反应瓶中,依次加入中间体SMP-34421-1(250.0mg,0.62mmol),N,N-二甲基甲酰胺(10mL),完全澄清后,加入PEG
MS(ESI)m/z:560[M/2+H]
步骤2:化合物SMP-28945-2的制备
于25mL反应瓶中,依次加入中间体SMP-28945-1(180.0mg,0.16mmol),N,N-二甲基甲酰胺(5mL),完全溶清后,依次加入6-马来酰亚胺基己酸(34.0mg,0.16mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(61.0mg,0.16mmol),N,N-二异丙基乙胺(62.0mg,0.48mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28945-2,重120.0mg,收率56.9%。
MS(ESI)m/z:656[M/2+1]
步骤3:化合物SMP-28945-3的制备
于10mL反应瓶中,依次加入中间体SMP-28945-2(120.0mg,0.092mmol),三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-28945-3,重80.0mg,收率72.9%。
MS(ESI)m/z:600[M/2+H]
步骤4:化合物SMP-28945-4的制备
于10mL反应瓶中,依次加入中间体SMP-28945-3(30.0mg,0.025mmol),中间体A(26.0mg,0.025mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(10.0mg,0.075mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(10mg,0.025mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28945-4,重20.0mg,收率35.9%。
MS(ESI)m/z:1115[M/2+H]
步骤5:化合物SMP-28945的制备
于10mL反应瓶中,依次加入中间体SMP-28945-4(20.0mg,0.009mmol),中间体B(7.6mg,0.009mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.4mg,0.009mmol),N,N-二异丙基乙胺(3.5mg,0.027mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28945,重2.6mg,收率9.5%。
MS(ESI)m/z:1017[M/3+H]
实施例57、化合物SMP-28823的制备
步骤1:化合物SMP-28823-1的制备
于50mL反应瓶中,依次加入氨基九甘醇单甲醚(300.0mg,0.70mmol),三光气(206.0mg,0.70mmol),二氯甲烷(10mL),完全澄清后加入三乙胺(1mL)。0℃搅拌反应20分钟,TLC显示反应完全,减压浓缩除去二氯甲烷,得到粗品化合物SMP-28823-1,重300.0mg。MS(ESI)m/z:454[M+H]
步骤2:化合物SMP-28823-2的制备
于50mL反应瓶中,依次加入中间体SMP-28823-1粗品(300.0mg,0.66mmol),中间体SMP-34421-1(300.0mg,0.75mmol),二氯甲烷(10mL),完全澄清后加入三乙胺(1mL)。室温搅拌反应20分钟,TLC显示反应完全,减压浓缩除去二氯甲烷,残余物经制备HPLC纯化得化合物SMP-28823-1,重300.0mg,收率53.1%。
MS(ESI)m/z:854[M+H]
步骤3:化合物SMP-28823-3的制备
于25mL反应瓶中,加入中间体SMP-28823-2(230.0mg,0.27mmol),N,N-二甲基甲酰胺(5mL),完全溶清后,依次加入马来酰亚胺-二聚乙二醇-羧酸(69.4mg,0.27mmol),N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(102.7mg,0.27mmol),N,N-二异丙基乙胺(104.5mg,0.81mmol).室温搅拌反应30分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28823-3,重200.0mg,收率67.9%。
MS(ESI)m/z:547[M+H]
步骤4:化合物SMP-28823-4的制备
于10mL反应瓶中,依次加入中间体SMP-28823-3(200mg,0.18mmol),三氟乙酸(3mL)。室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,HPLC制备得化合物SMP-28823-4,重40.0mg,收率22.3%。MS(ESI)m/z:491[M/2+H]
步骤5:化合物SMP-28823-5的制备
于10mL反应瓶中,依次加入中间体SMP-28823-4(40.0mg,0.041mmol),中间体A(42.9mg,0.041mmol),N,N-二甲基甲酰胺(3mL),N,N-二异丙基乙胺(16.8mg,0.13mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(15.7mg,0.041mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应30分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28823-5,重17.0mg,收率20.7%。MS(ESI)m/z:1005[M/2+H]
步骤6:化合物SMP-28823的制备
于10mL反应瓶中,依次加入中间体SMP-28823-5(17.0mg,0.0085mmol),中间体B(7.1mg,0.0085mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.3mg,0.0085mmol),N,N-二异丙基乙胺(3.3mg,0.026mmol)。室温搅拌反应30分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-28823,重12mg,收率50.1%。
MS(ESI)m/z:944[M/3+H]
实施例58、化合物SMP-53816的制备
/>
步骤1:化合物SMP-53816-1的制备
于100mL反应瓶中,依次加入轮环藤宁(1.0g,5.81mmol),苯甲氧羰酰琥珀酰亚胺(2.9g,11.62mmol),三氯甲烷(20mL)。室温搅拌反应24小时,TLC显示反应完全,减压除掉多余三氯甲烷,反应液经制备HPLC纯化得化合物SMP-53816-1,重2.0g,收率78.1%。
MS(ESI)m/z:441[M+H]
步骤2:化合物SMP-53816-2的制备
于50mL反应瓶中,依次加入中间体SMP-53816-1(1.0g,2.27mmol),N-叔丁氧羰基-7-氨基庚酸(556.2mg,2.27mmol),N,N-二甲基甲酰胺(20mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(863.2mg,2.27mol),N,N-二异丙基乙胺(879.0mg,6.81mol)。室温搅拌反应30分钟,TLC显示反应完全,反相制备得化合物SMP-53816-2,重300.0mg,收率19.7%。
MS(ESI)m/z:668[M+H]
步骤3:化合物SMP-53816-3的制备
于25mL反应瓶中,依次加入中间体SMP-53816-2(300.0mg,0.45mmol),马来酰亚胺-九聚乙二醇-羧酸(286.0mg,0.45mmol),N,N-二甲基甲酰胺(5mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(171.1mg,0.45mol),N,N-二异丙基乙胺(174.2mg,1.35mmol)。室温搅拌反应30分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53816-3,重300.0mg,收率60.4%。
MS(ESI)m/z:553[M/2+H]
步骤4:化合物SMP-53816-4的制备
于25mL反应瓶中,依次加入中间体SMP-53816-3(300.0mg,0.27mmol),甲醇(5mL),完全澄清后,加入钯碳(60mg),置换空气于氢气氛围,室温搅拌反应3小时。TLC显示反应完全,反应液过滤,滤液浓缩得化合物SMP-53816-4,重220.0mg,收率96.8%。
MS(ESI)m/z:838[M+H]
步骤5:化合物SMP-53816-5的制备
于25mL反应瓶中,依次加入中间体SMP-53816-4(220mg,0.26mmol),羧酸-四聚乙二醇-叔丁酯(182.0mg,0.52mmol),N,N-二甲基甲酰胺(3mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(197.8mg,0.52mol),N,N-二异丙基乙胺(100.6mg,0.78mol)。室温搅拌反应30分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53816-5,重360mg,收率91.2%。
MS(ESI)m/z:751[M/2+H]
步骤6:化合物SMP-53816-6的制备
于10mL反应瓶中,依次加入中间体SMP-53816-5(360.0mg,0.24mmol),三氟乙酸(5mL)。室温搅拌反应3小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-53816-6,重300.0mg,收率90.0%。
MS(ESI)m/z:695[M/2+H]
步骤7:化合物SMP-53816-7的制备
/>
于25mL反应瓶中,依次加入中间体SMP-53816-4(300.0mg,0.22mmol),N-甲氧基羰基顺丁烯二酰亚胺(68.2mg,0.44mmol),THF(3mL),饱和碳酸氢钠水溶液(3mL)。室温搅拌反应3小时,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53816-7,重260.0mg,收率87.9%。MS(ESI)m/z:685[M/2+H]
步骤8:化合物SMP-53816-8的制备
于25mL反应瓶中,依次加入中间体SMP-53816-7(100.0mg,0.073mmol),中间体A(74.3mg,0.073mmol),N,N-二甲基甲酰胺(3mL),N,N-二异丙基乙胺(28.2mg,0.22mmol),完全澄清后滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(27.8mg,0.073mmol)的N,N-二甲基甲酰胺(3mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53816-8,重40.0mg,收率22.8%。
MS(ESI)m/z:1200[M/2+H]
步骤9:化合物SMP-53816的制备
于10mL反应瓶中,依次加入中间体SMP-53816-8(40.0mg,0.017mmol),中间体B(14.3mg,0.017mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(6.5mg,0.017mmol),N,N-二异丙基乙胺(6.5mg,0.051mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-53816,重14.0mg,收率26.0%。
MS(ESI)m/z:1074[M/3+H]
实施例59、化合物SMP-23135的制备
步骤1:化合物SMP-23135-2的制备
于100mL反应瓶中,依次加入中间体SMP-23135-1(2.0g,3.64mmol),6-马来酰亚胺己酸(768.0mg,3.64mmol),N,N-二甲基甲酰胺(30mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(1.4g,3.64mmol),N,N-二异丙基乙胺(1.4g,10.92mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-23135-2,重1.1g,收率40.7%。
MS(ESI)m/z:743[M+H]
步骤2:化合物SMP-23135-3的制备
于100mL反应瓶中,依次加入中间体SMP-23135-2(1.1g,1.48mmol),苯酚(139.0mg,1.48mmol),33%的氢溴酸醋酸溶液(30mL),50℃搅拌反应过夜,LC-MS显示反应完全,将反应液冷却后,滴加到装有甲基叔丁基醚(300mL)的单口瓶中,析出固体,过滤,固体真空干燥得化合物SMP-23135-3,重350.0mg,收率54.4%。
MS(ESI)m/z:435[M+H]
步骤3:化合物SMP-23135-4的制备
于50mL反应瓶中,依次加入中间体SMP-23135-3(350.0mg,0.81mmol),溴乙酸叔丁酯(473.9mg,2.43mmol),N,N-二甲基甲酰胺(10mL),碳酸钾(335.3mg,2.43mmol)。室温搅拌反应3小时,LC-MS显示反应完全,过滤,滤液制备HPLC纯化得化合物SMP-23135-4,重85.0mg,收率15.9%。MS(ESI)m/z:663[M+H]
步骤4:化合物SMP-23135-5的制备
于25mL反应瓶中,依次加入中间体SMP-23135-4(85.0mg,0.13mmol),三氟乙酸(5mL),室温搅拌反应3小时,TLC显示反应完全,减压浓缩除去三氟乙酸,制备HPLC纯化得化合物SMP-23135-5,重50.0mg,收率70.8%。MS(ESI)m/z:551[M+H]
步骤5:化合物SMP-23135-6的制备
于10mL反应瓶中,依次加入中间体SMP-23135-5(50.0mg,0.091mmol),中间体A(95.4mg,0.091mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(35.2mg,0.27mmol),完全澄清后缓慢滴加N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(34.6mg,0.091mmol)的N,N-二甲基甲酰胺(1mL)溶液。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-23135-6,重23.0mg,收率16.0%。
MS(ESI)m/z:790[M/2+H]
步骤6:化合物SMP-23135的制备
于10mL反应瓶中,依次加入中间体SMP-23135-6(23.0mg,0.014mmol),中间体B(12.0mg,0.014mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(5.3mg,0.014mmol),N,N-二异丙基乙胺(5.4mg,0.042mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-23135,重12.0mg,收率34.3%。
MS(ESI)m/z:1201[M/2+H]
实施例60、化合物SMP-21139的制备
步骤1:化合物SMP-21139-1和SMP-68691-1的制备
于25mL反应瓶中,加入中间体K(56.0mg,0.05mmol),中间体F-5(85.0mg,0.10mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(19.0mg,0.05mmol),N,N-二异丙基乙胺(13.0mg,0.10mmol),N,N-二甲基甲酰胺(4mL),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-21139-1,重20.0mg和化合物SMP-68691-1,重18.0mg总收率36%。
MS(ESI)m/z:1059[M/2+H]
步骤2:化合物SMP-21139-2的制备
于10mL反应瓶中,加入中间体SMP-21139-1(20.0mg,0.010mmol),中间体B(10.0mg,0.010mmol),N,N-二甲基甲酰胺(2mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.0mg,0.010mmol),N,N-二异丙基乙胺(2.0mg,0.014mmol),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-21139-2,重15.0mg收率61%。
MS(ESI)m/z:1363[M/2+H]
步骤3:化合物SMP-21139-3的制备
于10mL反应瓶中,加入中间体SMP-21139-2(15.0mg,0.0055mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.0mg,0.013mmol),N,N-二甲基甲酰胺(2mL),室温搅拌反应20分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-21139-3,重8.0mg,收率58%。
MS(ESI)m/z:1252[M/2+H]
步骤4:化合物SMP-21139的制备
于10mL反应瓶中加入化合物SMP-51013-3(6.0mg,0.0047mmol),溶剂N,N-二甲基甲酰胺(2mL),待反应液澄清后依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(2.0mg,0.0052mmol),N,N-二异丙基乙胺(1.0mg,0.0077mmol),室温下反应5分钟后,加入化合物SMP-21139-3(8.0mg,0.0032mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-21139,重4.5mg,收率34%。
MS(ESI)m/z:1324[M/3+H]
实施例61、化合物SMP-68691的制备
步骤1:化合物SMP-68691-2的制备
于10mL反应瓶中,加入中间体SMP-68691-1(18.0mg,0.008mmol),中间体B(8.0mg,0.010mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(4.0mg,0.010mmol),N,N-二异丙基乙胺(2.0mg,0.013mmol),N,N-二甲基甲酰胺(2mL),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-68691-2,重12.0mg收率55%。
MS(ESI)m/z:1363[M/2+H]
步骤2:化合物SMP-68691-3的制备
于10mL反应瓶中,加入中间体SMP-68691-2(12.0mg,0.0044mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(1.0mg,0.007mmol),N,N-二甲基甲酰胺(2mL),室温搅拌反应20分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残留物经制备HPLC纯化得化合物SMP-68691-3,重8.0mg,收率73%。
MS(ESI)m/z:1252[M/2+H]
步骤3:化合物SMP-68691的制备
于10mL反应瓶中加入化合物SMP-51013-3(6.0mg,0.0047mmol),溶剂N,N-二甲基甲酰胺(1.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(2.0mg,0.0052mmol),N,N-二异丙基乙胺(1.0mg,0.0077mmol),室温下反应5分钟后,加入化合物SMP-68691-3(8.0mg,0.0029mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物HPLC纯化,得目标产物SMP-68691,重4.0mg,收率33%。
MS(ESI)m/z:1324[M/3+H]
实施例62、化合物SMP-60226的制备
步骤1:化合物SMP-60226-1的制备
10mL反应瓶中加入中间体SMP-93566-2(100.0mg,0.35mmol),中间体I(212.0mg,0.35mmol),N,N-二甲基甲酰胺(3mL),完全澄清后加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(133.0mg,0.35mmol),N,N-二异丙基乙胺(135.4mg,1.05mmol),室温搅拌反应20分钟,TLC显示反应完全,制备HPLC纯化得化合物SMP-60226-1,重200.0mg,收率65%。
MS(ESI)m/z:878[M+H]
步骤2:化合物SMP-60226-2的制备
10mL反应瓶中加入中间体SMP-60226-1(201.9mg,0.23mmol),三氟乙酸(3mL),室温搅拌反应2小时,TLC显示反应完全,减压浓缩除去三氟乙酸,残余物乙腈溶解后,制备HPLC纯化得化合物SMP-60226-2,重80.0mg,收率43%。
MS(ESI)m/z:823[M+H]
步骤3:化合物SMP-60226的制备
10mL反应瓶中加入中间体SMP-60226-4(32.9mg,0.04mmol),中间体B(33.6mg,0.04mmol),N,N-二甲基甲酰胺(2mL),完全澄清后加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(15.2mg,0.04mmol),N,N-二异丙基乙胺(10.3mg,0.08mmol),室温搅拌反应20分钟,LC-MS检测显示反应完全,反应液经制备HPLC纯化得化合物SMP-60226,重35.0mg,收率53%。
MS(ESI)m/z:823[M/2+H]
实施例63、化合物SMP-37860的制备
步骤1:化合物SMP-37860-2的制备
250mL反应瓶中,将九聚乙二醇单甲醚(7.0g,16.35mmol)用二氯甲烷(80mL)溶解,加入三乙胺(3.3g,32.67mmol),在冰浴下向上述反应液中缓慢加入甲基磺酰氯(2.2g,19.60mmol),室温搅拌反应20小时,TLC显示反应完全。用水(50mL)洗涤,有机相再用饱和氯化铵水溶液(30mL)洗涤后用无水硫酸钠干燥,减压浓缩,柱层析(二氯甲烷:甲醇=20:1),得化合物SMP-37860-2,重8.1g,收率98%。
MS(ESI)m/z:507[M+H]
1
步骤2:化合物SMP-37860-3的制备
100mL反应瓶中,将1,7-二-(N-叔丁氧羰基甲基)-1,4,7,10-四氮杂环十二烷(2.1g,5.33mmol)与化合物SMP-37860-2(8.1g,16.01mmol)用乙腈(30mL)溶解,加入碳酸钾(2.4g,17.07mmol),升温至55℃反应20小时,LC-MS检测反应完全。冷却至室温后过滤,滤液减压浓缩至干,残余物柱层析(二氯甲烷:甲醇=5:1),得化合物SMP-37860-3,重3.2g,收率64%。MS(ESI)m/z:612[M/2+H]
1
步骤3:化合物SMP-37860-4的制备
10mL反应瓶中,加入化合物SMP-37860-3(90.0mg,0.079mmol),然后加入三氟乙酸(2mL),室温搅拌反应3小时。LC-MS检测反应完全,减压浓缩,残留物用少量乙腈溶解后制备HPLC纯化得化合物SMP-37860-4,重20mg,收率25%。
MS(ESI)m/z:555[M/2+H]
步骤4:化合物SMP-37860-5的制备
50mL反应瓶中,将1-(2-氨基乙基)-1H-吡咯-2,5-二酮盐酸盐(95.0mg,0.54mmol)与化合物SMP-37860-4(500.0mg,0.45mmol)用N,N-二甲基甲酰胺(10mL)溶解,加入N,N-二异丙基乙胺(203.8mg,1.58mmol)。将N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(171.0mg,0.45mmol)用N,N-二甲基甲酰胺(10mL)溶解后滴入上述溶液中,室温搅拌反应3小时。LC-MS监测反应结束后,反应液经制备HPLC纯化得化合物SMP-37860-5,重275.0mg,收率50%。
MS(ESI)m/z:616[M/2+H]
步骤5:化合物SMP-37860-6的制备
25mL反应瓶中,加入中间体A-5(200.0mg,0.36mmol),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(163.4mg,0.43mmol),N,N-二异丙基乙胺(69.7mg,0.54mmol),N,N-二甲基甲酰胺(5mL),室温搅拌反应5分钟后加入一甲基澳瑞他汀E(258.1mg,0.36mmol),室温反应30分钟。TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=10:1)纯化得化合物SMP-37860-6,重300.0mg,收率65%。MS(ESI)m/z:630[M/2+H]
步骤6:化合物SMP-37860-7的制备
50mL反应瓶中,加入化合物SMP-37860-6(302.4mg,0.24mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(41.3mg,0.27mmol),N,N-二甲基甲酰胺(10mL),室温搅拌反应30分钟,TLC显示反应完全。减压浓缩,残余物制备HPLC纯化得化合物SMP-37860-7,重200.0mg,收率81%。
MS(ESI)m/z:1037[M+H]
步骤7:化合物SMP-37860的制备
25mL反应瓶中,加入中间体SMP-37860-5(20.7mg,0.02mmol),中间体SMP-37860-7(20.4mg,0.02mmol),N,N-二甲基甲酰胺(3mL),N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(15.2mg,0.04mmol),N,N-二异丙基乙胺(6.5mg,0.05mmol),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-37860,重20.0mg,收率47%。
MS(ESI)m/z:1126[M/2+H]
实施例64、化合物SMP-18777的制备
步骤1:化合物SMP-18777-1的制备
100mL反应瓶中,用二氯甲烷(30mL)与甲醇(10mL)混合溶液溶解中间体A-5(2.5g,4.38mmol),4-氨基苯甲醇(1.1g,8.77mmol),加入2-乙氧基-1-乙氧羰酰基-1,2-二氢喹啉(2.2g,8.77mmol),室温搅拌反应20小时,TLC显示反应完全。减压浓缩除去溶剂,残余物硅胶柱层析(二氯甲烷:甲醇=15:1)得化合物SMP-18777-1,重900.0mg,收率31%。
MS(ESI)m/z:664[M+H]
步骤2:化合物SMP-18777-2的制备
25mL反应瓶中,用N,N-二甲基甲酰胺(10mL)溶解中间体SMP-18777-1(1.0g,1.51mmol),加入二对硝基苯基碳酸酯(163.0mg,0.43mmol)与三乙胺(1979mg,1.96mmol),室温搅拌反应5小时,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物硅胶柱层析(二氯甲烷:甲醇=12:1)得化合物SMP-18777-2,重300.0mg,收率24%。
MS(ESI)m/z:829[M+H]
步骤3:化合物SMP-18777-3的制备
25mL反应瓶中,将盐酸多柔比星(52.2mg,0.09mmol)用N,N-二甲基甲酰胺(10mL)溶解,加入化合物SMP-18777-2(82.9mg,0.10mmol)与三乙胺(17.2mg,0.17mmol),室温搅拌反应18小时,TLC显示反应完全。减压浓缩除去N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-18777-3,重80.0mg,收率77%。
MS(ESI)m/z:614,425片段峰.
步骤4:化合物SMP-18777的制备
25mL反应瓶中,用N,N-二甲基甲酰胺(2mL)溶解化合物SMP-18777-3(20.0mg,0.02mmol)与化合物SMP-37860-5(9.0mg,0.024mmol),加入1H-苯并三唑-1-基氧三吡咯烷基六氟磷酸盐(10.4mg,0.02mmol),三乙胺(4.0mg,0.04mmol),室温搅拌反应5小时,LC-MS显示反应完全。反应液经制备HPLC纯化得化合物SMP-18777,重1.7mg,收率6%。
MS(ESI)m/z:819,914片段峰.
实施例66、化合物SMP-58054的制备
步骤1:化合物SMP-58054-1的制备
25mL反应瓶中,将一甲基澳瑞他汀E(200.7mg,0.28mmol)用N,N-二甲基甲酰胺(5mL)溶解,加入化合物SMP-18777-2(200.0mg,0.24mmol),三乙胺(48.5mg,0.48mmol)和1-羟基苯并三唑(37.8mg,0.28mmol),室温搅拌反应18小时,TLC显示反应完全。制备HPLC纯化,得化合物SMP-58054-1,重80.0mg,收率24%。
MS(ESI)m/z:425片段峰,1186[M+H]
步骤2:化合物SMP-58054的制备
25mL反应瓶中,加入中间体SMP-58054-1(15.0mg,0.013mmol),中间体SMP-37860-6(16.0mg,0.013mmol),N,N-二甲基甲酰胺(1mL),1-羟基苯并三唑(1.3mg,0.014mmol),三乙胺(2.0mg,0.019mmol),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物制备HPLC纯化得化合物SMP-58054,重20.0mg,收率67%。
MS(ESI)m/z:1200[M/2+H]
实施例67、化合物SMP-25274的制备
步骤1:化合物SMP-25274-1的制备
25mL反应瓶中,用N,N-二甲基甲酰胺(4mL)溶解化合物A-5(50.0mg,0.089mmol)与盐酸多柔比星(46.4mg,0.075mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(30.4mg,0.08mmol),三乙胺(8.0mg,0.08mmol),室温搅拌反应5小时,TLC显示反应完全。反应液经制备HPLC纯化得化合物SMP-25274-1,重70.0mg,收率74%。
MS(ESI)m/z:1084[M+H]
步骤2:化合物SMP-25274-2的制备
10mL反应瓶中,加入化合物SMP-25274-1(80.0mg,0.07mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(10.7mg,0.07mmol),N,N-二甲基甲酰胺(3mL),室温搅拌反应30分钟,TLC显示反应完全减压浓缩,残余物制备HPLC纯化得化合物SMP-25274-2,重50.0mg,收率79%。
MS(ESI)m/z:862[M+H]
步骤3:化合物SMP-25274的制备
25mL反应瓶中,用N,N-二甲基甲酰胺(1.5mL)溶解化合物SMP-25274-2(20.0mg,0.02mmol)与化合物SMP-37860-5(30.0mg,0.024mmol),加入1H-苯并三唑-1-基氧三吡咯烷基六氟磷酸盐(10.4mg,0.021mmol),三乙胺(4.0mg,0.04mmol),室温搅拌反应5小时,TLC显示反应完全。反应液经制备HPLC纯化得化合物SMP-25274,重14.0mg,收率34%。
MS(ESI)m/z:1038[M/2+H]
实施例68、化合物SMP-56875的制备
步骤1:化合物SMP-56875-1的制备
25mL反应瓶中,将1-(29-氨基-3,6,9,12,15,18,21,24,27-氧杂二十九烷基)-1H-吡咯-2,5-二酮(90.0mg,0.17mmol)与化合物SMP-37860-4(214.0mg,0.19mmol)用N,N-二甲基甲酰胺(2mL)溶解,加入N,N-二异丙基乙胺(54.2mg,0.42mmol)。将N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(64.6mg,0.17mmol)用N,N-二甲基甲酰胺(4mL)溶解后滴入上述溶液中,室温搅拌反应3小时,LC-MS显示反应完全。反应液经HPLC纯化得化合物SMP-56875-1,重70.0mg,收率26%。
MS(ESI)m/z:638[M/2+H]
步骤2:化合物SMP-56875的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(0.5mL)溶解化合物SMP-56875-1(11.0mg,0.005mmol)与中间体D(16.0mg,0.01mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(0.8mg,0.01mmol),室温搅拌反应2小时,TLC显示反应完全。制备HPLC纯化得化合物SMP-56875,重7.0mg,收率35%。
MS(ESI)m/z:1267[M/3+H]
实施例69、化合物SMP-82444的制备
步骤1:化合物SMP-82444-1的制备
化合物SMP-82444-1的合成方法参考中间体C的合成
MS(ESI)m/z:1184[M/2+H]
步骤2:化合物SMP-82444的制备
/>
4mL反应瓶中,用N,N-二甲基甲酰胺(0.5mL)溶解化合物SMP-82444-1(9.0mg,0.004mmol)与化合物SMP-37860-5(8.0mg,0.007mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(1.0mg,0.011mmol),室温搅拌反应2小时,TLC显示反应完全。反应液经制备HPLC纯化得化合物SMP-82444,重3.2mg,收率24%。MS(ESI)m/z:1194[M/3+H]
实施例70、化合物SMP-50309的制备
步骤1:化合物SMP-50309-1的制备
化合物SMP-50309-1的合成方法参考中间体C的合成
MS(ESI)m/z:907[M/3+H]
步骤2:化合物SMP-50309的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(0.5mL)溶解化合物SMP-82444-1(9.0mg,0.003mmol)与化合物SMP-37860-5(8.0mg,0.007mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(1.0mg,0.011mmol),室温搅拌反应2小时。反应液经制备HPLC纯化得化合物SMP-37860,重3.0mg,收率29%。
MS(ESI)m/z:1281[M/3+H]
实施例71、化合物SMP-20094的制备
步骤1:化合物SMP-20094-1的制备
4mL反应瓶中,将中间体D(10.0mg,0.005mmol)与化合物SMP-37860-4(14.0mg,0.013mmol)用N,N-二甲基甲酰胺(1.5mL)溶解,加入三乙胺(1.0mg,0.01mmol)。将N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol)用N,N-二甲基甲酰胺(1.5mL)溶解后缓慢滴入上述溶液中,室温搅拌反应1.5小时。LC-MS显示反应完全,反应液经制备HPLC纯化得化合物SMP-20094-1,重15.0mg,收率91%。
MS(ESI)m/z:1094[M/3+H]
步骤2:化合物SMP-20094的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(3mL)溶解1-(2-(2-(2-氨基乙氧基)乙氧基)乙基)-1H-吡咯-2,5-二酮(2.0mg,0.009mmol)与化合物SMP-20094-1(15.0mg,0.005mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),吡啶(0.9mg,0.01mmol),室温搅拌反应2小时。TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-20094,重1.5mg,收率10%。
MS(ESI)m/z:1164[M/3+H]
实施例72、化合物SMP-99559的制备
步骤1:化合物SMP-99559-1的制备
化合物SMP-99559-1的合成方法参考SMP-37860-5的合成
MS(ESI)m/z:924[M/2+H]
步骤2:化合物SMP-99559的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(1.0mL)溶解化合物SMP-99559-1(9.0mg,0.005mmol)与中间体D(10.0mg,0.005mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(1.0mg,0.012mmol),室温搅拌反应2小时。TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-99559,重6.0mg,收率30%。
MS(ESI)m/z:1005[M/4+H]
实施例73、化合物SMP-59623的制备
步骤1:化合物SMP-59623-1的制备
化合物SMP-59623-1的合成方法参考SMP-37860-5的合成
MS(ESI)m/z:572[M/2+H]
步骤2:化合物SMP-59623的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(1.0mL)溶解化合物SMP-59623-1(7.0mg,0.006mmol)与中间体D(10.0mg,0.005mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(2.0mg,0.02mmol),室温搅拌反应2小时。TLC显示反应完全,反应液经制备HPLC,得化合物SMP-59623,重7.2mg,收率36%。
MS(ESI)m/z:1105[M/3+H]
实施例74、化合物SMP-47610的制备
步骤1:化合物SMP-47610的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(1.0mL)溶解化合物SMP-59623-1(6.0mg,0.005mmol)与中间体C(10.0mg,0.004mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(2mg,0.02mmol),室温搅拌反应2小时。LC-MS显示反应完全,反应液经制备HPLC纯化得化合物SMP-47610,重6.5mg,收率38%。
MS(ESI)m/z:1138[M/3+H]
实施例75、化合物SMP-86467的制备
步骤1:化合物SMP-86467-1的制备
500mL反应瓶中,将6-((叔丁氧羰基)氨基)己酸(584.0mg,2.38mmol)与化合物SMP-53816-1(1500mg,2.15mmol)用N,N-二甲基甲酰胺(20mL)溶解,加入三乙胺(325.2mg,3.22mmol)。将N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(817.0mg,2.15mmol)用N,N-二甲基甲酰胺(20mL)溶解后滴入上述溶液中,室温搅拌反应2小时。TLC显示反应完全,减压浓缩后反应液经制备HPLC纯化得化合物SMP-86467-1,重788.0mg,收率55%。
MS(ESI)m/z:654[M+H]
步骤2:化合物SMP-86467-2的制备
100mL反应瓶中,将溴乙酸叔丁酯(312.0mg,1.60mmol)与化合物SMP-86467-1(788.0mg,1.20mmol)用乙腈(20mL)溶解,加入碳酸钾(828.0mg,6.00mmol),升温至55℃反应20小时。TLC显示反应完全,将反应液冷却至室温后,过滤,滤液减压浓缩至干,残余物硅胶柱层析(二氯甲烷:甲醇=20:1)得化合物SMP-86467-2,重900.0mg,收率97%。
MS(ESI)m/z:768[M+H]
步骤3:化合物SMP-86467-3的制备
100mL反应瓶中,将化合物SMP-86467-2(900.0mg,1.17mmol)用甲醇(20mL)溶解,加入钯炭催化剂(90.0mg),用氢气球置换瓶内空气,室温搅拌反应20小时。LC-MS显示反应完全,过滤,滤液减压浓缩至干得化合物SMP-86467-3,重467.0mg,收率80%。
MS(ESI)m/z:500[M+H]
步骤4:化合物SMP-86467-4的制备
50mL反应瓶中,将化合物SMP-86467-3(467.0mg,0.93mmol)与化合物SMP-37860-2(1.01g,2.00mmol)用乙腈(12mL)溶解,加入碳酸钾(552.0mg,4.00mmol),室温下反应20小时。LC-MS检测反应完全,过滤,滤液减压浓缩至干,硅胶柱层析(二氯甲烷:甲醇=12:1)得化合物SMP-86467-4,重737.0mg,收率60%。
MS(ESI)m/z:661[M/2+H]
步骤5:化合物SMP-86467-5的制备
10mL反应瓶中,加入化合物SMP-86467-4(737.0mg,0.56mmol),然后加入三氟乙酸(4mL),室温搅拌反应3小时。LC-MS检测反应完成,减压浓缩除去三氟乙酸得化合物SMP-86467-5,重609.0mg,收率90%。MS(ESI)m/z:1165[M+H]
步骤6:化合物SMP-86467-6的制备
25mL反应瓶中,将与化合物SMP-86467-5(609.0mg,0.52mmol)用纯水(6mL)溶解,加入碳酸氢钠(189.0mg,2.25mmol)。将N-甲氧基羰基顺丁烯二酰亚胺(124mg,0.80mmol)用四氢呋喃(3mL)溶解,滴入上述溶液中,反应2小时。LC-MS检测反应完成减压浓缩去除四氢呋喃,残余物经制备HPLC纯化得化合物SMP-86467-6,重620.0mg,收率95%。
MS(ESI)m/z:623[M/2+H]
步骤7:化合物SMP-86467的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(1.0mL)溶解化合物SMP-86467-6(15.0mg,0.012mmol)与中间体D(20.0mg,0.009mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.012mmol),三乙胺(2.0mg,0.015mmol),室温搅拌反应2小时。LC-MS检测反应完成,反应液经制备HPLC纯化得化合物SMP-59623,重11.0mg,收率36%。MS(ESI)m/z:1139[M/3+H]
实施例76、化合物SMP-76899的制备
步骤1:化合物SMP-76899-1的制备
50mL反应瓶中,用N,N-二甲基甲酰胺(15mL)溶解3-[(23-甲氧基-3,6,9,12,15,18,21-七氧杂二十三烷-1-基)氧基]丙酸(500.0mg,1.09mmol)与1,7-二-(N-叔丁氧羰基甲基)-1,4,7,10-四氮杂环十二烷(181.0mg,0.45mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(437.0mg,1.15mmol),三乙胺(141.4mg,1.40mmol),室温搅拌反应7小时。LC-MS检测反应完全,反应液经制备HPLC纯化得化合物SMP-76899,重448.0mg,收率78%。
MS(ESI)m/z:639[M/2+H]
步骤2:化合物SMP-76899-2的制备
10mL反应瓶中,加入化合物SMP-76899-1(448.0mg,0.34mmol),然后加入三氟乙酸(4mL),室温搅拌反应3小时。LC-MS检测反应完全,减压蒸馏除去三氟乙酸,残余液反应液经制备HPLC纯化得化合物SMP-76899-2,重350.0mg,收率86%。
MS(ESI)m/z:583[M/2+H]
步骤3:化合物SMP-76899-3的制备
25mL反应瓶中,将1-(2-氨基乙基)-1H-吡咯-2,5-二酮盐酸盐(39.0mg,0.22mmol)与化合物SMP-76899-2(350.0mg,0.29mmol)用N,N-二甲基甲酰胺(5mL)溶解,加入三乙胺(50.5mg,0.50mmol)。将N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(91.2mg,0.24mmol)用N,N-二甲基甲酰胺(3mL)溶解后滴入上述溶液中,室温搅拌反应3小时。LC-MS检测反应完全,反应液经制备HPLC纯化得化合物SMP-76899-3,重250.0mg,收率65%。
MS(ESI)m/z:644[M/2+H]
步骤4:化合物SMP-76899的制备
4mL反应瓶中,用N,N-二甲基甲酰胺(1.0mL)溶解化合物SMP-76899-3(9.0mg,0.007mmol)与中间体C(15.0mg,0.006mmol),加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),三乙胺(2mg,0.02mmol),室温搅拌反应2小时。LC-MS检测反应完全,反应液经制备HPLC纯化得化合物SMP-76899,重6.4mg,收率28%。
MS(ESI)m/z:1186[M/3+H]
实施例77、化合物SMP-27341的制备
步骤1:化合物SMP-27341-1的制备
25mL反应瓶中,加入化合物SMP-27341-0(300.0mg,0.40mmol),N,N-二甲基甲酰胺(8mL),完全澄清后加入N,N-二异丙基乙胺(7.8mg,0.78mmol)、1-羟基苯并三唑(27.0mg,0.20mmol)后一次性加入一甲基澳瑞他汀E(286.0mg,0.4mmol)室温搅拌2小时。LC-MS显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物经柱层析(二氯甲烷:甲醇=10:1)纯化得化合物SMP-27341-1,重475.0mg,收率89%。
MS(ESI)m/z:1344[M+H]
步骤2:化合物SMP-27341-2的制备
25mL反应瓶中,加入中间体SMP-27341-2(241.0mg,0.18mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(54.0mg,0.36mmol),N,N-二甲基甲酰胺(6mL),室温搅拌反应30分钟,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物制备HPLC纯化得化合物SMP-27341-2,重172.0mg,收率86%。
MS(ESI)m/z:1122[M+H]
步骤3:化合物SMP-27341的制备
4mL反应瓶中加入化合物SMP-37860-5(25.0mg,0.02mmol),溶剂N,N-二甲基甲酰胺(2mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.4mg,0.03mmol),N,N-二异丙基乙胺(3.9mg,0.03mmol),室温下反应5分钟后,加入化合物SMP-27341-2(22.0mg,0.02mmol)搅拌反应25分钟,TLC显示反应完全,反应液经制备HPLC纯化得到目标化合物SMP-27341,重23.0mg,收率51%。
MS(ESI)m/z:1168[M/2+H]
实施例78、化合物SMP-39205的制备
步骤1:化合物SMP-39205的制备
于10mL反应瓶中加入化合物SMP-30920-2(35.0mg,0.024mmol),溶剂N,N-二甲基甲酰胺(3mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.0mg,0.024mmol),N,N-二异丙基乙胺(4.0mg,0.03mmol),室温下反应5分钟后,加入化合物J(43.0mg,0.020mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-39205,重51.0mg,收率71%。MS(ESI)m/z:1187[M/3+H]
实施例80、化合物SMP-68962的制备
步骤1:化合物SMP-68962-1的制备
10mL反应瓶中,依次加入SMP-68962-0(33.5mg,0.060mmol),中间体G(30.0mg,0.030mmol),N,N-二甲基甲酰胺(2mL),N,N-二异丙基乙胺(19.4mg,0.150mmol),于冰水条件下缓慢滴加N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(11.4mg,0.030mmol,溶于0.5mL N,N-二甲基甲酰胺中),滴加完毕后继续反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-68962-1,重25.0mg,收率54.4%。
MS(ESI)m/z:767[M/2+H]
步骤2:化合物SMP-68962-2的制备
10mL反应瓶中,依次加入SMP-68962-1(25.0mg,0.016mmol),中间体B(16.5mg,0.019mmol),N,N-二异丙基乙胺(3.1mg,0.024mmol),N,N-二甲基甲酰胺(2mL),再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(7.4mg,0.019mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-68962-2,重20.0mg,收率53.1%。
MS(ESI)m/z:785[M/3+H]
步骤3:化合物SMP-68962-3的制备
10mL反应瓶中,依次加入SMP-68962-2(20.0mg,0.008mmol),N,N-二甲基甲酰胺(1.5mL),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.0mg,0.012mmol),于室温条件下搅拌反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-68962-3,重12.0mg,收率70.4%。
MS(ESI)m/z:711[M/3+H]
步骤4:化合物SMP-68962的制备
10mL反应瓶中,依次加入SMP-68962-3(12.0mg,0.0056mmol),SMP-07861-2(5.0mg,0.0067mmol),N,N-二异丙基乙胺(1.1mg,0.0084mmol),N,N-二甲基甲酰胺(1.5mL),再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.5mg,0.0067mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-68962,重9.6mg,收率60.0%。MS(ESI)m/z:953[M/3+H]
实施例81、化合物SMP-31135的制备
步骤1:化合物SMP-31135-1的制备
10mL反应瓶中,依次加入SMP-31135-0(39.4mg,0.060mmol),中间体G(30.0mg,0.030mmol),N,N-二异丙基乙胺(19.4mg,0.150mmol),N,N-二甲基甲酰胺(2mL),于冰水条件下缓慢滴加N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(11.4mg,0.030mmol,溶于0.5mL N,N-二甲基甲酰胺中),待滴加完毕后,继续在此温度下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-31135-1,重27mg,收率55.3%。
MS(ESI)m/z:815[M/2+H]
步骤2:化合物SMP-31135-2的制备
10mL反应瓶中,依次加入SMP-31135-1(27.0mg,0.016mmol),B(16.0mg,0.019mmol),N,N-二异丙基乙胺(3.1mg,0.024mmol),N,N-二甲基甲酰胺(2mL),室温搅拌,再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(7.2mg,0.019mmol),于此条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-31135-2,重22.0mg,收率56.1%。
MS(ESI)m/z:818[M/3+H]
步骤3:化合物SMP-31135-3的制备
10mL反应瓶中,依次加入SMP-31135-2(22.0mg,0.009mmol),N,N-二甲基甲酰胺(1.5mL),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(2.0mg,0.013mmol),于室温条件下搅拌反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-31135-3,重15.0mg,收率74.8%。
MS(ESI)m/z:744[M/3+H]
步骤4:化合物SMP-31135的制备
10mL反应瓶中,依次加入SMP-31135-3(15mg,0.0067mmol),SMP-61694-2(8.1mg,0.0081mmol),N,N-二异丙基乙胺(1.3mg,0.010mmol),N,N-二甲基甲酰胺(1.5mL),再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.1mg,0.0081mmol),于室温条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-31135,重11.2mg,收率52.1%。MS(ESI)m/z:1071[M/3+H]
实施例82、化合物SMP-64791的制备
步骤1:化合物SMP-64791-1的制备
10mL反应瓶中,依次加入SMP-49182-6(50.0mg,0.11mmol),中间体I(79mg,0.13mmol),N,N-二异丙基乙胺(20.6mg,0.16mmol),N,N-二甲基甲酰胺(4mL),室温搅拌,再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(49.4mg,0.13mmol),于此条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-64791-1,重45.0mg,收率38.8%。
MS(ESI)m/z:1055[M+H]
步骤2:化合物SMP-64791-2的制备
10mL反应瓶中,依次加入SMP-64791-1(45.0mg,0.043mmol),二氯甲烷(2mL),三氟乙酸(2mL),于室温条件下搅拌反应2小时,LC-MS显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得化合物SMP-64791-2,重30.0mg,收率70.0%。
MS(ESI)m/z:999[M+H]
步骤3:化合物SMP-64791的制备
10mL反应瓶中,依次加入SMP-64791-2(6.3mg,0.0063mmol),中间体C(12.0mg,0.0052mmol),N,N-二异丙基乙胺(1.0mg,0.0078mmol),N,N-二甲基甲酰胺(1.5mL),室温搅拌,再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(2.4mg,0.0063mmol),于此条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-64791,重8.6mg,收率52%。
MS(ESI)m/z:1089[M/3+H]
实施例83、化合物SMP-26598的制备
步骤1:化合物SMP-26598-2的制备
500mL反应瓶中,加入中间体SMP-26598-1(21.5g,56.49mmol)和乙腈(200mL),室温搅拌,随后依次加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(10.8g,56.49mmol),N-羟基丁二酰亚胺(6.5g,56.49mmol),于此条件搅拌反应过夜,TLC显示反应完全,将反应液过滤,所得固体真空干燥,得化合物SMP-26598-2,重22.0g,收率81%。
MS(ESI)m/z:478[M+H]
步骤3:化合物SMP-26598-3的制备
500mL反应瓶中,依次加入中间体L-天冬氨酸(6.0g,46.12mmol),碳酸氢钠(7.7g,92.24mmol),水(20mL),四氢呋喃(200mL),室温搅拌,待完全澄清后将化合物SMP-26598-2(22g,46.12mmol)溶于乙二醇二甲醚(50mL)中,缓慢加入到上述反应液中。继续搅拌反应过夜,TLC显示反应完全,反应液减压浓缩,残余物缓慢滴入0.5M盐酸水溶液(500mL)中,析出大量固体,过滤,所得固体真空干燥,得化合物SMP-26598-3,重15.0g,收率65%。
MS(ESI)m/z:497[M+H]
步骤4:化合物SMP-26598-4的制备
25mL反应瓶中加入化合物SMP-26598-3(450.0mg,0.90mmol),溶剂N,N-二甲基甲酰胺(8mL),室温搅拌,待溶液完全澄清后,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(410.4mg,1.08mmol),N,N-二异丙基乙胺(175.4mg,1.36mmol),反应5分钟后,加入化合物甘氨酸叔丁酯(141.5mg,1.08mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化,得中间体SMP-26598-4,重330.0mg,收率60.2%。
MS(ESI)m/z:610[M+H]
步骤5:化合物SMP-26598-5的制备
25mL反应瓶中加入化合物SMP-26598-4(330.0mg,0.54mmol),溶剂三氟乙酸(4mL),于室温条件下搅拌反应30分钟,LC-MS显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化,得中间体SMP-26598-5,重200.0mg,收率67.0%。
MS(ESI)m/z:554[M+H]
步骤6:化合物SMP-26598-6的制备
于50mL反应瓶中加入化合物SMP-26598-5(200.0mg,0.36mmol),溶剂四氢呋喃(20mL),室温搅拌,待溶液完全澄清后,依次加入四乙酸铅(191.8mg,0.44mmol),吡啶(44.8mg,0.56mmol),70℃搅拌反应过夜,TLC显示反应完全,反应液过滤,滤液减压浓缩,残余物经柱层析(二氯甲烷:甲醇=12:1)纯化,得中间体SMP-26598-6,重132.0mg,收率64.7%。MS(ESI)m/z:568[M+H]
步骤7:化合物SMP-26598-7的制备
25mL反应瓶中加入化合物SMP-26598-6(132.0mg,0.23mmol),溶剂四氢呋喃(10mL),羟基乙酸(21.0mg,0.28mmol),于冰水浴下降温至0℃,待温度降至0℃,一次性加入对甲苯磺酸(21.0mg,0.12mmol),而后缓慢升至室温并于此温度下搅拌反应1.5小时,TLC显示反应完全,反应液过滤后减压浓缩,残余物经制备HPLC纯化得中间体SMP-26598-7,重86.0mg,收率64.1%。
MS(ESI)m/z:584[M+H]
步骤8:化合物SMP-26598-8的制备
25mL反应瓶中加入化合物SMP-26598-7(62.2mg,0.107mmol),溶剂N,N-二甲基甲酰胺(3mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(40.5mg,0.107mmol),N,N-二异丙基乙胺(17.2mg,0.133mmol),反应5分钟后,加入化合物SMP-34048-5(45mg,0.089mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得中间体SMP-26598-8,重61.0mg,收率64.0%。MS(ESI)m/z:1072[M+H]
步骤9:化合物SMP-26598-9的制备
25mL反应瓶中,加入中间体SMP-26598-8(61.0mg,0.057mmol),N,N-二甲基甲酰胺(3mL),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(17.3mg,0.114mmol),于室温条件下搅拌反应30分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得化合物SMP-26598-9,重33.0mg,收率68.2%。MS(ESI)m/z:850[M+H]
步骤10:化合物SMP-26598的制备
25mL反应瓶中加入化合物SMP-93566-4(17.8mg,0.046mmol),溶剂N,N-二甲基甲酰胺(3mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(17.8mg,0.046mmol),N,N-二异丙基乙胺(7.5mg,0.058mmol),并于此温度下反应5分钟后,加入化合物SMP-26598-9(33.0mg,0.039mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化,得中间体SMP-26598,重27.0mg,收率57.0%。
MS(ESI)m/z:1215[M+H]
实施例85、化合物SMP-09168的制备
步骤1:化合物SMP-09168-1的制备
25mL反应瓶中加入化合物马来酰亚胺-四聚乙二醇-羧酸(30.0mg,0.087mmol),溶剂N,N-二甲基甲酰胺(3mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(39.6mg,0.104mmol),N,N-二异丙基乙胺(16.8mg,0.13mmol),反应5分钟后,加入化合物SMP-93566-2(25.0mg,0.087mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经柱层析(石油醚:乙酸乙酯=1:1)纯化,得中间体SMP-09168-1,重38.0mg,收率71.0%。
MS(ESI)m/z:616[M+H]
步骤2:化合物SMP-09168-2的制备
25mL反应瓶中加入化合物SMP-09168-1(38.0mg,0.062mmol),溶剂三氟乙酸(1mL),于室温条件下搅拌反应20分钟,LC-MS显示反应完全,反应液减压浓缩除去多余的三氟乙酸,残余物经制备HPLC纯化,得中间体SMP-09168-2,重29.0mg,收率83.5%。
MS(ESI)m/z:560[M+H]
步骤3:化合物SMP-09168的制备
25mL反应瓶中加入化合物SMP-09168-2(11.7mg,0.021mmol),溶剂N,N-二甲基甲酰胺(2mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(8.0mg,0.021mmol),N,N-二异丙基乙胺(3.3mg,0.026mmol),反应5分钟后,加入化合物SMP-58054-2(20.0mg,0.017mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得中间体SMP-09168,重23.0mg,收率78.4%。MS(ESI)m/z:1726[M+H]
实施例86、化合物SMP-87055的制备
步骤1:化合物SMP-87055-2的制备
500mL反应瓶中,加入中间体SMP-87055-1(13.5g,45.45mmol),和乙腈(200mL),室温搅拌,依次加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(10.5g,54.54mmol),N-羟基丁二酰亚胺(6.3g,54.54mmol),继续于此温度下搅拌反应过夜,TLC显示反应完全,反应液过滤,所得固体真空干燥,得化合物SMP-26598-2,重14.0g,收率78.4%。
MS(ESI)m/z:393[M+H]
步骤2:化合物SMP-87055-3的制备
500mL反应瓶中,加入中间体L-苯丙氨酸(6.4g,35.71mmol),碳酸氢钠(6.0g,71.42mmol),水(20mL),四氢呋喃(200mL),室温搅拌,待溶液完全澄清后将化合物SMP-87055-2(14.0g,35.71mmol)溶于乙二醇二甲醚(50mL)中,缓慢加入到上述反应液中。继续搅拌反应过夜,TLC显示反应完全,反应液减压浓缩,残余物缓慢滴入0.5M盐酸水溶液(500mL)中,析出大量固体,过滤,所得固体真空干燥,得化合物SMP-87055-3,重13.0g,收率82.0%。
MS(ESI)m/z:445[M+H]
步骤3:化合物SMP-87055-4的制备
25mL反应瓶中加入化合物SMP-87055-3(13.0g,29.28mmol),溶剂N,N-二甲基甲酰胺(30mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(11.1g,29.28mmol),N,N-二异丙基乙胺(5.6g,43.81mmol),反应5分钟后,加入化合物甘氨酸叔丁酯(4.6g,35.05mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物经柱层析(二氯甲烷:甲醇=15:1)纯化得中间体SMP-87055-4,重9.1g,收率55.8%。
MS(ESI)m/z:558[M+H]
步骤4:化合物SMP-87055-5的制备
25mL反应瓶中加入化合物SMP-87055-4(9.1g,16.34mmol),溶剂三氟乙酸(30mL),于室温条件下搅拌反应30分钟,LC-MS显示反应完全,反应液减压浓缩,残余物经制备HPLC纯化得中间体SMP-87055-5,重6.7g,收率81.8%。
MS(ESI)m/z:502[M+H]
步骤5:化合物SMP-87055-6的制备
100mL反应瓶中加入中间体SMP-87055-5(2.1g,4.19mmol),4-氨基苯甲醇(1.0g,8.38mmol),N,N-二甲基甲酰胺(3mL),室温搅拌,再加入2-乙氧基-1-乙氧羰酰基-1,2-二氢喹啉(2.1g,8.38mmol),继续搅拌反应2小时,反应液减压浓缩除去溶剂,残余物经硅胶柱层析(二氯甲烷:甲醇=15:1)得化合物SMP-87055-6,重1.7g,收率67.0%。
MS(ESI)m/z:607[M+H]
步骤6:化合物SMP-87055-7的制备
25mL反应瓶中,将中间体SMP-87055-6(900.0mg,1.48mmol)溶解于N,N-二甲基甲酰胺(10mL)中,室温搅拌,溶解再加入二对硝基苯基碳酸酯(676.1mg,2.22mmol)与三乙胺(298.7mg,2.96mmol),继续搅拌反应过夜,TLC监测原料反应完全,反应液减压浓缩,残余物经硅胶柱层析(二氯甲烷:甲醇=20:1)纯化得化合物SMP-87055-7,重740.0mg,收率64.7%。MS(ESI)m/z:772[M+H]
步骤7:化合物SMP-87055-8的制备
25mL反应瓶中,加入化合物SMP-87055-7(461mg,0.60mmol),N,N-二甲基甲酰胺(5mL),室温搅拌,待溶液完全澄清后,依次加入N,N-二异丙基乙胺(103.2mg,0.80mmol),1-羟基苯并三唑(27.0mg,0.20mmol),一甲基澳瑞他汀E(286.8mg,0.40mmol),继续室温搅拌2小时。LC-MS显示反应完全,反应液减压浓缩,残余物经柱层析纯化(二氯甲烷:甲醇=10:1),得化合物SMP-87055,重480.0mg,收率88.9%。
MS(ESI)m/z:1351[M+H]
步骤8:化合物SMP-87055-9的制备
25mL反应瓶中,加入中间体SMP-87055-8(240.0mg,0.18mmol),N,N-二甲基甲酰胺(4mL),室温搅拌,再加入1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(54.0mg,0.36mmol),继续反应20分钟,TLC显示反应完全,反应液减压浓缩,残余物制备HPLC纯化得化合物SMP-87055-9,重173.0mg,收率85.2%。
MS(ESI)m/z:1129[M+H]
步骤9:化合物SMP-87055的制备
10mL反应瓶中加入化合物SMP-93566-4(9.2mg,0.024mmol),溶剂N,N-二甲基甲酰胺(1.5mL),室温搅拌,依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(9.1mg,0.024mmol),N,N-二异丙基乙胺(3.9mg,0.030mmol),反应5分钟后,加入化合物SMP-87055-9(22.0mg,0.020mmol),继续搅拌反应25分钟,TLC显示反应完全,反应液减压浓缩,残余物制备HPLC纯化,得到目标产物SMP-87055,重12.0mg,收率40.1%。MS(ESI)m/z:1494[M+H]
实施例87、化合物SMP-34146的制备
步骤1:化合物SMP-34146-2的制备
50mL反应瓶中加入SMP-34146-1(500.0mg,0.83mmol),氯甲酸对硝基苯酯(251.0mg,1.25mmol),N,N-二甲基甲酰胺(10mL),完全澄清后加入N,N-二异丙基乙胺(321mg,2.49mmol),室温搅拌反应3小时,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=15:1),得化合物SMP-34146-2,重600.0mg,收率94%。
MS(ESI)m/z:767[M+H]
步骤2:化合物SMP-34146-3的制备
25mL反应瓶中加入SMP-34146-2(300.0mg,0.39mmol),艾立布林(285.0mg,0.39mmol),N,N-二甲基甲酰胺(5mL),完全溶清后,依次加入1-羟基苯并三唑(58.1mg,0.43mmol),N,N-二异丙基乙胺(150.9mg,1.17mmol),室温搅拌反应1小时,TLC显示反应完全,减压浓缩除去N,N-二甲基甲酰胺,残余物薄层层析纯化(二氯甲烷:甲醇=12:1),得化合物SMP-34146-3,重180.0mg,收率33.9%。
MS(ESI)m/z:679[M/2+H]
步骤3:化合物SMP-34146-4的制备
10mL反应瓶中加入SMP-34146-3(176.5mg,0.13mmol),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(29.1mg,0.19mmol),N,N-二甲基甲酰胺(3mL),室温搅拌反应30分钟,LC-MS检测显示反应完全,反应液经制备HPLC纯化得化合物SMP-34146-4,重90.0mg,收率61%。
MS(ESI)m/z:568[M/2+H]
步骤4:化合物SMP-34146的制备
10mL反应瓶中加入中间体SMP-34146-4(34.1mg,0.03mmol),SMP-93566-4(11.5mg,0.03mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(11.4mg,0.03mmol),N,N-二异丙基乙胺(10.3mg,0.08mmol),室温搅拌反应20分钟,LC-MS检测显示反应完全,反应液经制备HPLC纯化得化合物SMP-34146,重33.3mg,收率74%。
MS(ESI)m/z:750[M/2+H]
实施例88、化合物SMP-02692的制备
步骤1:化合物SMP-02692的制备
10mL反应瓶中,加入SMP-93566(10mg,0.007mmol),丙酮(1mL),碘甲烷(2.0mg,0.014mmol),氮气保护,室温搅拌反应过夜。LC-MS检测反应完全,反应液直接加入少量乙腈和水,冻干得化合物SMP-02692,重10.2mg,收率93.7%。
MS(ESI)m/z:1428[M+H]
II.靶向接头-药物偶联物的制备
偶联方法:采用抗体上的二硫键进行药物偶联生成抗体—药物偶联物,先将抗体制备成浓度为20mg/mL的溶液。取0.1mL抗体与1.5mL的离心管中,加入PBS(pH 7.4)/DTPA溶液(293uL),向其中添加5mM TCEP水溶液(6.4uL,相对于一分子抗体为2.4当量),于25℃孵育2小时,将抗体内铰链部的二硫键还原为巯基。然后向上述溶液中添加10%的医用DMSO和含有10mM的payload(13.3ul,相对于一分子抗体为10eq),在25℃下震荡(转速为每分钟400转)反应2小时,将药物接头和抗体连接,得到抗体—药物偶联物。
实施例89实施例13-实施例88对应抗体-药物偶联物的制备
将以上述实施例13-实施例88制备得到的化合物作为药物链接组装单元,与Her2抗体采用前述偶联方法偶联,得到对应的实施例抗体-药物偶联物。
抗体—药物偶联物的浓缩:将抗体-药物偶联物放入到5000K(MiI1iporeCo.)的超滤管中,使用高速冷冻离心机(GENESPEED 1580R)于2℃下进行离心操作(3500G离心10分钟)。
以下为对比样品的制备方法。
对比例部分
I.对比靶向接头-药物偶联物的制备
对比例1、化合物SMP-81641的制备
步骤1:化合物SMP-81641的制备
10mL反应瓶中,加入6-马来酰亚胺己酸(6.0mg,0.020mmol),中间体SMP-58054-1(21.0mg,0.018mmol),N,N-二甲基甲酰胺(3mL),1-羟基苯并三唑(2.7mg,0.021mmol),三乙胺(5.1mg,0.050mmol),室温搅拌反应30分钟。LC-MS检测反应完全,反应液经制备HPLC纯化得化合物SMP-81641,重8.9mg,收率23%。
MS(ESI)m/z:1378[M+H]
对比例2、化合物SMP-31896的制备
步骤1:化合物SMP-31896的制备
4mL反应瓶中加入6-马来酰亚胺己酸(2.1mg,0.006mmol),溶剂N,N-二甲基甲酰胺(0.5mL),待反应液澄清后依次加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.8mg,0.01mmol),N,N-二异丙基乙胺(1.3mg,0.01mmol),室温下反应5分钟后,加入中间体SMP-82444-1(14.0mg,0.006mmol),搅拌反应25分钟。TLC显示反应完全,反应液制备HPLC纯化,得化合物SMP-31896,重10.9mg,收率72%。
MS(ESI)m/z:1280[M/2+H]
对比例3、化合物SMP-74544的制备
步骤1:化合物SMP-74544的制备
10mL反应瓶中加入化合物6-马来酰亚胺己酸(13.0mg,0.06mmol),溶剂N,N-二甲基甲酰胺(3mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(22.8mg,0.06mmol),N,N-二异丙基乙胺(7.6mg,0.06mmol),室温下反应5分钟后,加入中间体D(131.0mg,0.06mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得化合物SMP-74544,重115.0mg,收率80%。MS(ESI)m/z:1192[M/2+H]
对比例4、化合物SMP-79786的制备
步骤1:化合物SMP-79786的制备
25mL反应瓶中加入化合物6-马来酰亚胺己酸(13.0mg,0.06mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(22.8mg,0.06mmol),N,N-二异丙基乙胺(7.7mg,0.06mmol),室温下反应5分钟后,加入中间体A(62.0mg,0.06mmol)室温下反应25分钟,TLC显示反应完全,减压浓缩,残余物经制备HPLC纯化得化合物SMP-79786,重48.0mg,收率65%。
MS(ESI)m/z:1241[M+H]
对比例5、化合物SMP-50206的制备
步骤1:化合物SMP-50206的制备
4mL反应瓶中加入化合物马来酰亚胺-四聚乙二醇-丙酸(2.0mg,0.006mmol),溶剂N,N-二甲基甲酰胺(0.5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(2.1mg,0.06mmol),N,N-二异丙基乙胺(10.3mg,0.08mmol),室温下反应5分钟后,加入中间体D(13mg,0.006mmol)搅拌反应25分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-50206,重11.1mg,收率72%。
MS(ESI)m/z:1259[M/2+H]
对比例6、化合物SMP-77169的制备
步骤1:化合物SMP-77169-1的制备
10mL反应瓶中,依次加入SMP-34048-5(50.0mg,0.099mmol),中间体B-1(76.5mg,0.119mmol),N,N-二异丙基乙胺(19.1mg,0.148mmol),N,N-二甲基甲酰胺(4mL),室温搅拌,再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(45.0mg,0.119mmol),于此条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-77169-1,重45.0mg,收率40.1%。MS(ESI)m/z:1134[M+H]
步骤2:化合物SMP-77169-2的制备
10mL反应瓶中,依次加入SMP-77169-1(45.0mg,0.040mmol),N,N-二甲基甲酰胺(3mL),1,8-二偶氮杂双螺环[5.4.0]十一-7-烯(9.0mg,0.060mmol),于室温条件下搅拌反应30分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-77169-2,重25.0mg,收率68.5%。
MS(ESI)m/z:913[M+H]
步骤3:化合物SMP-77169的制备
10mL反应瓶中,依次加入SMP-77169-2(25.0mg,0.027mmol),马来酰亚胺丙酸(5.6mg,0.033mmol),N,N-二异丙基乙胺(5.3mg,0.041mmol),N,N-二甲基甲酰胺(2mL),室温搅拌,再加入N,N,N′,N′-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(12.5mg,0.033mmol),于此条件下反应20分钟,LC-MS显示大部分为目标化合物分子量,反应液减压浓缩,得到粗产品,粗产品经制备HPLC纯化得化合物SMP-77169,重15.0mg,收率52.3%。MS(ESI)m/z:1063[M+H]
对比例7、化合物SMP-32666的制备
步骤1:化合物SMP-32666的制备
于10mL反应瓶中,依次加入中间体C(20mg,0.008mmol),马来酰亚胺-四聚乙二醇-羧酸(2.8mg,0.008mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.0mg,0.008mmol),N,N-二异丙基乙胺(3.0mg,0.024mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-32666,重10.0mg,收率43.7%。
MS(ESI)m/z:1307[M/2+H]
对比例8、化合物SMP-88394的制备
步骤1:化合物SMP-88394的制备
10mL反应瓶中加入中间体SMP-58054-2(34.0mg,0.03mmol),3-马来酰亚胺基丙酸(45.1mg,0.03mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(11.4mg,0.03mmol),N,N-二异丙基乙胺(10.3mg,0.081mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-88394,重25.0mg,收率79%。
MS(ESI)m/z:668[M/2+H]
对比例9、化合物SMP-49994的制备
步骤1:化合物SMP-49994的制备
于10mL反应瓶中,依次加入中间体C(20mg,0.008mmol),6-马来酰亚胺基己酸(1.7mg,0.008mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.0mg,0.008mmol),N,N-二异丙基乙胺(3.0mg,0.024mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-49994,重10。0mg,收率46.1%。
MS(ESI)m/z:1340[M/2+H]
对比例10、化合物SMP-54731的制备
步骤1:化合物SMP-54731的制备
于10mL反应瓶中,依次加入中间体C(20mg,0.008mmol),马来酰亚胺-八聚乙二醇-羧酸(4.2mg,0.008mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(3.0mg,0.008mmol),N,N-二异丙基乙胺(3.0mg,0.024mmol),室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-54731,重6.0mg,收率24.6%。
MS(ESI)m/z:1395[M/2+H]
对比例11、化合物SMP-02571的制备
步骤1:化合物SMP-02571的制备
于25mL反应瓶中加入化合物马来酰亚胺-二聚乙二醇-羧酸(20.0mg,0.078mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(30.0mg,0.079mmol),N,N-二异丙基乙胺(15.0mg,0.12mmol),室温下反应5分钟后,加入化合物H(200.0mg,0.081mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-02571,重160.0mg,收率74%。
MS(ESI)m/z:1352[M/2+H]
对比例12、化合物SMP-39835的制备
步骤1:化合物SMP-39835的制备
于25mL反应瓶中加入化合物马来酰亚胺丙酸(17.0mg,0.10mmol),溶剂N,N-二甲基甲酰胺(5mL),依次加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(38.0mg,0.10mmol),N,N-二异丙基乙胺(15.0mg,0.12mmol),室温下反应5分钟后,加入化合物A(84.0mg,0.08mmol)搅拌反应25分钟,TLC显示反应完全,减压浓缩除去多余的N,N-二甲基甲酰胺,残余物经制备HPLC纯化得到目标产物SMP-39835,重80.0mg,收率83%。MS(ESI)m/z:1199[M+H]
对比例13、化合物SMP-02524的制备
步骤1:化合物SMP-02524的制备
于10mL反应瓶中,依次加入中间体D(50.0mg,0.023mmol),马来酰亚胺-二聚乙二醇-羧酸(6.0mg,0.023mmol),N,N-二甲基甲酰胺(2mL),完全澄清后,加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(9.0mg,0.023mmol),N,N-二异丙基乙胺(9.0mg,0.069mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物SMP-02524,重35mg,收率63.1%。
MS(ESI)m/z:1215[M/2+H]
对比例14、化合物DS-8201的制备
步骤1:化合物DS-8201的制备
于10mL反应瓶中,依次加入中间体B(50.0mg,0.06mmol),马来酰亚胺己酸(12.6mg,0.06mmol),N,N-二甲基甲酰胺(2mL),完全溶清后,依次加入N,N,N’,N’-四甲基-O-(7-氮杂苯并三唑-1-基)六氟磷酸脲(22.2mg,0.06mmol),N,N-二异丙基乙胺(23.2mg,0.18mmol)。室温搅拌反应20分钟,TLC显示反应完全,反应液经制备HPLC纯化得化合物DS-8201,重35mg,收率56.4%。
MS(ESI)m/z:1034[M+H]
II.对比靶向接头-药物偶联物的制备
参照实施例部分制备靶向接头-药物偶联物的方法,分别以上述对比例1-对比例14制备得到的化合物作为药物链接组装单元,采用实施例89的偶联方法与Her2抗体偶联,得到对应的对比抗体-药物偶联物。
下述以抗体—药物偶联物(ADC)为例说明本发明在靶向接头-药物偶联物的连接子中引入式A所示结构给靶向接头-药物偶联物带来的效果:
实验例1:抗体—药物偶联物的检测
1.抗体—药物偶联物的检测方法
受试样品:前述实施例89制备得到的本发明实施例ADC和对比例制备得到的对比例ADC。
利用分子排阻高效液相色谱法(SE-HPLC)检测抗体—药物偶联物的聚体(高分子组分)。使用Biocore SEC色谱柱(7.8×300mm,5μm),流动相为含300mM氯化钠的50mM磷酸盐(pH6.8),流速0.5mL/min,进样样品50ug,进样体积10ul,观测280nm处的UV吸收度至少30min,以面积归一化法计算抗体—药物偶联物的聚体含量。
利用反相高效液相色谱-质谱法(RP-HPLC-MS)检测抗体—药物偶联物的药物抗体偶联比率(又称抗体-药物比例,简称DAR)。用50mmol/L的Tris缓冲液(pH8.0)稀释ADC样品至1mg/ml,加入新鲜制备的二硫苏糖醇(DTT)储备液,使DTT终浓度为50mmol/L,37℃孵育30min。使用PLRP-S色谱柱(
利用疏水作用色谱(HIC)检测抗体—药物偶联物中裸抗的含量。使用BiocoreHIC-Butyl色谱柱(4.6×150mm,5μm)。流动相A为含2M硫酸铵的100mM磷酸盐水溶液(pH7.0),流动相B为100mM磷酸盐水溶液(pH7.0):异丙醇=80:20(V/V)。进样样品50ug,进样10ul。流速1mL/min流动相A以100%运行3min。3~25min,流动相B从0%到100%,25.1流动相B降到0%,运行到30min。观测280nm处的UV吸收度。以抗体—药物偶联物的抗体定位裸抗峰的保留时间,根据面积归一化法计算抗体—药物偶联物的裸抗含量。
2.抗体—药物偶联物的检测结果
表1.抗体—药物偶联物的检测结果
/>
/>
上表1中,聚体含量表示的是利用分子排阻高效液相色谱法检测到的ADC中的聚体(高分子组分)百分比,过高的聚体含量可能会引起免疫原性反应;裸抗含量表示的是利用疏水作用色谱法检测到的ADC中裸抗的百分比,过高的裸抗含量可能会导致裸抗成为ADC的竞争性抑制剂。过高的聚体含量和裸抗含量会影响ADC和靶点的结合,从而影响其疗效。
DAR值表示一个抗体上偶联的药物链接组装单元的平均个数,DAR值太低无法实现有效的细胞杀伤,导致ADC疗效不足;在ADC允许的情况下,更高的DAR值能够实现更高效率的药物递送,但是随着DAR值的升高,疏水性payload的含量升高,导致ADC的疏水性增加,从而加速ADC在体内的清除,导致ADC半衰期缩短及毒性增加。
本发明实施例ADC和对比例ADC结构的区别在于连接子上是否含有式A所示结构。
同时,疏水性的增加在偶联步骤中可以通过聚体含量表现出来,当小分子部分疏水性增加时,受小分子的影响,抗体内部的疏水性氨基酸可能会暴露出来,从而使整个ADC的疏水性增加,导致ADC加速聚集,从而使聚体增加。抗体内部疏水性氨基酸的暴露还可能改变抗体高级结构,造成抗体结合活性的降低,从而降低ADC的靶向能力。通过在连接子上引入式A的结构,能够降低小分子的疏水性,阻止疏水性payload与抗体的非共价结合,组织抗体内部疏水性氨基酸的暴露,从而降低整个ADC的疏水性。比较表1中聚体含量、裸抗含量、DAR值的数据可以看出,对比例1-13ADC的聚体含量高、裸抗含量高,而对应的本发明实施例ADC聚体含量低、裸抗含量低;对比例14虽然聚体含量和裸抗含量不高,但是其在血浆稳定性上不如引入了式A结构的88480也证明了这一点。
实验结果说明,通过在ADC的连接子上引入式A所示结构,可以降低ADC聚体含量和裸抗含量,使得制备得到的ADC DAR值维持在合适的范围内,提高ADC的稳定性,降低其免疫原性,减少竞争抑制,提高药物疗效。
本发明制备得到的ADC聚体含量和裸抗含量低,DAR值合适,稳定性好,免疫原性低,纯度高。
实验例2:抗体—药物偶联物的稳定性测试
1.实验方法
受试样品:实施例制备得到的本发明实施例ADC和对比例制备得到的对比例ADC。
稳定性测试方法:将所得ADC进行14天稳定性考察,放置条件为40℃避光,取样点为第0、7、14天,按照实验例1的方法测试不同取样点样品的聚体含量及DAR值。
2.实验结果
表2.稳定性测试结果
/>
/>
上表2中,以ADC在40℃避光条件下放0、7、14天的聚体含量及DAR值来评价其放置稳定性。在放置14天后,ADC仍然能够保持低聚体含量及低DAR值,则说明该ADC具有优良的放置稳定性。
从表2的数据可以看出,本发明实施例ADC在放置14天的时间里能够保持低聚体含量及低DAR值,聚体含量和DAR值未发生明显变化,说明本发明实施例ADC具有优良的放置稳定性。
实验结果说明,通过在ADC的连接子上引入式A所示结构,可以提高ADC的放置稳定性。
本发明制备得到的ADC不仅具有低聚体含量及低DAR值,而且在放置14天的时间里能够保持低聚体含量及低DAR值,具有优良的放置稳定性。
实验例3:血浆稳定性测试
1.实验方法
受试样品:实施例制备得到的本发明实施例ADC和对比例制备得到的对比例ADC。
为了进一步评价ADC的特性,测试了ADC的血浆稳定性研究,血浆稳定性测试步骤如下:
步骤一:储备液与工作液的配制
采用超纯水将供试品储备液稀释成浓度为2.5mg/mL的工作液。现用现配,室温条件使用。
步骤二:孵育试验
按照下述步骤进行血浆样品孵育试验:
(1)取空白CD-1小鼠、食蟹猴和人血浆980μL(试验组N=2,对照组N=1)于37℃预孵育5min;
(2)加入20μL受试化合物工作液(或阳性对照药(payload)工作液),涡旋混匀(受试化合物终浓度100μg/mL、阳性对照药终浓度1μM)。立即取50μL血浆样品加入150μL冰沉淀剂的中,涡旋混匀作为0h样品;
(3)剩余血浆样品密封后于37℃继续孵育,按照表3预设的时间点吸取血浆样品50μL加入150μL冰沉淀剂中,涡旋混匀;
表3.取样时间点
(4)采集后的样品于-60~-90℃冰箱保存,待测。
步骤三:样品分析
采用液相色谱-串联质谱(LC-MS/MS)方法进行分析,测定payload的生成量,双毒素ADC分别测试两个payload的生成量。
2.实验结果
血浆稳定性是影响ADC成药性的关键因素。通过提高化合物的血浆稳定性有助于改善其在体内的药代动力学性质和药效。根据ADC的药物链接组装单元中药物的数量,将ADC分为两类:(1)单毒素ADC,指药物链接组装单元中含有1个药物的ADC;(2)双毒素ADC,指药物链接组装单元中含有2个药物的ADC。本实验测试了实施例ADC和对比例ADC中的单毒素ADC和双毒素ADC在小鼠、猴和人血浆中的稳定性。
本发明实施例ADC和对比例ADC结构的区别在于连接子上是否含有式A所示结构。
(1)单毒素ADC的血浆稳定性
单毒素ADC的血浆稳定性测试结果如图7所示。可以看出,对比例单毒素ADC(对比例14的DS-8201)在小鼠、猴和人血浆中的稳定性较差,本发明实施例单毒素ADC在小鼠、猴和人血浆中具有优良的稳定性。与对比例单毒素ADC(对比例14的DS-8201)相比,本发明实施例单毒素ADC在小鼠、猴和人血浆中的稳定性显著提高。
特别地,比较SMP-88480(实施例22化合物)所得单毒素ADC与DS-8201(对比例14)所得单毒素ADC发现,两者结构的差异仅在于SMP-88480(实施例22化合物)所得单毒素ADC的连接子中含有式A所示结构。但是,SMP-88480(实施例22)所得单毒素ADC在小鼠、猴和人血浆中的稳定性显著优于DS-8201(对比例14)所得所得单毒素ADC,说明在单毒素ADC的连接子上引入式A所示结构,可以显著提高ADC的血浆稳定性。
(2)双毒素ADC的血浆稳定性
双毒素ADC中Dxd的血浆稳定性结果如图8所示,双毒素ADC中艾日布林的血浆稳定性结果如图9所示。可以看出,对比例双毒素ADC(对比例5的SMP-50206)在小鼠、猴和人血浆中的稳定性较差,本发明实施例双毒素ADC在小鼠、猴和人血浆中具有优良的稳定性。与对比例双毒素ADC(对比例5的SMP-50206)相比,本发明实施例双毒素ADC在小鼠、猴和人血浆中的稳定性显著提高。
特别地,比较SMP-22682(实施例13)所得双毒素ADC与SMP-50206(对比例5)所得双毒素ADC发现,两者结构的差异仅在于SMP-22682(实施例13)所得双毒素ADC的连接子中含有式A所示结构。但是,SMP-22682(实施例13)所得双毒素ADC在小鼠、猴和人血浆中的稳定性显著优于SMP-50206(对比例5)所得双毒素ADC,说明在双毒素ADC的连接子上引入式A所示结构,可以显著提高ADC的血浆稳定性。
另外,根据图8和图9还可以看出,本发明实施例双毒素ADC的血浆稳定性甚至优于对比例单毒素ADC(对比例14的DS-8201)。进一步说明在双毒素ADC的连接子上引入式A所示结构,可以显著提高ADC的血浆稳定性。
实验结果说明,通过在ADC的连接子上引入式A所示结构,可以提高ADC的血浆稳定性。
本发明制备得到的ADC在小鼠、猴和人血浆中具有优良的稳定性,有助于改善其在体内的药代动力学性质和药效。
实验例4:体内抗肿瘤效果测试
1.实验方法
受试样品:实施例制备得到的本发明实施例ADC和对比例制备得到的对比例ADC。
1.1肿瘤模型建立
分别将肿瘤(卵巢癌SKOV-3、胃癌NCI-N87、乳腺癌JIMT-1)细胞培养于培养基,维持在含5% CO
收集对数生长期肿瘤细胞,重悬于基础培养基中,调整细胞浓度至4×10
1.2分组及给药观察
在肿瘤体积达到200mm
实验期间每周2次测定动物体重和肿瘤体积,每日观察记录动物临床症状。
2.实验结果
在动物模型上的抗肿瘤效果能够比较直接地反映ADC的疗效,本实验测试了实施例ADC和对比例ADC中的单毒素ADC和双毒素ADC在卵巢癌、胃癌、乳腺癌模型动物中的抗肿瘤效果。
(1)单毒素ADC的体内抗肿瘤效果
单毒素ADC对卵巢癌、胃癌、乳腺癌的体内抗肿瘤效果如图10所示。可以看出,对比例单毒素ADC(对比例4的SMP-79786、对比例14的DS-8201)对胃癌和乳腺癌的抗肿瘤效果较差;本发明实施例单毒素ADC对卵巢癌、胃癌、乳腺癌具有优良的抗肿瘤效果。与对比例单毒素ADC(对比例4的SMP-79786、对比例14的DS-8201)相比,本发明实施例单毒素ADC对胃癌的抗肿瘤效果显著提高;与对比例单毒素ADC(对比例14的DS-8201)相比,本发明实施例单毒素ADC对乳腺癌的抗肿瘤效果显著提高。
特别地,比较SMP-52573(实施例40)所得单毒素ADC与SMP-79786(对比例4)所得单毒素ADC发现,两者结构的差异仅在于SMP-52573(实施例40)所得单毒素ADC的连接子中含有式A所示结构。但是,SMP-52573(实施例40)所得单毒素ADC对胃癌的体内抗肿瘤效果显著优于SMP-79786(对比例4)所得单毒素ADC,说明在单毒素ADC的连接子上引入式A所示结构,可以显著提高ADC的抗肿瘤效果。
(2)双毒素ADC的体内抗肿瘤效果
双毒素ADC对胃癌的体内抗肿瘤效果如图11所示。可以看出,本发明实施例双毒素ADC对胃癌具有优良的抗肿瘤效果。
结合图10中的对比例单毒素ADC(对比例14的DS-8201)对胃癌的抗肿瘤效果可以看出,本发明实施例双毒素ADC对胃癌的体内抗肿瘤效果明显优于对比例单毒素ADC(对比例14的DS-8201),说明在双毒素ADC的连接子上引入式A所示结构,可以显著提高ADC的抗肿瘤效果。
实验结果说明,通过在ADC的连接子上引入式A所示结构,可以提高ADC的抗肿瘤效果。
本发明制备得到的ADC具有优良的体内抗肿瘤效果,临床应用前景广阔。
综上,本发明具体提供了一种具有特定连接子结构的药物链接组装单元,该药物链接组装单元能够与抗体连接形成靶向接头-药物偶联物,可以有效避免在提高靶向接头-药物偶联物的抗体-药物比例后引发的聚集现象,提高靶向接头-药物偶联物的稳定性,并最终提高其治疗效果。本发明的靶向接头-药物偶联物制备方法简单,在制备预防和/或治疗的抗肿瘤药物中具有广阔的应用前景。
- 包含肽接头的用于化学部分位点-特异性偶联的靶向化合物
- 靶向胎盘样硫酸软骨素A的多肽药物偶联物及其制备方法和应用
- 用经不可切割接头连接的细胞结合剂美登木素生物碱偶联物靶向特定细胞群的方法、所述偶联物和制备所述偶联物的方法
- 用经不可切割接头连接的细胞结合剂美登木素生物碱偶联物靶向特定细胞群的方法、所述偶联物和制备所述偶联物的方法
