基于CRISPR检测小血管闭塞相关基因PTGS2位点突变的试剂盒
文献发布时间:2023-06-19 19:28:50
技术领域
本发明属于基因突变检测技术领域,具体涉及一种基于CRISPR检测小血管闭塞相关基因PTGS2位点突变的试剂盒。
背景技术
世界范围内,脑卒中(stroke)是第二大死因,在所有脑卒中(stroke)患者中约87%是缺血性卒中。而在我国,急性缺血性脑卒中(acute ischemic stroke,AIS)约占70%。研究表明,约30%的缺血性脑血管病是小血管闭塞(smallarteryocclusion,SAO)所致,这类卒中的治疗和预防目前尚未取得显著进展。但大量病因学研究已经表明,IS的发生是一个多步骤、过阶段的复杂过程,是环境因素和遗传因素共同作用的结果。
根据当前国际普遍使用TOAST分型,IS分为大动脉粥样硬化(LAA)型、心源性脑栓塞(CE)型、小动脉闭塞(SAO)型、其他明确原因型和不明原因型。SAO约占所有IS的四分之一,其发病机制尚未明确。中风的原因有很多,如高血压、糖尿病、血脂异常、吸烟和遗传背景。特别是遗传背景占IS的30-40%。炎症对血栓形成的整个过程都有影响。首先,炎症不仅可能促进血栓形成,还可能抑制内源性纤维蛋白溶解以增强血栓稳定性其次,炎症介质吸附免疫细胞并溶入脑实质,进一步破坏血脑屏障,促进血栓形成。多种炎症相关介质参与这一过程。前列素内环氧化物合成酶2(prostaglandin endoperoxide synthase2 PTGS2),又称COX2,是血管内皮细胞、平滑肌细胞和血小板中重要的诱导酶。它是由细胞因子和生长因子诱导的,与动脉粥样硬化的形成密切相关多项研究报道了PTGS2基因多态性与IS风险之间的关联,并且进一步研究表明PTGS2 rs689466T>C和rs5275 A>G,增加小动脉闭塞风险。
现阶段临床一般通过定量即时聚合酶链锁反应(Quantitative real timepolymerase chain reaction,Q-PCR)、非放射性原位杂交技术(fluorescence insituhybridization,Fish)、多重引物PCR(multiplex PCR)等方式对患者进行基因突变检测,然而这些检测技术均存在检测时间长过程复杂或检测成本过高等问题,导致无法应用到大规模的临床样本研究中。因此亟需提供一种温度控制简单,且灵敏度、特异性高的特异性片段检测方法。
RNA引导的成簇规则间隔短回文重复序列-CRISPR(CRISPR-Cas)相关方法由于其高可靠性和特异性而在快速核酸检测方面显示出相当大的前景。目前已经开发了几种类型的Cas核酸酶用于CRISPR-Cas系统,例如Cas9、Cas12等。
发明内容
有鉴于此,本发明的目的在于解决现有技术中检测时间长、成本过高和准确性不高以致无法大规模检测临床样本基因突变的问题,提供了一种基于CRISPR技术检测与小血管闭塞相关的PTGS2基因是否存在rs689466和/或rs5275目标突变位点和检测该靶核酸在目标区域是否存在突变的试剂盒。
为达到上述技术目的,本发明的技术方案如下:
本发明首先提供一种检测小血管闭塞相关基因PTGS2位点突变的突变型crDNA或突变型crRNA,
所述突变型crDNA为如下任一:
A1).rs689466突变型crDNA,其序列如SEQ ID NO.1所示;
A2).rs5275突变型crDNA,其序列如SEQ ID NO.2所示;
A3).A1)和A2);
所述突变型crRNA为如下任一:
B1).rs689466突变型crRNA,其序列如SEQ ID NO.3所示;
B2).rs5275突变型crRNA,其序列如SEQ ID NO.4所示;
B3).B1)和B2)。
本发明其二提供一种基于CRISPR检测小血管闭塞相关基因PTGS2位点突变的试剂盒,包括上述突变型crDNA或突变型crRNA。
优选的,所述试剂盒包括以下任一:
C1).用于特异性扩增PTGS2基因上rs689466多态性位点的引物对,具体为:
rs689466-F,其序列如SEQ ID NO.5所示;
rs689466-R,其序列如SEQ ID NO.6所示;
C2).用于特异性扩增PTGS2基因上rs5275多态性位点的引物对,具体为:
rs5275-F,其序列如SEQ ID NO.7所示;
rs5275-R,其序列如SEQ ID NO.8所示;
C3).C1)和C2)。
可以理解的是,引物对的选择依据试剂盒中突变型crDNA或突变型crRNA的序列而定。
优选地,所述试剂盒包括荧光探针和cas12a蛋白;更加优选地,所述cas12a蛋白为Fncas12a蛋白。
优选地,所述试剂盒包括荧光探针,所述荧光探针的5’端标记有荧光报告基团,所述荧光探针的3’端标记有荧光猝灭基团;更加优选地,所述荧光报告基团选自FAM、VIC、HEX、TRT、Cy3、Cy5、ROX、JOE、Texas Red中的任意一种,所述荧光猝灭基团选自TAMRA、DABCYL、MGB、BHQ1、BHQ2、BHQ3中的任意一种。
优选地,所述试剂盒包括DNA酶抑制剂和无酶水。
本发明还提供上述任一种试剂盒在检测与小血管闭塞相关的PTGS2基因突变中的应用。
优选的,所述应用的过程具体为:对待测DNA样品进行PCR扩增,扩增完成后加入检测混合液反应,并采集荧光变化;所述检测混合液含有荧光探针和所述突变型crRNA;所述突变型crDNA在T7 RNA聚合酶作用下生成RNA,经回收纯化得到对应的crRNA。
更优选的,所述PCR扩增的程序为:95℃3min进行预变性;95℃10s,55-60℃20s,循环25-30次;最后降温至25℃,反应结束。
更优选的,所述检测混合液共50ul,具体为:250~500nM纯化的cas12a蛋白,250~500nM突变型crRNA,1~5μL荧光探针,2μL DNA酶抑制剂,无酶水余量。
与现有技术相比,本发明的有益效果包括:
针对PTGS2基因的rs689466和rs5275位点设计突变型crDNA和突变型crRNA,筛选得到的突变型靶标DNA的荧光值相较于野生型变化显著,灵敏度高;使用所述突变型crRNA判断样本是否存在待检基因突变时,检测结果与临床诊断结果基本一致,准确率高。另外,本发明基于CRISPR-Cas12a系统设计crRNA,cas12a核酸酶与crRNA配合,对DNA切割的效率更高、更精确,且构建方式简单、转化效率高。
附图说明
图1为PTGS2基因引物扩增电泳图;
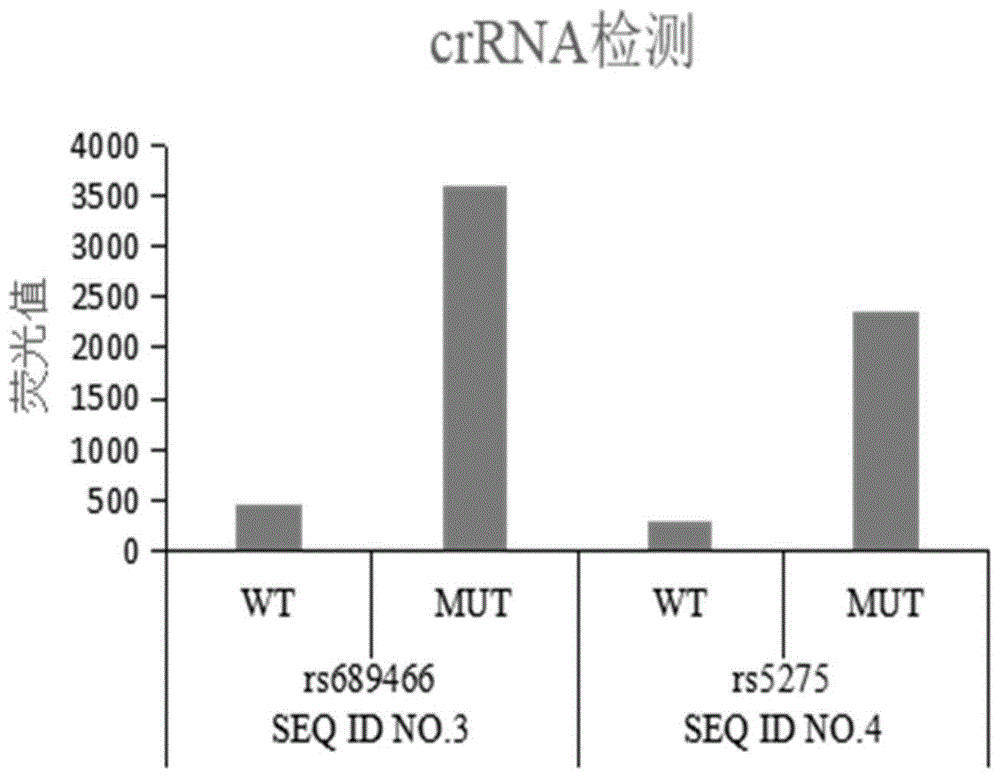
图2为PTGS2基因位点的crRNA荧光检测结果图;
图3为PTGS2基因中rs689466位点检测灵敏度结果图;
图4为PTGS2基因中rs5275位点检测灵敏度结果图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例1靶向基因突变位点crRNA的设计及获得
(1)靶向基因突变位点crRNA设计原则
由于CRISPR-Cas12a系统是一种新型的靶向DNA基因编辑系统,其中Cas12a与crRNA结合形成监测复合物,crRNA的向导区域用互补序列识别目标DNA,并且Cas12a降解目标DNA链。其中所述crRNA设计要求:crRNA包括蛋白锚定序列和向导序列,序列格式为:5`-与Cas12a蛋白结合的锚定序列-crRNA向导序列-3`,蛋白锚定序列需要根据Cas12a蛋白来确定,使其能够与选定的Cas12a蛋白匹配并结合;向导序列则与靶向DNA中的片段匹配。
(2)crDNA序列的选择
本实施例中选用的cas12a蛋白为FnCas12a,因此选定与Cas12a蛋白结合的锚定序列为UAAUUUCUACUCUUGUAGAU,所述crRNA序列根据现有技术已知的PTGS2基因rs689466和rs5275两个突变位点区域设计,每个突变位点设计了一个相应的crDNA,其序列具体为:
PTGS2基因rs689466突变位点1个crDNA:其序列如SEQ ID NO.1所示;
PTGS2基因rs5275突变位点1个crDNA:其序列如SEQ ID NO.2所示。
(3)crRNA的获得
使用T7高产量转录试剂盒(NEB)将crDNA用作crRNA生物合成的模板,转录反应体系如表1所示。在37℃下孵育4-16h后,将DNase I添加到反应溶液中,并在37℃下孵育30min以消化剩余的DNA片段。使用RNA纯化试剂盒纯化转录的crRNA,并储存在-80℃。
表1转录反应体系
所得crRNA为:
PTGS2基因rs689466突变位点1个crRNA:其序列如SEQ ID NO.3所示;
PTGS2基因rs5275突变位点1个crRNA:其序列如SEQ ID NO.4所示。
实施例2小血管闭塞相关PTGS2基因突变位点的检测试剂盒及检测方法
1、用于PTGS2基因与小血管闭塞相关突变位点检测的试剂盒的组成
1)2个突变型crRNA(如实施例1所示获得),其序列如SEQ ID NO.3~4所示;
或2个突变型crDNA(当试剂盒中为crDNA时,需要使用者先将crDNA片段分别在T7RNA聚合酶作用下生成RNA,回收纯化得到crRNA,具体见实施例1),其序列如SEQ ID NO.1~2所示。
2)一条特异性荧光探针,在本实施例中,荧光探针具体为表2中任一:
表2荧光探针序列
3)cas12a蛋白,在本实施例中,采用Fncas12a。
4)无酶水和DNA酶抑制剂。
5)用于特异性扩增PTGS2基因上rs689466和rs5275多态性位点的引物对,所述引物对序列如下所示:
rs689466-F,其序列如SEQ ID NO.5所示;
rs689466-R,其序列如SEQ ID NO.6所示;
rs5275-F,其序列如SEQ ID NO.7所示;
rs5275-R,其序列如SEQ ID NO.8所示;
所述两对引物扩增的电泳图见图1。
实施例3与小血管闭塞相关的PTGS2基因突变位点的检测体系建立
根据位点信息分别设计两个位点的野生型及突变型靶序列DNA(如序列SEQ IDNO.9-12所示),取不同的突变比例(0%、1%、10%、50%、100%)的靶标加入检测混合液(混合液中包含100~200nM纯化的FnCas12a,100~200nM crRNA,5-10μL合成的荧光探针,2μLDNA酶抑制剂和无酶水),在检测缓冲液(NEBuffer 2.1)37℃孵育0.5~1h,检测体系如表3所示:
表3检测体系
合成的野生型(WT)和突变型(MUT)的靶序列,分别利用实施例1设计的crRNA构建检测体系进行检测筛选,其中rs689466突变型crRNA,其序列如SEQ ID NO.3所示;rs5275突变型crRNA,其序列如SEQ ID NO.4所示。检测结果如图2所示,根据检测结果,突变靶标中荧光值相较于野生株变化显著,灵敏度高,验证了所使用的crRNA效果优异。同时根据突变率梯度检测试剂的灵敏度结果如图3和图4所示。
实施例4试剂盒在临床样本中的检测
选择多例临床样本检测rs689466和rs5275突变位点,并对结果进行汇总比对。
一、检测方法
1、样本处理
取10-20ul全血样本加入提前备有50-1000ul裂解液1的c号裂解管中,同时加入50-1000裂解液2,盖上管盖颠倒混匀7-8次将液体全部甩入管底静置15-30min。
2、添加试剂组装耗材
将上步充分裂解的反应液从滴管滴入提前加有扩增试剂的A管(滴入1-3滴,每滴定量10ul至总反应液为50ul)(扩增试剂中含有12.5ul扩增buffer mix、2ul扩增引物mix和适量无酶水);将B管通过连接口组装到A管上,同时转到1号锁止位使上下管断开连接,将50ul检测试剂(1ul检测蛋白、1ul检测crRNA、3ul检测buffer、适量探针及无酶水)加入B管盖上盖子。
耗材上机检测(上机耗材为202220603832.2专利)
二、检测结果
检测结果如表4所示:
表4 10例小血管闭塞临床样本检测结果
由上述结果可知,本发明实施例提供的试剂盒能有效实现小血管闭塞相关PTGS2基因rs689466和rs5275位点的突变筛查检测,判断标本是否存在待检基因突变。
以上所述本发明的具体实施方式,并不构成对本发明保护范围的限定。任何根据本发明的技术构思所做出的各种其他相应的改变与变形,均应包含在本发明权利要求的保护范围内。
/>
/>
/>
/>
/>
/>
/>
- 基于C2c2的肿瘤相关突变基因的gRNA、检测方法、检测试剂盒
- 一种EGFR基因T790M突变位点的数字PCR检测试剂盒
- 一种用于人类BRCA1和BRCA2基因全编码序列突变位点检测的引物、方法和试剂盒
- 检测TSC2基因位点突变的引物、方法和试剂盒
- 用于检测PIK3CD基因E1021K位点突变的探针和引物组合及试剂盒
- 基于CRISPR检测大血管闭塞相关基因ABO位点突变的试剂盒
- 基于CRISPR检测药物基因组基因CYP2C19位点突变的试剂盒
