吡啶并喹喏里西啶型生物碱在制备防治神经退行性疾病药物中的应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及天然药物化学和药理学领域,特别是涉及吡啶并喹喏里西啶型生物碱在制备防治神经退行性疾病药物中的应用。
背景技术
神经退行性疾病是一类病程无法逆转的以神经元进行性退化或死亡为特征的高度致残、致死性疾病,主要包括脑卒中(cerebral stroke,CS)、脑损伤(brain injury,BI)等急性神经退行性疾病,以及阿尔茨海默病(Alzheimer's disease,AD)、帕金森病(Parkinson's disease,PD)为主的慢性神经退行性疾病。衰老是引发神经退行性疾病的主要危险因素,在当前社会人口老龄化不断加剧的情况下,神经退行性疾病严重危害老年人身体健康并造成了沉重的社会经济负担;其病因病机尚且不明,临床所用药物也疗效不佳且存在一定的不良反应,因此迫切需要寻求其它更为安全有效的治疗策略。
一叶萩[Flueggea suffruticosa(Pall.)Baill.]为大戟科(Euphorbiaceae)白饭树属植物,又名叶底珠、狗杏条、黄恨子等,除西北外,在我国各省区均有分布。其枝、叶、根和花均可供药用,味辛、苦,性温,有微毒,具活血舒筋、健脾益肾等功效,可用于治疗面神经麻痹、小儿麻痹后遗症、神经衰弱及嗜睡症等。一叶萩中主要含有生物碱类成分,其中以一叶萩碱为代表的一叶萩型生物碱(Securinega alkaloids)为该植物的特征性成分。一叶萩型生物碱骨架复杂多变、立体构型多样,并多具有显著的中枢神经兴奋、抗病毒及抗肿瘤等药理活性,近年来一直是化学家和药理学家的研究热点。但是,目前尚未有将一叶萩型生物碱应用于神经退行性疾病治疗中的报道。
发明内容
本发明的目的是提供吡啶并喹喏里西啶型生物碱在制备防治神经退行性疾病药物中的应用,以解决上述现有技术存在的问题,本发明制备的生物碱具有治疗包括缺血性脑卒中和阿尔兹海默症等神经退行性疾病的潜力,为脑卒中和AD疾病提供新的治疗思路,具有广阔的应用开发前景。
为实现上述目的,本发明提供了如下方案:
本发明提供吡啶并喹喏里西啶型生物碱在制备预防和/或治疗神经退行性疾病药物中的应用,所述吡啶并喹喏里西啶型生物碱的结构式如下所示:
进一步地,所述神经退行性疾病包括缺血缺氧或β淀粉样蛋白导致的疾病。
进一步地,所述缺血缺氧导致的疾病包括脑卒中;所述β淀粉样蛋白导致的疾病包括阿尔茨海默病。
进一步地,所述吡啶并喹喏里西啶型生物碱通过减轻缺血缺氧诱导的神经元损伤,发挥治疗脑卒中的效果。
进一步地,所述吡啶并喹喏里西啶型生物碱通过减轻β淀粉样蛋白导致的神经元损伤及改善患者的认知障碍,治疗阿尔茨海默病。
本发明还提供一种预防和治疗神经退行性疾病的药物,包含有效剂量的所述吡啶并喹喏里西啶型生物碱。
进一步地,所述神经退行性疾病包括脑卒中和阿尔茨海默病。
进一步地,所述药物还包括药学上可接受的辅料。
进一步地,所述辅料包括赋形剂、乳化剂和表面活性剂中的一种或多种。
进一步地,所述药物的剂型包括片剂、胶囊剂、颗粒剂、注射剂或喷雾剂。
本发明公开了以下技术效果:
本发明首次发现制备的吡啶并喹喏里西啶型生物碱能够有效改善氧糖剥夺/复氧和β淀粉样蛋白诱导的神经元损伤,能够促进阿尔兹海默症小鼠模型的空间学习记忆能力,改善认知障碍。本发明实验结果证实制备获得的吡啶并喹喏里西啶型生物碱具有治疗包括缺血性脑卒中和阿尔兹海默症等神经退行性疾病的潜力,为脑卒中和AD疾病提供新的治疗思路,具有广阔的应用开发前景。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为化合物I的
图2为化合物I的
图3为化合物I的
图4为化合物I的HMBC谱;
图5为化合物I的NOESY谱;
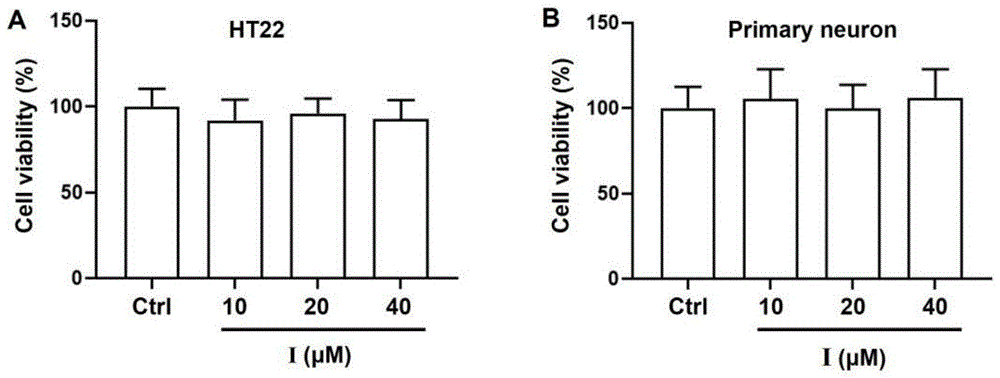
图6为化合物I对细胞存活率的影响;A:HT22细胞;B:原代神经元细胞;
图7为化合物I对OGD/R模型的保护作用;
图8化合物I对Aβ诱导的HT22神经毒性的保护作用;
图9为化合物I对APP/PS1小鼠模型的治疗作用。
具体实施方式
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本发明说明书和实施例仅是示例性的。
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
实施例1吡啶并喹喏里西啶型生物碱(化合物I)的制备和结构鉴定
一叶萩干燥枝叶60kg(采自安徽凤阳,经暨南大学药学院周光雄教授鉴定),粉碎后用95%乙醇溶液冷浸提取,合并提取液,减压浓缩得总浸膏约12.7kg。总提取物用水混悬,缓慢加入10%盐酸水溶液,调pH值至3,静置,用氯仿萃取除去中性成分。酸水层加氨水碱化至pH值9,静置,用氯仿萃取,萃取液减压回收溶剂,得到氯仿部位,即总生物碱部位120g。总生物碱部位(120g)采用硅胶柱层析(氯仿-甲醇梯度洗脱0:100→100:0,V/V),经TLC分析,合并相同流分,得到9个主流分(Fr.1~Fr.9)。其中,Fr.4(14.0g)经反复硅胶柱层析(氯仿-丙酮)、Sephadex LH-20(氯仿-甲醇)及制备型HPLC(甲醇-水)等色谱技术分离纯化得到吡啶并喹喏里西啶型生物碱纯品I(化合物I,纯度>98%)。
所得一叶萩碱型生物碱纯品为淡黄色油状物,旋光度:
UV光谱在198和257nm有最大吸收,提示该化合物结构中存在共轭体系。
IR光谱在3419、1647、1541和1384cm
HR-ESI-MS谱显示准分子离子峰m/z 313.1548[M+H]
核磁共振氢谱(
表1吡啶并喹喏里西啶型生物碱的
化合物I的
化合物I的
在化合物I的
在化合物I的HMBC谱(图4)中,可以观察到δ
化合物I的NOESY谱(图5)中,δ
实施例2MTT法测定化合物I的细胞毒性
HT22海马神经元细胞系(购于American type culture collection细胞库)复苏后,以生长培养基(DMEM+10%FBS+100U/mL的青霉素和100μg/mL的链霉素)培养,种植在100mm的培养皿中,放入37℃、含5%CO
原代皮层神经元培养:取孕18天SD大鼠的胚胎,取脑,在显微镜下分离皮层和海马,从皮层中提取原代皮层神经元,以生长培养基(Neurobasal培养基+2%B27无血清培养基+0.5%L-谷氨酰胺+0.4% D-(+)-葡萄糖+100U/mL的青霉素和100μg/mL的链霉素)培养,3~4小时之后等细胞贴壁然后换液,后面每3天换液一半,培养到第8天的时候开始正式实验。
取生长状态良好的HT22细胞及原代神经元细胞,设置对照组和不同浓度的样品组,铺板过夜后加入不同浓度药物,每组设4个平行复孔。培养24小时后,弃去培养基,加入还有10%MTT(5mg/ml,Sigama)的生长培养基继续培养4h后,弃去培养基加入DMSO溶解紫色沉淀,使用美国伯腾SynergyHT多功能酶标仪在490nm波长处检测吸光值,结果如图6所示。
从图6中A-B可看出,本发明化合物I在10~40μM范围对HT22细胞及原代神经元细胞存活率没有明显的改变作用,说明这些化合物在40μM或以下的浓度时无细胞毒性。
实施例3化合物I对氧糖剥夺/复氧(OGD/R)诱导神经元损伤模型的保护作用
神经元氧糖剥夺/复氧(OGD/R)模型可以模拟体内的脑缺血再灌注期间损伤病理过程,是研究缺血性脑卒中的经典细胞模型。
在原代皮层神经元培养到第8天的时候开始正式实验,预给药化合物I(10、20μM)2小时之后换成含药的无糖培养基,并放入缺氧箱中,通入95%N
从图7可看出,氧糖剥夺/复氧可以显著的降低原代皮层神经元的存活率,而本发明化合物I在10、20μM具有改善氧糖剥夺/复氧诱导神经元损伤的保护作用,证实该化合物I有治疗缺血性脑卒中等神经退行性疾病的潜力。
实施例4化合物I对Aβ诱导的损伤具有保护作用
β淀粉样蛋白(β-Amyloid 1-42,简称Aβ1-42),是根据阿尔茨海默病人大脑中的毒性物质β淀粉样蛋白的氨基酸序列设计合成的多肽,购于rPeptide生物技术公司。用500μl1%的氨水溶解,超声1分钟,再加PBS配成100μM的母液,混匀后分装放-80℃保存。使用之前,根据需要取适量体积放于37℃环境下老化20小时。取对数生长期HT22细胞进行实验,加入Aβ1-42(1μM)处理48小时,同时加入DMSO或化合物I(10、20μM),处理24小时,MTT实验检测细胞存活率。结果见图8。
从图8可看出,Aβ1-42处理后细胞存活率显著降低,而本发明化合物I和Aβ1-42共处理后的细胞存活率显著增加,提示化合物I对Aβ1-42诱导的HT22海马神经元损伤具有保护作用。
实施例5化合物I缩短小鼠在Morris水迷宫测试中的逃逸潜伏期
本实施例使用雄性APP/PS1双转基因小鼠(购自北京华阜康生物科技股份有限公司),该小鼠是经典阿尔兹海默症(AD)转基因小鼠模型,在4~5月龄时开始出现认知障碍。雄性7月龄APP/PS1转基因AD小鼠及野生型对照小鼠(WT)随机分组(每组6只鼠),进行腹腔注射化合物I(20mg/kg)药,每日一次,持续四周。
Morris水迷宫的主体是一个直径1.2米水池,水池其中一个区域放有一个水下的隐藏平台,并在水池的四周设置可供小鼠定位的标记。小鼠经过连续几天的训练,找到平台所需的时间(即逃逸潜伏期escape latency)反映了小鼠对于空间的学习记忆能力。正常小鼠的逃逸潜伏期会从第三天起大大缩短,代表学习记忆的增强。将各组小鼠按上述方法进行检测,结果如图9所示。
从图9中可以看出,相对于WT小鼠,APP/PS1转基因AD小鼠找到平台的时间更久,提示APP/PS1转基因AD小鼠记忆受损;而连续四周腹腔注射化合物I后的APP/PS1小鼠能更快地找到平台,说明化合物I具有促进AD小鼠空间学习记忆能力的活性,改善认知障碍。
上述实施例2–5中的实验结果的数据用mean±S.E.M表示,并用ANOVA检验和Student’s-t检验的方法进行统计学处理,当P<0.05时有统计学意义,*P<0.05,**P<0.01。
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
- 一种药物组合物及其制备方法和在制备防治神经退行性疾病的药物中的应用
- 菲并吲哚(或喹喏)里西啶生物碱衍生物以及它们的制备和抗植物病毒活性应用
