一种高效感染HT-22细胞的腺相关病毒突变体
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及病毒载体的包装及筛选,尤其涉及AAV突变体的包装及筛选,具体为一种高效感染HT-22细胞的腺相关病毒突变体。
背景技术
中枢神经系统疾病(Central nervous system,CNS)严重影响患者的身心健康和生活质量,且由于中枢神经系统自身的复杂性,血脑屏障(Blood-brainbarrier,BBB)对药物递送的障碍,常用的外科手术或者传统的药物来治疗神经系统的疾病仍很困难,所以目前各领域的科学家都在研究基于基因治疗方法来治疗神经系统性疾病的可行性。
腺相关病毒(adeno-associatedvirus,AAV)是一类微小、无被膜及具有二十面体结构的病毒,是目前发现的一类结构最简单的单链DNA缺陷型病毒。由于其安全性好、宿主细胞范围广(分裂和非分裂细胞)、免疫源性低,在体内表达外源基因时间长等特点,已经逐渐成为体内基因治疗递送的重要平台。然而,基因载体的递送效率是阻碍AAV介导中枢神经系统基因治疗发展的重要障碍。AAV与其他病毒载体不同,其不同的衣壳蛋白能够识别不同的宿主细胞表面受体,使得rAAV病毒载体能特异性感染不同组织。所以有许多研究分别利用细胞系,原代细胞,小鼠或者非人灵长类各种模型上筛选获得能高效感染的AAV衣壳蛋白,即AAV血清型。
HT-22细胞,是小鼠海马神经元细胞系,该细胞系是体外研究谷氨酸毒性的良好模型,在很多神经退化性疾病,例如阿兹海默(Alzheimer's Disease)和帕金森(Parkinson'sDisease)中均有很好的应用,也有很多研究者利用这株细胞进行相关的体外机制研究。我们前期发现,AAV9野生型血清型感染HT-22效率低,这样使得体外研究病毒用量较大,且病毒增大用量后对细胞状态有一定影响。
发明内容
针对现有技术中的缺陷,本发明设计并构建了一个AAV9的肽段突变文库,通过文库筛选获得可高效感染HT-22细胞系的AAV突变体,以便满足HT-22细胞系作为体外研究应用。
本发明公开了一种插入异源肽的AAV9血清型衣壳蛋白突变体;
所述异源肽为:氨基酸序列为SVADRMY(SEQ ID NO:12)所组成的多肽;
所述AAV9血清型衣壳蛋白氨基酸588~589之间被所述的异源肽插入。
本发明公开了编码上述AAV9血清型衣壳蛋白突变体的核酸分子。
本发明公开了可操作地连接上述核酸分子的核酸载体。
本发明公开了含有上述核酸载体的宿主细胞。
本发明公开了一种组合物或试剂盒,含有上述AAV9血清型衣壳蛋白突变体、核酸分子或核酸载体。
本发明公开了上述AAV9血清型衣壳蛋白突变体、核酸分子或核酸载体在用于感染HT-22细胞的用途,所述用途属于非诊断和治疗目的的。
本发明公开了上述AAV9血清型衣壳蛋白突变体、核酸分子或核酸载体在制备用于治疗中枢神经系统疾病的药物中的用途。
与现有技术相比,本发明有如下有益效果:
本技术方案通过构建AAV9的肽段突变文库,经过筛选验证获得插入了7个氨基酸的新的AAV9突变体,突变体可以有效的在MOI=1E+5情况下有效感染HT-22细胞,达到比天然AAV9血清型MOI=1E+5更高的感染效果,经过筛选获得的AAV9-HT 01的效果最好,在同样的MOI条件下,感染阳性率相对于对照AAV9血清型明显提升,通过luciferase(RLU)值检测统计其倍数为4.4倍,有效降低AAV感染细胞的使用量,节省实验成本,同时使得在HT-22细胞进行中枢神经类疾病基因治疗相关机制研究变得可行。
附图说明
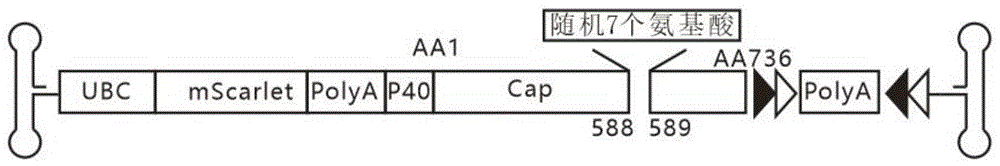
图1为实施例1中pAAV-shortUBC-mScarlet-polyA-P40-AAV9-Cap-FLEX-SV40polyA表达框图;
图2为实施例1中pAAV-shortUBC-mScarlet-polyA-P40-AAV9-Cap-FLEX-SV40polyA-WPRE图谱;
图3为AAV9文库构建及筛选流程图;
图4为实施例2中不同血清型感染HT-22细胞荧光图;
图5为实施例2中不同血清型感染HT-22细胞萤火虫荧光素值(RLU)图。
具体实施方式
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
实施例1、AAV97-mer随机肽段插入文库构建:
文库由以下载体构成:
文库穿梭载体:pAAV-short UBC-mScarlet-polyA-P40-AAV9-Cap-FLEX-SV40polyA,如图1-2所示。
实施例2、AAV9文库构建及筛选流程:
通过构建AAV9的肽段随机突变文库,筛选到插入了7个氨基酸的新的AAV9突变体,如图3所示。
1、突变体文库制备
1.1化学合成AAV9-7mer-NNS以下两个片段:
5'CCACCAGAGTGCCCAANNSNNSNNSNNSNNSNNSNNSGCACAGGCGCAG 3'(SEQ ID NO:1);
5'CGGTCTGCGCCTGTGCSNNSNNSNNSNNSNNSNNSNNTTGGGCACTCTG 3'(SEQ ID NO:2);
其中NNS代表随机编码序列。
1.2将合成的AAV9-7mer-NNS正链与反链引物各加10μL(引物的终浓度为10mM)采用退火的方式来获得AAV9-7mer-NNS模板。退火程序为:95℃,5min;95℃,1min;92min,1min;4℃,60min。其中,第二步和第三步,每个循环降3℃,一共25个循环。
1.3将质粒pAAV-short UBC-mScarlet-polyA-P40-AAV9-Cap-FLEX-SV40 polyA(其结构和插入位点如图1所示)用BsmBI进行单酶切,酶切体系(50uL)如表1所示。
表1
55℃酶切4h后进行1%琼脂糖凝胶电泳,紫外灯下用刀片将大片段切下并进行回收纯化。
1.4将1.3步得到的纯化的酶切产物和1.2步得到的AAV9-7mer-NNS核苷酸序列采用T4 DNA ligase进行连接。连接采用Takara的T4 DNA连接酶,10μL反应体系如表2所示,4℃过夜酶连。
表2
1.5将10μL酶连产物加入到50μL文库专用电转感受态细胞(购自Lucigen公司)中,混匀放置后转入已预冷的电极杯当中,使用伯乐公司的电转仪进行电转,电转完,向里面加入1mL在37℃预热的SOC液体培养基,随后37℃复苏1小时后,进行离心涂布。
1.6重复步骤1.4-1.5,直到克隆数量达到5×10
2.文库病毒包装及筛选
2.1AAV突变体文库病毒包装:按照每皿1.5×10
2.2病毒的纯化:将收集到的细胞样品在-80℃和37℃进行反复的冻融,离心,收集细胞上清,用0.45μm的PVDF滤器去除细胞碎片,随后,再采用AAV纯化试剂盒对收集的重组AAV病毒进行纯化来获取重组AAV病毒。
2.3重组AAV病毒滴度的测定:取20μL浓缩病毒液,加1μL RNase-free DNase,混匀,37℃,孵育30min,10000rpm离心10min,取20μL上清加80μL稀释Buffer至另一个无菌管中,混匀,100℃金属浴反应10min。自然冷却至室温,加入3μL蛋白酶K,37℃孵育60min,100℃金属浴反应10min,冷却至室温。将上述样品稀释后用做模板,采用实时定量PCR检测法测定重组AAV病毒滴度。qPCR反应体系及反应条件为:95℃,10min;95℃,30s;60℃,30s,35个循环。
2.4AAV病毒感染HT-22(小鼠海马神经元)细胞:
2.4.1细胞铺板:将HT-22细胞按40%汇合度接种到10cm细胞皿中,以每皿5×10
2.4.2病毒感染:用pAAV-short UBC-mScarlet-polyA-P40-AAV9-Cap-FLEX-SV40polyA–insertion表达载体文库病毒感染HT-22细胞。
2.5收集感染后的细胞,利用流式细胞分选仪进行荧光分选,选取红色荧光亮度在前5%的细胞作为筛选的目的细胞进行收集。分选收集后的细胞铺入细胞皿中,进行扩增后收集细胞。
2.6将收集到的细胞抽提基因组后进行PCR扩增,PCR产物高通量测序。
扩增引物:
AAV9-F:AACTACTAACCCGGTAGCAACGG(SEQ ID NO:3)(载体上的正向引物)
AAV9-R:CGTCCGTGTGAGGAATTTTGG(SEQ ID NO:4)(载体上的反向引物)加入接头和index序列的高通量测序使用引物使用如下:
NGS-AAV9-F:
TTACTATGCCGCTGGTGGCTCTAGATGTGAGAAAGGGATGTGCTGCGAGAAGGCTAGAAACTACTAACCCGGTAGCAACGG(SEQ ID NO:5)
NGS-R1:
GTTCGTCTTCTGCCGTATGCTCTACACTGACCTCAAGTCTGCACACGAGAAGG CTAGCGAGTAATCGTCCGTGTGAGGAATTTTGG(SEQ ID NO:6)
NGS-R2:
GTTCGTCTTCTGCCGTATGCTCTACACTGACCTCAAGTCTGCACACGAGAAGG CTAGTCTCCGGACGTCCGTGTGAGGAATTTTGG(SEQ ID NO:7)
NGS-R3:
GTTCGTCTTCTGCCGTATGCTCTACACTGACCTCAAGTCTGCACACGAGAAGG CTAGAATGAGCGCGTCCGTGTGAGGAATTTTGG(SEQ ID NO:8)
NGS-R4:
GTTCGTCTTCTGCCGTATGCTCTACACTGACCTCAAGTCTGCACACGAGAAGG CTAGGGAATCTCCGTCCGTGTGAGGAATTTTGG(SEQ ID NO:9)
NGS-R5:
GTTCGTCTTCTGCCGTATGCTCTACACTGACCTCAAGTCTGCACACGAGAAGG CTAGTTCTGAATTTCCGTCCGTGTGAGGAATTTTGG(SEQ ID NO:10)
预期获得的测序序列为:
AACTACTAACCCGGTAGCAACGGAGTCCTATGGACAAGTGGCCACAAACCACCAGAGTGCCCAANNSNNSNNSNNSNNSNNSNNSGCACAGGCGCAGACCGGCTGGGTTCAAAACCAAGGAATACTTCCGGGTATGGTTTGGCAGGACAGAGATGTGTACCTGCAAGGACCCATTTGGGCCAAAATTCCTCACACGGACG(SEQ ID NO:11)
分析高通量测序结果,将出现频率高的突变体分别命名为AAV9-HTxx;如01号肽段则为:AAV9-HT01。
3、AAV9突变体的筛选和验证
3.1AAV9突变体的构建
以天然血清型AAV2/9为载体,在588-589为氨基酸处插入候选突变体AAV9-HTxx等片段,获得新的血清型载体AAV9-HTxx等,根据高通量测序的结果,构建了30多个突变体。
3.2使用穿梭载体pAAV-CBh-mScarlet-P2A-Luc2,分别以AAV9-HTxx等作为血清型载体包装获得各种突变血清型的AAV病毒。
3.3使用WPRE引物对以上病毒进行病毒滴度测定,并使用考染确认病毒VP1、VP2、VP3表达情况。
3.4将pAAV-CBh-mScarlet-P2A-Luc2的AAV9-HTxx等病毒,以MOI=1×10
- 一种适用于特异感染U87-MG细胞的腺相关病毒突变体
- 一种适用于特异感染U251细胞的腺相关病毒突变体
