山捻子多糖在制备预防或治疗炎症性肠病的药物中的应用
文献发布时间:2024-04-18 19:58:21
技术领域
本发明涉及中药技术领域,具体涉及山捻子多糖在制备预防或治疗炎症性肠病的药物中的应用。
背景技术
炎症性肠病(Inflammatory bowel disease,IBD)是一组病因尚不十分清楚的慢性非特异性肠道炎症性疾病,对人们的健康和生活质量产生严重威胁,包括溃疡性结肠炎(Ulcerative colitis,UC)和克罗恩病(Crohn’s disease,CD)。主要临床表现为:腹痛、腹泻、血便、体重减轻等。IBD的发生发展伴随着多种严重的并发症,如结肠癌、结肠纤维化、抑郁焦虑和代谢紊乱等。IBD的发病机理尚不明确,近年来认为可能与外界环境、肠道微生物、黏膜免疫、遗传等因素有关。目前临床上IBD的治疗多采用药物疗法,常见药物包括有氨基水杨酸类、糖皮质激素类、免疫调节剂、生物制剂类等。然而这些药物具有多种药物不良反应,显著降低了患者的依从性,使临床治疗效果明显减弱。
山捻子为桃金娘科植物桃金娘的果实,山捻子以其丰富的营养成分,被广泛用作传统中药材。山捻子中含有黄酮类、酚性成分、氨基酸和多糖类等多种活性成分,具有养血止血、涩肠固精、生津止渴、提高免疫力等作用。研究表明,山捻子中所含的黄酮类物质可以促进血管扩张,降低血压及胆固醇水平,更可防止血栓和肿瘤的发生。然而目前尚未见山捻子多糖在制备预防或治疗炎症性肠病药物中的文献报道。
发明内容
鉴于此,本发明的目的在于提供山捻子多糖在制备预防或治疗炎症性肠病的药物中的新应用,以期为研究预防或治疗炎症性肠病的新药物提供理论依据和临床基础。
本发明所述的山捻子多糖的制备方法,包括如下步骤:
(1)以水为提取溶剂,将山捻子药材加热提取,合并提取液并减压浓缩,浓缩液离心,取上清液加入无水乙醇至乙醇终浓度为30%,醇沉后静置,分离得沉淀1和醇沉上清液1,收集沉淀1得山捻子粗多糖30;
(2)取醇沉上清液1继续加入无水乙醇至乙醇终浓度为60%,醇沉后静置,分离得沉淀2和醇沉上清液2,收集沉淀2得山捻子粗多糖60;
(3)取醇沉上清液2继续加无水乙醇至终浓度为90%,醇沉后静置,分离
得沉淀3和醇沉上清液3,收集沉淀3得山捻子粗多糖90;
(4)将山捻子粗多糖30、山捻子粗多糖60、山捻子粗多糖90溶于去离子
水中,离心,在上清液中加入Sevage试剂进行除蛋白,得到除蛋白后的多糖溶液,浓缩,流水透析后干燥,分别得山捻子多糖30、山捻子多糖60和山捻子多糖90。
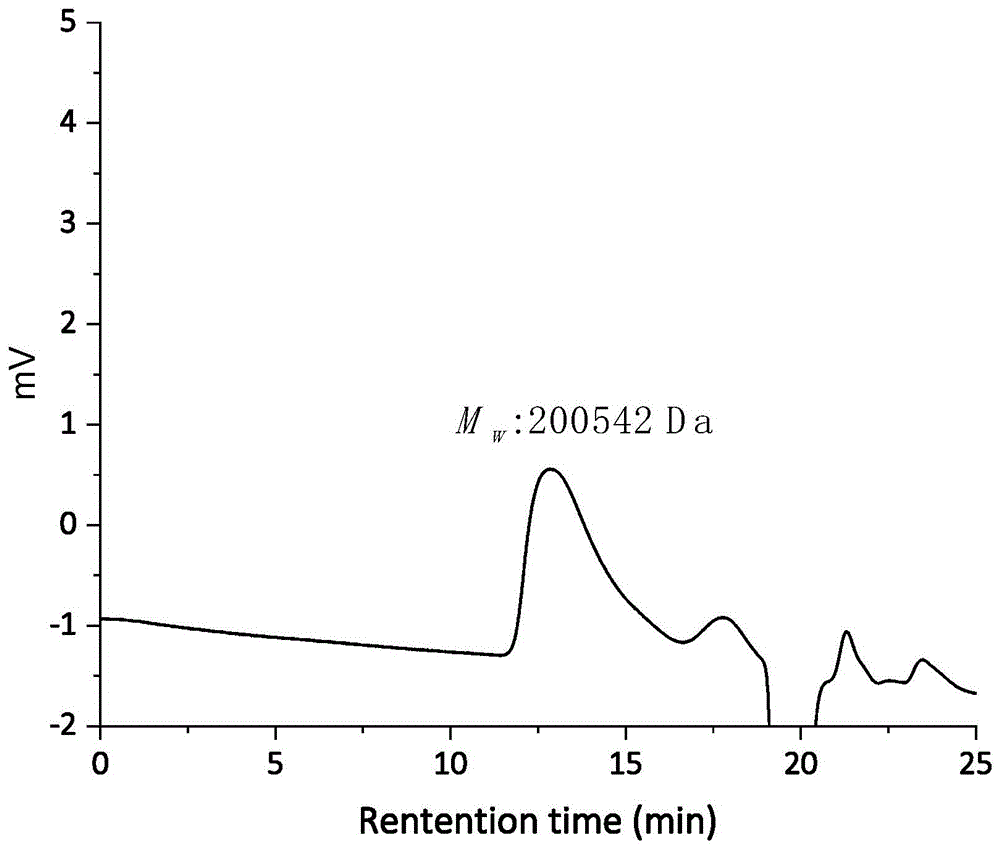
所述山捻子多糖30中多糖的质量含量为40-50%,多糖的平均分子量为200542Da,蛋白质的质量含量为15-20%。
所述山捻子多糖60中多糖的质量含量为60-65%,多糖的平均分子量为2374Da,蛋白质的质量含量为4-6%。
所述山捻子多糖90中多糖的质量含量为80-90%,多糖的平均分子量为997Da,蛋白质的质量含量为3-5%。
本发明所述的炎症性肠病(Inflammatory bowel disease,IBD)包括溃疡性结肠炎和克罗恩病。
本发明选用C57BL/6小鼠作为试验动物,通过葡聚糖硫酸钠(DSS)诱导IBD小鼠模型。结果显示,山捻子多糖30、山捻子多糖60、山捻子多糖90均对炎症性肠病造成的体重减轻具有明显的逆转作用,通过每天观察小鼠粪便黏稠度和粪便出血情况,计算出DAI,发现山捻子多糖组的DAI评分显著降低;测量小鼠结肠长度,发现山捻子多糖可以显著延长IBD小鼠的结肠长度。以上结果表明,山捻子多糖30、山捻子多糖60、山捻子多糖90均能明显改善IBD小鼠症状,对IBD有显著的治疗作用。
本发明所述药物包含有效含量的山捻子多糖和药学上可接受的载体。所述药学可接受的载体为选自药学上可接受的水提物。由此可以使得所述药物能够制剂成型,呈现临床用药物制剂适于给药的形式。
优选的,所述药物的剂型为水提物。
本发明与现有技术相比,具有如下优异效果:
本发明提供了山捻子多糖在制备预防或治疗炎症性肠病药物中的新用途,通过建立葡聚糖硫酸钠(DSS)诱导的IBD小鼠模型,结果显示,山捻子多糖对DSS诱导的结肠炎有显著的治疗作用,能明显改善IBD症状,为临床防治IBD的新药物提供理论依据和临床基础。
附图说明
图1为SNZ30重均分子量检测结果;
图2为SNZ60重均分子量检测结果;
图3为SNZ90重均分子量检测结果;
图4.为SNZ对结肠炎小鼠体重的影响,***p<0.001(模型组VS空白组);##P<0.01,###P<0.001(SNZ组VS模型组)。
图5.为SNZ对结肠炎小鼠疾病活动指数的影响,***p<0.001(模型组VS空白组);##P<0.01,###P<0.001(SNZ组VS模型组)。
图6为SNZ对结肠炎小鼠结肠长度的影响,***p<0.001(模型组VS空白组);###P<0.001(SNZ、5-ASA组VS模型组)。
具体实施方式
下面通过具体实施方式来进一步说明本发明,以下实施例为本发明具体的实施方式,但本发明的实施方式并不受下述实施例的限制。
实施例1:山捻子多糖对小鼠IBD的治疗作用
1.材料和方法
1.1药物
通过水提醇沉法制备山捻子多糖。取山捻子药材7kg,80℃条件下提取3h,料液比为1:10,提取3次,合并提取液,浓缩至原体积的1/8,4000rpm离心10分钟,取上清加入无水乙醇进行醇沉,醇沉终浓度为30%,醇沉后4℃条件下静置48h,分离沉淀和醇沉上清,醇沉沉淀为SNZ30。取醇沉上清继续加入无水乙醇至乙醇终浓度为60%,分离沉淀和醇沉上清,醇沉沉淀为SNZ60。取醇沉60%的上清液继续加无水乙醇至终浓度为90%,分离沉淀和醇沉上清,醇沉沉淀为SNZ90。取醇沉沉淀(SNZ30、SNZ60、SNZ90)溶于去离子水中,4000rpm离心10min,取上清液和Sevage试剂(正丁醇:氯仿=1:4)按照体积比为1:4的比例进行除蛋白,除蛋白次数为4次。随后取除蛋白液浓缩,流水透析48h后进行冷冻干燥,冻干后样品得干燥的山捻子粗多糖SNZ30、SNZ60及SNZ90。采用浓硫酸-苯酚法检测多糖含量、考马斯亮蓝法检测蛋白含量及HPGPC法分析多糖纯度与平均分子量,测定条件如下:色谱柱:TSK G-3000PW
柳氮磺胺吡啶(lot:J2212276)购自上海阿拉丁生化科技股份公司。葡聚糖硫酸钠购自MP Biomedicals(lot:S7980)。
1.2仪器
MTB1000D电子天平(深圳市美孚电子有限公司)。
1.3动物
C57BL/6小鼠(购自广东省医学实验动物中心,许可证编号SCXK(粤)2022-0002粤监证字2006A018)雄性,体重19-21g。小鼠饲养于广东医科大学实验动物中心,12小时光照/黑暗,自由饮食。
1.4方法
小鼠经标准饮食和水进行适应性饲养(24-25℃,湿度70-75%,12小时光照/黑暗)7天后,将小鼠随机分为6组,每组6只,包括对照组、模型组、5-ASA组(200mg/kg)、SNZ30组(200mg/kg,po)、SNZ60组(200mg/kg,po)、SNZ90组(200mg/kg,po)。SNZ30、SNZ60、SNZ90预防性口服给药5天,模型组连续口服纯化水5天(从第0天至第5天),在第5天时小鼠自由饮用2.5%DSS、持续给药7天(从第5天到第12天),空白组自由饮用纯化水。每天观察并记录小鼠体重、粪便黏稠度和粪便出血情况。第12天,麻醉小鼠取血后处死。取小鼠结肠组织测量长度。
按疾病活动指数(DAI)评价:根据体重减轻情况确定疾病活动指数得分(无损失记录0分,损失1%~5%记录1分,损失5%~10%记录2分,损失10%~5%记录3分,损失大于15%记录4分),粪便粘度(正常大便记0分,软便记1分,稀湿便记2分,腹泻干便记3分,腹泻湿便记4分),IBD小鼠的粪便出血(无血记录0分,轻微血记录1分,潜血记录2分,出血记录少3分,大出血记录4分)。DAI计算:DAI=(体重减轻评分+粪便粘稠度评分+便血程度评分)/3
1.5统计学方法
使用Graphpad Prism7.0统计分析软件对结果进行分析。各组数据
2.结果
2.1SNZ多糖糖含量、蛋白含量、多糖纯度及平均分子量测定
SNA多糖及蛋白含量如表1所示,多糖纯度及平均分子量测定如图1、2、3所示。
表1.SNZ多糖含量及蛋白含量分析
2.2SNZ对IBD小鼠体重的影响
实验结果表明,SNZ对IBD引起的体重下降具有抑制作用,如图4所示,SNZ30与模型组体重比较有显著性差异(p<0.001),SNZ60与模型组比较有显著性差异(P<0.01),SNZ90与模型组比较有显著性差异(P<0.01),模型组与空白组体重比较具有显著性差异(P<0.001)。结果见表2。
表2.TSXL对结肠炎小鼠体重的影响(x
***p<0.001(模型组VS空白组);##P<0.01,###P<0.001(SNZ组VS模型组)。
2.3SNZ对结肠炎小鼠疾病活动指数的影响
SNZ治疗后,IBD小鼠的腹泻、直肠出血和体重下降症状显著减轻,DAI评分显著降低。SNZ30组与模型组DAI比较,具有显著性差异(P<0.01),SNZ60与模型组DAI比较有显著性差异(P<0.001),SNZ90与模型组DAI比较有显著性差异(P<0.01),模型组与空白组DAI比较有显著性差异(p<0.001)。结果见表3、图5。
表3.SNZ对结肠炎小鼠疾病活动指数的影响(x
***p<0.001(模型组VS空白组);##P<0.01,###P<0.001(SNZ组VS模型组)。
2.4SNZ治疗对结肠长度的影响
与空白组相比,模型组的结肠长度明显缩短(P<0.001),而SNZ治疗12天后,结肠长度缩短显著逆转,SNZ30组与模型组结肠长度比较有显著性差异(p<0.001),SNZ60组与模型组结肠长度比较有显著性差(p<0.001),SNZ90组与模型组结肠长度比较有显著性差(p<0.001)。结果见表4、图6。
表4.SNZ对结肠炎小鼠结肠长度的影响(x
***p<0.001(模型组VS空白组);###P<0.001(SNZ、5-ASA组VS模型组)。
综上可以看出,从体重、DAI评分、结肠长度三个指标评价,SNZ30、SNZ60、SNZ90组与模型组相比较,都具有显著性差异,由此可得出结论,SZN对DSS诱导的结肠炎有显著的治疗作用,能明显改善IBD症状。
- 冬青苷B在制备治疗炎症性肠病的药物的应用
- 艾叶多糖在制备预防和治疗炎症性肠病药物中的应用
- 附子多糖在制备治疗炎症性肠病和肠黏膜炎的药物中的应用
