舍曲林联合PD-1单抗的应用及药物组合物
文献发布时间:2024-04-18 19:58:21
技术领域
本发明涉及生物医药技术领域,尤其是涉及一种舍曲林联合PD-1单抗用于制备治疗结肠癌的药物中的应用及药物组合物。
背景技术
结直肠癌是世界第三大最常见的恶性肿瘤。目前,结直肠癌的治疗以手术切除为主,化放疗、靶向治疗为辅。然而,患者一旦出现耐药、转移仍会使治疗限于困境。近年来,免疫检查点抑制剂如PD-1单抗的快速发展为结直肠癌患者带来了希望,但临床研究结果发现只有少数dMMR/MSI-H的患者(仅占15%)能从免疫检查点抑制剂治疗中获益。
CD8
发明内容
本发明的目的在于提供一种舍曲林联合PD-1单抗用于制备治疗结肠癌的药物中的应用及药物组合物,以解决现有技术中的PD-1单抗在结肠癌中疗效不佳的技术问题。本发明提供的诸多技术方案中的优选技术方案所能产生的诸多技术效果详见下文阐述。
为实现上述目的,本发明提供了以下技术方案:
第一方面,本发明提供的一种舍曲林联合PD-1单抗在制备治疗结肠癌的药物中的应用。
根据一种优选实施方式,所述应用包括舍曲林作为增效剂在PD-1单抗治疗结肠癌药物中的应用。
第二方面,本发明还提供了一种抗结肠癌的药物组合物,所述药物组合物包括舍曲林和PD-1单抗。
根据一种优选实施方式,所述药物组合物中所述舍曲林的剂量为30mg/kg/天。
根据一种优选实施方式,所述药物组合物中所述PD-1单抗的剂量为10mg/kg/3天。
根据一种优选实施方式,所述药物组合物中所述舍曲林为口服药物,所述PD-1单抗为腹腔注射药物。
基于上述技术方案,本发明的舍曲林联合PD-1单抗在制备治疗结肠癌的药物中的应用及药物组合物至少具有如下有益技术效果:
本申请提供了舍曲林联合PD-1单抗在制备治疗结肠癌的药物中的应用,通过舍曲林能够有效促进肿瘤组织免疫微环境中CD8
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1是本申请实施例1中舍曲林于转录后上调MHC-I表达图,其中,图1A为人结肠癌细胞SW480、HCT116在采用对照组和舍曲林组药物处理后的蛋白免疫印迹实验中MHC-I和GAPDH的表达图;图1B为人结肠癌细胞SW480、HCT116在采用对照组和舍曲林组药物处理后肠癌细胞MHC-I的编码基因HLA-A、HLA-B、HLA-C的基因表达水平图。
图2是本申请实施例2中舍曲林抑制MHC-I在溶酶体内的降解并上调其在细胞膜上的富集图,其中,图2A为人结肠癌细胞SW480、HCT116在采用不同药物组处理后的蛋白免疫印迹实验中MHC-I和GAPDH的表达图;图2B为人结肠癌胞SW480和HCT116加入不同药物组进行处理后的免疫荧光检测图;图2C为培养人结肠癌胞SW480后提取细胞膜蛋白及溶酶体蛋白,后进行蛋白免疫印迹实验,检测MHC-I(目的蛋白)、ATP1A1(细胞膜内参蛋白)、LAMP2(溶酶体内参蛋白)的蛋白水平图。
图3是本申请实施例3中舍曲林促进结肠癌肿瘤微环境中CD8
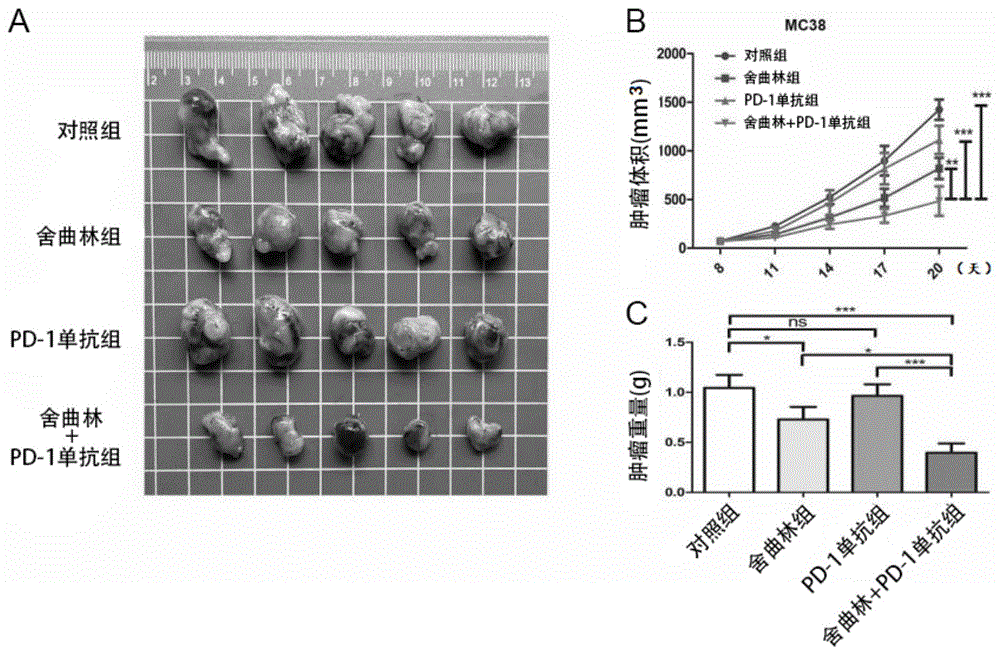
图4是本申请实施例4中舍曲林增加结肠癌对PD-1敏感性图,其中,图4A为各实验组的肿瘤大小图,图4B为各实验组的肿瘤生长曲线,图4C为各实验组的肿瘤瘤重。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将对本发明的技术方案进行详细的描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本发明所保护的范围。
MHC-I是肿瘤抗原呈递的关键成分,也是诱导CD8
舍曲林为用于临床治疗抑郁症的药物,其安全性和有效性都是有迹可循。申请人发现舍曲林能够抑制MHC-I在溶酶体中的降解来上调肿瘤细胞表面的MHC-I表达,恢复肿瘤抗原呈递促进肿瘤微环境中CD8
基于此,本申请提供了一种舍曲林联合PD-1单抗在制备治疗结肠癌的药物中的应用。
实施例1
本实施例1提供了舍曲林于转录后上调MHC-I的表达。
1.1实验材料。
(1)药物:舍曲林(购买自MedChemExpress,货号:HY-B0176A)。
(2)肿瘤细胞:人结肠癌细胞SW480、HCT116。
1.2实验方法。
(1)蛋白免疫印迹。
分别对处于对数生长期的细胞SW480和HCT116加入不同药物进行处理,实验分组如下:
①对照组:加入DMSO;
②舍曲林组:分别加入浓度为5μM、10μM、15μM的舍曲林(舍曲林使用时预先用DMSO配制成浓度为5mM、10mM、15mM的溶液);
各组加入药物的体积(1uL舍曲林(或DMSO)/mL培养基)相同。
细胞培养48h后,提取细胞总蛋白,进行蛋白免疫印迹实验,检测MHC-I(目的蛋白)、GAPDH(内参蛋白)的蛋白水平。
(2)荧光定量聚合酶链式反应。
分别对处于对数生长期的细胞SW480和HCT116加入不同药物进行处理:分组如下:
①对照组:加入DMSO;
②舍曲林组:加入浓度为15μM的舍曲林;
各组加入药物的体积(1uL舍曲林(或DMSO)/mL培养基)相同。
细胞培养24h后,提取细胞总RNA,进行荧光定量聚合酶链式反应实验,检测MHC-I编码基因HLA-A、HLA-B、HLA-C(目的基因)的mRNA水平及GAPDH(内参基因)的mRNA水平并计算HLA-A、HLA-B、HLA-C的相对基因表达水平。
1.3实验结果。
如图1所示,实验结果显示:蛋白免疫印迹结果显示在舍曲林处理后肿瘤细胞MHC-I表达均呈现明显的上调,如图1A,这提示舍曲林可能通过增强肿瘤细胞的抗原提呈来增加肿瘤免疫微环境中CD8
实施例2
实施例2提供了舍曲林抑制MHC-I在溶酶体内的降解并上调其在细胞膜上的富集。
2.1实验材料。
(1)药物:舍曲林(购买自MedChemExpress,货号:HY-B0176A)。
(2)肿瘤细胞:人结肠癌细胞HCT116、SW480。
2.2实验方法。
(1)蛋白免疫印迹。
分别对处于对数生长期的细胞SW480和HCT116加入不同药物进行处理,实验分组如下:
①对照组:加入DMSO。
②舍曲林组:加入浓度为15μM的舍曲林。
③巴佛洛霉素A1组:加入浓度为20nM的巴佛洛霉素A1。
④舍曲林组+巴佛洛霉素A1组:分别加入浓度为15μM的舍曲林和浓度为20nM的巴佛洛霉素A1。
各组加入药物的体积(1uL舍曲林(和/或巴佛洛霉素A1)(或DMSO)/mL培养基)相同。
细胞培养48h后,提取细胞总蛋白,进行蛋白免疫印迹实验,检测MHC-I(目的蛋白)、GAPDH(内参蛋白)的蛋白水平。
(2)免疫荧光。
分别对处于对数生长期的细胞SW480和HCT116加入不同药物进行处理,实验分组如下:
对照组:加入DMSO。
舍曲林组:加入浓度为15μM的舍曲林。
各组加入药物的体积(1uL舍曲林(或DMSO)/mL培养基)相同。
细胞培养48h后,通过免疫荧光实验分别检测细胞中MHC-I的定位(绿色荧光)及LAMP1(溶酶体标志物)定位(红色荧光),并检测MHC-I与LAMP1(溶酶体)的共定位。细胞核用DAPI(蓝色)染色。比例尺:25μm。
(3)细胞膜蛋白、溶酶体蛋白提取及蛋白免疫印迹实验。
分别对处于对数生长期的细胞SW480和HCT116加入不同药物进行处理。实验分组如下:
对照组:加入DMSO;
舍曲林组:分别加入浓度为15μM、20μM的舍曲林;
各组加入药物的体积(1uL舍曲林(或DMSO)/mL培养基)相同。
细胞培养48h后,分别提取细胞膜蛋白及溶酶体蛋白,后进行蛋白免疫印迹实验,检测MHC-I(目的蛋白)、ATP1A1(细胞膜内参蛋白)、LAMP2(溶酶体内参蛋白)的蛋白水平。
2、实验结果。
实验结果如图2所示,图2显示:同时使用溶酶体抑制剂巴佛洛霉素A1及舍曲林对细胞进行处理,巴佛洛霉素A1能增强舍曲林对MHC-I的上调,如图2A。免疫荧光结果显示在舍曲林处理后细胞内MHC-I定位显著增加,且MHC-I与溶酶体的共定位也显著增加,如图2B。蛋白免疫印迹实验也表明舍曲林处理能够增加MHC-I在细胞膜中的富集,减少MHC-I在溶酶体中的富集如图2C。这些结果表明舍曲林能够通过抑制MHC-I在溶酶体中的降解,从而使更多的MHC-I被循环回收重新定位到细胞膜上,增强肿瘤抗原递呈,使肿瘤细胞能够被CD8
实施例3
本实施例3提供了探索舍曲林对小鼠结肠癌细胞皮下移植瘤免疫微环境的影响。
3.1实验材料。
(1)药物:舍曲林(购买自MedChemExpress,货号:HY-B0176A)。
(2)肿瘤细胞:小鼠结肠癌细胞(MC38)(南方医科大学冶亚平教授课题组赠送)。
(3)免疫健全C57BL/6小鼠(购买自北京华阜康生物科技股份有限公司)。
3.2实验分组。
(1)对照组:空白对照,即结肠癌荷瘤小鼠,不经过任何药物处理。
(2)舍曲林组:使用舍曲林处理结肠癌荷瘤小鼠。
3.3 C57BL/6小鼠结肠癌皮下移植瘤模型检测舍曲林对结肠癌肿瘤免疫微环境的影响。
(1)分别将1.5×10
(2)当皮下肿瘤可触及时:舍曲林组每只小鼠给予每日一次口服灌胃30mg/kg舍曲林。
(3)每2天测量一次肿瘤大小(用游标卡尺记录肿瘤最长直径(l)和垂直方向最大横径(w),依照公式v=l×w
(4)2周后,处死小鼠,取出肿瘤组织,将一部分新鲜肿瘤组织制备成单细胞悬液,行流式细胞术检测免疫微环境中CD8
3.4实验结果。
结果如图3所示,图3A及图3B的肿瘤生长曲线和图3C的肿瘤瘤重表明舍曲林能够显著抑制小鼠结肠癌细胞皮下移植瘤的生长。参照图3D-图3F,流式结果显示舍曲林处理组肿瘤免疫微环境中CD8
实施例4
本实施例4提供了舍曲林与PD-1单抗联合治疗对结肠癌皮下移植瘤大小的影响。
4.1实验材料。
(1)药物:舍曲林(购买自MedChemExpress,货号:HY-B0176A);PD-1单抗:anti-mouse PD-1(CD279)(购买自BioXcell,货号:BE0146)。
(2)肿瘤细胞:小鼠结肠癌细胞(MC38)。
(3)免疫健全C57BL/6小鼠。
4.2实验分组。
(1)对照组:空白对照,即结肠癌荷瘤小鼠,不经过任何药物处理。
(2)舍曲林组:使用舍曲林处理结肠癌荷瘤小鼠。
(3)PD-1单药治疗组:使用PD-1单抗处理结肠癌荷瘤小鼠。
(4)舍曲林和PD-1联合治疗组:使用舍曲林和PD-1单抗处理结肠癌荷瘤小鼠。
4.3免疫健全的C57BL/6小鼠结肠癌皮下成瘤实验检测舍曲林与PD-1单抗联合治疗对结肠癌的影响。
(1)分别将1.5×10
(2)当肿瘤可触及时:舍曲林组每只小鼠给予每日一次口服灌胃30mg/kg舍曲林;PD-1组每只小鼠给予每三日一次腹腔注射10mg/kg PD-1单抗;舍曲林与PD-1单抗联合治疗组每只小鼠给予每日一次口服灌胃30mg/kg舍曲林及每三日一次腹腔注射PD-1单抗10mg/kg。
(3)每3天测量一次肿瘤大小(用游标卡尺记录肿瘤最长直径(l)和垂直方向最大横径(w),依照公式v=l×w
(4)20天后,处死小鼠,取出肿瘤组织。
结果如图4所示,图4A为各实验组的肿瘤,图4B为各组肿瘤生长曲线,图4C为各组肿瘤瘤重,图4A、图4B和图4C表明舍曲林与PD-1单抗联合治疗能够显著抑制结肠癌小鼠皮下移植瘤生长。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以所述权利要求的保护范围为准。
- 盐酸舍曲林的新多晶型物和含有它们的组合物,制备盐酸舍曲林多晶型物和无定形物的新方法
- 盐酸舍曲林的新多晶型物和含有它们的组合物,制备盐酸舍曲林多晶型物和无定形物的新方法
