一种锂离子筛吸附剂材料及其制备方法和应用
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于能源材料技术领域,尤其涉及一种锂离子筛吸附剂材料及其制备方法和应用。
背景技术
锂因广泛用于能源、电子、化工、宇航等领域,目前全球约四分之三的锂资源用于制造锂离子电池。随着新能源汽车行业和储能行业的增长,锂离子电池和锂资源的需求量也与日俱增。盐湖卤水中蕴藏有巨量的锂资源,约占世界锂资源的60%,如何从盐湖卤水中高效地提取锂已成为一个亟需解决的问题。
在盐湖卤水提锂方面,吸附剂法、溶剂萃取法、膜法等是最主要的方法。其中吸附法由于离子选择性好、环境友好、循环利用率高等特点,被认为是目前最有前景的盐湖提锂方法之一。吸附法的核心是吸附剂材料,其中离子筛型氧化物是目前研究最多且性能最好的吸附剂。现有的离子筛吸附剂主要包括铝系、锰系和钛系,特别是尖晶石型锰系(HMn
然而,传统的锂离子筛材料需要采用锂源(如氢氧化锂或碳酸锂)作为原料,先制备出含锂前驱体,然后通过稀硫酸或稀盐酸洗去晶格中的锂获得离子筛材料。不仅工序复杂、成本高,且消耗大量淡水和酸,污染严重。在后续的使用过程中,传统的锂离子筛材料采用质子-锂离子交换的工作原理实现卤水提锂,并通过酸洗脱实现循环使用,具有稳定性不足等问题。
发明内容
鉴于此,本发明提供了一种锂离子筛吸附剂材料及其制备方法和应用,主要目的是解决锂离子筛吸附剂的合成原料中锂源用量大、制备工艺复杂、酸洗污染严重的技术问题。
一方面,本发明提供了一种锂离子筛吸附剂材料,所述锂离子筛吸附剂材料的化学分子式为式I;
M1
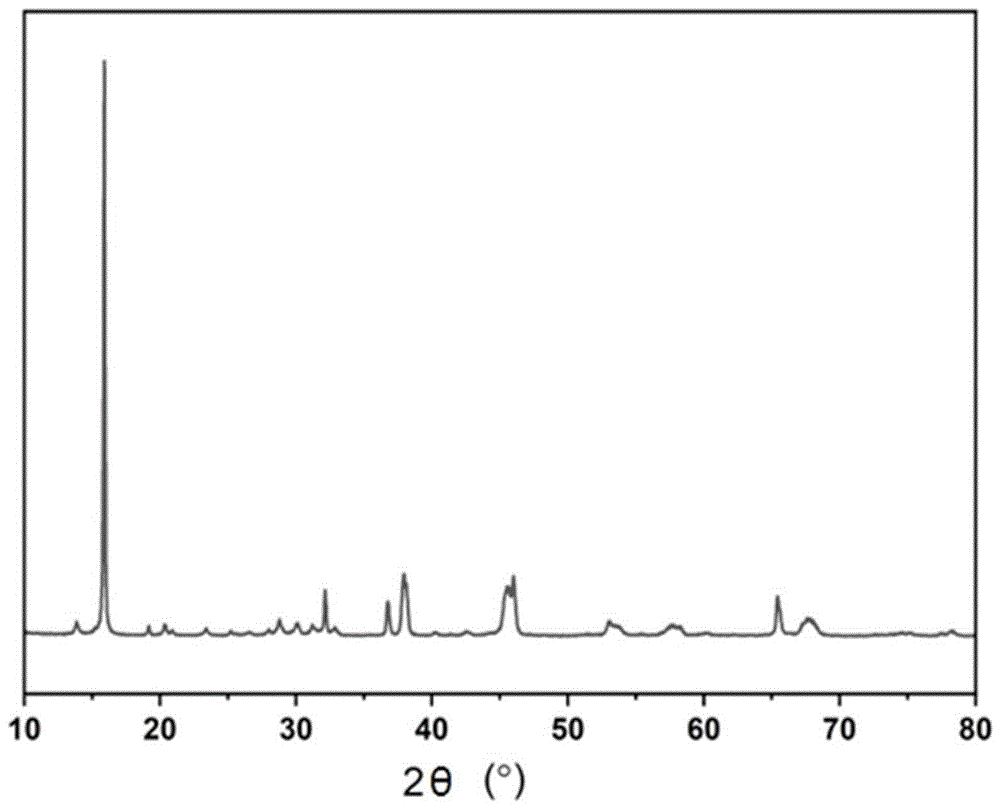
式I中的M1选自非锂的碱金属元素中的至少一种,0 式I中的M2选自过渡金属元素中的至少一种; Li和过渡金属元素M2共占据一个晶格位置,0≤x<0.5。 本发明上述式I中的x和y表示相应金属元素间的摩尔比。 可选地,式I中y选自0.05、0.1、0.15、0.2、0.25、0.3、0.35、0.4、0.45、0.5、0.55、0.6、0.65、0.7、0.75、0.8、0.85、0.9、0.95、1.0中的任意值或任意两者之间的范围值。 可选地,式I中x选自0、0.05、0.1、0.15、0.2、0.25、0.3、0.35、0.4、0.45、0.49中的任意值或任意两者之间的范围值。 本发明人在锂离子吸附剂研发过程中发现传统锂离子筛吸附剂在制备过程中需要以大量的锂源作为分子筛的原料,需要先制备出含锂前驱体,再通过酸洗工序去除分子筛晶格中的锂,进而获得锂离子筛吸附剂材料。该方法中锂源使用量较大,增加了生产成本,酸洗水严重污染环境;针对上述问题,本发明人创新性的提出如何减少锂源使用量和不使用酸洗工序仍可以制备出一种具有纯度高、吸附量高、稳定性好的锂离子筛吸附剂材料;为了解决上述技术问题,本发明人首次提出了一种锂离子筛吸附剂材料,其与传统吸附剂相比,具有不同的元素组成和不同的工作原理;具体的,本发明创新性的在锂离子筛吸附剂的元素组成上引入了非锂碱金属M1,利用非锂碱金属M1与含锂溶液中锂离子可自发进行离子交换的工作原理,实现了锂离子筛吸附剂材料可以吸附含锂溶液中锂离子的目的,进而达到在减少锂源使用量(本发明锂源使用量为传统吸附剂材料锂源的50%以下)和不使用酸洗工序的条件下仍可以制备得到纯度高、吸附量高、稳定性好的锂离子筛吸附剂材料的目的。 可选地,所述式I中的M1选自非锂的碱金属元素Na、K、Rb和Cs中的至少一种。 可选地,所述式I中的M2选自过渡金属元素Fe、Co、Ni和Mn中的至少一种。 本发明的上述锂离子筛吸附剂材料中的非锂碱金属离子与溶液中锂离子通过自发进行离子交换,实现含过渡金属系的分子筛材料可以吸附溶液中锂离子的目的;本发明的锂离子筛吸附剂的吸附锂的功能主要通过非锂碱金属元素M1和过渡金属元素M2复合实现,该复合金属的化合物可以选用其氧化物实现吸附溶液中锂离子的目的。 第二方面,本发明提供了上述锂离子筛吸附剂材料的制备方法,包括以下步骤: S1:非锂的碱金属源、锂源、过渡金属源混合,得到混合物; S2:所述混合物经过高温固相烧结,再降温后得到锂离子筛吸附剂材料。 本发明在上述制备方法的原料中引入了非锂的碱金属源,可以降低锂源使用量,不需要酸洗过程,简化了制备工艺,降低了生产成本。 可选地,步骤S1中所述非锂的碱金属源和所述过渡金属源的摩尔比为0.3~2:1。 可选地,所述非锂的碱金属源和所述过渡金属源的摩尔比选自0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2中的任意值或任意两者之间的范围值。 可选地,步骤S1中所述锂源和所述过渡金属源的摩尔比为0~0.3:1。 可选地,所述锂源和所述过渡金属源的摩尔比为0、0.05、0.1、0.15、0.2、0.25、0.3中的任意值或任意两者之间的范围值。 可选地,步骤S1中,所述锂源选自锂的氧化物、锂的碳酸盐、锂的草酸盐、锂的醋酸盐以及锂的氢氧化物中的至少一种; 所述非锂的碱金属源中的钠源选自钠的氧化物、钠的碳酸盐、钠的草酸盐、钠的醋酸盐以及钠的氢氧化物中的至少一种; 所述非锂的碱金属源中的钾源选自钾的氧化物、钾的碳酸盐、钾的草酸盐、钾的醋酸盐以及钾的氢氧化物中的至少一种; 所述非锂的碱金属源中的铷源选自铷的氧化物、铷的碳酸盐、铷的草酸盐、铷的醋酸盐以及铷的氢氧化物中的至少一种; 所述非锂的碱金属源中的铯源选自铯的氧化物、铯的碳酸盐、铯的草酸盐、铯的醋酸盐以及铯的氢氧化物中的至少一种; 所述过渡金属源中的铁源选自铁的氧化物、铁的碳酸盐、铁的草酸盐、铁的醋酸盐以及铁的氢氧化物中的至少一种; 所述过渡金属源中的钴源选自钴的氧化物、钴的碳酸盐、钴的草酸盐、钴的醋酸盐以及钴的氢氧化物中的至少一种; 所述过渡金属源中的镍源选自镍的氧化物、镍的碳酸盐、镍的草酸盐、镍的醋酸盐以及镍的氢氧化物中的至少一种; 所述过渡金属源中的锰源选自锰的氧化物、锰的碳酸盐、锰的草酸盐、锰的醋酸盐以及锰的氢氧化物中的至少一种。 可选地,步骤S1中,所述非锂的碱金属源、所述锂源和所述过渡金属源经过手工研磨、球磨、溶液蒸干法以及共沉淀法中的至少一种方式进行混合。 可选地,步骤S2中,所述高温固相烧结的温度为500℃~1000℃,所述高温固相烧结的时间为0.5h~24h。 优选地,所述高温固相烧结的温度为500℃~850℃,所述高温固相烧结的时间为0.5h~6h。 进一步优选地,所述高温固相烧结的温度为500℃~700℃。 可选地,所述高温固相烧结的温度选自500℃、550℃、600℃、650℃、700℃、750℃、800℃、850℃、900℃、950℃、1000℃中的任意值或任意两者之间的范围值。 可选地,所述高温固相烧结的时间选自0.5h、1h、1.5h、2h、2.5h、3h、3.5h、4h、4.5h、5h、5.5h、6h、6.5h、7h、7.5h、8h、8.5h、9h、9.5h、10h、10.5h、11h、11.5h、12h、12.5h、13h、13.5h、14h、14.5h、15h、15.5h、16h、16.5h、17h、17.5h、18h、18.5h、19h、19.5h、20h、20.5h、21h、21.5h、22h、22.5h、23h、23.5h、24h中的任意值或任意两者之间的范围值。 可选地,步骤S2中的降温是自然冷却至室温。 第三方面,本发明提供了上述锂离子筛吸附剂材料在吸附含锂溶液中锂离子中的应用;所述锂离子筛吸附剂材料中的非锂的碱金属离子M1与所述含锂溶液中的锂离子自发进行离子交换。 可选地,所述含锂溶液包括盐湖卤水、矿石提锂沉锂母液、含锂废液、锂离子电池回收中产生的含锂溶液及其各自提纯高含锂溶液。 可选地,所述盐湖为高原等各类型的盐湖。 可选地,所述锂离子筛吸附剂材料和其他材料混合后,可作为吸附塔的填料,用于盐湖原卤或老卤中的锂离子提取。 本发明的上述锂离子筛吸附剂材料可适用于任何类型或组成的含锂离子的溶液,其均可实现吸附锂离子的目的。 第四方面,本发明提供了上述锂离子筛吸附剂材料在储能材料的应用。 可选地,所述锂离子筛吸附剂材料吸附锂离子后,直接作为原料之一,用于合成锂离子电池正极材料。 本发明的上述锂离子筛吸附剂材料在吸附锂离子之后,形成一种含有大量锂离子的过渡金属化合物的新材料。 本发明基于上述锂离子筛吸附材料吸附锂离子之后形成的新的锂离子材料,充分考虑到该新的锂离子材料中所含有的大量的锂离子的应用价值,创新性提出可以将该新的锂离子材料应用于储能或动力领域,尤其适用于锂离子电池的正极材料中。 第五方面,本发明提供了上述锂离子材料在储能材料中的应用。 可选地,上述锂离子材料可直接作为原料,用于制备锂离子电池过渡金属氧化物的正极材料。 第六方面,本发明提供了一种锂离子电池的正极材料,所述正极材料的原料中包括上述锂离子材料。 可选地,所述正极材料包括锂离子电池三元正极材料,如Li(Ni,Co,Mn)O 可选地,所述正极材料包括锂离子电池锰基材料,如LiMn 可选地,所述正极材料包括锂离子电池钴酸锂材料。 本发明至少包括以下创新性技术: (1)本发明的锂离子筛吸附剂材料分子式为M1 (2)本发明的锂离子筛吸附剂材料在制备过程中,使用的锂源比传统吸附剂材料少一半以上,且只需要一步烧结就可以制备,无需经过酸洗过程。 (3)本发明的锂离子筛吸附剂材料可用于吸附溶液中的锂离子。 (4)本发明的锂离子筛吸附剂材料吸附溶液中锂离子之后形成新的锂离子材料又可以用于储能领域,尤其可直接作为原料制备锂电池正极材料。 与现有技术相比,本发明具有以下有益效果: (1)本发明的锂离子筛吸附剂材料的原料锂源的使用量为传统吸附剂材料的锂源用量的50%以下,降低了成本。 (2)本发明的锂离子筛吸附剂材料制备方法为一种全新的方法,该方法采用一步烧结,无需酸处理,可降低成本,无需消耗淡水和酸,对环境友好。 (3)本发明的锂离子筛吸附剂材料具有优异的锂离子选择性和很高的吸锂容量(30-40mg/g),可以用于盐湖提锂的原卤直提,具有很好的应用前景。 (4)本发明的锂离子筛吸附剂材料在吸附锂离子后,可以直接用于制备高性能锂离子电池正极材料,无需进行脱锂,避免了脱锂过程中淡水和酸的消耗,实现了真正的绿色提锂和用锂。 附图说明 图1为本发明实施例1制备的多元锂离子筛吸附剂材料X射线粉末衍射图; 图2为本发明实施例1制备的多元锂离子筛吸附剂材料的扫描电镜图; 图3为本发明实施例1制备的三元正极材料的X射线粉末衍射图; 图4为本发明实施例1制备的三元正极材料的首圈充放电曲线图。 具体实施方式 下面将对本发明实施方式中的技术方案进行清楚、完整地描述,显然,所描述的实施方式仅仅是本发明一部分实施方式,而不是全部的实施方式。基于本发明中的实施方式,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施方式,都属于本发明保护的范围。 如无特别说明,本申请的实施例中的原料均通过商业途径购买。 下述实施例1~实施例4制备式I所示化合物; M1 式I中的M1选自非锂的碱金属元素中的至少一种,0 M2选自过渡金属元素中的至少一种; Li和过渡金属元素M2共占据一个晶格位置,0≤x<0.5; x和y表示相应金属元素间的摩尔比。 实施例1 制备吸附剂:称取分析纯碳酸锂0.370g,碳酸锰4.597g、碳酸钠1.059g和碳酸钾2.073g,在研钵中混合充分研磨2小时,转移至刚玉坩埚,在箱式马弗炉中,以10℃/min的速度升温至700℃,保温10小时,自然降温至室温,即获得锂离子筛型化合物。其X射线衍射图如图1,其扫描电镜图如图2,该锂离子筛吸附剂的分子式为(Na 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为200mg/L的溶液中,8小时后达到吸附平衡,测得其平衡吸附容量为30.8mg/g。 平衡吸附容量是指吸附达到平衡后,吸附溶液中锂离子减少的质量与吸附剂质量的比值。 锂离子减少的质量=(溶液中锂离子初始浓度-吸附平衡后锂离子浓度)×溶液体积。 制备正极材料:称取吸附锂离子后的吸附剂材料0.611g、氧化镍0.747g、四氧化三钴0.321g、碳酸锂0.517g,400转/分钟球磨12小时,在900℃下烧结12小时,降温后得到镍钴锰三元正极材料Li(Ni,Co,Mn)O 实施例2 制备吸附剂:称取分析纯碳酸锂0.370g,(Ni 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为100mg/L的溶液中,8小时后达到吸附平衡,测得其平衡吸附容量为33.5mg/g。 实施例3 制备吸附剂:在100mL去离子水中加入醋酸钾2.213g、六水硫酸镍4.159g、四水硫酸锰1.004g以及二水醋酸锂0.235g,充分搅拌溶解。将溶液在80度烘箱中蒸干,将粉末装入刚玉坩埚,转移至马弗炉中,继续以5℃/min的速率升温至800℃保温10小时,自然冷却至室温,即获得锂离子筛型化合物;该锂离子筛吸附剂的分子式为K(Li 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为150mg/L的溶液中,8小时后达到吸附平衡,测其平衡吸附容量为37.4mg/g。 实施例4 制备吸附剂:称取分析纯碳酸锂0.740g,(Ni 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为100mg/L的溶液中,8小时后达到吸附平衡,测其平衡吸附容量为36.5mg/g。 对比例1 制备吸附剂:称取分析纯碳酸锂0.739g和碳酸锰4.597g,在研钵中混合充分研磨2小时,转移至刚玉坩埚,在箱式马弗炉中,以10℃/min的速度升温至800℃,保温10小时,自然降温至室温,得到传统锂离子筛型化合物(HMn 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为200mg/L的溶液中,8小时后达到吸附平衡,测得其平衡吸附容量为15.8mg/g。 对比例2 制备吸附剂:称取分析纯氢氧化锂1.200g和羟基氧化锰3.518g,加入含有20ml去离子水的50mL水热罐中,在120℃下保温1天,过滤洗涤干燥,得到中间产物LiMnO 吸附溶液中锂离子:称取0.5g锂离子筛吸附剂材料置于400mL锂离子浓度为200mg/L的溶液中,8小时后达到吸附平衡,测得其平衡吸附容量为28.2mg/g。 本发明的实施例1-实施例4均成功制备出锂离子筛吸附剂材料;将该吸附剂材料用于吸附溶液中锂离子时,其吸附效果明显;以该吸附剂吸附锂离子后的新材料成功制备出正极材料,其充放电性能良好。 本发明以实施例1制备的锂离子筛吸附剂材料为例,该吸附剂分子式为:(Na 本发明实施例2-实施例4的X射线衍射图与图1相似,分析表明实施例2-实施例4的锂离子筛吸附剂材料依次具有以下分子式结构: (Na K(Li (Na 本发明制备的锂离子筛吸附剂材料具有以下化学通式: M1 其中,M1选自非锂的碱金属元素中的至少一种,0 M1优选碱金属元素Na、K、Rb和Cs中的至少一种; M2选自过渡金属元素中的至少一种,优选Fe、Co、Ni和Mn中的至少一种;Li和过渡金属元素M2共占据一个晶格位置,0≤x<0.5;x和y表示相应金属元素间的摩尔比。 本发明以实施例1制备的锂离子筛吸附剂材料为例,采用该吸附剂吸附溶液中锂离子后的材料制备的正极材料的充放电曲线如图4所示,说明本发明实施例1的吸附剂在吸附锂离子后制备的正极材料具有良好的电学性能。 本发明的实施例2-4的充放电曲线与图4相似,分析表明实施例2-实施例4的锂离子筛吸附剂材料吸附锂离子后制备的正极材料具有良好的充放电性能;表明本发明的锂离子吸附剂材料在吸附锂离子后获得的新材料作为原料之一,可成功制备出具有良好电学性能的锂离子电池正极材料。 通过上述实验及其结果说明采用本发明提供的锂离子筛吸附剂材料、吸附锂离子后形成的新锂离子材料均可应用于储能或动力领域,尤其可用于制备锂离子电池的正极材料。 本发明实施例1-实施例4在制备锂离子筛吸附剂材料中,锂源的使用量在原料总量中的占比依次为4.5wt%、2.1wt%、3.1wt%、5.2wt%左右;对比例1和对比例2的锂源使用量在原料总量中的占比依次为13.8wt%、25.4wt%左右;通过对比可知,本发明方法制备的锂离子筛吸附剂材料中锂源的使用量大约为传统方法中锂源使用量的0.08-0.38倍左右,其远远小于对比例1和对比例2方法中锂源的使用量。 对比例1和对比例2中制备方法中将锂源和锰源混合焙烧后仅得到吸附剂的前驱体如LiMn 本发明实施例1-实施例4在制备锂离子筛吸附剂材料的方法为: S1:非锂的碱金属源、锂源和过渡金属源混合,得到混合物; S2:混合物经过高温固相烧结,再降温后得到锂离子筛吸附剂材料。 优选地,非锂的碱金属源和过渡金属源的摩尔比为0.3~2:1。 优选地,锂源和过渡金属源的摩尔比为0~0.3:1。 通过上述实施例1-4和对比例1-2可知,本发明在上述制备方法的原料中通过引入非锂的碱金属源,首先大大降低了锂源使用量,同时也不需要酸洗过程,又简化了制备工艺,直接降低了生产成本。因此,本发明的上述制备方法与传统技术相比具有非常显著的技术效果。 本发明实施例1-4制备的锂离子筛吸附剂材料的吸附量依次为30.8mg/g、33.5mg/g、37.4mg/g、36.5mg/g;在基本相同的测试条件下,对比例1和对比例2传统方法制备的吸附剂的吸附量依次为15.8mg/g、28.2mg/g;通过对比可知,本发明的吸附剂的锂离子吸附量基本是对比例1和对比例2吸附剂锂离子吸附量的1.5-2倍左右,表明本发明的吸附剂对于锂离子的吸附能力更强。同时,本发明的锂离子吸附剂可重复循环使用。 本发明提供的一种全新的制备方法以及合理的原料配比制备的锂离子吸附剂材料具有锂离子吸附能力和电学性能。 本发明提供的锂离子筛吸附剂材料具有结构稳定、吸附量大的优点,且该吸附剂材料在吸附锂离子后又可以直接用于制备锂离子电池的正极材料,该正极材料又具有良好的电学性能,其为储能领域提供了一种新型材料。 本发明提供的锂离子筛吸附剂材料的制备方法操作方便,锂源使用量大大减少,省去了酸洗工艺,既提高了生产效率,又降低了生产成本,且对环境友好;本发明的制备方法拓展了新能源材料尤其锂电池电极材料的原料来源,其具有很大的工业前景。 以上所述,仅是本申请的几个实施例,并非对本申请做任何形式的限制,虽然本申请以较佳实施例揭示如上,然而并非用以限制本申请,任何熟悉本专业的技术人员,在不脱离本申请技术方案的范围内,利用上述揭示的技术内容做出些许的变动或修饰均等同于等效实施案例,均属于技术方案范围内。
- 一种表面掺杂的长寿命锂离子筛吸附剂的制备方法
- 一种由天然材料改性的吸附剂及其制备方法和应用
- 一种天然材料复合吸附剂及其制备方法、应用
- 一种用于染料吸附的聚脒/碳纳米材料吸附剂的制备方法及应用
- 一种制备锂离子筛吸附剂颗粒的方法和应用
- 一种高吸附速率钛系锂离子筛吸附剂制备方法及应用
