基于金属有机框架分层负载级联酶系统的纸基传感器
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于生物催化领域,尤其涉及一种基于金属有机框架分层负载级联酶系统的纸基传感器及应用。
背景技术
生物体内发生着大量酶级联反应(例如,光合过程、呼吸过程、代谢过程等),生物系统通过将多种酶催化系统限制在亚细胞区室中有效保证这一系列复杂化学反应高效、有序地进行。限域微环境有效降低了级联反应中的扩散势垒、提高中间体的局部浓度,具有高度的原子经济性。在框架结构中组装多种酶,以模拟高效的生物级联酶系统,具有非常重要的应用价值和发展潜力。MOFs(metal organic frameworks,金属有机框架)具有比表面积高、孔径可调、组分多样、表面易功能化等诸多优点,是封装酶的理想框架材料之一。然而,传统的多酶系统封装策略采取单腔室的金属有机框架,随机无序组装使其易受不相容性和交叉反应的限制。受生物体内多酶催化构建策略的启发,基于隔室化思想项目申请人构建了层次化支架实现多酶系统有序隔室化封装,通过精准调控中间体扩散路径,有效提高了酶协同催化效率。
可通过级联酶特异性催化和报告分子识别信号转导实现生物标志物的特异性检测,这些串联催化电路和信号输出元件具有广泛的医学应用潜力。然而,基于级联酶的串联催化电路在实验室外的应用受到了级联酶和报告分子的储存和运输条件的限制。如何在提高级联酶催化效率的前提下,延长传感器中酶和报告分子保存稳定性以及保证传感器的即用性是基于级联酶的生物传感器的研究重点。纸基平台作为介质为合成生物学提供了一个可替代的、多功能的操作场所。将体外无转录检测系统通过冷冻干燥负载到纸盘上,可提高其长期稳定储存、避免冷链运输和冷藏;通过再水合作用后,无细胞系统可以在纸盘上执行任何遗传回路。故基于冷冻干燥的纸基检测系统是实现传感器检测组件长期稳定储存的有潜力的策略。
针对酶生物传感器应用亟待解决的级联酶催化信号串扰、级联效率、运输和保存的稳定性共性瓶颈问题,构建了基于金属有机框架分层负载级联酶系统的纸基传感器,可用于不同疾病相关生物标志物的高灵敏检测。
发明内容
本发明的目的在于针对现有技术的不足,提供一种基于金属有机框架分层负载级联酶系统的纸基传感器及应用,MOFs的限域效应有效隔绝复杂的催化环境对酶活性的影响,提高酶在室温存储的稳定性;分层负载实现酶的有序隔室化封装,通过精准调控中间体扩散路径,有效提高了酶协同催化效率,可用于不同疾病相关生物标志物的高灵敏检测。
本发明的目的是通过以下技术方案实现的:一种基于金属有机框架分层负载级联酶系统的纸基传感器,其特征在于,通过以下制备方法得到:通过外延逐层生长策略,实现级联酶系统的分层负载,制备多壳层酶微晶体“酶1@MOFs@酶2@MOFs”;将制备的多壳层酶微晶体“酶1@MOFs@酶2@MOFs”与偶联显色底物共负载在纸基介质上,制得基于金属有机框架分层负载级联酶系统的纸基传感器;
其中,酶1为肌氨酸氧化酶或尿酸氧化酶,酶2为辣根过氧化物酶。
进一步地,所述偶联显色底物为Amplex Red。
进一步地,所述外延逐层生长策略是指先制备酶1@MOFs,然后以酶1@MOFs为种子固定酶2,制备得到多壳层酶微晶体“酶1@MOFs@酶2@MOFs”;包括以下步骤:
(1)向浓度为790mM的2-MI和浓度为0.55mM的CTAB的水溶液中,加入浓度为1mg/mL-5mg/mL的酶1,搅拌均匀;然后加入浓度为97.5mM的硝酸锌溶液,搅拌均匀;搅拌结束后,室温静置3-5h;离心收集酶1@MOFs,洗涤若干次,分散在磷酸缓冲盐溶液中;所述2-MI/CTAB的水溶液、酶1和硝酸锌溶液体积比为1.75:0.60:0.25;
(2)向浓度为790mM的2-MI和浓度为0.55mM的CTAB的水溶液中,加入浓度为1mg/mL-5mg/mL的酶1@MOFs,搅拌均匀;然后加入浓度为97.5mM的硝酸锌溶液,搅拌均匀;搅拌结束后,加入浓度为1mg/mL-5mg/mL的酶2,搅拌均匀;搅拌结束后,室温静置1-2h;离心收集酶1@MOFs@酶2@MOFs,洗涤若干次,分散在磷酸缓冲盐溶液中;所述2-MI/CTAB的水溶液、酶1@MOFs、酶2和硝酸锌溶液的体积比为1.75:0.20:0.60:0.25。
进一步地,所述酶1和酶2的质量比为1:1。
进一步地,所述将制备的多壳层酶微晶体“酶1@MOFs@酶2@MOFs”与偶联显色底物共负载在纸基介质上具体为:将滤纸在0.01wt%的双乙酰吡碳酸中孵育12h,并用无核酸水清洗
进一步地,所述预冷冻的时间不低于5s;所述冷冻干燥的时间不低于6h。
一种基于上述的基于金属有机框架分层负载级联酶系统的纸基传感器在检测肌氨酸中的应用,其中,酶1为肌氨酸氧化酶,酶2为辣根过氧化物酶。
一种基于上述的基于金属有机框架分层负载级联酶系统的纸基传感器在检测尿酸中的应用,其中,酶1为尿酸氧化酶,酶2为辣根过氧化物酶。
上述的基于金属有机框架分层负载级联酶系统,可用于不同疾病相关生物标志物的高灵敏检测;所述不同疾病相关生物标志物为对应于肌氨酸氧化酶(sarcosineoxidase,SOX)的肌氨酸,SOX可根据待检测的生物标志物为尿酸而更换为尿酸氧化酶(urate oxidase,UOX)。
本发明的有益效果是:(1)MOFs作为载体材料可区室化封装固定酶的活性构象,MOFs的限域环境有效隔绝复杂的催化环境对酶活性的影响,提高酶在室温存储的稳定性;(2)分层负载实现酶的有序隔室化封装,通过精准调控中间体扩散路径,选择性使底物扩散进入酶的活性位点,降低扩散势垒、提高底物及中间体的局部浓度显著提高反应的原子经济性,有效提高了酶协同催化效率;(3)区室化级联酶MOFs系统和荧光报告分子在醋酸纤维纸盘上共负载保证级联酶生物传感器具备即用性。
附图说明
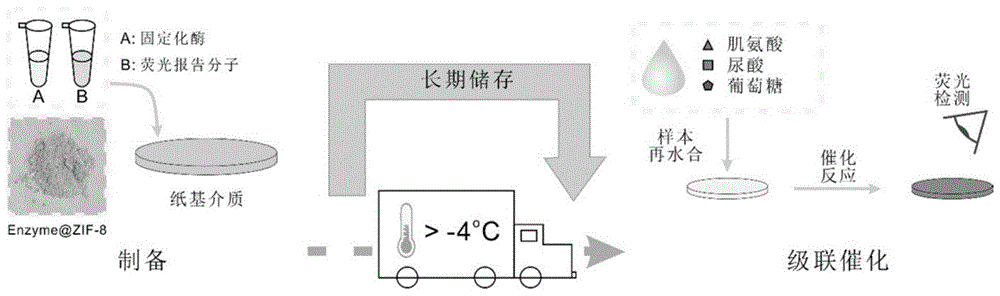
图1是本发明提供的基于金属有机框架分层负载级联酶系统的纸基传感器的示意图;
图2是合成的ZIF-8、SOx、HRP、SOx@ZIF-8@HRP@ZIF-8、纸基介质和肌氨酸传感器的傅里叶变换红外光谱图;
图3是制备肌氨酸传感器的扫描电子显微镜(SEM)图;
图4是不同浓度的肌氨酸的动力学荧光成像图;
图5是合成的ZIF-8、UOx、HRP、UOx@ZIF-8@HRP@ZIF-8、纸基介质和尿酸传感器的傅里叶变换红外光谱图;
图6是制备尿酸传感器的扫描电子显微镜(SEM)图;
图7是不同浓度的尿酸的动力学荧光成像图。
具体实施方式
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
这里将详细地对示例性实施例进行说明,其示例表示在附图中。下面的描述涉及附图时,除非另有表示,不同附图中的相同数字表示相同或相似的要素。以下示例性实施例中所描述的实施方式并不代表与本发明相一致的所有实施方式。相反,它们仅是与如所附权利要求书中所详述的、本发明的一些方面相一致的装置和方法的例子。
本发明的基于金属有机框架分层负载级联酶系统的纸基传感器,通过外延逐层生长策略,实现级联酶系统的分层负载,制备多壳层酶微晶体“酶1@MOFs@酶2@MOFs”。所述的多壳层酶微晶体“酶1@MOFs@酶2@MOFs”中的酶1和酶2被分别固定在酶微晶体的内外层;将制备的多壳层酶微晶体“酶1@MOFs@酶2@MOFs”通过冷冻干燥方式,与偶联显色底物共负载在纸基介质上,通过含有目标生物标志物的样本在水和事件,实现不同疾病相关生物标志物的高灵敏检测,如图1所示。
实施例1:
(1)向1.75mL 2-甲基咪唑(2-MI,790mM)和十六烷基三甲基溴化铵(CTAB,0.55mM)的水溶液中,加入0.60mL、5mg/mL的肌氨酸氧化酶(sarcosine oxidase,SOX),搅拌1min;然后加入0.25mL硝酸锌(Zn(NO
(2)向1.75mL 2-MI(790mM)和CTAB(0.55mM)的水溶液中,加入0.20mL SOX@MOFs,搅拌5min;搅拌结束后,加入0.60mL、5mg/mL的辣根过氧化物酶(horseradish peroxidase,HRP),搅拌1min;然后加入0.25mL Zn(NO
(3)清洁的滤纸被打孔成直径为8mm的纸基圆盘,然后将其在0.01%的双乙酰吡碳酸中孵育12h,并用无核酸水清洗3次;随后,将25μL、0.24mg/mL多壳层酶微晶体SOX@MOFs@HRP@MOFs和5μL、1mM偶联显色底物滴加在纸基圆盘上,先将其在液氮中预冷冻5s,取出后置于冷冻干燥机中冻干6h。
结果:
(1)对实施例1中制备的肌氨酸纸基传感器进行傅里叶变换红外光谱,如图2所示,固定化酶显示出比游离的SOX(1555cm
(2)对实施例1中制备的肌氨酸纸基传感器用扫描电子显微镜(SEM)进行形貌表征,如图3所示,SOX@MOFs@HRP@MOFs微晶体均匀分散在纸基介质上。
以上结果表明成功制备了肌氨酸纸基传感器。
实施例2:
肌氨酸纸基传感器在25℃和环境湿度下进行测试,将5μL含有不同浓度的肌氨酸(5-1000μM)滴加在纸基传感器正中心,结果如图4所示。
结果:
(1)对实施例1中的不同浓度的肌氨酸的荧光成像强度进行统计,发现随肌氨酸浓度升高,强度逐渐增强,且在5-1000μM浓度区间表现出良好线性。
(2)通常,肌氨酸的浓度为1-3μM,而在前列腺癌患者的尿液样本中增加约一个数量级左右,表明该传感器满足临床前列腺癌生物标志物的检测需求。
实施例3:
(1)向1.75mL 2-甲基咪唑(2-MI,790mM)和十六烷基三甲基溴化铵(CTAB,0.55mM)的水溶液中,加入0.60mL、5mg/mL的尿酸氧化酶(urate oxidase,UOX),搅拌1min;然后加入0.25mL硝酸锌(Zn(NO
(2)向1.75mL 2-MI(790mM)和CTAB(0.55mM)的水溶液中,加入0.20mL上述UOX@MOFs,搅拌5min;搅拌结束后,加入0.60mL、5mg/mL的辣根过氧化物酶(horseradishperoxidase,HRP),搅拌1min;然后加入0.25mL Zn(NO
(3)清洁的滤纸被打孔成直径为8mm的纸基圆盘,然后将其在0.01%的双乙酰吡碳酸中孵育12h,并用无核酸水清洗若干次;随后,将25μL、0.12mg/mL多壳层酶微晶体UOX@MOFs@HRP@MOFs和5μL、1mM偶联显色底物滴加在纸基圆盘上,先将其在液氮中预冷冻5s,取出后置于冷冻干燥机中冻干6h。
结果:
(1)对实施例3中制备的尿酸纸基传感器进行傅里叶变换红外光谱,如图5所示,固定化酶显示出比游离的UOX(1537cm
(2)对实施例3中制备的尿酸纸基传感器用扫描电子显微镜(SEM)进行形貌表征,如图6所示,UOX@MOFs@HRP@MOFs微晶体均匀分散在纸基介质上。
以上结果表明成功制备了尿酸纸基传感器。
实施例4:
尿酸纸基传感器在25℃和环境湿度下进行测试,将5μL含有不同浓度的尿酸(0.05-5.00mM)滴加在纸基传感器正中心,结果如图7所示。
结果:
(1)对实施例3中的不同浓度的尿酸的荧光成像强度进行统计,发现随尿酸浓度升高,强度逐渐增强,且在0.05-5.00mM浓度区间表现出良好线性。
(2)通常,男性患者尿液中的尿酸浓度高于0.417mM,女性患者尿液中的尿酸浓度高于0.357mM,表明该传感器满足临床高尿酸症生物标志物的检测需求。
综上所述,根据本发明提供的基于金属有机框架分层负载级联酶系统的纸基传感器,解决了酶生物传感器应用亟待解决的级联酶催化信号串扰、级联效率、运输和保存的稳定性共性瓶颈问题,根据本发明制备的基于金属有机框架分层负载级联酶系统的纸基传感器稳定性好和级联效率高,在疾病相关的生物标志物检测方面具有显著优势,为疾病的早期精准诊断提供了新思路。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明保护的范围之内。
以上实施例仅用于说明本发明的设计思想和特点,其目的在于使本领域内的技术人员能够了解本发明的内容并据以实施,本发明的保护范围不限于上述实施例。所以,凡依据本发明所揭示的原理、设计思路所作的等同变化或修饰,均在本发明的保护范围之内。
本领域技术人员在考虑说明书及实践这里公开的内容后,将容易想到本申请的其它实施方案。本申请旨在涵盖本申请的任何变型、用途或者适应性变化,这些变型、用途或者适应性变化遵循本申请的一般性原理并包括本申请未公开的本技术领域中的公知常识或惯用技术手段。说明书和实施例仅被视为示例性的。
应当理解的是,本申请并不局限于上面已经描述并在附图中示出的精确结构,并且可以在不脱离其范围进行各种修改和改变。
- 一种金属有机框架-分子印迹纸基拉曼传感器制备及其在噻菌灵检测中的应用
- 一种金属有机框架材料修饰的纸基传感器及其检测挥发性含硫化合物的应用
