抗肿瘤组合物
文献发布时间:2024-04-18 19:58:26
本申请是申请号为202010123739.7、申请日为2020年2月27日、发明名称为“抗肿瘤组合物”的中国发明专利申请的分案申请。
技术领域
本申请涉及一种抗肿瘤组合物,更具体涉及长型双歧杆菌与免疫检查点抑制剂的联合使用。
背景技术
治愈癌症一直是医学领域的一大难题,传统的化疗、放疗等治疗方式都会对患者带来较大的副作用和痛苦。近几年,癌症的免疫疗法在血液瘤和部分实体瘤中展现了惊人的疗效,且给患者带来的副作用较小,给人类治愈癌症带来了巨大的希望。
正常情况下,肿瘤细胞的表面存在可被人体免疫T细胞识别的抗原,而人体的免疫系统是能够识别并杀死肿瘤细胞的,然而肿瘤细胞为了生存和生长,会采用各种方式来躲避免疫系统的识别和杀伤。肿瘤免疫疗法就是识别并破坏掉肿瘤细胞的这种伎俩,使人体恢复正常的抗肿瘤免疫反应,从而可以控制和消除多种肿瘤。肿瘤免疫疗法主要包括五种类型:(1)治疗性抗体;(2)癌症疫苗;(3)细胞治疗,即CAR-T疗法;(4)免疫调节剂;(5)免疫检查点抑制剂。
人体免疫系统的活性受共刺激分子的调控,共刺激分子就是免疫检查点。当发生抗原识别时,其他分子与免疫细胞和靶细胞表面分子相互作用,进而确定相互作用的平衡。如果很大程度上信号是正性的,免疫细胞会被激活并攻击靶细胞呈递的抗原。反之,如果信号是负性的,免疫细胞会失活,这种失活有时是永久性的,并且抗原被识别为正常/自身抗原。已经相对研究清楚的癌症相关免疫检查点包括CTLA-4,PD-1和PD-L1。免疫检查点抑制剂就是针对相应的免疫检查点研发的一些单抗类药物,其主要作用为阻断表达免疫检查点的肿瘤细胞与免疫细胞之间的作用,从而阻断肿瘤细胞对免疫细胞的抑制作用。目前广泛应用的免疫检查点抑制剂包括靶向程序性死亡蛋白1(PD-1)及其配体(PD-L1)的单克隆抗体。PD-1抗体对于阻断晚期黑色素瘤、非小细胞肺癌和肾细胞癌非常有效,在治疗肿瘤上取得了重大的突破。但由于肿瘤致病机理复杂、患者个体差异较大,再加上环境因素的影响,免疫检查点抑制剂目前只能对约25%的患者起效。
越来越多研究表明,肠道微生物也是影响癌症免疫治疗效果的重要因素。
2015年,Marie Vétizou等人发现给经过抗生素处理或者无菌小鼠体内接种的肿瘤,不会对CTLA-4抑制剂产生响应,而给小鼠饲喂脆弱拟杆菌后,CTLA-4抑制剂抗肿瘤的效果得以恢复。2017年,Routy B等人的研究表明抗PD-1抑制剂与某些特定的肠道菌群联合使用,显著提高了肿瘤患者对其的响应,并显著提高了患者的平均无进展生存期(PFS)。综上,肠道微生物在改善免疫检查点抑制剂的疗效上具有巨大的应用潜力。因此,本领域需要开发一种新的抗肿瘤组合物,其具有更好的抗肿瘤效果,特别是对于特定的肿瘤具有更好的治疗效果。
发明内容
本申请的发明人发现,长型双歧杆菌与免疫检查点抑制剂联合使用可有效抑制各种肿瘤,包括但不限于,结肠癌、肺癌、乳腺癌、黑色素瘤、肾癌、尿路上皮癌等等。
本申请一方面提供了一种抗肿瘤组合物,其包括:
(A)长型双歧杆菌;以及
(B)免疫检查点抑制剂。
在本申请的一个实例中,所述长型双歧杆菌是长型双歧杆菌6-1。
在本申请的一个实例中,所述长型双歧杆菌与其他菌(如双歧杆菌、乳杆菌、梭菌、屎肠球菌、粪便普雷沃氏菌、瘤胃球菌)组合在一起。
在本申请的一个实例中,所述长型双歧杆菌和免疫检查点抑制剂混合在一起制备单一制剂,或者物理上分离分别使用。
在本申请的一个实例中,所述长型双歧杆菌是口服或注射剂型。
在本申请的一个实例中,所述抗肿瘤组合物还包括抗生素。
在本申请的一个实例中,所述肿瘤选自结肠癌、肺癌、胃癌、肝癌、头颈癌、宫颈癌、乳腺癌、淋巴癌、乳腺癌、黑色素瘤、肾癌或尿路上皮癌。
本申请还提供了长型双歧杆菌在制备治疗肿瘤的药物中的用途。
在本申请的一个实例中,所述长型双歧杆菌与免疫检查点抑制剂制剂联合使用。
在本申请的一个实例中,所述用途是提高免疫检查点抑制剂抑制肿瘤的效果,优选地,所述肿瘤选自结肠癌、肺癌、胃癌、肝癌、头颈癌、宫颈癌、乳腺癌、淋巴癌、乳腺癌、黑色素瘤、肾癌或尿路上皮癌。
附图说明
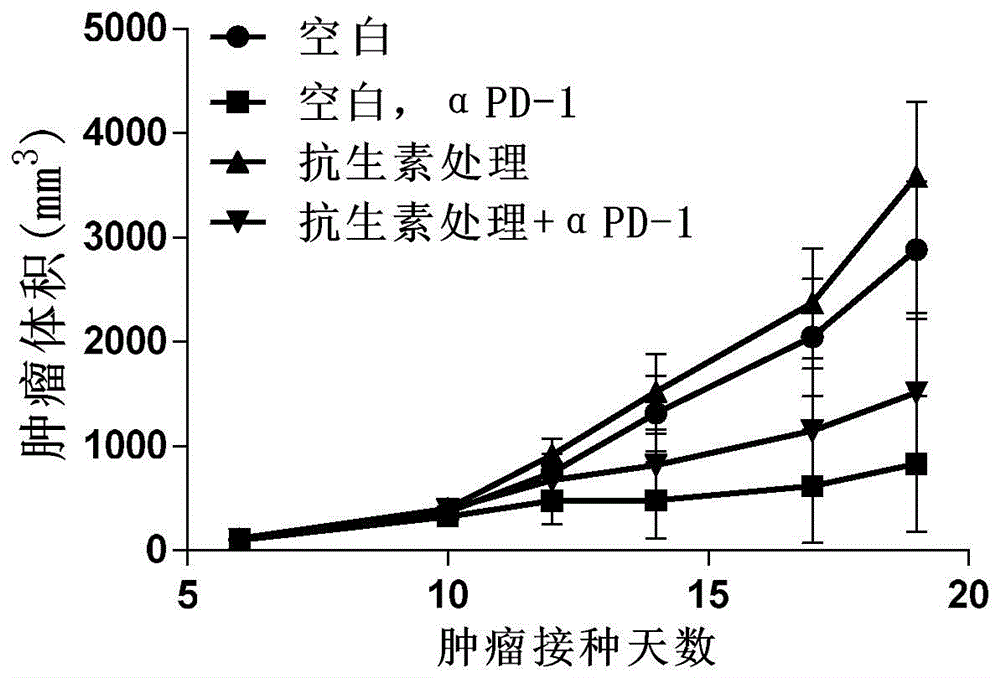
图1描述了抗生素破坏肠道菌群对MC38荷瘤小鼠肿瘤生长及anti-mPD-1治疗效果的影响。
图2描述了单独注射anti-mPD-1和单独口服长型双歧杆菌6-1分别对MC38荷瘤小鼠的肿瘤生长的影响。
图3描述了anti-m PD-1和长型双歧杆菌6-1的联合使用对MC38荷瘤小鼠的肿瘤治疗效果。
图4描述了不同益生菌与anti-m PD-1联合使用对MC38荷瘤小鼠的肿瘤治疗效果差异。
图5描述了anti-m PD-1单独注射,和与长型双歧杆菌6-1联合使用时MC38荷瘤小鼠体内平均CD3细胞数。
图6描述了anti-m PD-1单独注射,和与长型双歧杆菌6-1联合使用时MC38荷瘤小鼠体内肿瘤浸润的CD8 T细胞数。
图7描述了anti-m PD-1单独注射,以及和长型双歧杆菌6-1联合使用对4T1肿瘤的治疗效果。
图8描述了anti-m PD-1单独注射,以及和长型双歧杆菌6-1联合使用对LLC1肿瘤的治疗效果。
具体实施方式
在本发明中,如果没有特别的说明,百分数(%)或者份都指相对于组合物的重量百分数或者重量份。
在本发明中,如果没有特别的说明,所涉及的各组分或其优选组分可以相互组合形成新的技术方案。
在本发明中,如果没有特别的说明,本文所提到的所有实施方式以及优选实施方式可以相互组合形成新的技术方案。
在本发明中,如果没有特别的说明,本文所提到的所有技术特征以及优选特征可以相互组合形成新的技术方案。
在本发明中,如果没有相反的说明,组合物中各组分的含量之和为100%。
在本发明中,如果没有相反的说明,组合物中各组分的份数之和可以为100重量份。
在本发明中,除非有其他说明,数值范围“a-b”表示a到b之间的任意实数组合的缩略表示,其中a和b都是实数。例如数值范围“0-5”表示本文中已经全部列出了“0-5”之间的全部实数,“0-5”只是这些数值组合的缩略表示。
在本发明中,除非有其他说明,整数数值范围“a-b”表示a到b之间的任意整数组合的缩略表示,其中a和b都是整数。例如整数数值范围“1-N”表示1、2……N,其中N是整数。
在本发明中,除非有其他说明,“其组合”表示所述各元件的多组分混合物,例如两种、三种、四种以及直到最大可能的多组分混合物。
如果没有特别指出,本说明书所用的术语“一种”指“至少一种”。
如果没有特别指出,本发明所述的百分数(包括重量百分数)的基准都是所述组合物的总重量。
本文所公开的“范围”以下限和上限的形式。可以分别为一个或多个下限,和一个或多个上限。给定范围是通过选定一个下限和一个上限进行限定的。选定的下限和上限限定了特别范围的边界。所有可以这种方式进行限定的范围是包含和可组合的,即任何下限可以与任何上限组合形成一个范围。例如,针对特定参数列出了60-120和80-110的范围,理解为60-110和80-120的范围也是预料到的。此外,如果列出的最小范围值1和2,和如果列出了最大范围值3,4和5,则下面的范围可全部预料到:1-3、1-4、1-5、2-3、2-4、和2-5。
在本文中,除非另有说明,各组分的比例或者重量都指干重。
在本文中,除非另有说明,“不变”表示变化在±10%以内,较好在±5%以内,更好在±2%以内,最后在±1%。
在本文中,长型双歧杆菌包括衍生自长型双歧杆菌的活性成分,或者测序鉴定结果与长型双歧杆菌的序列相似性至少99%的菌株。
长型双歧杆菌
本申请所述的长型双歧杆菌可通过市售渠道获得,也可通过现有技术获得。例如,所述长型双歧杆菌可根据CN103830278A、CN103131647A、CN101244090A、CN101244089A、CN1223865A或US6368591获得。
本发明所述的长型双歧杆菌在本领域中是常规的,可分离自健康成人粪便。例如,它已经公开在已授权的US6368591中,其中长型双歧杆菌的保藏号为CCTCC M98003。
长型双歧杆菌为厌氧性细菌,革兰氏染色阳性,着色不均匀,无芽孢,无荚膜,无鞭毛,菌体呈直形或弯曲状,可出现“Y”或“V”型的分叉状,棒状等多多形态。在本发明的一个优选实例中,所述长型双歧杆菌为长型双歧杆菌(6-1)。
在本申请的一个优选实例中,所述长型双歧杆菌可以是长型双歧杆菌菌粉的形式。在本申请的一个实例中,长型双歧杆菌菌粉包含双歧杆菌和第一保护剂,所述第一保护剂含脱脂奶粉8-50%、谷氨酸钠0.01-10%、异乳糖8-50%、Vc-Na0.01-5%、淀粉4-30%,以所述第一保护剂的总重量计。
所述长型双歧杆菌菌粉可制成各种合适的剂型,例如口服液、片剂、胶囊、口崩片、冻干粉等等。在本申请的一个优选实例中,所述剂型为胶囊。在本申请的另一个优选实例中,所述剂型为片剂。所述剂型优选为冻干菌剂,其中的活菌数优选10
在本申请的一个优选实例中,所述长型双歧杆菌还可与其他菌株(包括但不限于双歧杆菌、乳杆菌、梭菌、屎肠球菌、粪便普雷沃氏菌、瘤胃球菌等)一起使用。
免疫检查点抑制剂
本申请使用的免疫检查点抑制剂可以是任意市售产品,如PD-1抑制剂、PD-L1抑制剂、CTLA-4抑制剂等。在一个优选的实例中,所述免疫检查点抑制剂包括可瑞达(Keytruda)、特善奇(Tecentriq)、纳武利尤单抗注射液(Nivolumab Injection)、Bavencio(Avelumab)、拓益(特瑞普利单抗注射液)。
抗肿瘤组合物
在本申请中,所述长型双歧杆菌和免疫检查点抑制剂可混合在一起制备单一制剂一起使用,也可以物理上分离分别使用。在本申请的一个实例中,所述长型双歧杆菌和免疫检查点抑制剂物理上分离分别使用。在本申请的另一个实例中,所述长型双歧杆菌可以在施用免疫检查点抑制剂之前施用给患者。通常,所述长型双歧杆菌可以任何合适的方式(包括但不限于口服、注射等等)施用给患者。所述免疫检查点抑制剂可以任何合适的方式(包括但不限于口服、注射等)施用给患者。所述长型双歧杆菌或免疫检查点抑制剂的使用方法是本领域常规的,本领域普通技术人员根据说明书的描述再结合现有技术可直接确定。
在本申请中,所述抗肿瘤组合物还可包括抗生素。所述抗生素可以是任何合适的抗生素,例如但不限于喹诺酮类抗生素、β-内酰胺类抗生素、大环内酯类、氨基糖苷类抗生素等。在本申请的一个优选实例中,所述抗生素包括但不限于β-内酰胺类抗生素(如青霉素、氨苄西林、羧苄西林、甲氧西林、苯挫西林、双氯西林、氟氯西林、头孢拉定、头孢噻肟、头孢氨苄、头孢曲松、头孢匹罗、头孢克肟、头孢托仑酯、头孢地尼、头孢丁烯、头孢帕胯酯、亚胺培南、氨曲南、头孢米诺钠、比安培南、亚胺培南、美罗培南等);大环内酯类抗生素(如红霉素、白霉素、罗红霉素、琥乙红霉素、阿奇霉素、克拉霉素、乙酰螺旋霉素、麦白霉素、麦迪霉素、交沙霉素、泰利霉素等);氨基糖苷类抗生素(链霉素、庆大霉素、阿贝卡星、丁胺卡那霉素等);喹诺酮类抗菌素(如环丙沙星、左氧氟沙星、诺氟沙星等);其他抗生素及抗菌药物(如四环素类、氯霉素类、林可霉素、利福霉素类如利福喷丁、多肽类如万古霉素、磺胺类如新诺明、甲硝唑类等);抗真菌药物(如二性霉素、灰黄霉素、达克宁等);抗肿瘤抗生素(如丝裂霉素、放线菌素D、博莱霉素、阿霉素等)等。
在本申请中,所述抗生素可与其他组分分开包装,并单独施用。
在本申请的一个优选实例中,所述抗肿瘤组合物还包括说明书,所述说明书描述施用长型双歧杆菌一段时间(例如1-10天),然后再施用PD-1抑制剂一段时间(例如10-100天)。优选的,长型双歧杆菌剂量范围:10
所述说明书还描述在施用长型双歧杆菌和PD-1抑制剂之前,先施用抗生素一段时间(例如1-3天)。优选地,抗生素的剂量范围:1-500mg/kg。
本申请的抗肿瘤组合物可有效治疗各种肿瘤,特别是(但不限于)结肠癌、肺癌、乳腺癌、黑色素瘤、肾癌、尿路上皮癌等等。
本申请另一方面提供了长型双歧杆菌在制备治疗肿瘤的药物中的用途。
在本申请中,所述长型双歧杆菌可联合免疫检查点抑制剂抑制肿瘤(例如结肠癌、肺癌、乳腺癌、黑色素瘤、肾癌、尿路上皮癌等)的生长。发明人发现,当患者使用抗生素时,免疫检查点抑制剂抑制肿瘤生长的效果受到限制,但是在给予免疫检查点抑制剂之前或同时施用长型双歧杆菌可有效提高免疫检查点抑制剂抑制肿瘤的效果。
本申请另一方面提供了长型双歧杆菌在治疗肿瘤中的用途。在本申请的一个实例中,所述用途包括抑制肿瘤生长。优选地,所述长型双歧杆菌可与免疫检查点抑制剂联合使用。通常,所述肿瘤包括但限于结肠癌、肺癌、乳腺癌、黑色素瘤、肾癌、尿路上皮癌等。
以下结合实施例详细描述本申请,但本申请的范围并不局限于此。
实施例所用原料如下:
6-8周SPF级雄性C57BL/6J小鼠(20-26g),来自于江苏集萃药康生物科技有限公司,质量合格证号为201805120。饲养条件为温度控制在(23±3)℃,湿度为40-70%,小鼠自由饮食饮水。
PD-1抑制剂购自亦康(北京)医药科技有限公司,浓度为7.09mg/mL,2-8℃避光储存。加入适量磷酸缓冲盐溶液混匀至指定浓度的溶液。
氨苄青霉素(Ampicillin)购自安徽安丰堂动物药业有限公司,链霉素(Streptomycin)购自Solarbio公司,硫酸粘菌素可溶性粉(Colistin)购自山东鲁西兽药股份有限公司。
MC38肿瘤细胞购自如汀生物技术(北京)有限公司,用灭火的10%胎牛血清,100U/mL的青霉素和100μg/mL的链霉素以及2mM谷氨酰胺的DMEM培养基在37℃、5%CO
小鼠乳腺癌4T1细胞(ATCC,货号:CRL-2539),LLC1肺癌细胞(购自上海生命科学研究院)。
长型双歧杆菌6-1为长型双歧杆菌6-1(CCTCC M98003)。
肿瘤体积的测量:
肿瘤体积:每周使用游标卡尺对肿瘤体积进行3次的测量,测量肿瘤的长径和短径,其体积计算公式为:体积=0.5×长径×短径
实施例1
6-8周龄的雄性C57BL/6J小鼠48只,适应环境一周后,按照体重随机分成4组,每组12只,分别为:第1组(无抗生素处理,空白,i.p.)、第2组(无抗生素处理,anti-mPD-1,10mg/kg,i.p.)、第3组(抗生素处理,空白,i.p.)、第4组(抗生素处理,anti-mPD-1,10mg/kg,i.p.)。抗生素处理是使用广谱抗生素Ampicillin(1mg/mL)+colistin(1mg/mL)+streptomycin(5mg/mL)饮水给药5天。所有组别接种磷酸缓冲盐溶液(PBS)重悬的MC38肿瘤细胞,浓度为1×10
MC38肿瘤细胞购自如汀生物技术有限公司,用含有灭活的10%胎牛血清,100U/mL的青霉素和100μg/mL的链霉素以及2mM谷氨酰胺的DMEM培养基在37℃、5%CO
试验结果列在图1中。结果表明:抗生素处理破坏了小鼠肠道菌群,小鼠的肿瘤生长加快,肿瘤体积增加,并对anti-m PD-1治疗效果产生了一定程度的影响。肠道菌群影响小鼠肿瘤生长以及anti-m PD-1的治疗效果。
实施例2
6-8周雄性C57BL/6J小鼠(20-26g,SPF级)36只,适应环境一周后,按照体重随机分为3组,第1组(抗生素处理,空白,i.p.)、第2组(抗生素处理,anti-mPD-1,10mg/kg,i.p.)、第3组(抗生素处理,长型双歧杆菌6-1,p.o.)。抗生素处理是使用广谱抗生素Ampicillin(1mg/mL)+colistin(1mg/mL)+streptomycin(5mg/mL)饮水给药5天。第3组的小鼠开始给与长型双歧杆菌冻干样品,灌胃浓度为1.0×10
MC38肿瘤细胞购自如汀生物技术有限公司,用含有灭活的10%胎牛血清,100U/mL的青霉素和100μg/mL的链霉素以及2mM谷氨酰胺的DMEM培养基在37℃、5%CO2的培养箱培养肿瘤细胞,每隔3天左右待细胞长满后分瓶传代,将处于对数生长期的肿瘤细胞用于体内肿瘤的接种。
试验结果列在图2中。肠道菌群破坏的肿瘤小鼠,经口服长型双歧杆菌6-1可以达到和注射anti-m PD-1治疗一样的效果,长型双歧杆菌6-1具有一定抑制肿瘤生长的效果。
实施例3:
6-8周雄性C57BL/6J小鼠(20-26g,SPF级)36只,适应环境一周后,按照体重随机分为3组,第1组(抗生素处理,空白,i.p.)、第2组(抗生素处理,anti-mPD-1,10mg/kg,i.p.)、第3组(抗生素处理,长型双歧杆菌6-1,p.o.,anti-mPD-1,10mg/kg,i.p.)。抗生素处理是使用广谱抗生素Ampicillin(1mg/mL)+colistin(1mg/mL)+streptomycin(5mg/mL)饮水给药5天。第3组小鼠开始给与长型双歧杆菌冻干样品,灌胃浓度为1.0×10
肿瘤细胞的培养:用含有灭活的10%胎牛血清,100U/mL的青霉素和100μg/mL的链霉素以及2mM谷氨酰胺的DMEM培养基在37℃、5%CO
结果如图3所示。结果表明口服长型双歧杆菌6-1与注射anti-m PD-1联合使用可以更好地抑制肿瘤的生长,减小肿瘤体积,对肿瘤达到更好的治疗效果。
实施例4
6-8周雄性C57BL/6J小鼠(20-26g,SPF级)48只,适应环境一周后,按照体重随机分为4组,第1组(抗生素处理,空白,i.p.)、第2组(抗生素处理,长型双歧杆菌6-1,p.o.,anti-mPD-1,10mg/kg,i.p.)、第3组(抗生素处理,长型双歧杆菌BL2(健康人的粪便样本),p.o.,anti-mPD-1,10mg/kg,i.p.)、第4组(抗生素处理,长型双歧杆菌BL3(健康人的粪便样本),p.o.,anti-mPD-1,10mg/kg,i.p.)。抗生素处理是使用广谱抗生素Ampicillin(1mg/mL)+colistin(1mg/mL)+streptomycin(5mg/mL)饮水给药5天。第2-4组小鼠开始给与长型双歧杆菌冻干样品,灌胃浓度为1.0×10
MC38肿瘤细胞的培养:用含有灭活的10%胎牛血清,100U/mL的青霉素和100μg/mL的链霉素以及2mM谷氨酰胺的DMEM培养基在37℃、5%CO2的培养箱培养肿瘤细胞,每隔3天左右待细胞长满后分瓶传代,将处于对数生长期的肿瘤细胞用于体内肿瘤的接种。
结果如图4所示,结果表明口服长型双歧杆菌6-1与注射anti-m PD-1联合治疗可以更好地抑制肿瘤的生长,减小肿瘤体积。
实施例5
实施例3中的小鼠于肿瘤接种后第19天安乐处死,流氏细胞术检测肿瘤细胞内的CD3、CD4、CD8、FOXP3、CD25、CXCR3、Gata3、Granzyme B、CD69、PD-1、CTLA-4,和CD11b、MHCⅡ、CD206、CD40、CSF1R、PD-L1、Gr-1。免疫因子分析包括TNF-α、IL-17、IL-13、IL-12p70、IL-10、IL-6、IL-5、IL-4、IL-2、IL-1b、IFNy、GM-CSF、G-CSF、M-CSF、MIG、IP-10、MIP1b和MAC-1。结果如图5所示,结果表明口服长型双歧杆菌6-1与注射anti-m PD-1联合治疗后,小鼠平均CD3细胞数显著性增加,增强了小鼠免疫系统应答。图中均与抗生素处理组相比,P<0.05表明存在显著性差异,*P<0.05,***P<0.001。
实施例6:
实施例3中的小鼠于肿瘤接种后第19天安乐处死,流氏细胞术检测肿瘤细胞内的CD3、CD4、CD8、FOXP3、CD25、CXCR3、Gata3、Granzyme B、CD69、PD-1、CTLA-4,和CD11b、MHCⅡ、CD206、CD40、CSF1R、PD-L1、Gr-1。实验结果如图6所示。结果表明相较于单独注射anti-mPD-1,口服长型双歧杆菌6-1与注射anti-m PD-1联合治疗后,肿瘤浸润的CD8 T细胞数显著性增加,小鼠免疫系统应答增强。表中均与抗生素处理组相比,P<0.05表明存在显著性差异,**P<0.01。
实施例7
6-8周雄性C57BL/6J小鼠(20-26g,SPF级)48只,适应环境一周后,按照体重随机分为4组,第1组(空白,i.p.)、第2组(anti-mPD-1,10mg/kg,i.p.)、第3组(长型双歧杆菌6-1,p.o.)、第4组(长型双歧杆菌6-1,p.o.,anti-mPD-1,10mg/kg,i.p.)。第3和4组小鼠用长型双歧杆菌6-1冻干样品灌胃,灌胃浓度为1.0×10
结果如图7所示。在对anti-mPD-1治疗不敏感的4T1乳腺癌模型中,长型双歧杆菌6-1与anti-mPD-1的联合治疗显著增强了anti-mPD-1对4T1乳腺癌的治疗效果,显著降低了肿瘤体积(P<0.0001),结果表明,长型双歧杆菌6-1能够增强机体对anti-mPD-1的响应,扩大anti-mPD-1治疗肿瘤的应用范围。
实施例8:
6-8周雄性C57BL/6J小鼠(20-26g,SPF级)36只,适应环境一周后,按照体重随机分为3组,第1组(空白,i.p.)、第2组(anti-mPD-1,10mg/kg,i.p.)、第3组(长型双歧杆菌6-1,p.o.,anti-mPD-1,10mg/kg,i.p.)。第3组小鼠用长型双歧杆菌6-1冻干样品灌胃,灌胃浓度为1.0×10
如图8所示,在对anti-m PD-1治疗不敏感的LLC1肺癌模型,长型双歧杆菌6-1与anti-m PD-1的联合治疗,相较于anti-m PD-1单独治疗,有效提高了机体对anti-m PD-1治疗的响应,显著抑制了肿瘤生长,减小了肿瘤体积。表中显著性差异均为与对照组相比,**P<0.001,****P<0.0001。
- 一种新晶型的抗肿瘤化合物及其制备方法和含其的组合物
- 一种九合一抗肿瘤外敷药贴组合物
- 洗涤剂组合物原液、以及包含该洗涤剂组合物原液的洗涤剂组合物
- 药物活性的膦基-烃基Ⅷ族金属络合物,含有这些络合物的抗肿瘤组合物和制备这些络合物或抗肿瘤组合物的方法
- 用于制备抗肿瘤剂的组合物以及用于制备基于所述组合物的抗肿瘤剂的方法
