妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测方法
文献发布时间:2024-04-18 19:58:53
技术领域
本申请属于药物分析技术领域,尤其是涉及一种妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测方法。
背景技术
妥布霉素地塞米松滴眼液,是一种含有糖皮质激素的抗生素滴眼液,临床主要用于治疗对肾上腺皮质激素有反应的眼科炎性病变及眼部表面的细菌感染或有感染危险的情况;适用于眼脸、球结膜、角膜、眼球前段组织及一些可接受激素潜在危险性的感染性结膜炎等炎性疾病,可以减轻水肿和炎症反应;也适用于慢性前葡萄膜炎、化学性、放射性、灼伤性及异物穿透性角膜病变。其主成分之一妥布霉素为氨基糖苷类广谱抗生素,其生产工艺主要为菌种发酵、吸附、解吸、浓缩、纯化、结晶和包装等。
目前,妥布霉素地塞米松滴眼液收录在《中国药典》2020年版二部、《美国药典》2021及进口药品注册标准中。其中,《中国药典》2020年版二部采用蒸发光散射法(ELSD)对妥布霉素地塞米松滴眼液中妥布霉素有关物质进行分析,该法流动相体系较简单,洗脱方式为等度洗脱,但相较来说,ELSD法灵敏度低、检测范围窄、重现性差,无法很好地对妥布霉素有关物质进行有效分离及定量分析。《美国药典》2021年版未对妥布霉素地塞米松滴眼液中妥布霉素有关物质进行规定;而进口注册标准则采用柱前衍生-紫外检测法进行,此法操作繁琐、重现性差、同时容易引入其他未知杂质。
妥布霉素原料药在生产过程和储存过程中容易引入6”-O-氨甲酰妥布霉素、卡那霉素B、新霉胺、2,6-二氨基-2,3,6-脱氧核糖-己糖等多种有关物质。而目前报道的分析方法不能将妥布霉素地塞米松滴眼液中妥布霉素的工艺杂质及降解杂质得到有效分离,同时重现性差会导致检测不准确。因此,开发一种更为适宜的检测方法对于妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测具有实际意义。
发明内容
为了解决现有技术的不足,本申请提供一种妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测方法,该方法能够对妥布霉素的工艺杂质及降解杂质进行有效分离,进而能够对妥布霉素有关物质进行准确检测,提高了妥布霉素有关物质检测的灵敏度和检测的准确度,对妥布霉素地塞米松滴眼液的质量控制具有重要意义。
为此,本申请第一方面提供了一种妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测方法,所述方法采用HPLC-CAD法进行检测,检测步骤包括:将妥布霉素地塞米松滴眼液作为供试品溶液进样至色谱柱中,然后采用流动相对所述色谱柱进行梯度洗脱,洗脱液进入电喷雾检测器中进行检测,获得检测结果;所述流动相包括流动相A和流动相B,所述流动相A为三氟乙酸水溶液,所述流动相B为乙腈;所述妥布霉素有关物质包括妥布霉素、尼伯拉胺、新霉胺、卡那霉素B、6-O-(3-氨基-3-脱氧-α-D-吡喃葡萄糖)-2-脱氧-D链霉胺和2,6-二氨基-2,3,6-脱氧核糖-己糖中的一种或多种。
本申请所述检测方法采用妥布霉素地塞米松滴眼液直接作为供试品溶液,无需对妥布霉素地塞米松滴眼液进行样品处理即可进行进样检测。检测过程中采用特定的流动相对色谱柱中的供试品溶液进行梯度洗脱,使供试品溶液中的妥布霉素有关物质里的工艺杂质和降解产物有效分离,洗脱后的洗脱液可以直接进入到电喷雾检测器中进行检测,若供试品溶液含有妥布霉素有关物质中各被测物,检测后的色谱图会在其相应的保留时间位置出峰,根据峰面积即可计算出各有关物质的含量。本申请所述方法能够对妥布霉素地塞米松滴眼液中妥布霉素有关物质里的工艺杂质和降解产物完全分离并进行准确检测,提高了妥布霉素有关物质检测的灵敏度和准确度,对妥布霉素地塞米松滴眼液的质量控制具有重要意义。同时该方法专属性强、准确度好、精密度高、重复性好,符合药物质量研究标准的技术要求,所得结果稳定可靠。
本申请所述方法检测过程中采用的流动相包括特定的流动相A-三氟乙酸水溶液和特定的流动相B-乙腈,采用上述组成的流动相进行梯度洗脱能够对供试品溶液中的妥布霉素有关物质(妥布霉素、尼伯拉胺、新霉胺、卡那霉素B、6-O-(3-氨基-3-脱氧-α-D-吡喃葡萄糖)-2-脱氧-D链霉胺和2,6-二氨基-2,3,6-脱氧核糖-己糖中的一种或多种)进行有效分离,使检测结果的出峰效果好,进而提高检测结果的准确性和稳定性。
本申请中,所述妥布霉素有关物质中妥布霉素、尼伯拉胺、新霉胺、卡那霉素B、6-O-(3-氨基-3-脱氧-α-D-吡喃葡萄糖)-2-脱氧-D链霉胺和2,6-二氨基-2,3,6-脱氧核糖-己糖的结构式如表1所示。
表1
在一些实施方式中,所述妥布霉素有关物质包括妥布霉素、尼伯拉胺、新霉胺和卡那霉素B。
本申请所述检测方法能够对妥布霉素地塞米松滴眼液中的妥布霉素、尼伯拉胺、新霉胺和卡那霉素B进行有效分离和准确检测,克服了现有分析方法不能将妥布霉素地塞米松滴眼液中妥布霉素的工艺杂质及降解杂质进行有效分离,进而导致检测不准确的问题。
在一些实施方式中,所述三氟乙酸水溶液中三氟乙酸的浓度为0.15~0.25mol/L。
在一些优选的实施方式中,所述三氟乙酸水溶液中三氟乙酸的浓度为0.2mol/L。
本申请通过将流动相A-三氟乙酸水溶液中三氟乙酸的浓度控制在上述范围内,能使采用该流动相A进行梯度时,对被检测物的分离效果更好,有助于进一步提高检测效果。
在一些实施方式中,所述流动相进行梯度洗脱的流速为0.3~0.5mL/min;所述梯度洗脱设置如下:
0~30min:95~100%A,5~0%B;
30~60min:95~100%A,5~0%B→0~5%A,100~95%B;
60~65min:0~5%A,100~95%B→95~100%A,5~0%B;
65~73min:95~100%A,5~0%B。
梯度洗脱的流动相体积百分比组成具体如表2所示。
表2
在一些优选的实施方式中,所述流动相进行梯度洗脱的流速为0.4mL/min;所述梯度洗脱设置如下:
0~30min:100%A,0%B;
30~60min:100%A,0%B→0%A,100%B;
60~65min:0%A,100%B→100%A,0%B;
65~73min:100%A,0%B。
梯度洗脱的原理为采用几种不同极性的溶剂形成流动相,通过改变流动相中各溶剂组成的比例改变流动相的极性,使每个流出的组分都有合适的容量因子k,并使待测样品中的所有组分可在最短时间内实现最佳分离。本申请通过采用三氟乙酸水溶液和乙腈作为流动相,在上述梯度洗脱流速和梯度洗脱程序设置条件下,能够使供试品溶液中妥布霉素相关物质的分离效率和分离效果最佳,提升柱效和检测结果的准确性。
在一些实施方式中,所述供试品溶液的进样量为8~12μL,进样温度为5~7℃;所述电喷雾检测器的雾化温度为50~55℃。
在一些优选的实施方式中,所述供试品溶液的进样量为10μL,进样温度为6℃;所述电喷雾检测器的雾化温度为50℃。
本申请采用电喷雾检测器对洗脱液进行检测,具有方法便捷、灵敏度高、重现性好、检测范围更宽等优势。
本申请通过选用上述参数设置,能进一步提升妥布霉素相关物质检测的准确性和稳定性。
在一些实施方式中,所述色谱柱中的填充剂为十八烷基硅烷键合硅胶颗粒,柱温为25~35℃。
在一些优选的实施方式中,所述色谱柱的柱温为30℃。
本申请中,所述十八烷基硅烷键合硅胶颗粒的粒径可以为1~10μm,优选为5μm。
本申请通过选用上述填充剂和柱温,有助于进一步提升妥布霉素相关物质的分离效率和分离效果。
在一些实施方式中,所述色谱柱为ZORBAX SB-C18,色谱柱规格为250mm×4.6mm、直径为5μm。
在一些实施方式中,所述方法还包括如下步骤:配制含妥布霉素有关物质的系统适用性溶液,对所述系统适用性溶液进行进样检测,确定所述妥布霉素有关物质中各被测物的保留时间。
本申请对系统适用性溶液进行进样检测的步骤和参数同供试品溶液。本申请中所述系统适用性溶液中含有特定含量的妥布霉素有关物质。在一些实施方式中,所述系统适用性溶液中含有2~3mg/mL的妥布霉素、40~45μg/mL的尼伯拉胺、25~30μg/mL的卡那霉素B和25~30μg/mL的新霉胺。在一些具体的实施方式中,所述系统适用性溶液中含有3mg/mL的妥布霉素、45μg/mL的尼伯拉胺、30μg/mL的卡那霉素B和30μg/mL的新霉胺。
本申请通过对系统适用性溶液进行检测,根据系统适用性溶液的色谱图检测结果,可以确定出在该检测条件下妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的保留时间,进而在后续检测中根据相应的保留时间即可确定在该保留时间下所出现的峰为何种被测物。
在一些实施方式中,所述方法还包括以下步骤:配制系列浓度的含妥布霉素有关物质的线性对照溶液,对所述线性对照溶液分别进行进样检测;根据所确定的各被测物的保留时间,获取所述线性对照溶液中各被测物的峰面积,进而建立妥布霉素有关物质中各被测物浓度与峰面积的标准曲线,以对供试品溶液中妥布霉素有关物质进行定量检测。
本申请中,对线性对照溶液进行进样检测的步骤和参数同供试品溶液。在一些实施方式中,所述线性对照溶液中含有特定浓度的妥布霉素、尼伯拉胺、卡那霉素B和新霉胺。在一些具体实施方式中,系列浓度的含妥布霉素有关物质的线性对照溶液包括:含600μg/mL的妥布霉素、450μg/mL的尼伯拉胺、300μg/mL的卡那霉素B和300μg/mL的新霉胺的线性对照溶液1,含60μg/mL的妥布霉素、45μg/mL的尼伯拉胺、30μg/mL的卡那霉素B和30μg/mL的新霉胺的线性对照溶液2,含6μg/mL的妥布霉素、4.5μg/mL的尼伯拉胺、3μg/mL的卡那霉素B和3μg/mL的新霉胺的线性对照溶液3,和含1μg/mL的妥布霉素、0.9μg/mL的尼伯拉胺、0.5μg/mL的卡那霉素B和0.5μg/mL的新霉胺的线性对照溶液4。
本申请通过对上述线性对照溶液进行检测,能够分别建立线性关系良好的妥布霉素度-峰面积的标准曲线、尼伯拉胺-峰面积的标准曲线、卡那霉素B-峰面积的标准曲线和新霉胺度-峰面积的标准曲线。根据所建立的标准曲线,以及对供试品溶液检测后各被测物(妥布霉素、尼伯拉胺、卡那霉素B和新霉胺)的峰面积,即可对供试品溶液中妥布霉素有关物质进行定量检测。
本申请的有益技术效果为:本申请所提供的妥布霉素地塞米松滴眼液中妥布霉素有关物质的检测方法,能够对妥布霉素的工艺杂质及降解杂质进行有效分离,具有高灵敏度、分离度的特点,且重复性、耐用性良好,进而能够对滴眼液中妥布霉素有关物质进行准确检测,对妥布霉素地塞米松滴眼液的质量控制具有重要意义。同时该方法专属性强、准确度好、精密度高、重复性好,符合药物质量研究标准的技术要求,所得结果稳定可靠,具有更好的实用价值。
附图说明
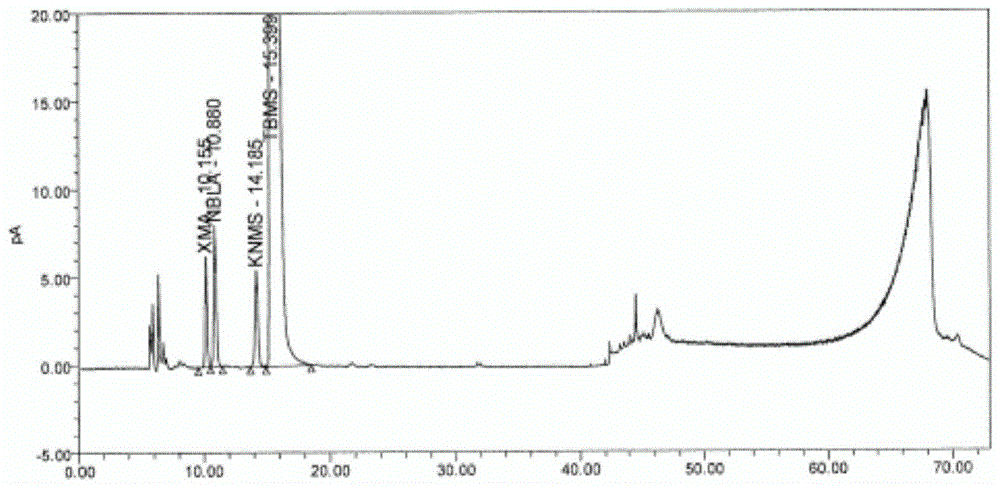
图1为实施例1中系统适用性溶液的色谱图检测结果。
图2为实施例2中供试品溶液的色谱图检测结果。
图3为对比例1中供试品溶液的色谱图检测结果。
图4为对比例2中供试品溶液的色谱图检测结果。
具体实施方式
为使本申请更加容易理解,下面将结合实施例来进一步详细说明本申请,这些实施例仅起说明性作用,并不局限于本申请的应用范围。本申请中所使用的原料或组分若无特殊说明均可以通过商业途径或常规方法制得。
实施例1:妥布霉素有关物质中各被测物的保留时间的确定
配制系统适用性溶液:精密称取尼伯拉胺、卡那霉素B、新霉胺和妥布霉素适量,加水使溶解并稀释制成含尼伯拉胺(45μg/mL)、卡那霉素B(30μg/mL)、新霉胺(30μg/mL)、妥布霉素(3mg/mL)的混合溶液,作为系统适用性溶液。
进样检测:
(1)色谱条件和检测器条件
色谱柱:ZORBAX SB-C18,250mm×4.6mm,5μm;色谱柱填充剂:颗粒粒径为5μm的十八烷基硅烷键合硅胶颗粒;流动相A:0.2mol/L的三氟乙酸溶液,流动相B:乙腈;流动相流速:0.4mL/min;柱温:30℃;进样温度:6℃,进样体积:10μL;梯度洗脱的程序设置如表3所示;电喷雾检测器(CAD);电喷雾检测器雾化温度:50℃。
表3
(2)将系统适用性溶液进样至色谱柱中,然后采用流动相对色谱柱进行梯度洗脱,洗脱液进入电喷雾检测器中进行检测,获得系统适用性溶液的色谱图检测结果,具体如图1所示。从图1可知系统适应性溶液出峰顺序依次为新霉胺峰、尼伯拉胺峰、卡那霉素B峰和妥布霉素峰,进而确定新霉胺、尼伯拉胺、卡那霉素B和妥布霉素的保留时间,且卡那霉素B峰和妥布霉素峰的分离度不小于1.2,其他相邻峰之间的分离度不小于1.5,表明本申请的方法能够对系统适用性溶液中的新霉胺、尼伯拉胺、卡那霉素B和妥布霉素进行有效分离。
实施例2:妥布霉素有关物质浓度-峰面积标准曲线的建立
取妥布霉素、尼伯拉胺、卡那霉素B和新霉胺适量,加水溶解并稀释制成含妥布霉素(600μg/mL)、尼伯拉胺(450μg/mL)、卡那霉素B(300μg/mL)、新霉胺(300μg/mL)的溶液,作为储备液。分别移取储备液适量,用水稀释至刻度,制备系列浓度的含妥布霉素有关物质的线性对照溶液。其中系列浓度的含妥布霉素有关物质的线性对照溶液包括:含600μg/mL的妥布霉素、450μg/mL的尼伯拉胺、300μg/mL的卡那霉素B和300μg/mL的新霉胺的线性对照溶液1,含60μg/mL的妥布霉素、45μg/mL的尼伯拉胺、30μg/mL的卡那霉素B和30μg/mL的新霉胺的线性对照溶液2,含6μg/mL的妥布霉素、4.5μg/mL的尼伯拉胺、3μg/mL的卡那霉素B和3μg/mL的新霉胺的线性对照溶液3,和含1μg/mL的妥布霉素、0.9μg/mL的尼伯拉胺、0.5μg/mL的卡那霉素B和0.5μg/mL的新霉胺的线性对照溶液4。
对上述线性对照溶液1-4分别进样检测,进样检测的色谱条件和检测器条件以及具体的检测步骤同实施例1,检测后分别获得上述线性对照溶液1-4色谱图。根据实施例1所确定的新霉胺、尼伯拉胺、卡那霉素B和妥布霉素的保留时间找出各被测物所对应的峰,进而获取线性对照溶液中各被测物的峰面积,以峰面积对浓度进行线性回归,建立妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的浓度与峰面积的标准曲线。所建立的妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的浓度与峰面积的标准曲线的具体信息如表4所示。
表4
从表4可知,采用本申请所述方法建立的妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的标准曲线在线性浓度范围内具有良好的线性关系,相关系数均大于0.99,进而根据所建立的标准曲线能够对供试品溶液中的妥布霉素相关物质进行准确定量检测。
实施例3:精密度测试
取妥布霉素地塞米松滴眼液适量作为供试品溶液,将供试品溶液进样至色谱柱中,然后采用流动相对色谱柱进行梯度洗脱,洗脱液进入电喷雾检测器中进行检测,进样检测的色谱条件和检测器条件以及具体的检测步骤同实施例1,检测后获得供试品溶液的色谱图检测结果。根据获得的检测结果,结合实施例2建立的妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的浓度与峰面积的标准曲线,即可计算出供试品溶液中妥布霉素的含量。
对供试品溶液平行进样检测6次,其中图2示例性给出了供试品溶液其中一次检测后的色谱图结果。检测结果显示:供试品溶液6次平行检测出的妥布霉素的结果与其平均结果的差值均<0.20%,6次平行检测出的尼伯拉胺的结果与其平均结果的差值均<0.20%,6次平行检测出的卡那霉素B的结果与其平均结果的差值均<0.20%,6次平行检测出的新霉胺的结果与其平均结果的差值均<0.20%。说明本申请所建立的方法对妥布霉素地塞米松滴眼液中妥布霉素相关物质进行检测的精密度好、准确性高。
实施例4:定量限与检测限的检测
取妥布霉素、尼伯拉胺、卡那霉素B和新霉胺适量,配制成含不同浓度的妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的一系列溶液,然后对配制的系列溶液进行进样检测,进样检测的色谱条件和检测器条件以及具体的检测步骤同实施例1。检测后,将检测结果S/N≈10时的溶液,作为定量限溶液;将检测结果S/N≈3时的溶液,作为检测限溶液。妥布霉素、尼伯拉胺、卡那霉素B和新霉胺的定量限和检测限结果见表5。
表5
从表5可知,本申请所建立的方法对妥布霉素、尼伯拉胺、卡那霉素B和新霉胺进行检测的检测限和定量限好,表明该方法对妥布霉素相关物质进行检测的灵敏度高、准确性好。
综上可知,本申请所建立的方法能使供试品溶液中妥布霉素及其工艺杂质以及降解产物完全分离,该方法专属性强、准确度好、精密度高、重复性好,符合药物质量研究标准的技术要求,所得结果稳定可靠。
实施例5:流动相对妥布霉素地塞米松滴眼液中妥布霉素有关物质检测的影响对比流动相1:流动相A:0.15mol/L的三氟乙酸溶液,流动相B:乙腈
对比流动相2:流动相A:0.25mol/L的三氟乙酸溶液,流动相B:乙腈
对比流动相3:流动相A:0.10mol/L的三氟乙酸溶液,流动相B:乙腈
对比流动相4:流动相A:0.20mol/L的三氟乙酸溶液,流动相B:甲醇;
分别利用上述4种对比流动相对实施例3中的供试品溶液进行6次平行检测,检测过程和条件除流动相外其余均同实施例3。
检测结果显示:采用对比流动相1进行检测后,供试品溶液6次平行检测出的妥布霉素的结果与其平均结果的差值最大为0.24%,6次平行检测出的尼伯拉胺的结果与其平均结果的差值最大为0.31%,6次平行检测出的卡那霉素B的结果与其平均结果的差值最大为0.39%,6次平行检测出的新霉胺的结果与其平均结果的差值最大为0.28%。
采用对比流动相2进行检测后,供试品溶液6次平行检测出的妥布霉素的结果与其平均结果的差值均<0.20%,6次平行检测出的尼伯拉胺的结果与其平均结果的差值最大为0.26%,6次平行检测出的卡那霉素B的结果与其平均结果的差值最大为0.32%,6次平行检测出的新霉胺的结果与其平均结果的差值均<0.20%。
采用对比流动相3进行检测后,供试品溶液6次平行检测出的妥布霉素的结果与其平均结果的差值最大为0.57%,6次平行检测出的尼伯拉胺的结果与其平均结果的差值最大为0.72%,6次平行检测出的卡那霉素B的结果与其平均结果的差值最大为0.83%,6次平行检测出的新霉胺的结果与其平均结果的差值最大为0.72%。
采用对比流动相4进行检测后,供试品溶液主峰峰型差,与相邻杂质未能完全分离,影响妥布霉素相关物质定量结果判断。
上述结果表明,改变流动相后检测结果的精密度和准确性均不同程度下降,其中对比流动相4不能将新霉胺和尼伯拉胺进行有效区分。
实施例6:梯度洗脱参数对妥布霉素地塞米松滴眼液中妥布霉素有关物质检测的影响分别按照下表6和7所示的梯度洗脱的程序设置对实施例3中的供试品溶液进行6次平行检测,检测过程和条件除度洗脱程序设置外其余均同实施例3。
表6
表7
采用表6的洗脱程序进行检测后的结果显示:供试品溶液6次平行检测出的妥布霉素的结果与其平均结果的差值均<0.20%,6次平行检测出的尼伯拉胺的结果与其平均结果的差值最大为0.23%,6次平行检测出的卡那霉素B的结果与其平均结果的差值最大为0.27%,6次平行检测出的新霉胺的结果与其平均结果的差值均<0.20%。检测结果的精密度和准确性相较于实施例3略有降低。
采用表7的洗脱程序进行检测后的结果显示:供试品溶液主峰峰型差,与相邻杂质未能完全分离,影响妥布霉素相关物质定量结果判断。
对比例1:《中国药典》方法对妥布霉素地塞米松滴眼液中妥布霉素有关物质进行检测
(1)色谱条件和检测器条件
色谱柱:Hypersil ODS,250mm×4.6mm,5μm;流动相:0.2mol/L的三氟乙酸溶液,进行等度洗脱;流动相流速:0.4mL/min;柱温:30℃;进样体积:10μL;蒸发光散射检测器检测,漂移管温度:110℃。
(2)将实施例3中的供试品溶液进样至色谱柱中,然后采用流动相对色谱柱进行等度洗脱,洗脱液进入蒸发光散射检测器中进行检测,获得供试品溶液的色谱图检测结果,具体如图3所示。从图3可知,在该色谱条件下,供试品溶液主峰峰型差,供试品溶液中的新霉胺、尼伯拉胺、卡那霉素B和妥布霉素未能有效分离,影响妥布霉素相关物质定量结果判断。
对比例2:进口注册标准方法对妥布霉素地塞米松滴眼液中妥布霉素有关物质进行检测
(1)色谱条件和检测器条件
色谱柱:Agela Venusil ASB C18,250mm×4.6mm,5μm;流动相:Tris缓冲液[取三羟甲基氨基甲烷(Tris)2.0g,加水800mL使溶解,加1mol/L的硫酸溶液20mL,用50%氢氧化钠溶液调节pH值至3.0±0.1]-乙腈(40:60),进行等度洗脱;流动相流速:1.2mL/min;柱温:30℃;进样体积:20μL;紫外检测器检测波长:365nm。
(2)取适量实施例3中的妥布霉素地塞米松滴眼液,精密加入适量Tris试剂和DNFB试剂,振摇,在60℃水浴中加热,进行衍生化反应,反应结束后,加入适量乙腈,摇匀,作为供试品溶液。将制得的供试品溶液进样至色谱柱中,然后采用流动相对色谱柱进行等度洗脱,洗脱液进入紫外检测器中进行检测,获得供试品溶液的色谱图检测结果,具体如图4所示。从图4可知,在该色谱条件下,供试品溶液中的新霉胺、尼伯拉胺、卡那霉素B能有效分离,但由于受衍生化试剂影响,容易引入其他未知杂质,导致总杂超出限度要求。
应当注意的是,以上所述的实施例仅用于解释本申请,并不构成对本申请的任何限制。通过参照典型实施例对本申请进行了描述,但应当理解为其中所用的词语为描述性和解释性词汇,而不是限定性词汇。可以按规定在本申请权利要求的范围内对本申请作出修改,以及在不背离本申请的范围和精神内对本发明进行修订。尽管其中描述的本申请涉及特定的方法、材料和实施例,但是并不意味着本申请限于其中公开的特定例,相反,本申请可扩展至其他所有具有相同功能的方法和应用。
- 一种妥布霉素地塞米松纳米混悬滴眼液及其制备方法
- 一种妥布霉素地塞米松纳米混悬滴眼液及其制备方法
