一种辅酶I晶型及其应用
文献发布时间:2024-04-18 20:00:50
技术领域
本发明涉及烟酰胺腺嘌呤二核苷酸制备技术领域,具体涉及一种辅酶I晶型及其应用。
背景技术
烟酰胺腺嘌呤二核苷酸(Nicotinamide adenine dinucleotide),简称NAD,是存在于包括人类细胞在内的所有活细胞中的一种生理物质,对身体无副作用,这种物质是很多可催化氧化—还原反应的酶的辅助因子,因此被称为辅酶Ⅰ。辅酶Ⅰ在生物体内参与物质和能量代谢,产生于糖酵解和细胞呼吸作用中的柠檬酸循环,并作为生物氢的载体和电子供体,在线粒体内膜上通过氧化磷酸化过程,转移能量供给ATP合成。如今,辅酶Ⅰ被广泛应用于化工催化反应、原料药生产、保健品生产、以及化妆品等行业,而随着对辅酶Ⅰ在疾病的治疗和预防方面的深入研究,辅酶Ⅰ作为医药保健品的重要性日益凸显出来,市场需求量逐年增加。
现有的辅酶Ⅰ的制备方法主要分为化学合成法和生物催化法,其中的生物催化法又包括生物发酵法和酶催化法,因其相较于化学合成法具有绿色环保无公害的优点而逐渐成为主流方向。通过生物催化法制备辅酶Ⅰ得到的粗产物溶液(酶反应液或者生物发酵液)中除辅酶Ⅰ外还含有大量杂质,再经过一些列的提纯和干燥后得到辅酶Ⅰ。
然而,现有的辅酶Ⅰ主要为冻干粉状,通过冻干粉状制备成给药片剂含有一定量的杂质,并且随着保存时间的延长,冻干粉状制备的片剂中杂质在缓慢的增加,影响了产品的质量。
发明内容
(一)解决的技术问题
针对现有技术的不足,本发明提供了一种辅酶I晶型及其应用,解决背景技术中提出的至少一个技术问题。
(二)技术方案
第一方面,本发明提供一种辅酶I晶型,所述辅酶I晶型为三斜晶系,且具有Pl或Pl的空间基团;晶格常数为:
优选地,所述辅酶I晶型从0%至80%的相对湿度的引湿增重为2.43%。
第二方面,本发明提供一种辅酶I晶型的制备方法,所述制备方法的具体步骤为:
调节NAD酶促反应液pH至3.0-3.2,纳滤膜过滤;
过滤后的NAD酶促反应液进行脱盐;
脱盐后的NAD酶促反应液进行浓缩,浓缩后终浓度为100-150g/L;
浓缩后的NAD酶促反应液分批次加入有机溶剂,低速搅拌进行结晶;
结晶停止后固液分离,使用与结晶相同的有机溶剂进行淋洗,干燥得到辅酶I晶型。
优选地,通过分批次添加的方式使浓缩液中含有机溶剂的体积百分比达到10%-80%。
第三方面,本发明提供一种辅酶I固体制剂,采用上述任一所述的辅酶I晶型制备。
优选地,所述辅酶I固体制剂包括片剂、胶囊剂或散剂。
第四方面,本发明提供一种辅酶I片剂,所述片剂的组分包括上述任一所述的辅酶I晶型、稀释剂、崩解剂、助流剂、润滑剂和薄膜包衣预混剂。
优选地,所述片剂的各组分含量分别为:
所述辅酶I晶型为30~45%、所述稀释剂为40~60%、所述润湿剂为0.5~1%、所述崩解剂为2%~6%、所述助流剂为0.1%~3%、所述润滑剂为0.1~3%和所述膜包衣预混剂为1~3%。优先的,所述薄膜包衣预混剂成分如下:羟丙甲纤维素1~5%、滑石粉1~5%、聚乙二醇1~4%、二氧化钛1~4%和60%乙醇85~90%。
优选地,所述稀释剂选自微晶纤维素、甘露醇、乳糖中的一种、两种或多种的组合;
和/或所述润湿剂选自20%~50%的乙醇水溶液;
和/或所述崩解剂选自羧甲基淀粉钠、低取代羟丙甲纤维素、交联聚乙烯吡咯烷酮中的一种、两种或多种的组合;
和/或所述助流剂选自微粉硅胶、滑石粉中的一种、两种的组合;
和/或所述润滑剂选自硬脂酸镁、硬脂酸钙中的一种、两种的组合。
优选地,所述稀释剂选自微晶纤维素、和/或所述崩解剂选自低取代羟丙甲纤维素、和/或所述助流剂选自微粉硅胶、和/或所述润滑剂选自硬脂酸镁。
(三)有益效果
本发明提供了一种辅酶I晶型及其应用,与现有技术相比,具有以下有益效果:
本发明提供的辅酶I晶型具有高结晶度的水合物晶型,具有良好的固态性质,有效成分含量明显高于冻干原料(无定形)的样品,且最大单质和总杂都显著低于冻干原料(无定形)的样品,并且随着保存时间过得延长,保存至12个月最大单质和总杂含量都没有明显提高。
附图说明
下面结合附图和实施例对本发明作进一步说明:
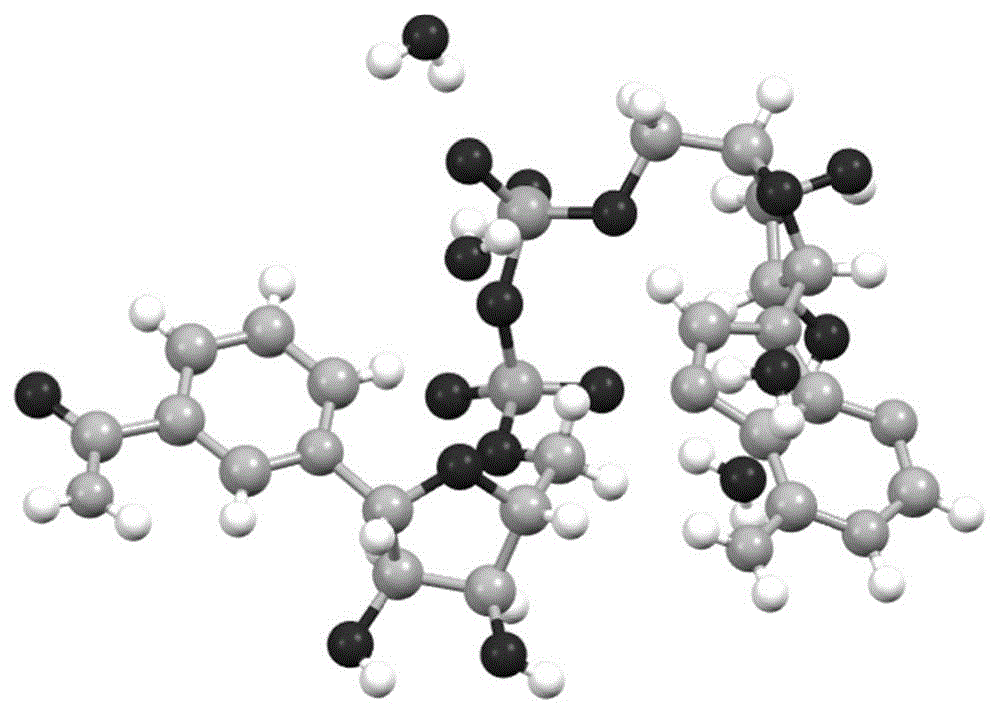
图1为辅酶I晶型晶体结构图;
图2为辅酶I晶型单晶衍射数据模拟得到的XRPD图谱。
具体实施方法
为使本发明实施例的目的、技术方案和优点更加清楚,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
为了更好的理解上述技术方案,下面将结合说明书附图以及具体的实施方式对上述技术方案进行详细的说明:
本发明实施例提供一种辅酶I晶型的制备方法,具体为:
调节NAD酶促反应液pH至3.0-3.2,纳滤膜过滤;
过滤后的NAD酶促反应液进行脱盐;
脱盐后的NAD酶促反应液进行浓缩,浓缩后终浓度为100-150g/L;
浓缩后的NAD酶促反应液分批次加入有机溶剂,低速搅拌进行结晶;
结晶停止后固液分离,使用与结晶相同的有机溶剂进行淋洗,干燥得到辅酶I晶型。
进一步的,上述辅酶I晶型的制备方法的详细步骤为:
(1)调pH:量取一定量的NAD酶促反应液使用盐酸调pH到3.0-3.2(25℃),0.22um孔径的滤膜过滤。其中所述NAD酶促反应液通过底物烟酰胺单核苷酸(NMN)(12-16.0g/L)和三磷酸腺苷(ATP)(20-29.9g/L)在33-37℃水浴烟酰胺单核苷酸腺苷转移酶(NMNAT酶)的作用下合成2-3小时而获得。
(2)脱盐:过滤后的NAD酶促反应液使用300-500Dal孔径的膜设备进行脱盐,脱盐全程使用冷却循环水降温,使料液温度不超过25℃。
(3)浓缩:使用旋转蒸发仪对脱盐后的NAD酶促反应液进行浓缩,设置真空度为10-30mbar,温度30-35℃,转速50-100rpm。浓缩后终浓度需达到100-150g/L。
(4)结晶:使用有机溶剂,通过分批次添加的方式使浓缩液中含有机溶剂的体积百分比达到10%-80%,之后置于2-8℃的环境下维持低速搅拌进行结晶。具体的有机溶剂可以为醚类、醚类、酯类、酮类或者二醇衍生物,如甲醇、乙醇、异丙醇、丙酮、甲基丁酮、甲基异丁酮等。
(5)收取晶体:结晶20-48小时后停止,固液分离后,使用10%-80%浓度的与结晶相同的有机溶剂进行淋洗,体积为结晶料液的1-4倍。
(6)干燥:将上述(5)得到的固体放入30-35℃的真空干燥箱中干燥,2-6小时后取出,粉碎后即得到本发明实施例晶型的辅酶I晶体。
下面结合具体的实施例进行详细的说明:
实施例1
辅酶I晶体的制备
通过底物烟酰胺单核苷酸(NMN)(140g/L)和三磷酸腺苷(ATP)(25g/L)在35℃水浴烟酰胺单核苷酸腺苷转移酶(NMNAT酶)的作用下合成2.5小时而获得NAD酶促反应液;
调pH:量取一定量的NAD酶促反应液使用盐酸调pH到3.1(25℃),0.22um孔径的滤膜过滤。其中所述
脱盐:过滤后的NAD酶促反应液使用400Dal孔径的膜设备进行脱盐,脱盐全程使用冷却循环水降温,使料液温度不超过25℃。
浓缩:使用旋转蒸发仪对脱盐后的NAD酶促反应液进行浓缩,设置真空度为20mbar,温度32℃,转速80rpm。浓缩后终浓度需达到125g/L。
结晶:使用有机溶剂,通过分批次添加的方式使浓缩液中该有机溶剂的体积百分比达到45%,之后置于5℃的环境下维持低速搅拌进行结晶。具体的有机溶剂为乙醇。
收取晶体:结晶40小时后停止,固液分离后,使用45%浓度的与结晶相同的有机溶剂进行淋洗,体积为结晶料液的2倍。
干燥:将上述得到的固体放入33℃的真空干燥箱中干燥,4小时后取出,粉碎后即得到本发明实施例晶型的辅酶I晶体。
本发明实施例以上述辅酶I晶体为原料,进行单晶培养,具体的单晶培养步骤为:
称取约50mg辅酶I晶体加入1mL水使其溶清,之后过滤,将滤液于样品瓶中,再敞口置于装有乙腈的环境下进行气液扩散,得到一个块状晶体。该块状晶体即为本发明实施例的辅酶I晶型,对该辅酶I晶型的结构进行分析,分析结果如下,将在水-乙腈体系中气液扩散获得的单晶进行单晶检测与解析:
本发明实施例提供的一种辅酶I晶型,所述辅酶I晶型为三斜晶系,且具有Pl或Pl的空间基团;晶格常数为:
具体的,相关的晶体学数据及结构精修参数见下表,通过单晶衍射数据模拟得到的X射线衍射图谱见图2,晶体结构图见图1;
上表中括号里面的数值为误差范围,例如a=8.5894(12)指a=8.5894±0.0012。
对于本发明实施例的辅酶I晶型进行了吸湿性研究及结构解析。吸湿性研究结果显示辅酶I晶型从0%至80%RH的引湿增重为2.43%。单晶解析结构显示辅酶I晶型中含有4个水,为四水化合物。
以冻干原料(无定形)作为参照,冻干原料为采用现有技术制备的,以水作介质的冻干材料。检测了本发明实施例的辅酶I晶型与冻干原料(无定形)的质量标准,检测方法按中国药典检测项进行检测,统一在25℃条件下的结果为:
基于上表能够知晓,冻干原料(无定形)虽然符合质量标准,但是随着保存时间的延长,最大单质以及总杂都在不断的提高。
其中,冻干原料(无定形)的制备方法为:通过底物烟酰胺单核苷酸(NMN)(140g/L)和三磷酸腺苷(ATP)(25g/L)在35℃水浴烟酰胺单核苷酸腺苷转移酶(NMNAT酶)的作用下合成2.5小时而获得NAD酶促反应液;获得的NAD酶促反应液经纳滤膜过滤得到辅酶I浓缩液,辅酶I浓缩液进行冷冻干燥,具体的冷冻干燥工艺为:
将板层温度降至-45℃±2,辅酶I浓缩液温度降至-35℃以下,保温3h;打开“冷凝器阀”将后箱冷凝器温度降至-40℃以下;一次升华干燥:开启真空泵、大小蝶阀,当冻干箱真空度<15pa后,对制品进行升华干燥,板层温度3小时爬坡升至-30℃,保温1-2小时;继续爬坡3小时升温至-20℃,保温1-2小时;继续爬坡4小时升温至-10℃保温1-3小时,继续爬坡3-4小时升温至8℃;二次升华:对制品进行升温干燥,冻干箱真空度<15Pa,继续爬坡3小时升温至25℃,保温1-3小时得到冻干原料(无定形)。
而,本申请实施例的辅酶I晶型为:
能够知晓,本发明实施例的有效成分含量明显高于冻干原料(无定形)的样品,且最大单质和总杂都显著低于冻干原料(无定形)的样品,并且随着保存时间过得延长,保存至12个月最大单质和总杂含量都没有明显提高。
进一步,本发明实施例提供了上述辅酶I晶型的应用,本发明实施例提供了通过上述辅酶I晶型制备的辅酶I固体制剂,其中所述辅酶I固体制剂包括片剂、胶囊剂或散剂。
本发明实施例提供一种辅酶I片剂,所述片剂的组分包括上述任一所述的辅酶I晶型、稀释剂、崩解剂、助流剂、润滑剂和薄膜包衣预混剂。
具体的,所述片剂的各组分含量分别为:所述辅酶I晶型为30~45%、所述稀释剂为40~60%、
所述润湿剂为0.5~1%、所述崩解剂为2%~6%、所述助流剂为0.1%~3%、所述润滑剂为0.1~3%和所述膜包衣预混剂为1~3%。
一实施例中,所述薄膜包衣预混剂成分如下:羟丙甲纤维素1~5%、滑石粉1~5%、聚二醇1~4%、二氧化钛1~4%和60%乙醇85~90%。
一实施例中,所述稀释剂选自微晶纤维素、甘露醇、乳糖中的一种、两种或多种的组合;
和/或所述润湿剂选自20%~50%的乙醇水溶液;
和/或所述崩解剂选自羧甲基淀粉钠、低取代羟丙甲纤维素、交联聚乙烯吡咯烷酮中的一种、两种或多种的组合;
和/或所述助流剂选自微粉硅胶、滑石粉中的一种、两种的组合;
和/或所述润滑剂选自硬脂酸镁、硬脂酸钙中的一种、两种的组合。
一实施例中,所述稀释剂选自微晶纤维素、和/或所述崩解剂选自低取代羟丙甲纤维素、和/或所述助流剂选自微粉硅胶、和/或所述润滑剂选自硬脂酸镁。
实施例2
辅酶I片剂的制备
通过该辅酶I晶型制备辅酶I片剂,具体的:
(1)称取处方量的辅酶I晶型原料即上述实施例1制备的辅酶I晶体40%、崩解剂羧甲基淀粉钠3%、稀释剂甘露醇50%、助流剂滑石粉1.5%置于混合机中混合均匀,加入润湿剂40%的乙醇水溶液0.7%,湿法制粒,用18目筛制粒;
(2)物料烘干后,加入润滑剂硬脂酸镁2%混合过16目筛;
(3)压制规定的片重即成素片;
(4)包衣,加入膜包衣预混剂2.8%,包衣工艺参数:压缩空气压力0.3Mpa,热风温度105℃,片床温度30~40℃,包衣锅转速5-6r/min,喷液速度0.5~1g/min。具体的,所述薄膜包衣预混剂成分如下:羟丙甲纤维素3%、滑石粉4%、聚乙二醇3%、二氧化钛3%和60%乙醇87%。
以上述冻干原料(无定形)和上述辅酶I晶型分别制备片剂,且,冻干原料(无定形)的制片工艺与辅酶I晶型片剂工艺相同,仅仅为将上述组分中的辅酶I晶体替换为冻干原料(无定形)。在25℃条件下质检检测结果入下:
能够得到,冻干原料制备的片剂保存12个月,最大单质和总杂明显增加,甚至增加数十倍。而,以上述辅酶I晶型原料制备的片剂,随着保存时间过得延长,保存至12个最大单质和总杂含量都没有明显提高。
需要说明的是,在本文中,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 商品状态识别方法、装置、电子设备及可读存储介质
- 烹饪机及其烹饪控制方法和装置、以及可读存储介质
- 一种浴室加热装置和用于控制浴室加热装置的方法、设备、电子设备及计算机可读存储介质
- 模态框构建方法、装置、电子设备、计算机可读存储介质
- 食物烹饪状态调控方法、装置、电子设备及可读介质
- 食物自动切片装置、智能烹饪机及其控制方法和计算机可读存储介质
