Cu2O@CeO2复合材料、催化剂及其制备和应用
文献发布时间:2024-04-18 20:01:23
技术领域
本发明涉及一种Cu
背景技术
近年来,恶性黑色素瘤(MM)的发病率和死亡率急剧上升。MM患者的中位生存率相对低于其他实体肿瘤,严重威胁人类健康,给临床癌症治疗带来很大困难。目前制定的常规策略,包括手术、化疗和放射治疗,存在一些缺点,例如治疗效率有限、副作用或耐药性。因此,迫切需要更具创新性和效率的方法来克服这些瓶颈。
随着纳米科学和纳米技术的出现,各种基于活性氧物种(ROS)的纳米药物被创造出来,作为有效的化学动力学疗法(CDT),可通过利用肿瘤微环境(TME)的酸性环境和过度表达的H
光动力疗法(PDT)和声动力疗法(SDT)是一种快速发展的治疗方法,通过敏化剂在光或超声波下激活O
近期,几种具有光敏/声敏特性的ROS催化纳米制剂已通过集成CDT、PDT或SDT用于协同抗肿瘤,例如无机半导体(例如TiO
发明内容
基于上述缺陷,本发明基于碳氮化物优异的光敏特性和独特的电子结构,提供了一种以金属氧化物-碳氮化物Cu
本发明的技术方案:
本发明要解决的第一个技术问题是提供一种生物催化剂,包括载体和活性中心,所述催化剂的活性中心为Cu
进一步,所述生物催化剂Cu
进一步,所述生物催化剂具有过氧化物酶活性和过氧化氢酶活性。
本发明要解决的第二个技术问题是提供上述生物催化剂的制备方法,所述制备方法为:以Cu
进一步,所述Cu
进一步,所述生物催化剂的制备方法为:将Cu
进一步,所述含碳氮化合物包括:双氰胺、三聚氰胺或尿素。
进一步,所述Cu
本发明要解决的第三个技术问题是提供上述生物催化剂在制备抗肿瘤药物、非抗生素类抗菌或声光增敏中的用途。
进一步,所述抗肿瘤药物中的肿瘤为恶性黑色素瘤。
进一步,上述生物催化剂即可作为一种抗肿瘤药物。
本发明要解决的第四个技术问题是提供一种Cu
进一步,所述铜盐选自:二水氯化铜、硫酸铜、硝酸铜、醋酸铜或氯化铜。
进一步,所述铈盐选自:七水氯化铈。
本发明要解决的第五个技术问题是提供一种Cu
本发明要解决的第六个技术问题是指出上述Cu
进一步,所述Cu
本发明的有益效果:
本发明提供了一种以金属配位碳氮化物Cu
附图说明:
图1:本发明实施例所得生物催化剂Cu
图2:(a)Cu
图3:实施例4所得生物催化剂Cu
图4:本发明实施例1所得催化剂Cu
图5:本发明实施例1所得催化剂Cu
图6:(a)为实施例1所得催化剂Cu
图7:(a)和(b)为本发明实施例1所得催化剂的能量色散X射线能谱(EDX)的元素面扫结果图。
图8:本发明实施例1所得催化剂Cu
图9:本发明实施例1所得催化剂的碳氮化物上超小Cu
图10:(a)-(c)为本发明实施例1所得催化剂的HAADF-STEM图。
图11:本发明实施例1所得催化剂的原子级EDX元素面扫结果图。
图12:本发明实施例1所得催化剂碳氮基上Cu
图13:(a)为实施例1所得催化剂中CeO
图14:实施例1中所得催化剂的PXRD和放大的PXRD图图。
图15:Cu
图16:Cu
图17:Cu
图18:不同温度下得到的相应产物中C=N-C和C≡N基团的含量图。
图19:Cu
图20:Cu
图21:Cu
图22:Cu
图23:实施例1中Cu
图24:(a)Cu
图25:实施例1所得催化剂动力学图,以H
图26:本发明实施例1所得催化剂与现有其他POD催化剂的TON值比较结果图。
图27:用于检测不同系统产生的·O
图28:本发明前驱体Cu
图29:TMB的紫外-可见吸收光谱图,以及本发明实施例1所得催化剂有或没有超声照射的紫外-可见吸收光谱图;其中,曲线从上至下依次对应的是TMB+Cu-CNx@CeO
图30:实施例1的Cu
图31:实施例1所得产物有或无光照射的TA荧光光谱图。
图32:(a)实施例1所得Cu
图33:不同产品的吸光度-波长结果图,表明Cu
图34:实施例1所得催化剂活性位点毒性试验结果图:a)类POD和b)类CAT催化剂对Cu
图35:不同浓度本发明实施例1所得催化剂孵育24h后HUVEC活力图。
图36:DCFH-DA染色的B16F10细胞的不同治疗后的相应定量图。
图37:US+L(超声+光照)处理后DCFH-DA染色的B16F10细胞的荧光图。
图38:B16F10细胞经Cu
图39:US+L后B16F10细胞的荧光素-膜联蛋白V-FITC和PI染色分析图。
图40:B16F10细胞的荧光素-膜联蛋白V-FITC和PI染色测定图。
图41:DCFH-DA染色的B16F10细胞的不同处理后的相应定量分析图。
图42:钙黄绿素AM/PI染色的B16F10细胞不同治疗后的相应定量图。
图43:US+L后钙黄绿素AM/PI染色的B16F10细胞的荧光图。
图44:在用膜联蛋白V-FITC和PI染色后进行了流式细胞术细胞凋亡测定图。
图45:用膜联蛋白V-FITC和PI染色后进行的流式细胞仪凋亡测定图。
图46:用膜联蛋白V-FITC和PI染色后进行的流式细胞仪凋亡测定揭示的细胞凋亡率结果图。
图47:US+L后B16F10细胞荧光素-annexin V-FITC和PI染色测定图。
图48:钙黄素AM/PI染色的B16F10细胞的荧光图像。
图49:B16F10肿瘤的肿瘤生长曲线图。
图50:B16F10在不同治疗下的肿瘤图。
图51:B16F10肿瘤生长抑制率结果图。
图52:热图显示的体重变化图。
图53:对小鼠主要脏器(心、肝、脾、肺、肾)进行H&E染色,观察催化剂的潜在积累情况及不同处理后的组织学变化图。
图54:(a-e)为标记物ALP2L、ALTL、ASTL、CERA和UREAL的血液生化分析图。
图55:不同治疗15天后,肿瘤组织和肿瘤血管的H&e和CD31染色图。
图56:US+L 15天后肿瘤组织和肿瘤血管的H&E和CD31染色图。
图57:不同治疗组肿瘤切片的TUNEL、Ki67和CRT染色图。
图58:不同治疗组肿瘤切片的TUNEL的定量分析结果图(*p<0.05,**p<0.01,***p<0.001)。
图59:不同治疗组肿瘤切片的Ki67的定量分析结果图(*p<0.05,**p<0.01,***p<0.001)。
图60:不同治疗组肿瘤切片的CRT定量分析结果图(*p<0.05,**p<0.01,
***p<0.001)。
图61:US+L治疗肿瘤切片的TUNEL、Ki 67和CRT染色图。
具体实施方式
下面结合实施例对本发明的具体实施方式做进一步的描述,并不因此将本发明限制在所述的实例范围之中。
本发明实施例所使用的材料:
二水氯化铜(CuCl
实施例1~3:
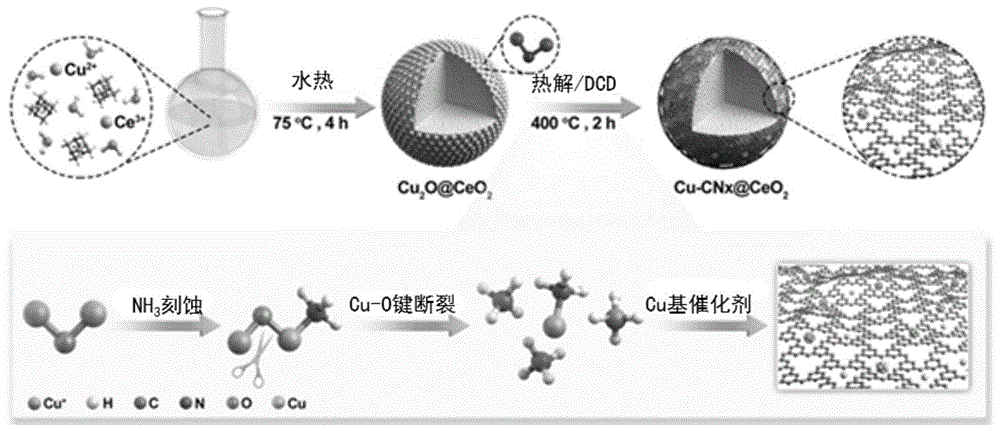
采用一步水热法合成前驱体Cu
将CuCl
生物催化剂Cu
将20mg上述制备的前体Cu
本发明实施例所得生物催化剂Cu
实施例4:
前驱体Cu
实施例5:
前驱体Cu
实施例6:
前体Cu
试验例1微观结果表征:
1、检测方法:
用铜Kα辐照Rigaku Ultima IV进行粉末XRD分析,确定了所有产物的晶体结构。衍射图案以2°min的扫描速率在20°和80°的0.02°步骤下收集。采用扫描电子显微镜(SEM)和高分辨率透射电子显微镜(HR-TEM,Tecnai G2 F20 S-TWIN)和能量色散x射线能谱(EDX)对催化剂的表面形貌、尺寸和元素组成进行了分析。为了进行像差校正扫描透射电子显微镜(AC-STEM)分析,在200kV电压下对FEI Titan Themis 60-300进行了STEM研究。采用x射线光电子能谱(XPS,ESCAL 250)和Al Kα单色x射线源测定了表面元素组成和所有结合能。利用KBr颗粒技术在Nicolet-ls50型FTIR光谱仪上记录了傅立叶变换红外光谱。电子顺磁共振(EPR)测量是通过Bruker EPR EMX Plus(Bruker Ltd,USA)在9.8GHz频率(微波功率:1mW)下进行的。电感耦合等离子体质谱(ICP-MS)记录在Thermo Scientific iCAP RQ上。
2、微观结构表征结果:
通过SEM和TEM记录在不同温度(300、400、500和600℃)下合成形貌和结构演变;图2a显示Cu
由TEM结果可知:实施例1所得Cu
利用高角度环形暗场成像扫描透射电子显微镜(HAADFSTEM)研究了实施例1所得催化剂Cu
相应的原子级的EDX元素面扫观察到Cu、O、C和N的均匀分布,并证明Cu
为了进一步研究本发明催化剂形成过程并验证其化学结构,本发明通过粉末X射线衍射(PXRD)、X射线光电子能谱(XPS)和傅里叶变换红外光谱(FTIR)来探索它们的详细特性。首先,PXRD分析如图14所示,在不同热处理下的所有样品均在28.7°、33.2°和47.7°处显示出尖峰,这些峰可归属于CeO
Cu
相应地,N 1s光谱(图19)观察到所有热处理样品的主要包含吡啶N(399.4eV)和吡咯烷N(398.4eV),类似C1s的结果,样品在600℃高温时氰基N含量最多(397.0eV),表明碳氮化物中CN杂环结构的破坏。此外,Cu 2p光谱表明Cu
FTIR提供了更多关于Cu
试验例2过氧化物酶(POD)性能:
通过典型的3,3′,5,5′-四甲基联苯胺(TMB)比色法,本发明研究了POD样生物催化活性对ROS生成的影响。在H
然后,计算了本发明实施例1在固定浓度(12.5μg mL
试验例3确定催化所产生ROS的种类:
通过使用5,5-二甲基-1-吡咯烷-N-氧化物(DMPO)作为捕获试剂,对实施例所得生物催化剂进行电子顺磁共振(EPR)分析,以确定ROS的种类,该捕获试剂给出强·O
试验例4氧化氢酶(CAT)性能:
本发明还研究细胞的过氧化氢酶(CAT)样能力,如图28所示,实施例1所得Cu
试验例5光动力/声动力增强产ROS的能力:
将本发明实施例1的Cu
二氢乙二胺(HE)跟踪方法验证了超声增强·O
9,10-二苯蒽醌(DPA)染料检测到通过Ⅱ型机理产生的
上述实验结果表明,本发明实施例1~5所得催化剂具有较高的催化活性和声/光响应能力,这得益于Cu
此外,还通过使用硫氰酸钾试剂(KSCN)进行活性位点毒性试验,以验证生物催化剂中Cu
试验例6生物实验:
受上述卓越的ROS生成能力的启发,本发明进一步评估了实施例1所得催化剂对MM肿瘤细胞的治疗效果。在评估肿瘤细胞的效率之前,首先研究Cu
进一步,本发明使用2,7-二氯荧光素二乙酸酯(DCFH-DA)直观地记录Cu
此外,流式细胞仪获得的结果与荧光数据的结果相似,表明Cu
为了研究本发明催化剂在B16F10细胞上生物催化杀灭能力,用实施例1所得Cu
考虑到细胞凋亡与线粒体功能障碍高度相关,本发明通过JC-1进一步研究线粒体膜电位。如图48所示,在对照组(对照组指无催化剂空白对照)中只观察到不健康去极化线粒体的绿色荧光信号略微增加,而JC-1染料从红色聚集体(健康极化线粒体)恢复到其他组的绿色单体,这意味着线粒体受到严重损伤,表明线粒体膜协同去极化和损伤。
试验例7体内实验:
本发明还对Cu
此外,各组的肿瘤组织用苏木精和伊红(H&E)染色,如图55所示,对照组(对照组指无催化剂空白对照))的肿瘤细胞可以保持正常形态,而无明显组织损伤,而肿瘤在Cu
此外,本发明还进行了末端脱氧核苷酸转移酶dUTP缺口末端标记(TUNEL)和Ki-67染色,以探讨各组的肿瘤凋亡和细胞增殖情况。与其他组相比,Cu
- 一种仿生结构含羞草状碳负载硫的复合材料及其制备方法、锂硫电池正极及电池
- 一种锂离子电池的负极膨胀抑制结构和负极及其制备方法
- 一种接触钝化晶体硅太阳能电池结构及制备方法
- 一种非金属外壳的圆柱电池结构及制备方法
- 一种N型单晶硅HBC太阳能电池结构及其制备方法
- 一种P型HBC电池结构及其制备方法
